水热-离子交换法制备m-LiMnO2及工艺优化
2017-01-20郑宇亭郝晓剑潘保武
郑宇亭,郝晓剑,潘保武,
(1.中北大学材料科学与工程学院,山西太原030051;2.国防科技重点实验室,山西太原030051)
水热-离子交换法制备m-LiMnO2及工艺优化
郑宇亭1,郝晓剑2,潘保武1,2
(1.中北大学材料科学与工程学院,山西太原030051;2.国防科技重点实验室,山西太原030051)
单斜层状m-LiMnO2,合成方法单一且苛刻。为降低其成本及合成复杂性,以NaMnO2为研究对象,用高温固相法将Mn2O3和无水Na2CO3合成α-NaMnO2,在此研究钠与锰的浓度不同、煅烧温度不同、保温时间不同、有无碳粉保护的不同对α-NaMnO2结构的影响。以得到的α-NaMnO2为前驱体探究通过水热-离子交换法在不同条件下得到m-LiMnO2,并对水热-离子交换法进行优化探索,效果优于目前的回流蒸馏法。
高温固相法;前驱体;水热-离子交换法;m-LiMnO2
锂离子电池在工业领域是发展速度最快的高能量存储设备,而电极材料的发展是锂离子电池发展的关键。作为能量来源,其广泛应用于电子设备,甚至电动车/混合动力汽车,而正极材料能量密度和功率的最大化将大大促进这些技术的应用[1]。锂锰氧化物因其污染小、储量大、价格低,特别是不存在过充安全性问题,成为目前最具吸引力的正极材料,其主要为尖晶石LiMn2O4和层状结构的LiMnO2。尖晶石型LiMn2O4因放电可逆比容量仅为110 mAh/g而制约了其发展;而层状结构拥有着特殊的化学和物理特性,具有二维空间氧化物层能够允许离子或质子反复地实现嵌入和脱出,这种结构使其能够在可充电电池的电极材料中实现应用[2-3],因此层状结构的LiMnO2实际放电可逆容量可达200 mAh/g以上,是一种具有极大发展前景的正极材料[4-5]。Armstrong等[6]首次用离子交换法合成了单斜层状LiMnO2(m-LiMnO2),以类似结构的层状α-NaMnO2为原料,用Li+置换Na+,在合适的有机溶剂中进行离子交换,制得了无水纯净的m-LiMnO2。其属于C2/m空间群,结构较之正交o-LiMnO2(Pmnm空间群)更有利于Li+脱嵌。然而,从稳定性来看,由于m-LiMnO2材料对称性比层状LiNiO2及层状LiCoO2略逊一筹,在热力学平衡条件下,Li-MnO2的正交相更加稳定[7],大量研究表明通过掺杂和包覆等一系列改性方法能够有效地改善其稳定性,Velikokhatnyi[8]对前驱体α-NaMnO2掺杂硼做了理论和实验证明,其结构稳定性及电化学性能均有显著提高。

图1 α-NaMnO2离子交换生成m-LiMnO2
NaMnO2具有不同的层状结构,为层状的α-NaMnO2和β-NaMnO2,他们分别属于C2/m和Pmnm空间群[9]。如图1,α-NaMnO2中MnO6八面体共边而形成片层状,类似于水钠锰矿的Na+位于两片层之间,决定了其通过离子交换得到的m-LiMnO2的结构。另一种为β-NaMnO2有着锯齿形的MnO6八面体组成的片层,Na+位于其间。
通过优化合成条件可以提高材料的电化学性能。锂离子电池正极材料的电化学性能很大程度上取决于合成时采用的方法和工艺条件。国内外对用作锂离子电池正极材料层状LiMnO2的制备方法较普遍使用的有高温固相反应法和水热合成法等多种方法。但m-LiMnO2的制备方法目前仍然只有离子交换法一种,该方法有着产品质量好,原料损失少等优点,普遍采用在有机溶液中以高的Li/Mn摩尔比,高温下回流蒸馏,并用有机溶剂冲洗后干燥而得。但其有着效率低、成本较高、废弃溶剂污染等缺点。水热制备方法反应条件温和,可制备出纯度高、结晶性好、形貌规整、粒度分布均匀、电化学性能优越的产物。水热-离子交换法是将两者优点相结合,克服原有离子交换法的缺点,制备质量优异的m-LiMnO2。
1 实验
1.1 原料与仪器
氢氧化锂(LiOH·H2O)、无水碳酸钠(Na2CO3)、无水氯化锂(LiCl)、二氧化锰(MnO2)、无水乙醇(CH3CH2OH),以上均为分析纯;Mn2O3(自制:由MnO2经800℃煅烧12 h)。
DH-500A型高精密电子天平,精度为0.01 g;采用SX2-2.5-12型箱式电阻炉制备Mn2O3;采用ND-7系列行星式球磨机对粉末进行机械活化;SG-5404A型恒温磁力加热搅拌器;采用DH101-3S型电热恒温鼓风干燥箱对反应釜进行加热,提供反应所需高温高压环境,以及产物干燥;采用日本理学D/Max-rB X射线衍射仪进行物相鉴定,Cu-Kα辐射源(波长为0.154 179 nm),工作电流100 mA,工作电压40 kV,扫描速度5(°)/min,步长为0.01°;采用Nova Nano SEM-430型及SU-1500型扫描电子显微镜进行产物形貌和元素分析。
1.2 实验过程
1.2.1 前驱体NaMnO2的制备
实验使用高温固相法制备层状锰酸锂的前驱体α-NaMnO2。其工艺流程可简述为:原料→混料→球磨→煅烧→筛分→终产物。球磨步骤起到机械活化作用,改善粉料化学活性,对于产物的固相反应都有着促进作用,也使产物在较为低能耗的环境下发生反应。本实验以无水Na2CO3和Mn2O3为原料,按n(Na+)∶n(Mn3+)=1∶1和1.5∶1,通过2 h球磨机械活化后,于700、750、800℃下,于原料表层覆盖碳粉和无保护两组分别煅烧16、18、24和30 h,取出研磨。
1.2.2 水热-离子交换法制备m-LiMnO2
水热-离子交换法是以水热法实现离子交换。取经过定性分析后一定量研细的α-NaMnO2分别在去离子水中与不同的含锂化合物LiOH·H2O和LiCl进行离子交换。在n(Li+)∶n(Mn3+)=4∶1、8∶1和10∶1的条件下,与去离子水通过磁力搅拌2 h配制成溶液,置于高温反应釜中,分别在150、180和200℃下均保持8、10和12 h;将离子交换后的产物用去离子水冲去数次,pH测试为中性即可,过滤产物并于80℃干燥12 h,即得到离子交换后的产物。
2 结果与讨论
2.1 α-NaMnO2的组成分析、表征与对比优化
图2,3为煅烧温度700℃、24 h,不同n(Na+)/n(Mn3+)下有无碳粉保护所得产物的XRD图。从图中可见相对高的n(Na+)/n(Mn3+)明显杂峰较多,n(Na+)/n(Mn3+)为1∶1时有碳还原保护未出现Na0.7MnO2.05,但缺Na化合物Na0.7MnO2。通过对比实验结果得出:在700到800℃,温度越高杂质越多,α-NaMnO2几乎不存在;且长达30 h的煅烧对于α-NaMnO2不利,在没有还原保护下更长时间的高温环境会加强产物的氧化,对于工业化生产亦是不可取。遂将讨论结果集中在800℃,30 h以内更为合理的条件下的产物进行对比。

图2 煅烧温度700℃、24 h,不同n(Na+)/n(Mn3+)下有碳粉保护所得产物的XRD图

图3 煅烧温度700℃、24 h,不同n(Na+)/n(Mn3+)下无碳粉保护所得产物的XRD图

图4 不同条件下煅烧所得产物的SEM照片
图4 为图2,3所示的不同条件下煅烧所得产物的SEM照片。对比SEM照片,只有 (d)照片中不含有棒状结晶,从XRD衍射图谱发现只有该条件下不存在 Na0.7MnO2.05,故Na0.7MnO2.05以棒状形态存在;对比照片(a)与(c)的制备条件得出温度较高颗粒反而较大,对比(b)与(c)得出煅烧时间较长有助于晶体颗粒的完整性;在n(Na2CO3)∶n(Mn2O3)=1∶1时,有碳粉覆盖的情况下煅烧温度700℃、24 h,即(d)图所示产物,其形态与(a)(b)(c)的颗粒状不同,结晶粒密而细小呈片层状,结晶状况良好,有利于进行后续离子交换发应。
针对其中较低的n(Na+)/n(Mn3+)比会出现缺Na化合物出现,对Na2CO3的实验比例微调,使得n(Na2CO3)∶n(Mn2O3)= 1.2∶1,在已确定的最优实验条件,700℃下碳粉还原保护煅烧24 h,制备所得产物的XRD衍射图如图5,结论与文献[10]基本一致,所得α-NaMnO2属C2/m空间群。其中Na0.7MnO2.05是由于α-NaMnO2不稳定,测试过程与空气中水分子发生作用发生晶格重排[10]。
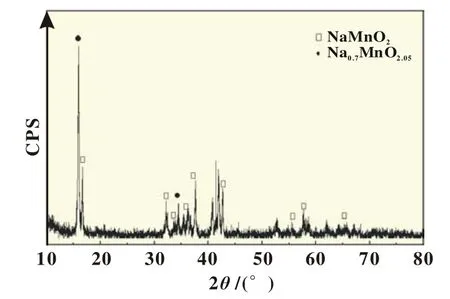
图5 700℃碳还原保护下煅烧24 h所得样品的XRD图
2.2 m-LiMnO2的组成分析、表征与对比优化
以LiCl为锂源,通过对n(LiCl)∶n(α-NaMnO2)为不同Li+/Mn3+摩尔比,于120、150、180和200℃水热8、10和12 h的产物分析,发现采用LiCl进行水热反应得到的生成物主要是尖晶石LiMn2O4,只有n(LiCl)∶n(α-NaMnO2)为5∶1、180℃下水热8 h的样品有少量m-LiMnO2,得出卤素锂盐在高温高压反应釜中的水热-离子交换法中并不适用。相比蒸馏回流法,在固定的液态高温高压环境下,卤素离子的存在似乎阻碍了离子交换的顺利进行,故后续实验的锂盐改为LiOH·H2O。
对LiOH·H2O与α-NaMnO2在n(Na+)/n(Mn3+)=4∶1、8∶1、10∶1(摩尔比),从不同温度下加热不同时间所得产物进行XRD、SEM物相鉴定及实验规律得出:(1)从n(Li+)/n(Mn3+)角度来看:Li浓度过低,富锂条件达不到使得反应不完全;Li浓度过高会出现其他类型的锂锰氧化物如Li2Mn2O4,同时发现过多的LiOH影响了LiMnO2的结晶,且成本过高;(2)从温度角度来看:高温200℃短时间8 h可以产生m-LiMnO2,但产物难以达到最稳定状态,且仍会出现其他类型的锂锰氧化物;而150℃难以合成且杂质存在;(3)从时间来看,(相对)低温长时间和高温短时间均可生成,但产物结晶度并不理想;(4)从去离子水洗涤次数来看,与n(Li+)/n(Mn3+)相同数值的洗涤次数达到溶液pH合格,在达到合成条件的基础上,可降低了洗涤次数和废液产量。
基于以上实验结论,改进实验条件,使n(Li+)/n(Mn3+)=5∶1,基于150℃低温长时间12 h,提高温度至180℃,相比200℃的加热时间适当延长水热时间使产物充分结晶。
图6为优化条件下水热不同时间的XRD图。从图中可以看出,水热时间为8 h时,样品主相为Li2MnO3;水热时间为10 h时,样品几乎为纯净的m-LiMnO2,与预测分析吻合。故采用最合理工艺进行多组实验,洗涤次数为4~6次,抽查检测溶液pH值为7,并进行抽样检测。

图6 水热-离子交换法不同时间下的XRD图
图7 为制备工艺优化后的制备条件下随机抽取的产物的XRD图谱及SEM照片,产物纯净,制备的样品颗粒小,晶形排布均匀,颗粒分散性好,空隙率高,且形状规整,故在180℃下以n(Li+)/n(Mn3+)为5∶1水热10 h,对于水热-离子交换法的大量制备来说是可行的。
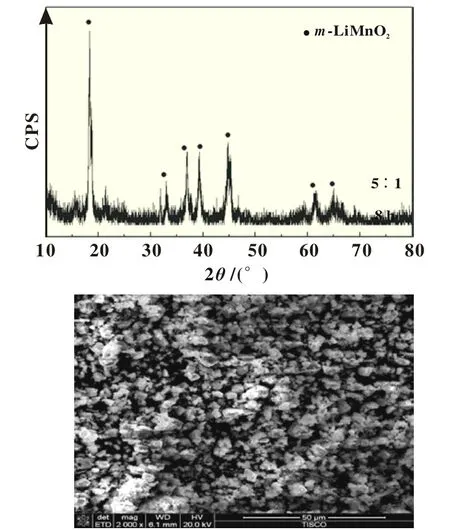
图7 随机选取样品的XRD图及SEM扫描照片
上述实验将前驱体α-NaMnO2与锂的离子化合物及去离子水混成溶液,在反应釜中的高温高压环境下实现Na+和Li+的交换,与蒸馏回流法相比,本合成方法的工艺更简单、时间更短,克服了离子交换法反应周期长,离子交换不彻底、合成产物的纯度也不高的缺点。与有机溶液和卤素锂盐离子交换相比,有着成本低,排放物无污染,更适合工业化生产。
3 结论
(1)合成了前驱体α-NaMnO2,通过控制变量对比得出最优合成条件:n(Na2CO3)∶n(Mn2O3)=1.2∶1;700℃下碳粉还原保护煅烧24 h;纯净的α-NaMnO2制备需要无自由氧环境,同时保存需要干燥环境;
(2)通过优化实验条件,在180℃下n(LiOH·H2O)/n(α-NaMnO2)为5∶1水热10 h,水热-离子交换法合成了纯净m-LiMnO2;
(3)锂盐的选择对实验结果起关键作用,卤素锂盐不适用于高温高压水热-离子交换法;
(4)优化后的水热-离子交换法制备m-LiMnO2不仅较之蒸馏法效率高,产量大,且达到了成本最优化。
[1]AIFANTIS K E,HACKNEY S A,KUMAR R V.高能量密度锂离子电池:材料、工程及应用[M].赵铭姝,译.北京:机械工业出版社,2012:85-87.
[2]PAULSEN J M,DAHN J R.Studies of the layered manganese bronzes,with M=Co,Ni,Li,andprepared by ion-exchange[J].Solid State Ionics,1999(126):3-24.
[3]KIM D,KANG S H,BALASUBRAMANIAN M,et al.High-energy and high-power Li-rich nickel manganese oxide electrode materials [J].Electrochemistry Communications,2010(12):1618-1621.
[4]SHAJU K M,RAO G V S,CHOWDARI B V R.Performance of layered Li(Ni1/3Co1/3Mn1/3)O2as cathode for Li-ion batteries[J].Electrochem Commun,2002,4:633-634.
[5]SCROSATI B.Recent advances in lithium ion battery materials[J].Electrochim Acta,2000,45(15/16):2461-2466.
[6]ARMSTRONG A R,BRUCE P G.Synthesis of layered LiMnO2as an electrode for rechargeable lithium batteries[J].Nature,1996,381 (6582):499-500.
[7]赵世玺,李强.锂离子电池正极材料LiMnO2的结构稳定性及电化学过程中的相变[J].材料导报,2002,16(9):40-43.
[8]VELIKOKHATNYI O I,CHOI D,KUMTA P N.Effect of boron on the stability of monoclinic NaMnO2:Theoretical and experimental studies[J].Materials Science and Engineering B,2006(128):115-124.[9]FENG Q,KANOH H,OOI K.Manganese oxide porous crystals[J].J Mater Chem,1999,9:319-333.
[10]薛明明.单斜NaMnO2的结构表征及性质研究[D].长春:东北师范大学,2010:4-7.
Hydrothermal-ion exchange preparation of monoclinic layered LiMnO2and commercial optimization

Monoclinic layered LiMnO2,with unitary and relatively harsh synthetic conditions,therefore,the purpose was to reduce the complexity of synthetic and costing.NaMnO2as the research object,the high temperature solid state method to synthesize Mn2O3and anhydrous Na2CO3was used.The different concentration of sodium and manganese,calcination temperature,holding time,and the presence of carbon powder to protect the influence of different structure of α-NaMnO2were investigated.Moreover,the α-NaMnO2as the precursor to explore through hydrothermal-ion exchange process under different conditions for the monoclinic layered LiMnO2was studied,and optimized the hydrothermal-ion exchange method to good commercial process result in the effect was better than that of reflux distillation method.
high temperature solid state method;precursor;hydrothermal-ion exchange method;m-LiMnO2
TM 912
A
1002-087 X(2016)03-0507-03
2015-08-30
国家自然科学基金面上项目(61473267);国防技术基础科研基金(JSJC2013408C009)
郑宇亭(1990—),男,山西省人,硕士生,主要研究方向为层状锰酸锂的制备与掺杂改性。
潘保武,E-mail:pan_mail@nuc.edu.cn
