巧用平衡常数化解高中化学平衡疑难问题
2017-01-17邵斅农
邵斅农
摘 要: 化学平衡是高中新课标人教版化学选修④《化学反应原理》中非常重要的内容之一,也是近几年高考的热点,针对高考中涉及的许多化学平衡疑难问题,充分巧用好平衡常数这个重要工具,能大幅度提高解决化学平衡疑难问题的效率。
关键词: 平衡常数 化学平衡 疑难问题
近年来,化学平衡常数成为新课标地区高考命题的热点和难点,每年高考理综试卷中都对化学平衡常数进行了不同程度的考查,并且试题趋于综合性强、知识网络程度大、能力要求高,可见化学平衡常数是化学反应原理中非常重要的知识点之一,同时化学平衡常数是解决化学平衡疑难问题的一种重要有效手段和方法,如果对化学平衡常数这个解题工具能做到灵活利用,对解决高中化学平衡疑难问题就能起到事半功倍的效果。
一、利用化学平衡常数判断反应进行的程度问题
化学平衡常数值的大小可判断一个可逆反应进行的程度,一个可逆反应的化学平衡常数K值越大,正反应进行的程度越大,反应物的转化率越高;化学平衡常数K值越小,正反应进行的程度越小,反应物的转化率越低。
【典例】下列数据是一些反应的平衡常数,请判断:表示反应进行得最接近完全的是( )。
二、利用化学平衡常数判断反应的热效应问题
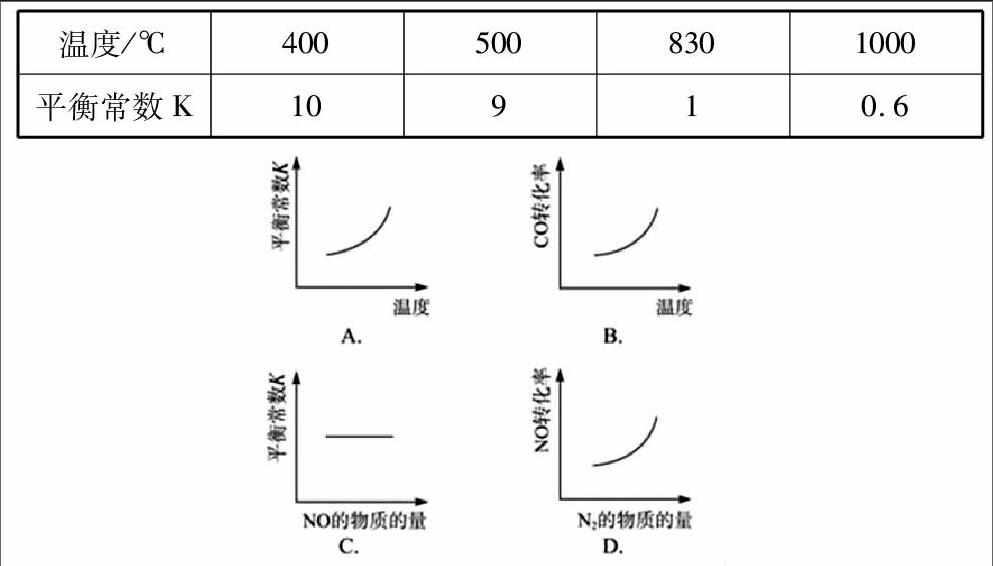
化学平衡常数K值只受温度影响,与浓度、压强和是否使用催化剂无关。若升高温度化学平衡常数增大,则正反应为吸热反应;若升高温度化学平衡常数减小,则正反应为放热反应;若降低温度化学平衡常数减小,则正反应为吸热反应;若降低温度化学平衡常数增大,则正反应为放热反应。
【解析】该反应正向为气体计量数减小的放热反应,温度升高平衡逆向移动,生成物浓度减小,反应物浓度增大,化学平衡常数减小,故A项错误;同理升高温度化学平衡常数减小,反应物一氧化碳的转化率减小,故B项错;化学平衡常数只与温度有关,与物质的量无关,故C对;增加氮气的物质的量平衡逆向移动,一氧化碳的转化率减小,故D项错误。
总之,巧用化学平衡常数能灵活解决化学平衡中的疑难问题,不仅降低学生学习化学平衡的抽象思维难度,有助于同学们理解化学平衡的实质,还能更有效地培养学生的化学思维能力。
参考文献:
[1]赵承志.化学平衡常数解决平衡疑难问题的一般思想.考试周刊,2015(62).
[2]史良君.化学平衡常数的灵活应用.中学化学,2010(4):30-33.
[3]高静.巧用化学平衡常数解决化学问题.考试与招生,2012(2).
[4]丁贺彬.浅谈高中化学平衡常数的巧应用.中学生数学理化:高二版,2011(9).
[5]杨湘庆.谈化学平衡常数的教学[J].天津教育,1981(03).
此文为甘肃省教育科学“十三五”规划课题“高中化学教学中‘疑难问题解决策略研究”(课题编号:GS[2016]GHB0070)成果之一。
