苏铁叶抗氧化剂的制备
2017-01-16宋照风赵海全
宋照风,赵海全
(佛山科学技术学院环境与化学工程学院化学工程系,广东 佛山 528000)
苏铁叶抗氧化剂的制备
宋照风,赵海全
(佛山科学技术学院环境与化学工程学院化学工程系,广东 佛山 528000)
研究了以苏铁叶为原料超声波提取苏铁叶抗氧化剂的工艺。以单因素实验为基础,进而进行正交实验来达到优化提取工艺的目的。实验得到最佳的提取条件为:浸提时间在10 h,液固比为14:1,超声时间为1.5 h。用从苏铁叶中提取的抗氧化剂进行实验可知:苏铁叶抗氧化剂能够比等浓度的抗坏血酸更好的清除自由基,并且随着苏铁叶抗氧化剂浓度的增加清除自由基的效果增强。
苏铁叶;超声波提取;提取工艺;抗氧化剂;正交实验
苏铁叶(Cycas revolute Thunb)又名铁树,常绿木本植物叶子,苏铁树高1~4 m[1]。铁树,常用做景观植物,不耐寒冷,在日常生活中也可用做入药。苏铁叶含有的化学成分主要是苏铁双黄酮(sotetsuflavone),扁柏双黄酮(hinokiflavone),穗花杉双黄酮(amentoflavone),2,3-二氢扁柏双黄酮(2,3-dihydrohinokiflavone),2,3-二氢穗花杉双黄酮(2,3-dihydroamentoflavone)等[2]。
铁树一般都会被认作是观赏类植物[3],但在中医方面,铁树可是极具药用价值的植物,苏铁叶在中医层面被广泛应用,但不单单是苏铁叶具有药用价值,根、花和种子同样具有优秀的药用价值[4]。苏铁在西南地区广泛种植,在缺少食物的情况下,苏铁也可用于入食充饥。中医一般用苏铁叶来治愈出血、胃炎、胃溃疡、高血压、神经痛、闭经、癌症等[5]。
苏铁树是被成为植物中的活化石,同时也是世界上最古老的裸子植物,目前也是主要在两广地区生长[6-7]。苏铁树的寿命很长,而且也是一年常青的。因此,在一年四季都能够采摘到苏铁叶。
抗氧化剂是消除和淬灭氧自由基,延缓自由基的特殊的一种抵抗氧化连锁反应的物质[8]。抗氧化剂是一种隔离氧气不良影响的一种物质,它是通过捕捉并中和自由基,从而去除自由基对人体的伤害[9]。抗氧化剂按照来源分一般分为天然抗氧化剂和人造抗氧化剂,天然抗氧化剂一般都来源于植物类,动物类的抗氧化剂相对少。天然抗氧化剂在疾病的治疗,化妆品,日用化学品和饲料中的运用较为广泛[10]。
抗氧化剂按溶解性可分为油溶性、水溶性和兼容性三类[11]。油溶性包括人工合成的抗坏血酸酯类、丁羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)等;水溶性包括抗坏血酸、异抗坏血酸及其盐类、苯多酚等。目前食品工业主要使用人工合成抗氧化剂BHA和TBHQ[12]。
抗氧化剂通过还原反应来降低食品内部及周围的氧含量,抗坏血酸和异抗坏血酸是非常好的抗氧化剂[13],因为它们本身对氧非常敏感,它们能够对非常快的对食物中的氧进行反应,从而降低氧对食物的破坏。抗氧化剂是通过释放出自身的氢原子来和氧原子反应,从而阻止氧化,同时也能降低氧化酶的活性,使其不能催化氧化反应[14]。将能催化及引起氧化反应的物质封闭,如络合能催化氧化反应的金属离子等[15]。通过科学家的研究发现,法国冠心类疾病的低发生率的原因就是他们喜欢喝红酒,因为在红酒里有一种叫做原花色素的多酚类化合物[16-17],这就是抗氧化剂的一种,可以帮助消除体内的氧原子及油脂。
由于提取抗氧化剂的原材料不同,抗氧化剂所存在的部位也不同,因此,就有多种不同的抗氧化剂提取方法。常用的有超声波辅助提取法、微波辅助提取法、酸碱提取法、酶解法等[18]。
本文所使用的方法则是超声辅助提取法。近年来越来越多植物有效成分的提取都会采用超声波技术,因为其具有成本低、安全、操作简单、无污染等一系列优点[19]。超声波产生的长时间强烈振动能够破坏细胞壁,去掉细胞壁的阻隔,从而让溶剂能直接渗入细胞内进行有效浸提抗氧化剂,加速了抗氧化剂提取的进程,减短实验所需要的时间,大大提高了抗氧化剂产率,是改善提取效果的一种新方法[20]。
1 实 验
1.1 实验材料和仪器
材料:苏铁叶,采集于学校荷花池边;无水乙醇(分析纯)、石油醚(分析纯)、抗坏血酸(分析纯)、乙酸乙酯(分析纯)、磷酸二氢钾(分析纯)、过硫酸钾(分析纯)、ABTS(分析纯)等,上海丰显化学股份有限公司。
仪器:722型可见光分光光度计;TKD-1006A型单槽式超声波清洗机;T500型电子天平;FA2004电子分析天平;D2KW-D-2型电热恒温水浴锅;101-1A型电热恒温干燥箱等。
1.2 工艺流程

图1 苏铁叶抗氧化剂的提取流程
1.3 实验步骤
1.3.1 处理苏铁叶
将新鲜摘下的苏铁叶剪下,并且清洗干净,将适量苏铁叶置于搅拌机中,开启搅拌机,将苏铁叶打烂至粉碎,将所有苏铁叶粉碎之后,将其置于60 ℃的烘箱之后,待其恒重时,即可得到干燥的原材料。
1.3.2 浸提及超声
取6.0 g干燥苏铁叶于烧杯中,加入16倍其质量数值的75%乙醇,浸提7 h。浸提结束之后,将烧杯置于50 ℃的超声机中,超声1 h,此过程中必须严格控制好温度,避免温度变化引起产品的纯度。超声结束后,将溶液倒入覆有滤纸的长颈漏斗中,静置过滤,取其滤液进行下部操作(滤液背光为深红色,透光为深绿色)。
1.3.3 除乙醇
将恒温水浴锅设置为75 ℃,将盛有滤液的烧杯置于恒温水浴锅中,并且将水浴锅置于通风橱下,这样可加快乙醇的挥发速度,将溶液浓缩至快干时,结束水浴,将其置于通风橱下晾干,结束除乙醇步骤。
1.3.4 萃取产物
往盛有干燥产物的烧杯中加入少量蒸馏水,搅拌使其成为悬浊液。量取20 mL石油醚对悬浊液进行萃取,去除萃取液,重复三次石油醚萃取。接着再量取20 mL乙酸乙酯,同样对悬浊液进行萃取3次,合并三次萃取液即可得含有抗氧化剂的萃取液(萃取液呈墨绿色,透明,且产量越高,颜色越深)。
1.3.5 浓缩干燥产物
将恒温水浴锅温度设置为75 ℃,并且置于通风橱下,将盛有萃取液的烧杯置于水浴锅中,浓缩产物。用电子分析天平称取一个干燥的25 mL坩埚,记录坩埚质量,待产物浓缩至很少时,将浓缩液转移到干燥坩埚中,小心将坩埚放进烘箱,将烘箱温度设为60 ℃对产物进行干燥。
1.3.6 取下产物
从烘箱之中取出干燥之后的坩埚,让坩埚降至常温,接着用分析天平称量坩埚即可知产物质量,接着用干燥的药勺从坩埚表面刮下产物,墨绿色产物即为苏铁叶抗氧化剂。
1.4 抗氧化剂的测定
1.4.1 ABTS+溶液的制备
取0.385 g ABTS试剂于50 mL容量瓶中,定容可得14 mM/L的ABTS溶液。
取0.06615 g过硫酸钾粉末与50 mL容量瓶中,定容可得4.9 mM/L的过硫酸钾溶液。
将5 mL,14 mM/L的ABTS溶液与5 mL,4.9 mM/L的过硫酸钾溶液混合,振荡摇匀,避光静置16 h后取出。
1.4.2 样品溶液的制备
由于最小样品溶液的浓度太低,无法从低到高逐级稀释,故在此用从高到低稀释的方法,每次稀释完都将移液管清洗干净,保证不对下个浓度产生影响。
取250 mg产品溶于无水乙醇中(产物不溶于水),定容至50 mL,用移液管取出25 mL于烧杯中,加入25 mL无水乙醇,摇匀,做上标记2。将从标记为2的烧杯中取出25 mL于25 mL无水乙醇混合摇匀,标记为3。以此类推直至标记为9为止。则溶液浓度分别为5 mg/L,2.5 mg/L,1.25 mg/L,0.62 mg/L,0.31 mg/L,0.15 mg/L,0.075 mg/L,0.037 mg/L,0.018 mg/L。1.4.3 工作液的制备
将25 mL,0.02 mol/L的磷酸二氢钾加入到100 mL的容量瓶中,再加入19.5 mL,0.02 mol/L的氢氧化钠溶液,最后定容,摇匀,即可得pH=7.4的5 mM/L磷酸盐缓冲液。
将避光静置16 h的ABTS+溶液取出倒入烧杯中,逐渐加入缓冲液,并且要测其吸光度,当在波长为734 nm下,吸光度为0.7时(偏差不过0.02),即可配成工作液。
1.4.4 样品的测定
取一滴1号样品溶液于试管中,用移液管加入5 mL工作液,静置5 min后测吸光度(Asample),依次处理至9号样品溶液,最后再取一滴无水乙醇于试管中,用移液管加入5 mL工作液,静置5 min,再测量其吸光度(Acontrol),作为标准液。
同样方法处理抗坏血酸,得到标准对照组(表2)。
1.4.5 半数抑制率的计算
半数抑制率是指在清除率为50%时所消耗的抗氧化剂的浓度,可见公式如下:
清除率=[(Acontrol-Asample)/Acontrol]×100%
1.4.6 抗氧化剂的测定结果
样品的吸光度如表1所示。

表1 浓度-清除率对应表
续表1

06207711977031078618210150907561007509352700037094021900180953083
无水乙醇Acontrol的吸光度为0.961。
由表1可得出:当清除率为50%时,半数抑制率IC50=1.50 mg/mL。
抗坏血酸的吸光度如表2所示。
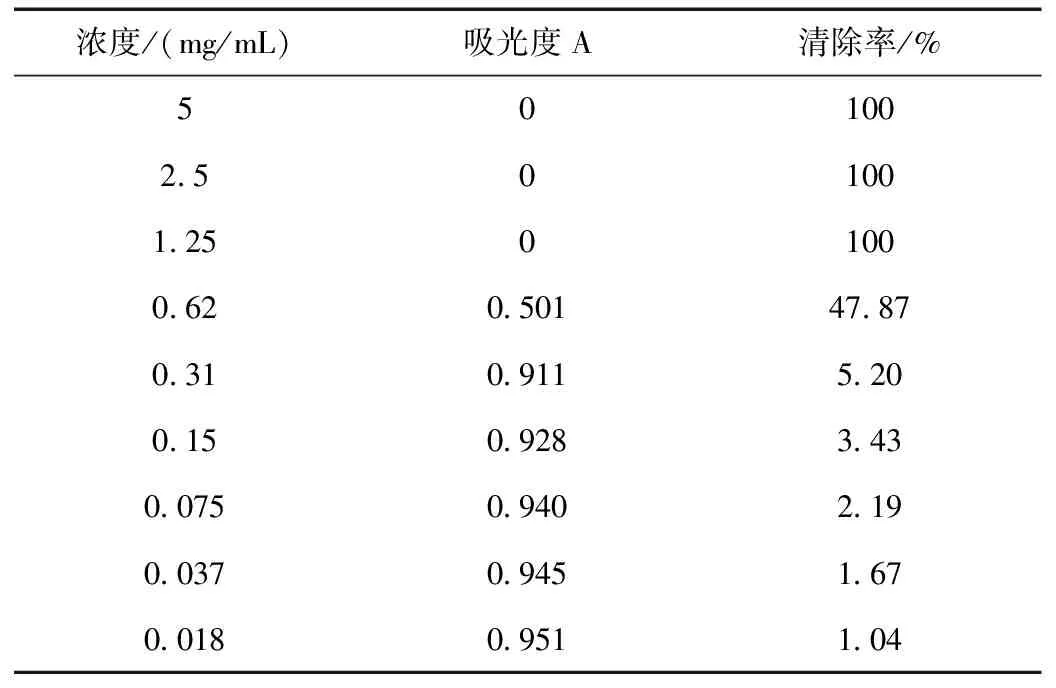
表2 抗坏血酸清除率对应表
由表2可得出:当清除率为50%时,IC50=0.64 mg/mL。
苏铁叶抗氧化剂对比结果如表3所示。

表3 苏铁叶抗氧化剂对比表
由表3可知,苏铁叶抗氧化剂的清除自由基能力比抗坏血酸还要好,具有较强的抗氧化能力,能够很好地清除ABTS自由基。
2 结果与讨论
2.1 单因素实验
2.1.1 超声时间对提取抗氧化剂的关系研究
准确称量8.0 g干燥苏铁叶于烧杯中,准确称量5份,将统一配置好的75%乙醇倒入100 mL,浸提8 h,浸提结束后,将烧杯放入超声机中,温度设为50 ℃,将超声时间控制为0.5 h、1 h、1.5 h、2 h、2.5 h,分别再进行下面的操作之后,得出以下的实验结果。

表4 超声时间与产量关系表

图2 超声时间与产量的关系研究
由图2可知,在超声时间为1 h以内时,产量相对较少,但是在1 h之后,产量有明显上升趋势,并且在2 h时,可得到最大产量,而超过2 h之后,产量又呈下降趋势。超声可使原材料中的抗氧化剂通过物理作用振荡出来,但是超过一定限度之后就会形成反效果,会使产量减少。因此,选择1 h,1.5 h,2 h,2.5 h进行正交试验。
2.1.2 浸提时液固比对产量的关系研究
准确称量6.0 g干燥苏铁叶于烧杯中,准确称量5份,配置好75%乙醇,分别倒入乙醇体积为苏铁叶质量的14倍,16倍,18倍,20倍,22倍,浸提8 h,浸提结束后,将烧杯放入超声机中,温度设为50 ℃,超声1 h,分别再进行下面的操作之后,得出实验结果见表5。

表5 液固比对产量的关系研究表

图3 液固比对产量的关系研究
由图3可知,当加入的乙醇体积是苏铁叶质量的20倍时,可得到最大产量,在20倍之前都呈上升趋势,随着乙醇量的增加而增加,而在20倍时达到饱和,故增加一定量的乙醇可使产量增加。因此,选择乙醇体积为苏铁叶质量的16倍,18倍,20倍,22倍进行正交实验。
2.1.3 浸提时间对产量的关系研究
准确称量6.0 g干燥苏铁叶于烧杯中,准确称量5份,将统一配置好的75%乙醇倒入100 mL,分别浸提8 h,9 h,10 h,11 h,12 h,浸提结束后,将烧杯放入超声机中,温度设为50 ℃,超声1 h,分别再进行下面的操作之后,得出实验结果见表6。

表6 浸提时间与产量的关系研究表

图4 浸提时间与产量的关系研究
由图4可知,产量随浸提时间的增加而增加,在在浸提11 h后,长时间的浸提效果不明显,故饱和值可判定在11 h处。因此,取浸提时间分别为9 h,10 h,11 h,12 h来进行正交试验。
2.2 正交试验优化苏铁叶抗氧化剂提取条件
已通过单因素实验得到一系列有效数据,可以用产量来判断优化结果,本文选择用浸提时间,液固比(75%乙醇的体积与苏铁叶的质量比),超声提取时间三个因素来进行考察,每个因素设三个水平,选择L16(34)正交表,正交实验设计如表7~表9所示。
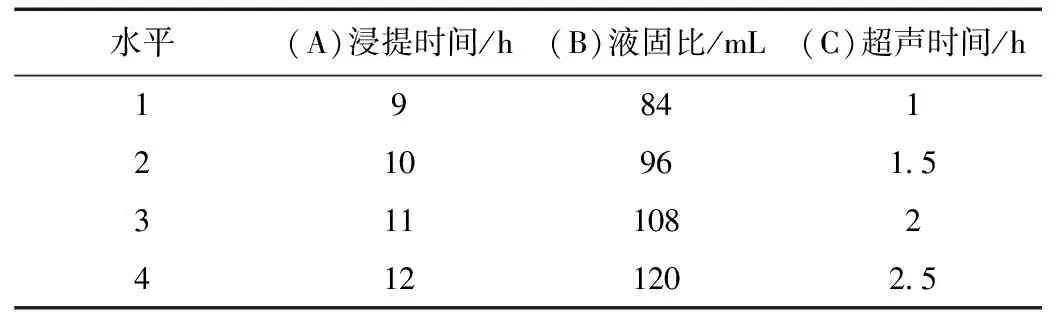
表7 正交实验设计表

表8 正交实验结果
续表8

313319341441865212237622117672341718243145931317710324171113311721234219713414200144231761543221616441187均值1184192167均值2199184221均值3179188180均值4195191187极差R430854
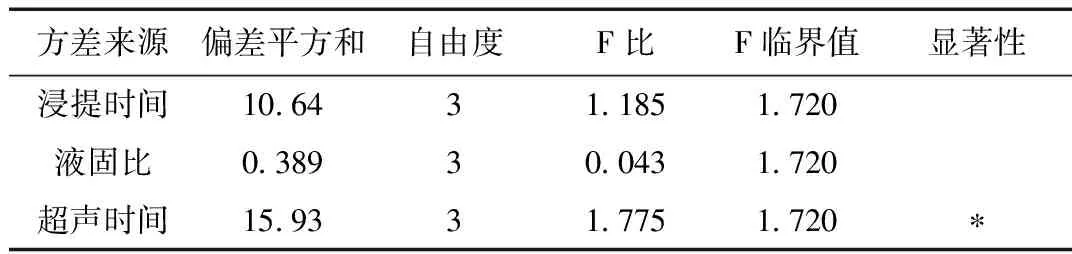
表9 方差分析
根据表8中的极差可以看出各因素对苏铁叶提取抗氧化剂的影响程度是不一样的,极差越大,影响越大,其因素影响次序为C(超声时间)>A(浸提时间)>B(液固比)。表9的方差分析表明,在A,B,C三个因素中,C的影响效果较为明显,有显著性,也就是超声时间对抗氧化剂的提取的影响较大,充分震荡能够使抗氧化剂更加彻底的脱离苏铁叶,使得产品产率更高。试验得出最佳水平为A2B1C2,也就是浸提时间在10 h,液固比为14:1,超声时间为1.5 h时,可得到最高产量。
3 结 论
本文采用了超声辅助提取苏铁叶抗氧化剂的工艺,经过单因素和正交试验的方法,确定了提取苏铁叶抗氧化剂工艺的最佳条件,即浸提时间在10 h,液固比为14:1,超声时间为1.5 h,最大提取率为0.4%。
从影响提取率的因素来看,并不是液固比越高,超声时间越长,抗氧化剂的提取率就会越高。当浸提时间到达一定时,在浸提下去不会有更多的产物生成,会浪费制取时间,使得成本增加。而液固比要控制在一定范围内才好,盲目的增加乙醇体积会造成一定的浪费,也会使得成本上升,超声时间在1.5 h时,就会达到饱和。
[1] 李艳彩,王俊河.苏铁叶片变黄原因及防治措施[J].中国花卉园艺,2008(12):85-86.
[2] 杨春光,高松.扁担杆正丁醇提取物抗炎作用及机制研究[J].辽宁师范大学学报:自然科学版,2013,36(4):539-542.
[3] 梁湘沅.苏铁类植物复原随笔[J].化石,1988,3:73-76.
[4] 农保选.中国苏铁科部分种类的RAPD分析及其亲缘关系的研究[M].广西大学出版社,2013:125-130.
[5] 刘世彪,彭小列,吕江明,等.苏铁种子的营养成分及急性毒性实验[J].营养学报,2010,32(5): 510-512.
[6] 高锦鹏.浅谈银杏树的药用价值[J].今日湖北:中旬刊,2013(7):71-75.
[7] 吴棣飞,潘海波.神奇铁树开14朵花[M].中国花卉盆景,2009(10):115-118.
[8] 尼加提.王苏甫.简论抗氧化剂的性能及其应用[J]. 和田师范专科学校学报:汉文综合版,2008,28(4):222-223.
[9] 李小刚.抗氧化剂的临床应用现状[R].中国卒中杂志,2010,5(2):33-35.
[10]赵永杰,张静.抗氧化剂在个人护理品中的研究进展[J].日用化学品科学,2008, 31(3):66-70.
[11]黄起鹏,赵绪妙.食品抗氧剂的现状和发展趋势[J].广州食品工业科技,1992(2):80-81.
[12]朱将伟.天然抗氧化剂的研究概况[M]. 饲料工业,2007,24:100-102.
[13]孙文敬,谢红,高润香.食品抗氧化剂-D-异抗坏血酸的生产工艺研究[J].食品科学,1999(04):50-53.
[14]戚凤奎,尹荣兰,尹荣焕,等.喹乙醇对小鼠血清抗氧化酶系活性的影响[J].中国农学通报,2011,27(11):43-45.
[15]李凤林,黄聪亮,余蕾.食品添加剂[J].北京:化学工业出版社,2008:25-28.
[16]马文帅,王海昌.白藜芦醇对心肌微血管内皮细胞缺血再灌注损伤的保护作用[J].中华老年心脑血管病杂志, 2009,11(7):88-90.
[17]赵永杰,张静.抗氧化剂在个人护理品中的研究进展[J].日用化学品科学,2008, 31(3):25-29.
[18]Júnior Dario,Krug Francisco. Currents on Ultrasound-Assisted Extraction for Sample Preparation and Spectroscopic Analytes Determination.Applied Spectroscopy Reviews, 2006, 41(3): 305-321.[19]聂少平,谢明勇,罗珍.微波技术提取茶多糖的研究[J].食品科学,2005,26(11)B:103-106.
[20]郭孝武.超声提取及其应用[M].西安:陕西师范大学出版社,2003:51-53.
Study on Preparation of Cycas Leaf Antioxidant and Performance
SONGZhao-feng,ZHAOHai-quan
(Department of Chemical Engineering, School of Environment and Chemical Engineering,Foshan University, Guangdong Foshan 528000, China)
Taking Cycas revolute Thunb as raw material, antioxidant from Cycas revolute Thunb was extracted by ultrasonic wave. Based on a single factor in the experiment, the orthogonal experiment was studied to achieve the purpose of optimizing the extraction process. The best extraction conditions were as follows: extraction time was 10 h, the solid-liquid ratio was 14:1, ultrasonic time was 1.5 h. The study showed that the antioxidants from Cycas revolute Thunb had better scavenging free radicals than identical concentration of vitamin C, and the free radical scavenging effect was enhanced with the increase of the concentration of Cycas revolute Thunb antioxidant.
Cycas revolute Thunb; ultrasonic extraction; extraction process; antioxidants; orthogonal
宋照风(1984-),女,实验师,主要从事实验室工作,研究方向为天然产物的制备和应用。
Q946.3
A
1001-9677(2016)023-0066-05
