德氏乳杆菌吸附铅离子的机制研究
2017-01-13于上富丁秀云窦明理霍贵成
于上富,靳 妲,丁秀云,窦明理,霍贵成,*
(1.东北农业大学食品学院,乳品科学教育部重点实验室,黑龙江哈尔滨 150030;2.四川省食品药品检验检测院,四川成都 611731)
德氏乳杆菌吸附铅离子的机制研究
于上富1,靳 妲1,丁秀云1,窦明理2,霍贵成1,*
(1.东北农业大学食品学院,乳品科学教育部重点实验室,黑龙江哈尔滨 150030;2.四川省食品药品检验检测院,四川成都 611731)
该研究以具有较高去除铅离子能力的德氏乳杆菌(Lactobacillusdelbrueckii)KLDS1.0207为研究对象,利用热力学模型及动力学模型对LactobacillusdelbrueckiiKLDS1.0207结合铅离子的过程进行模拟分析,同时结合扫描电镜-能谱及傅里叶红外光谱对其结合铅离子的状态进行分析,最后得出,Langmuir-Freundlich模型比Langmuir模型和Freundlich模型更适合其结合铅离子的过程,R2达0.9820,准二级动力学模型的R2为0.9916,比准一级动力学模型更适合,说明该菌与铅的作用的机制为化学吸附,而不是物理吸附。由扫描电镜和能谱分析可以看出菌体表面不完全分布着铅的颗粒,推断出参与吸附过程中其主要作用的是含C、O的基团和傅里叶红外光谱,可以推测出参与铅离子结合的基团有羧基、氨基、酰胺基、羟基,推测菌与铅的作用机制可能为化学吸附、离子交换、化学沉淀等的共同作用的结果。
乳酸菌,热力学模型,动力学模型,铅离子
近年来,重金属污染问题日益严重。许多金属加工厂、矿井、电池厂、化工厂、染料厂等向环境中排出一定量的重金属,以及汽车尾气、燃煤向空气中排放,同时我国绝大数城市存在着水污染的问题,未经处理的城市垃圾、工业废水和生活污水以及大气污染物不断沉降到水体中,使水中重金属含量升高。在我国,每年释放到环境中铅的量约为3.5万吨[1]。2004年太湖底泥中铜、铅、镉的含量均处于轻度污染水平。黄浦江干流表层沉积物中镉含量超标2倍,铅含量超1倍、汞含量明显增加。重金属进入环境后,可能被植物或者水生动物吸收,通过食物链富集,进而损害人体健康[2]。20世纪40年代,美国人均摄入的铅含量大约在400~500 μg/d,由于认识到铅的毒性,经过不断改进,现在下降为不大于20 μg/d。美国环境保护组织限定饮用水中铅含量<0.015 mg/L,污水处理后铅含量<0.1 mg/L。常见的处理重金属的方法有反向渗透、离子交换、化学沉淀、生物吸附四大类[3]。生物吸附有投资小、环境破坏小、操作简单等优点,对于低浓度的重金属污染处理有较好适用性。研究表明许多微生物能去除重金属,如屎肠球菌[4]、鼠李糖乳杆菌[5]、植物乳杆菌[6-8],枯草芽孢杆菌[9]、酿酒酵母[10]、假单胞杆菌[11]等。研究结果表明乳酸菌确实能在体外吸附重金属,且这种吸附能力具有菌株特异性,其中乳酸菌的应用已有很长历史,其许多益生功能,如降胆固醇、抗癌、治疗结肠癌、提高免疫力、预防心血管疾病等也已经被证实。乳酸菌体外可以去除重金属,体内具有益生功能,可以将乳酸菌应用于暴露于重金属下动物的研究。但是,对于乳酸菌吸附重金属的机理目前没有统一定论,大致有四个理论,离子交换、物理沉降、基团吸附、膜渗透。
本研究对实验室筛选的具有高去除铅离子能力的德式乳杆菌进行吸附模型的研究,旨在揭示德氏乳杆菌与重金属离子的结合机理,为以后筛选及改良乳杆菌螯合重金属提供理论依据。
1 材料与方法
1.1 材料与仪器
德氏乳杆菌(Lactobacillusdelbrueckii)KLDS1.0207 由东北农业大学教育部重点实验室工业微生物菌种保藏中心提供;酵母粉 XOID公司;蛋白胨、胰蛋白胨、牛肉膏、氯化钠、氢氧化钠 奥博星生物技术公司;硝酸、硝酸铅 国药集团化学试剂有限公司;铅标准品(色谱纯) 德国默克集团有限公司。
900H原子吸收光谱仪 美国PERKINELMER公司;GL-21M高速冷冻离心机 上海市离心机械研究所;HVE-50灭菌锅 日本HIRAYAMA公司;S-3400N扫描电子显微镜 日本日立公司;能谱QuantaFEG250 美国康塔公司;红外仪器型号TENSOR27spectrometer 德国布鲁克公司。
1.2 实验方法
1.2.1 菌的培养 将保存于冻存管中的菌液按2%的比例接种于液体MRS培养基中,于37 ℃培养箱中培养24 h重复两代以提高菌株的活性。
1.2.2 菌体的收集 按照文献[12]中的方法收集菌体。
1.2.3 金属溶液制备 称取不同量的硝酸铅溶于超纯水中配制为10、20、30、40、50、60、70、80、90、100 mg/L浓度的铅离子溶液,用灭菌的0.5 mol/L的HNO3和NaOH将其pH调为6。
1.2.4 吸附实验 将收集到的菌体分别置于1.2.3中的不同铅离子浓度溶液中,使菌体浓度达到4 g/L(湿菌体重),37 ℃条件下振荡孵育4 h直至吸附平衡,随后8000×g离心10 min,取上清液用原子吸收测量铅离子浓度,菌体对铅离子的吸附量按下述公式计算:
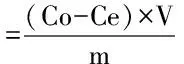
其中,Co为初始铅离子浓度,Ce为平衡液中铅离子浓度,V铅离子溶液的体积,m湿菌体的质量,V/m=4 L/g。
1.2.5 动力学实验 将培养得到的乳酸菌,8000×g离心10 min,用灭菌的超纯水清洗两次,同样条件下离心,将菌体置于14个同样体积的50 mg/L铅离子溶液中,使菌体浓度达到4 g/L(湿菌体重),37 ℃条件下振荡孵育,分别在5、10、15、20、25、30、40、50、60、90、120、150、180、240 min[12]时间点,取样品进行8000×g离心10 min,测定上清的铅离子浓度。菌体对铅离子的吸附量按下述公式计算:
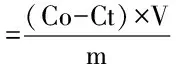
其中,Ct为t时间后溶液中铅离子浓度,其他同1.2.4。
1.2.6 扫描电镜观察 取不含铅离子溶液的菌体和含50 mg/L铅离子吸附后的菌体,于8000×g条件下离心20 min,再用灭菌的超纯水冲洗三次后,同上条件离心,随后立即倒入戊二醛固定1.5 h,用磷酸缓冲液冲洗3次,然后置于6000×g条件下离心10 min,再分别用不同浓度(50%、70%、90%、100%)的乙醇脱水一次,后6000×g条件下离心10 min,再用乙醇和叔丁醇混合液(1∶1)以及纯叔丁醇洗脱一次,后6000×g条件下离心10 min,将菌体放入-20 ℃下冷冻30 min,放入冷冻干燥仪中干燥4 h,最后用离子溅射镀膜仪在样品表面镀一层厚100~150 A的金属膜,放入观察室进行观察。
1.2.7 傅里叶红外光谱测定 不含铅离子溶液的菌体和含50 mg/L铅离子吸附后的菌体,于8000×g条件下离心20 min,超纯水冲洗三次后,同样条件离心,置于70 ℃条件下的烘箱中,烘干至恒重,取干燥的细胞于研钵中与KBr粉末1∶5比例混合研磨,随后压片观察。
1.3 数据处理
数据处理采用“平均值+标准差”表示,利用SPSS 19.0和Origin 9.0软件对数据进行处理[13]。
2 结果与分析
2.1 热力学分析
2.1.1 Langmuir模型分析 该模型假设吸附剂表面的吸附位点是均匀的,金属吸附于表面单分子层,每个吸附位点对应一个金属离子,是以化学吸附为主的,吸附和解吸是动态平衡[14]。Langmuir模型的公式[15]如下:
式中,qe为平衡时菌体吸附的量,qm为最大的吸附量,Ce为平衡是溶液中铅离子浓度,b(L/mg)为吸附系数,表示吸附的强度,其值的大小与吸附质的本性和温度有关,值越大则吸附能力越强。
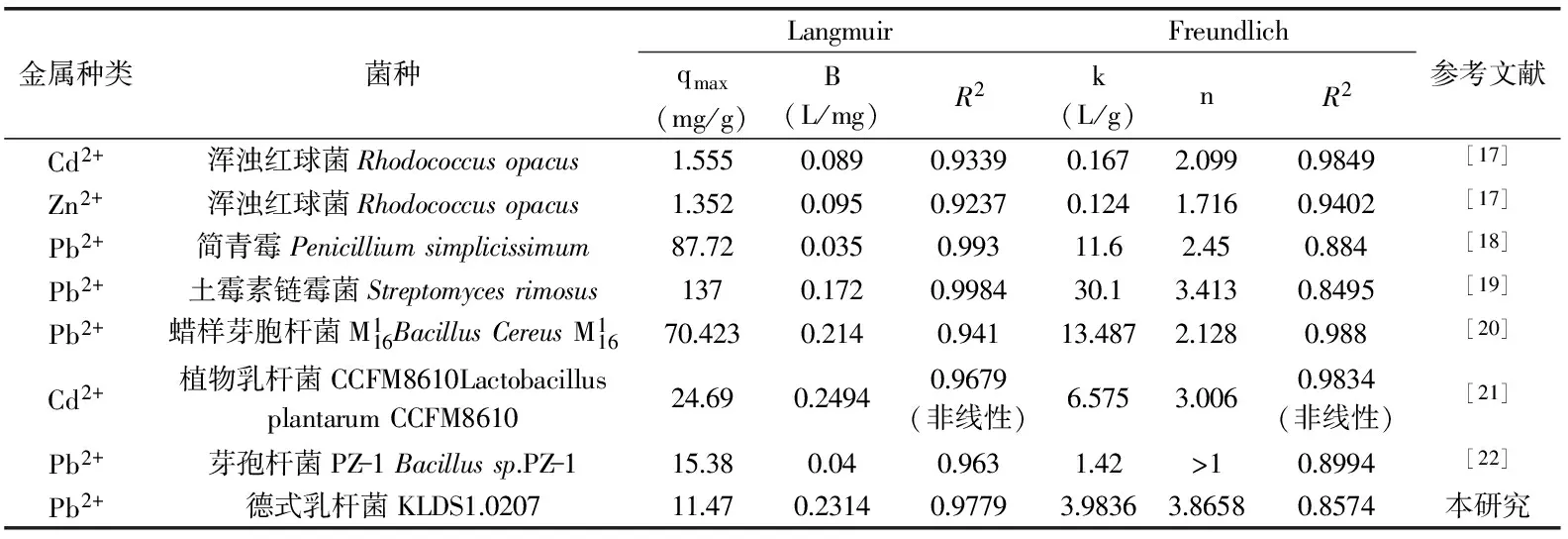
表1 Langmuir和Freundlich模型的吸附参数
模拟的结果见图1,qmax为11.47 mg/g,b为0.2314,R2为0.9779,且拟合结果11.47 mg/g和实际值10.60 mg/g相差不大。
2.1.2 Freundlich模型分析 该模型假设的是吸附发生在非均匀介质表面,Freundlich模型公式[16]如下:
其中,qe为平衡时菌体吸附的量,Ce为平衡时溶液中铅离子浓度,k为吸附平衡常数,其值的大小表示浓度对吸附量影响的强弱,越小表示吸附性能越好。
拟合结果见图2,k为3.9836,n为3.8658,R2为0.8574。表1详细罗列了其他几种微生物吸附金属离子的模拟参数及其最大吸附量。可以看出本研究的Langmuir模拟的拟合相关系数是比较好的。
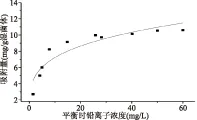
图2 德氏乳杆菌KLDS1.0207吸附铅离子的Freundlich模型分析Fig.2 Freundlich isotherm model study on Pb2+ biosorption by Lactobacillus delbrueckii KLDS1.0207
2.1.3 Langmuir-Freundlich模型分析 Langmuir-Freundlich公式[23]如下:
式中,qe为平衡时菌体吸附的量,k(L/g)为吸附平衡常数,b为一个不均匀的参数。
该模型的结果见图3,k为1.9337,a为0.1778,b为1.250,R2为0.9820,b代表菌体吸附不均匀的参数,若理想下表面均匀吸附时,b为1;大于1,代表菌体吸附不均匀[24],吸附过程可能涉及物理吸附和离子交换过程。
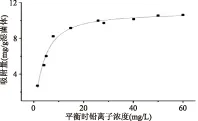
图3 德氏乳杆菌KLDS1.0207吸附铅离子的Langmuir-Freundlich模型分析Fig.3 Langmuir-Freundlich isotherm model study on Pb2+ biosorption by Lactobacillus delbrueckii KLDS1.0207
2.2 动力学模型分析
2.2.1 吸附实验结果 不同时间下的吸附量见表2。
2.2.2 准一级动力学模型分析 准一级动力学模型的公式[25-26]如下:
式中,qt为t时刻是菌体吸附金属的量,将其变形为线性形式如下:
一般情况下该模型适合吸附过程的前30~50 min,而不适合整个吸附过程[25],本实验结果图4显示,前14 min的拟合相关系数R2达0.9666,同样说明在前期短时间内,铅离子快速吸附在细胞表面,但随时间的延长,发生的不仅有物理吸附,可能还存在铅离子往细胞内部迁移、化学沉淀等现象。

图4 准一动力学模型线性分析Fig.4 Study of pseudo first-order reaction model
2.2.3 准二级动力学模型分析 准二级动力学模型[27]的线性公式为:
将其形式变为线性形式如下
以t/qt为纵坐标,以t为横坐标做线性拟合,可以求出k2。该模型是假设化学吸附的过程。实验结果图5如下,得出R2为0.9916,说明菌体吸附铅离子的过程不是单纯的物理吸附,存在其他的离子交换、化学沉淀等现象。
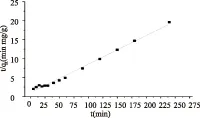
图5 准二级动力学模型线性分析Fig.5 Study of pseudo second-order reaction model
2.3 菌体结合铅离子的扫描电镜观察
从扫描电镜图6可以看出,空白组菌体表面无亮点,表面光滑,铅吸附组是表面多亮点,不规则的分散在细胞表面,并没有全部覆盖,推测是铅形成的颗粒,经过EDS能谱分析图7及表3的定量分析,可以得出亮点确实为含铅的颗粒,主要组成为C、O、K、Pb,说明铅主要与菌体细胞表面的含C、O键的物质结合。

图6 德氏乳杆菌KLDS1.0207吸附铅离子的扫描电镜观察(5000×)Fig.6 Scanning electron micrographs of Lactobacillus delbrueckii KLDS1.0207(5000×)注:a为空白对照组;b为50 mg/L铅吸附组。

图7 德氏乳杆菌KLDS1.0207吸附铅的能谱分析Fig.7 EDS analysis of Lactobacillus delbrueckii KLDS1.0207注:对图6中的菌体表面的亮点进行元素分析。
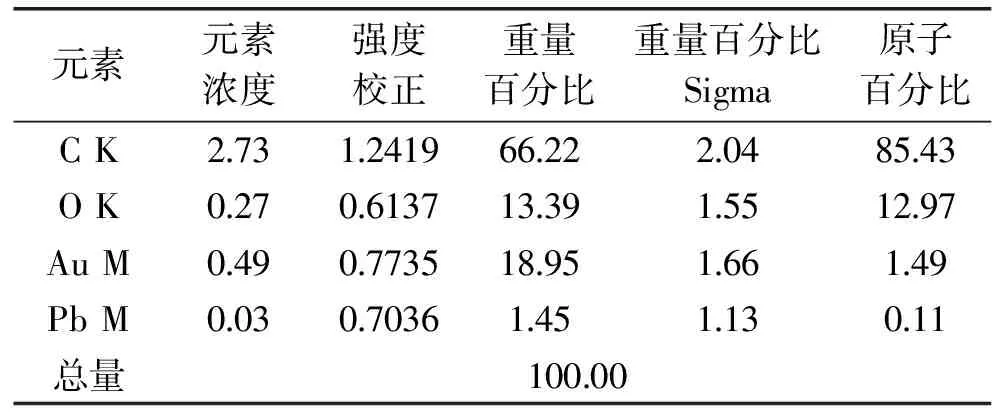
元素元素浓度强度校正重量百分比重量百分比Sigma原子百分比CK2731241966222048543OK0270613713391551297AuM049077351895166149PbM00307036145113011总量10000
2.4 红外光谱分析
微生物的红外光谱通常因为细胞壁成分的不同而主要分为以下5个区域。3000~2800 cm-1:细胞膜的脂肪酸;1800~1500 cm-1:蛋白质和多肽的酰胺;1500~1200 cm-1:蛋白质和脂肪酸;1200~900 cm-1:细胞壁中的多糖;900~500 cm-1为未知的特殊官能团区域[28]。
由图8可看出,大部分活性基团的吸收强度增大,表明菌体对铅的积累能力增强,主要有以下峰值:3500~3200 cm-1有宽的吸收峰处,强度增强,可能为酰胺N-H的伸缩振动,醇酚类分子间OH键的伸缩的振动;3000~2500 cm-1处羧酸的OH伸缩振动;1720~1700 cm-1羧酸的C=O的吸收1650 cm-1和1550 cm-1分别为蛋白质酰胺Ⅰ带的C-O的伸展振动和酰胺Ⅱ带中N-H弯曲振动和 C-H伸展振动的叠加1465~1440 cm-1肽链中C-H的弯曲振动;1400~1410 cm-1为酰胺Ⅱ带的-CN伸缩振动和-NH的面弯曲振动,也可能为肽链末端羧基-C=O的对称伸缩振动;1250~1200 cm-1为脂4类和多糖P=O的伸缩振动峰,也可能为C-O与O-H的叠加吸收峰,或羧酸的C-O的伸缩振动,处理后消失,推测参与吸附铅;1200~1150 cm-1多聚糖中的C-O的伸缩振动,吸附后消失,推测参与了吸附过程。
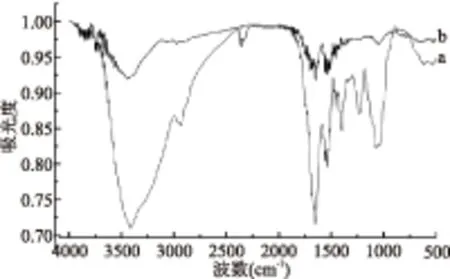
图8 德氏乳杆菌KLDS1.0207的傅里叶红外光谱图Fig.8 FTIR spectra of Lactobacillus delbrueckii KLDS1.0207注:a为空白组,b为与铅离子作用后的图。
这些组成中可与金属离子相结合的主要官能团有羧基、磷酰基、羟基、氨基和酰胺基等,其中氮、氧、磷、硫作为配位原子与金属离子配位络合。从红外光谱分析可以推测乳酸菌与铅结合的机制包括络合反应、离子交换、物理吸附(静电引力),作用官能团包括羟基、羧基、磷酸基、酰胺基、烃基,作用大分子生物包括脂肪酸、多糖、S层蛋白、磷壁酸等。该推测结果和Naik、金羽、Ren等提出的铅离子可以羧基、羟基、酰胺基等相互作用结论[22,29-30]一致。
3 结论
乳酸菌有许多功能特性,广泛应用在食品中,乳酸菌去除重金属特性也受到越来越多学者的研究,本实验对筛选的较高去除铅离子能力的LactobacillusdelbrueckiiKLDS1.0207进行研究,扫描电镜结果显示,该铅离子浓度下菌体状态没有出现裂解,表面完整,与空白组相比没有明显的不同,对菌表面的结晶进行能谱分析显示主要含C、O的基团参与铅的结合。通过热力学模型和动力学模型模拟菌体吸附铅离子的实验,可以得出Langmuir-Freundlich模型比Langmuir模型和Freundlich模型更适合乳酸菌吸附铅离子,准二级动力学模型能较好的模拟该吸附过程,结合扫描电镜及红外光谱分析可以得出,乳酸菌结合铅离子不仅仅是单纯物理吸附,可能还涉及离子交换、化学吸附、化学沉淀等。
[1]谢志宜,陈能场. 微胶囊EDTA对2种土壤中铅释放的影响[J]. 生态环境学报,2012,21(6):1131-1137.
[2]王家强.生物吸附法去除重金属的研究[D].长沙:湖南大学,2010.
[3]Amirnia S. Biosorption Processes for Removal of Toxic Metals from Wastewaters[D]. The University of Western Ontario,2015.
[4]Topcu A,Bulat T. Removal of cadmium and lead from aqueous solution by Enterococcus faecium strains[J]. J Food Sci,2010,75(1):T13-T17.
[5]Ibrahim F,Halttunen T,Tahvonen R,et al. Probiotic bacteria as potential detoxification tools:assessing their heavy metal binding isotherms[J]. Canadian Journal of Microbiology,2006,52(9):877-885.
[6]Tian F,Zhai Q,Zhao J,et al. Lactobacillus plantarum CCFM8661 Alleviates Lead Toxicity in Mice[J]. Biological Trace Element Research,2012,150(1-3):264-271.
[7]Zhai Q,Wang G,Zhao J,et al. Protective Effects of Lactobacillus plantarum CCFM8610 against Acute Cadmium Toxicity in Mice[J]. Applied and Environmental Microbiology,2013,79(5):1508-1515.
[8]Zhai Q,Wang G,Zhao J,et al. Protective Effects of Lactobacillus plantarum CCFM8610 against Chronic Cadmium Toxicity in Mice Indicate Routes of Protection besides Intestinal Sequestration[J]. Applied and Environmental Microbiology,2014,80(13):4063-4071.
[9]Chen Z,Pan X,Chen H,et al. Biomineralization of Pb(II)into Pb-hydroxyapatite induced by Bacillus cereus 12-2 isolated from Lead-Zinc mine tailings[J]. Journal of Hazardous Materials,2016,301:531-537.
[10]Farhan S N,Khadom A A. Biosorption of heavy metals from aqueous solutions by Saccharomyces Cerevisiae[J]. International Journal of Industrial Chemistry,2015,6(2):119-130.
[11]Hussein H,Ibrahim S F,Kandeel K,et al. Biosorption of heavy metals from waste water usingPseudomonassp.[J]. Electronic Journal of Biotechnology,2015,6(2):119-130.
[12]于上富,徐敏,丁秀云,等. 一株乳酸菌吸附Pb2+的条件优化[J].中国酿造,2016,35(2):109-114.
[13]余建英,何旭宏. 数据统计分析与 SPSS 应用[M]. 人民邮电出版社,2003:4.
[14]Mishra V,Balomajumder C,Agarwal V K. Biological removal of heavy metal zinc from industrial effluent by Zinc sequestering bacterium VMSDCM[J]. Clean Technologies and Environmental Policy,2014,16(3):555-568.
[15]Liu Y,Liu Y. Biosorption isotherms,kinetics and thermodynamics[J]. Separation and Purification Technology,2008,61(3):229-242.
[16]Vijayaraghavan K,Padmesh T,Palanivelu K,et al.
Biosorption of nickel(II)ions onto Sargassum wightii:Application of two-parameter and three-parameter isotherm models[J]. Journal of Hazardous Materials,2006,133(1-3):304-308.
[17]Vásquez T G P,Botero A E C,de Mesquita L M S,et al. Biosorptive removal of Cd and Zn from liquid streams with a Rhodococcus opacus strain[J]. Minerals Engineering,2007,20(9):939-944.
[18]Fan T,Liu Y,Feng B,et al. Biosorption of cadmium(II),zinc(II)and lead(II)by Penicillium simplicissimum:Isotherms,kinetics and thermodynamics[J]. Journal of Hazardous Materials,2008,160(2-3):655-661.
[19]Selatnia A,Boukazoula A,Kechid N,et al. Biosorption of lead(II)from aqueous solution by a bacterial dead Streptomyces rimosus biomass[J]. Biochemical Engineering Journal,2004,19(2):127-135.
[20]Lalitagauri R,Subham P,Debabrata B,et al. Bioaccumulation of Pb(II)from aqueous solutions by Bacillus cereus M16[J]. J Hazard Subst Res,2000,5:516-529.
[21]翟齐啸.乳酸菌减除镉危害的作用及机制研究[D]. 无锡:江南大学,2015.
[22]Ren G,Jin Y,Zhang C,et al. Characteristics ofBacillussp. PZ-1 and its biosorption to Pb(II)[J]. Ecotoxicology and Environmental Safety,2015,117:141-148.
[23]Nahm M H,Herzenberg L A,Little K,et al. A new method of applying the Sips equation[J]. The Journal of Immunology,1977,119(1):301-305.
[24]Umpleby R J,Baxter S C,Chen Y,et al. Characterization of Molecularly Imprinted Polymers with the Langmuir-Freundlich Isotherm[J]. Analytical Chemistry,2001,73(19):4584-4591.
[25]Aksu Z. Equilibrium and kinetic modelling of cadmium(II)biosorption by C. vulgaris in a batch system:effect of temperature[J]. Separation and Purification Technology,2001,21(3):285-294.
[26]Lagergren S. About the theory of so-called adsorption of soluble substances[J]. 1898,4(24):1-39.
[27]Ho Y. Second-order kinetic model for the sorption of cadmium onto tree fern:A comparison of linear and non-linear methods[J]. Water Research,2006,40(1):119-125.
[28]倪奕弘.耐受重金属铜的乳酸菌的筛选及其铜结合性能的研究[D]. 广州:暨南大学,2014.
[29]Naik M M,Pandey A,Dubey S K. Biological characterization of lead-enhanced exopolysaccharide produced by a lead resistant Enterobacter cloacae strain P2B[J]. Biodegradation,2012,23(5):775-783.
[30]金羽,曲娟娟,李影,等. 一株耐铅细菌的分离鉴定及其吸附特性研究[J]. 环境科学学报,2013,33(8):2248-2255.
Study on the mechanism of adsorption of lead ions biosorption by lactic acid bacteria
YU Shang-fu1,JIN Da1,DING Xiu-yun1,DOU Ming-li2,HUO Gui-cheng1,*
(1.Key Laboratory of Dairy Science of Ministry of Education,College of Food Science, Northeast Agricultural University,Harbin 150030,China; 2.Sichuan Institute for Food and Drug Control,Chengdu 611731,China)
Using the lactic acid bacteria KLDS1.0207 with good sequestering Pb2+as the research object,the thermodynamic model and kinetic model were served to analysis the process of lactic acid bacteria KLDS1.0207 binding lead ion,at the same time combined with scanning electron microscopy-energy spectrum and Fourier infrared spectrum analysis of the combination of lead ion state. Finally the result concluded that the adsorption equilibrium data fitting showed the Langmuir Freundlich model(R2=0.9820)was more suitable for the process of the combination of lead ions aganist the Langmuir model and Freundlich model. Pseudo second order model(R2=0.9916)had dominance in comparison to pseudo first order,indicating that the mechanism of action of the bacteria and lead to chemical adsorption,rather than physical adsorption.By the SEM and EDS analysis could be seen in the cell surface was not completely distributed lead particles,inferred involved in the adsorption process and its main role was to contain C,O group. Through the SEM-EDS and FTIR spectra,could be inferred the function groups like carboxyl,amino,amide,hydroxyl were taken part in the process of lactic acid bacteria binding the lead ions. The mechanism might include chemical adsorption,ion exchange,chemical precipitation,etc.
lactic acid bacteria;thermodynamic model;kinetic model;Pb2+
2016-05-27
于上富(1989-),男,硕士研究生,研究方向:食品微生物与生物技术,E-mail:yushangf@163.com。
*通讯作者:霍贵成(1958-),男,博士,教授,研究方向:食品微生物与生物技术,E-mail:gchuo58@126.com。
国家自然科学基金(31401512);国家高技术研究发展计划(863计划)(2011AA100902)。
TS201.3
A
1002-0306(2016)22-0116-06
10.13386/j.issn1002-0306.2016.22.015
