维生素C荧光光谱的机理研究
2017-01-13陈亚斌何建国马天兰丁佳兴吴龙国贺晓光王松磊刘贵珊
陈亚斌,何建国,马天兰,丁佳兴,吴龙国,贺晓光,王松磊,刘贵珊
(宁夏大学农学院,宁夏银川 750021)
维生素C荧光光谱的机理研究
陈亚斌,何建国*,马天兰,丁佳兴,吴龙国,贺晓光,王松磊,刘贵珊
(宁夏大学农学院,宁夏银川 750021)
以VC标品为研究对象,利用荧光分光光度计分别采集了280~350 nm激发波长下的荧光发射光谱,结果表明:VC溶液的最大荧光峰位于EX310 nm/EM400 nm,VC光谱的二阶导数有4个极值点和3个拐点,分别为:328、345、355、372、395、425、525 nm。通过理论分析,证实395 nm是-OH发生的n→σ*电子跃迁,二烯醇结构π→π*电子跃迁产生的荧光峰由于共轭体系的作用发生红移而位于425、525 nm。分子中的各个荧光团相互叠加且彼此制约,在分子团簇作用和水分子的H键的共同作用下,最终使得VC溶液在400 nm有最大荧光峰。
维生素C,荧光光谱,荧光峰
随着人们生活水平的提高,人们更加提倡合理的膳食结构。VC是一种水溶性维生素易从体内流失,但由于人体不能合成VC,因此合理的补充VC对人体健康至关重要。VC是一个具有5元环平面刚性的多-OH化合物,其分子的双烯醇式-OH极易解离,释放出H+而被氧化成脱氢VC,是供电子体可清除自由基[1]。当VC缺乏时胶原蛋白的合成受阻,结缔组织改变[2]。同时VC可改善铁、钙和叶酸的利用,预防动脉硬化,还与膝骨关节炎密切相关[3]。但同样VC也有危害,如果一次性摄入VC2.5~5.0 g以上的药剂,可能致使红细胞大量破裂而出现溶血等现象[4]。可见如何准确的检测出VC的含量对消费者至关重要。
果蔬中VC常用的测量方法有2,6-二氯靛酚滴定法、2,4-二硝基苯肼分光光度法、纸色谱法、薄层色谱法、高效液相色谱法、荧光分光光度法等[5]。针对不同的方法许多学者进行了研究,李天华等[6]用2,6-二氯靛酚滴定法结合近红外实现了对番茄VC含量的预测。朱娜[7]采用HPLC法对果汁中VC的含量进行测定。傅维等[8]采用荧光分光光度法测定了几种市售水果中VC的含量,建立了回归方程。龚时琼等[9]用分子荧光光谱仪测定了西红柿、青椒的VC含量,检出限为0.03 μg/mL。一般的研究仅仅是针对其含量进行定量分析建模,即使测定其荧光也仅仅考虑溶剂、pH、离子等荧光促灭效应,针对光谱的发射机理和荧光特性的研究却很少。
本文以VC标品为研究对象,利用日立F-7000荧光分光光度计测定不同激发波长下的VC的荧光光谱,并结合VC的化学结构从理论上对VC荧光光谱的发射机理和荧光特性进行研究,旨在解释VC的荧光光谱机理,为VC的荧光检测与评价提供依据。
1 材料与方法
1.1 材料与仪器
VC标品 纯度为100%,中国食品药品检定研究院。
日立F-7000荧光分光光度计 日立高新技术公司;石英比色皿(12.4 mm×12.4 mm×45 mm) 上海光谱仪器有限公司。
1.2 实验方法
1.2.1 待测溶液 用超纯水将VC稀释成浓度为1 mg·mL-1的溶液。
1.2.2 荧光光谱的采集 使用日立F-7000荧光分光光度计,用没有荧光的石英比色皿装待测溶液,并将其放在荧光池中心点上。激发狭缝(EX Slit)10.0 nm,发射狭缝(EM Slit)10.0 nm,光电倍增管负高压(PMT Voltage)400 V,扫描速度(Scan speed)2400 nm/min。采用波长扫描方式,发射波长的采集范围下限比原激发波长大20 nm,分别采集280~350 nm的不同激发波长(激发波长每隔5 nm测量一次)下VC水溶液和蒸馏水的荧光发射光谱,得到相应的荧光谱图。所有样本测量均在常温下完成(20~25 ℃)。
2 结果与分析
2.1 荧光发射图谱分析
荧光光谱是受激发电子从激发态以辐射的形式回到不同振动能级的基态时所发出的光[10]。激发光谱则是分子从基态跃迁至第一电子激发态或更高电子激发态的各个不同振动能级所吸收的光能量。由于荧光光谱中存在的一个普遍现象—斯托克斯位移[11],斯托克斯位移是指荧光光谱与相应的吸收光谱相比出现的红移现象,所以导致物质的发射波长大于原激发波长。实验利用F-7000荧光分光光度计分别采集了280~350 nm的不同激发波长下的VC溶液和蒸馏水水的荧光发射光谱,结果如图1、图2所示。
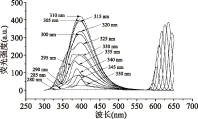
图1 VC溶液的荧光发射光谱图Fig.1 Fluorescence spectra of vitamin C solution
从图1、图2得到的数据来看,在荧光发射光谱中550 nm之后的峰值是原激发波2次衍射造成的,不是VC的荧光,所以550 nm之后的峰不在考虑的范围之内。图1可以看出VC的荧光随着激发波长的增加而发生不规则变化。激发波长从280~330 nm时,最大荧光峰出现在400 nm处一直不变。但当激发波长为335 nm时荧光峰变为370 nm处。在激发波长大于335 nm以后,最大荧光峰从370 nm向400 nm移动。激发波长为330~335 nm之间最大荧光峰有较大的位移。为了了解溶剂对溶质荧光光谱的影响,测量了蒸馏水在不同激发波长下的荧光光谱。从图2可以看出蒸馏水在280~350 nm不同激发波长下的荧光发射光谱随着激发波长的变化与VC溶液变化趋势相同,在280~310 nm激发波长下最大荧光峰在335 nm处。当激发波长为315~330 nm时,最大荧光峰从355 nm移动到370 nm,蒸馏水激发波长为310~315 nm之间最大荧光峰有较大的位移。
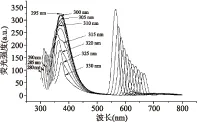
图2 蒸馏水的荧光发射光谱图Fig.2 Fluorescence spectra of distilled water
VC水溶液发射光谱在激发波长330~335 nm之间最大荧光峰有较大的位移,而蒸馏水发射光谱在激发波长为310~315 nm之间最大荧光峰也有较大的位移,两者峰位置不一致的原因在于VC水溶液中VC的-OH跃迁以及水分子团簇和H键的作用下使得荧光出现了较大的红移现象。VC水溶液的荧光在激发波长大于330 nm时最大荧光峰有较大的位移,这是由于激发波长大于330 nm时激发波的光子能量不足以使得VC结构中的电子发生跃迁,溶液中的跃迁主要表现为水的荧光,所以最大荧光峰出现了较大的位移。
2.2 有机物分子中电子的存在形式
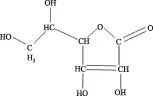
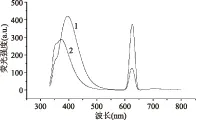
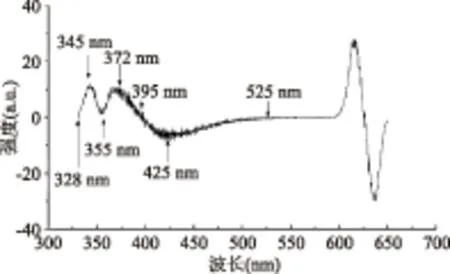
有机物电子以三种形式存在:形成单键的σ电子、形成双键的π电子、未成键的n电子。基态时电子都处在各自最低能及轨道上,即σ成键轨道、π成键轨道上和n非成键轨道上。当激发的光子能量适合、碰撞方式正确时,处于基态的电子吸收合适的能量后,就会跃迁到任意一个较高能级的反键轨道上。一个允许的跃迁不仅要考虑能量的因素,还需符合动量守恒、自旋动量守恒以及受轨道对称性的制约。即使是允许的跃迁,它们的跃迁概率也是不相同的。跃迁的情况如图3所示,跃迁时吸收能量的大小顺序为:n→π*<π→π* 图3 能级图Fig.3 Energy level diagram 2.3 VC结构与荧光的分析 VC的结构式如图所示,可以看出维生素C是由一个五元环构成封闭的大的平面共轭体系结构,含有多个手性C原子,且平面结构可以增大分子的吸光截面,增大摩尔吸光系数,增强荧光强度,所以有利于荧光的产生[12]。同时VC具有给电子取代基-OH,由于-OH 上的n电子云几乎与双烯醇的π电子轨道平行,因此它们共享了共轭π电子轨道,形成了p-π共轭,扩大了共轭体系,增强了VC的荧光特性[13]。VC的结构由于-OH中的n电子吸收激发光光子,结构容易发生n→σ*跃迁,其吸收峰值位置在近紫外区。荧光峰值在395 nm 处经理论分析表明该荧光是由基团C-OH 中的孤对电子产生的。VC中的二烯醇具有很强的还原性,容易发生n→σ*峰跃迁和π→π*的跃迁,再考虑到分子中的共轭结构以及助色团,使得VC溶液的吸收峰出现红移现象。 图4 VC结构图Fig.4 Structure of vitamin C 2.4 溶质与溶剂之间的关系 为了探究溶质与溶剂之间的关系,分别在同一激发波长下同时激发获得VC溶液和蒸馏水的荧光光谱。从图1、图2可以看出,随着激发波长的增加发射波长的荧光先增加后减小。VC水溶液的荧光在310 nm激发波长下出现最大荧光峰。溶液中分子的团簇现象使得物质的结构更加复杂,因此推测VC分子和水分子混合发生团簇形成新的结构类型。由于VC中富含-OH结构,O原子与H原子共用一对电子,所以使得VC分子结构容易吸引水分子与其形成团簇分子结构,并且水中的分子会形成H键,H键与VC分子之间作用,从而增大了VC的平面钢性结构提高了VC水溶液的荧光量子效率。当水溶液的浓度较低时,H键结构占主导结构,且共轭体系中π电子共轭度越大荧光强度越大,同时也伴随着荧光峰红移。如图5为310 nm激励波长下的蒸馏水的和VC的荧光光谱图,水的荧光峰位置为370 nm,在VC中-OH电子的跃迁在395 nm处,分子团簇作用和水分子的H键的共同作用下,使得VC水溶液在400 nm处有最大吸收峰[14]。 图5 激发波长310 nm下VC水溶液与蒸馏水的荧光发射图Fig.5 Fluorescence spectra of vitamin c solution and distilled water were measured with the excitation wavelength at 310 nm注:1为VC水溶液,2为蒸馏水。 2.5 VC溶液荧光光谱的二阶导数 VC水溶液在310 nm激发波长下荧光强度最强,经过光谱理论分析,将最佳激发波长得到的荧光发射光谱求二阶导数。二阶导数函数中的极值点、拐点波长处可能与VC不同荧光团发射的荧光相对应[15]。本文采用在Origin 7.5软件对荧光发射光谱求二阶导数,荧光的二阶导数图如图6所示。 图6 VC溶液的二阶导数荧光光谱Fig.6 Second order derivation of fluorescence spectra of vitamin c VC溶液的二阶导数荧光光谱存在四个极小值点,分别为345、355、372、425 nm,三个零点分别对应原光谱的拐点,分别为328、395、525 nm,因此这7个波段可能对应与7种不同的荧光团。虽然从图5可以看出,VC溶液只有一个明显的荧光峰,但这个荧光峰可能是这7个波段所对应的荧光团的共同作用相互影响的结果。由于荧光物质具有加和性,345、372 nm处是水的荧光峰。物质中的C=C、C=O等结构上的π电子吸收光子产生π→π*的跃迁,通常单独的双键结构如乙烯,其π→π*的跃迁发射光谱在170~200 nm,然而VC具有大的共轭结构,使得π→π*的跃迁的波长都发生了红移。萘环的π电子发生π→π*跃迁的荧光峰为530、687、635 nm[16],所以推测425、525 nm的波长处是由于VC中的双键上的跃迁引起的。由于不同的荧光团对荧光发射光谱的作用程度各不相同,在生成荧光的过程中,各个荧光团相互叠加且彼此制约,最终使得VC溶液的荧光发射光谱中只出现了一个明显的荧光峰。 系统研究了VC的荧光光谱,分别采集了280~350 nm的激发波长下的荧光发射光谱,VC溶液的最大荧光峰位于EX310 nm/EM400 nm。为了研究水对VC溶液荧光的影响,同时采集了蒸馏水的荧光发射光谱。蒸馏水的最大荧光峰位于EX295 nm/EM370 nm。对VC溶液的荧光光谱求二阶导数,发现荧光光谱有4个极值点和3个拐点,分别为328、345、355、372、395、425、525 nm。通过对荧光光谱的理论分析,认为395 nm是由-OH发生的n→σ*的电子跃迁引起的、二烯醇结构发生π→π*电子跃迁的荧光位于425、525 nm。由于不同的荧光团对荧光发射光谱的作用程度各不相同,VC结构中n→σ*跃迁和π→π*的跃迁在分子团簇作用和水分子的H键的共同作用下,使得VC水溶液在400 nm处有最大荧光峰。 [1]崔乃杰,崔乃强,傅强,等.维生素C抗氧化促氧化双向作用的研究[J].中国中西医结合外科杂志,2004,10(6):419-421. [2]Ahmet Unlu,Onder Kirca,Mustafa Ozdogan. High-dose vitamin C and cancer[J].Journal of Oncological Science,2016(1):10-12. [3]R K Chaganti,Tolstykh M K Javaid. High plasma levels of vitamin C and vitamin E are associated with incident radiographic knee osteoarthritis[J].Osteoathritis and Cartilage,2014(22): 190-196. [4]陆基宗.过量使用维生素C的危害[J].东方食疗与保健,2007(11):22-23. [5]谢志方.氢氧化钠两点电位滴定法测定维生素C含量[J]. 广州化工,2011(15):125-127. [6]李天华,施国英,魏珉,等.番茄维生素C含量近红外预测光谱的小波去噪[J].农业机械学报,2013(44):200-204. [7]朱娜.高效液相色谱法测定维生素C含量[J].实验室研究与探索,2013,32(10):315-328. [8]傅维,杨彩霞.荧光分光光度法测定几种天津市售水果中维生素的含量[J].安徽农业科学,2011,39(23):14392-14393. [9]龚时琼,赵丽华,陈芳.荧光法快速检测水果和蔬菜中的抗坏血酸[J].实验室研究与探索,2012,31(10):19-32. [10]王欢博,张玉钧,肖雪.等.三种酚类化合物的三维荧光光谱特性研究[J].光谱学与光谱分析,2010,30(5):1271-1274. [11]何迪洁.芳香族化合物的斯托克斯位移[J].发光与显示,1983(3):25-26. [12]张春艳. 基于固体粉末态物质的荧光光谱实验及其机制研究[D].天津:南开大学,2010. [13]王芳芳. 有机π-电子共轭材料的线性与非线性光学性质研究[D].开封:河南大学,2007. [14]兰秀风,刘莹,高淑梅,等.乙醇溶液的荧光光谱及其特性的研究[J].激光技术,2003(5):477-479. [15]金海龙,严冰,王玉田.基于导数荧光光谱的活体海藻识别方法研究[J].燕山大学学报,2005(6):493-496. [16]史爱敏,朱拓,顾恩东,等.胭脂红荧光光谱机理研究[J]. 光谱学与光谱分析,2009(1):193-195. Study on fluorescence spectra mechanism of vitamin C CHEN Ya-bin,HE Jian-guo*,MA Tian-lan,DING Jia-xing,WU Long-guo, HE Xiao-guang,WANG Song-lei,LIU Gui-shan (Ningxia University School of Agriculture,Yinchuan 750021,China) Taken standard vitamin C for research objects,fluorescence emission spectra were measured with fluorescence spectrophotometer and the excitation wavelength were 280~350 nm. The results showed that the fluorescence excitation and emission wavelengths of the vitamin C solution were 310 nm and 400 nm. The second order derivation of fluorescence spectrum had four extreme points and three inflection points which were 328,345,355,372,395,425,525 nm.Based on the theory analysis,we come to the conclusion that the fluorescence peak at 395 nm was formed by-OH n→σ*-electron jumps. The dienes alcohols structure emitted a π→π*-electron jumps of maximum peak that were a little red shift at 425 nm and 525 nm. The reason was strong affected by conjugated system. Each of molecule fluorescent group were restricted and superimposed. The molecular clusters and H bond of water molecule made maximum fluorescence peak of vitamin C solution at 400 nm. vitamin C;fluorescence spectrum;fluorescence peak 2016-05-27 陈亚斌(1990-),男,硕士研究生,研究方向:农产品无损检测,E-mail:shenyang12536@126.com。 *通讯作者:何建国(1960-),男,教授,研究方向:农业工程装备及机电一体化技术、农产品无损检测,E-mail:hejg@nxu.edu.cn。 国家自然科学基金项目(31560481)。 TS201 A 1002-0306(2016)22-0112-04 10.13386/j.issn1002-0306.2016.22.014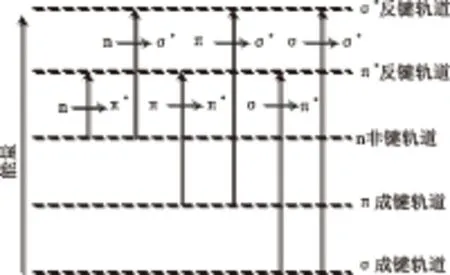
3 结论
