2,4-二氨基嘧啶对冷轧钢在HCl溶液中的缓蚀作用
2017-01-06李向红谢小光
李向红,谢小光
(1. 西南林业大学 理学院,昆明 650224; 2. 云南大学 化学科学与工程学院,昆明 650091)
试验研究
2,4-二氨基嘧啶对冷轧钢在HCl溶液中的缓蚀作用
李向红1,2,谢小光2
(1. 西南林业大学 理学院,昆明 650224; 2. 云南大学 化学科学与工程学院,昆明 650091)
通过浸泡试验、电化学试验和扫描电子显微镜(SEM)观察研究了2,4-二氨基嘧啶(DAP)在1.0 mol/L HCl溶液中对冷轧钢的缓蚀作用。结果表明:DAP在HCl溶液中对冷轧钢具有良好的缓蚀作用;缓蚀率随缓蚀剂含量的增大而增大,DAP浓度为10.0 mmol/L时缓蚀率最大,可达94.8%;DAP为混合型抑制型缓蚀剂,DAP在冷轧钢表面的吸附符合Langmuir吸附等温式,缓蚀率随温度的升高而下降。
冷轧钢;HCl溶液;2,4-二氨基嘧啶;缓蚀;吸附
嘧啶类化合物可作为钢的酸性缓蚀剂,取代基对嘧啶衍生物的缓蚀性能有较大的影响[1]。氨基(-NH2)为常见的极性取代基,在嘧啶环上取代后也会增加N-杂环的电子云密度,从而提高2-氨基嘧啶在HCl溶液中的吸附性能和缓蚀性能[2]。Awad等[3]系统地研究了嘧啶和几种氨基嘧啶衍生物在2.0 mol/L HCl溶液中对纯铁的缓蚀作用。结果表明,氨基取代后,缓蚀率会上升,同时缓蚀性能随氨基取代基数量的增加而增强。Abdallah等[4]通过失重法和极化曲线法研究了4种氨基嘧啶衍生物(2-氨基嘧啶、2,4-二氨基嘧啶、2,4-二氨基-6-羟基嘧啶、2,4,6-三氨基嘧啶)在0.05 mol/L HNO3中对碳钢的缓蚀作用,其中2-氨基嘧啶(AP)和2,4-二氨基嘧啶(DAP)的最大缓蚀率仅为36.3%和42.6%。Masoud等[5]用高斯软件进行量子化学计算,通过结构参数探究了文献[4]中的缓蚀性能的差异性,然而对于质子化作用及缓蚀剂分子在金属表面的吸附体系并未作研究。作者所在课题组[6]最近也通过试验和分子模拟方法研究了AP和DAP在H2SO4溶液中对1018碳钢的缓蚀作用,并在理论计算时考虑了质子化作用,得到缓蚀性能与氨基的取代基数量成正比的结论。
目前,关于DAP在HCl溶液中对冷轧钢(CRS)缓蚀性能研究的报道比较少。为此,本工作采用浸泡试验、电化学试验研究了DAP缓蚀剂在20 ~ 50 ℃的1.0 mol/L HCl溶液中对冷轧钢的缓蚀作用,并讨论了DAP在钢表面的吸附行为及其机理。
1 试验
1.1 材料和试剂
试验钢采用冷轧钢片,其化学成分(质量分数)为:C 0.07%,Si 0.01%,Mn 0.3%,P 0.022%,S 0.01%,Al 0.030%,Fe余量。试验采用的盐酸、丙酮均为分析纯;缓蚀剂为2,4-二氨基嘧啶(DAP,C4H6N4),从国药集团化学试剂有限公司购置,其分子结构式见图1。

图1 2,4-二氨基嘧啶(DAP)的分子结构式Fig. 1 Molecular structure of 2,4-diaminopyrimidine (DAP)
1.2 浸泡试验
浸泡试验用试样为尺寸25.0 mm×20.0 mm×0.60 mm的冷轧钢片,并按文献[6]对试样进行表面处理,用电子天平(±0.1 mg)称试样的质量。然后,将试样用玻璃钩全浸悬于20 ℃含有不同含量DAP的1.0 mol/L HCl溶液中,恒温浸泡6 h后取出,清洗、吹干、精确称量。采用失重法计算腐蚀速率(v)和缓蚀率(ηw)[6]。另外,在DAP浓度为10.0 mol/L条件下,改变试验温度(20~50 ℃),研究了温度对其缓蚀性能的影响。
1.3 电化学试验
电化学试验在PARSTAT2273电化学工作站(美国Princeton Applied Research公司)上采用三电极体系进行。其中,参比电极为套有卢金毛细管的饱和KCl甘汞电极(SCE),辅助电极为铂电极,工作电极为冷轧钢电极。制备工作电极时,用环氧树脂(固化剂为聚酰胺树脂)灌封,使其裸露面积为1.0 cm×1.0 cm。用500号,800号,1 000号耐水砂纸依次打磨工作电极的裸露面至镜面光亮,再经丙酮脱脂后,放入250 mL的1.0 mol/L HCl溶液中。测开路电位-时间的曲线,测试时间为3 h。动电位极化曲线和电化学阻抗谱(EIS)测量则在开路、浸泡2 h后进行。动电位极化曲线扫描区间为-250~250 mV(相对于开路电位),扫描速率为0.5 mV/s。电化学阻抗谱(EIS)的测量频率为10-2~105Hz,交流激励信号的幅值为10 mV,数据点采集数为30。电化学试验温度均为20 ℃。然后,分别根据腐蚀电流密度(Jcorr)和电荷转移电阻(Rt)计算缓蚀率(ηp)和(ηR)[6]。
1.4 扫描电子显微镜观察
将10.0 mm×10.0 mm×0.60 mm的冷轧钢片按文献[6]进行表面处理后,恒温(20 ℃)浸泡于含有10.0 mmol/L DAP的1.0 mol/L HCl溶液中,6 h后取出。用蒸馏水冲洗、吹风机冷风吹干后,立即用S-3000N型扫描电子显微镜(SEM)观察其表面形貌。
2 结果与讨论
2.1 浸泡试验
2.1.1 腐蚀速率和缓蚀率
由图2可见,在未添加DAP的空白1.0 mol/L HCl中,冷轧钢的腐蚀速率高达4.67 g/(m2·h-1),但加入DAP后,冷轧钢的腐蚀速率显著下降,且随DAP浓度的增加而不断减小,当DAP浓度为10.0 mmol/L时,腐蚀速率下降至0.24 g/(m2·h-1);缓蚀率随DAP浓度的增加而增大,DAP浓度为10.0 mmol/L时,缓蚀率为94.8%,这表明在HCl溶液中DAP对冷轧钢具有良好的缓蚀作用。当DAP浓度增加至5.0 mmol/L后,缓蚀率几乎不再随DAP浓度变化,这表明在该浓度下,DAP在钢表面的吸附趋于饱和。
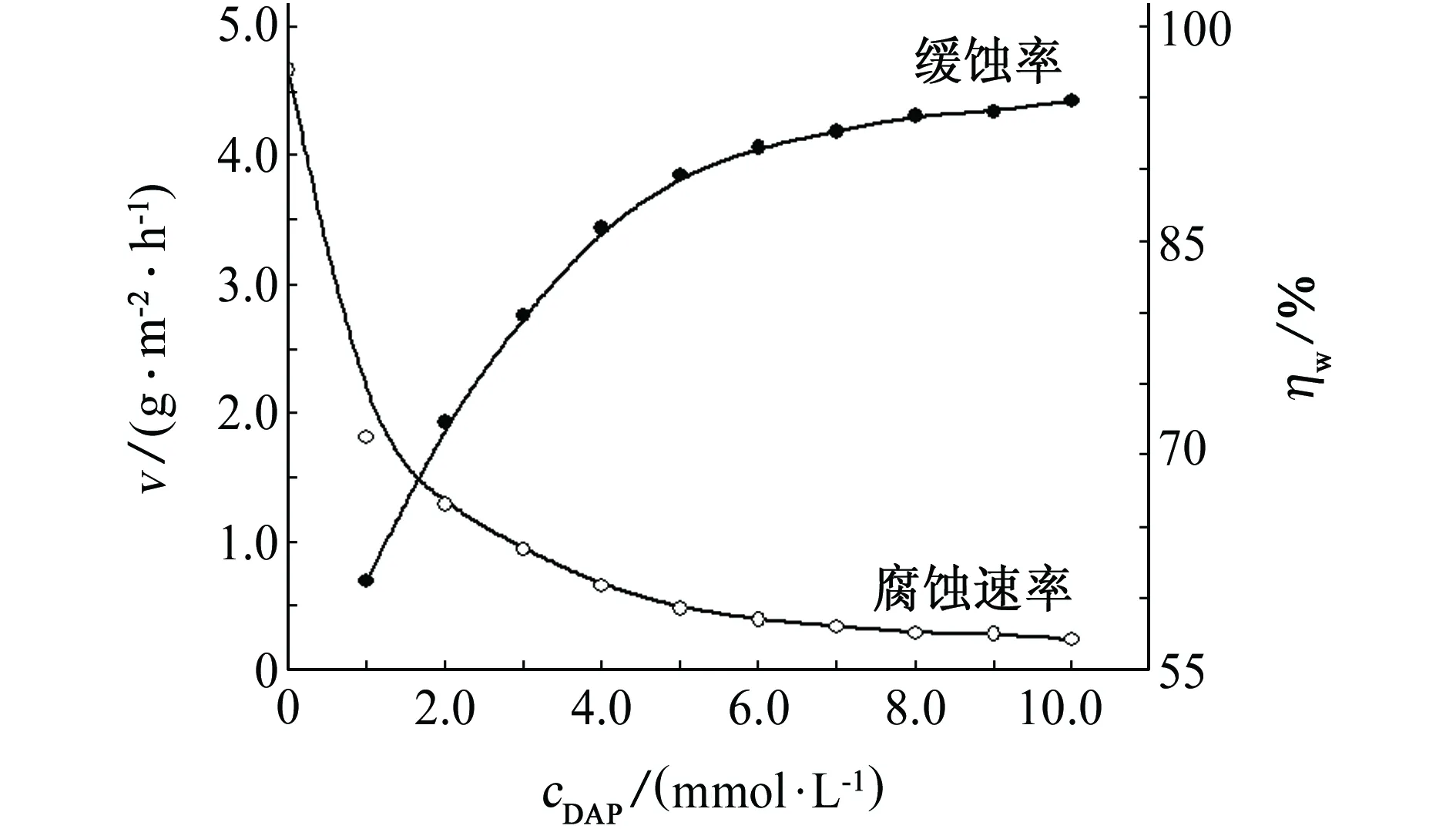
图2 在20 ℃的1.0 mol/L HCl溶液中腐蚀速率、缓蚀率与DAP浓度的关系曲线Fig. 2 Relationships between concentration of DAP and corrosion rate and inhibition efficiency in 1.0 mol/L HCl solution at 20 ℃
在酸性介质中,DAP中的氮原子与H+发生质子化:
HCl溶液中的Cl-可通过特性吸附在钢表面,使钢表面带负电荷,然后质子化的[DAPHx]x+通过静电引力吸附在钢表面。此外,由于DAP含有2个氮杂原子的六元杂环和2个极性取代氨基,从而具有丰富的孤对电子和π电子,是良好的螯合配位体。故它可以与铁的空d轨道形成配位键发生化学吸附[6],在冷轧钢表面形成良好的缓蚀剂吸附膜层,对冷轧钢起到了良好的缓蚀作用。最后,DAP也可能与溶液中的Fe2+形成螯合物,而后吸附覆盖在钢表面。
根据课题组前期报道[2],20 ℃时,浓度为10.0 mmol/L的AP对钢的缓蚀率为92.4%,故DAP的缓蚀性能优于AP的。这表明缓蚀性能随氨基取代基的数目的增加而增大。和AP相比,DAP的分子结构中4位上多了氨基取代,量子化学计算结果表明[6],除了嘧啶环外,4位上的氨基也是吸附中心,它既可以给出电子对和钢表面形成配位键又可以接受钢表面的电子对形成反馈键,使吸附更为牢固;此外,分子动力学模拟结果表明[6],DAP和AP分子均平行吸附于Fe(001)表面,且DAP的表面吸附能(Eads)高于AP的,故DAP的缓蚀性能优于AP的。
2.1.2 吸附等温式和标准吸附自由能
在1.0 mol/L HCl溶液中,DAP在钢表面的吸附遵循Langmuir吸附模型[2],见式(2)。
式中:c为缓蚀剂的浓度,mmol/L;K为吸附平衡常数,L/mol。
用缓蚀率(ηw)近似代替表面覆盖度(θ),根据c/θ,c数据作图,见图3。结果表明,c/θ和c之间具有明显的直线关系,相应的线性相关系数(0.999 8)和斜率(0.98)均十分接近1。这说明DAP在钢表面的吸附满足Langmuir吸附等温方程式,与文献[6]结论一致。通过直线截距可换算出DAP的吸附平衡常数(K)为1.36×103L/mol;同等条件下,AP在1.0 mol/L HCl中的钢表面的吸附平衡常数(K)为9.76×102L/mol[2],故两个氨基嘧啶衍生物的吸附平衡常数排序为:DAP>AP。这表明缓蚀剂DAP的吸附性能强于AP的。

图3 20 ℃时1.0 mol/L HCl中DAP在冷轧钢表面的Langmuir吸附等温式Fig. 3 Langmuir adsorption isotherm of DAP on the surface of cold rolled steel in 1.0 mol/L HCl at 20 ℃
标准吸附自由能(ΔG0)可按式(3)计算[7]。
式中:R为气体常数;T为热力学温度。
根据式(3)计算得到的标准吸附自由能为-27.4 kJ/mol。绝对值较大,表明DAP可在钢表面产生较强的吸附作用;且绝对值在20~42 kJ/mol内,表明DAP在冷轧钢表面上的吸附属于物理吸附和化学吸附的混合吸附[7]。
2.1.3 温度对缓蚀性能的影响
缓蚀性能受温度的影响较大。温度上升会加速钢的腐蚀,但也会使缓蚀剂分子在钢表面吸附得更为坚固和致密,故在缓蚀体系中很难直接判断缓蚀率随温度的变化规律。由图4可见,在添加10.0 mmol/L DAP 的1.0 mol/L HCl溶液中,随温度的升高,冷轧钢的缓蚀率小幅降低,在50 ℃时,缓蚀率仍然高达88.9%,此结果与AP在HCl溶液中的缓蚀率随温度的变化规律相类似[2]。原因主要是在此温度区间内,腐蚀加剧的程度和缓蚀剂化学吸附加快的程度基本一致,即整个缓蚀体系在此温度区间内波动不大。
根据Arrhenius公式,见式(4),钢在酸性溶液中的腐蚀速率的自然对数(lnv)和热力学温度的倒数(1/T)之间存在直线关系式[8]。

图4 在添加10.0 mmol/L DAP的1.0 mol/L HCl溶液中缓蚀率随温度的变化曲线Fig. 4 Relationship between inhibition efficiency and temperature in 1.0 mol/L HCl solution added with 10.0 mmol/L DAP
式中:Ea为表观活化能;A为指前因子;v为腐蚀速率。
图5为在添加和未添加10.0 mmol/L DAP的1.0 mol/L HCl溶液中lnv-1/T关系曲线。由图5可见,lnv-1/T具有良好的线性关系。对lnv-1/T进行直线回归处理,根据lnv-1/T直线的斜率和截距可分别计算出Ea和A,结果见表1。
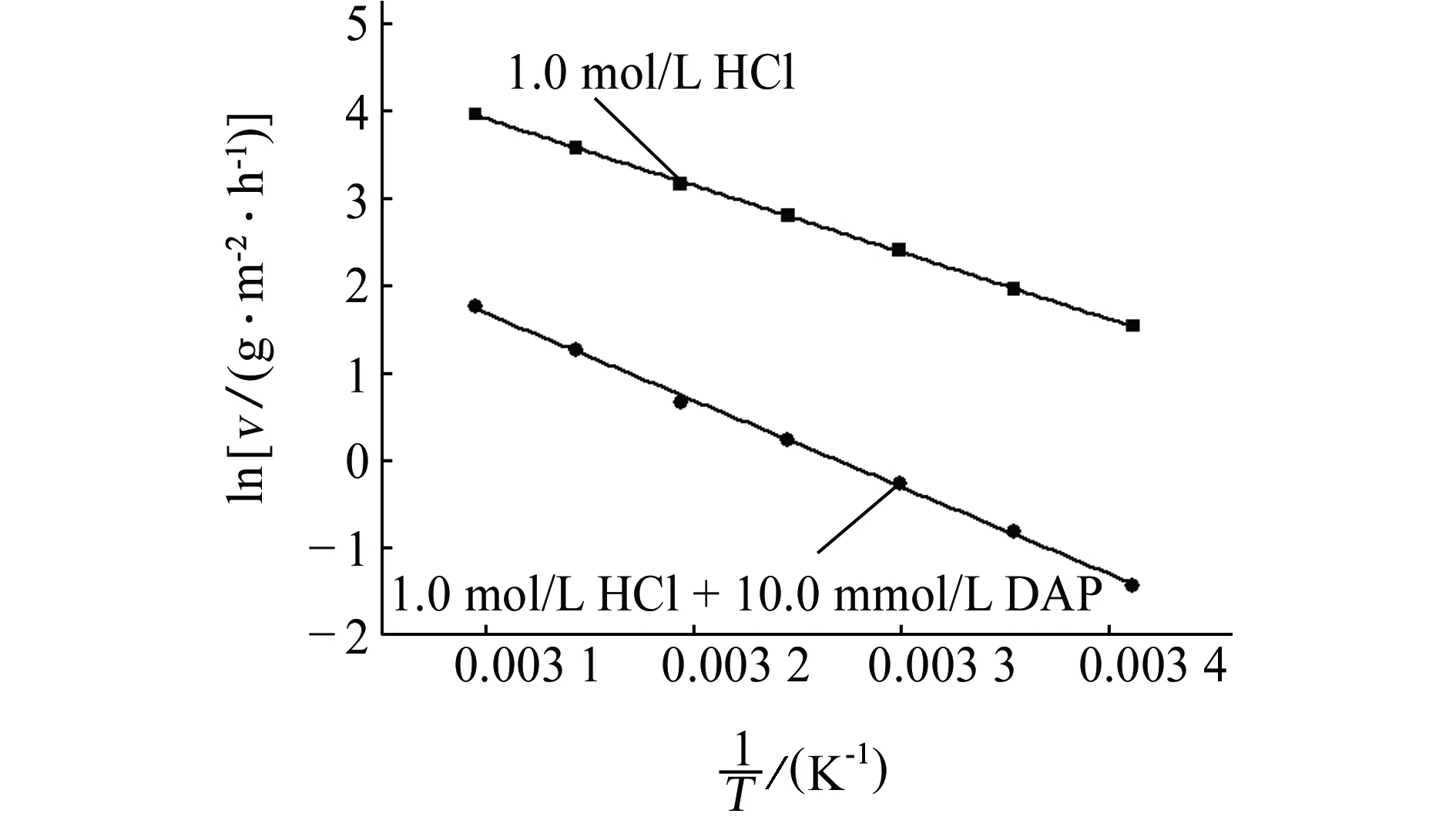
图5 在添加和未添加10.0 mmol/L DAP的1.0 mol/L HCl溶液中lnv-1/T的关系曲线Fig. 5 Curves of lnv-1/T in 1.0 mol/L HCl solution added with and without 10.0 mmol/L DAP

表1 在添加和未添加10.0 mmol/L DAP 的1.0 mol/L HCl溶液中lnv-1/T直线的参数Tab. 1 Parameters of the straight line of lnv-1/T in 1.0 mol/L HCl solution added with and without 10.0 mmol/L DAP
在酸性溶液中,如果添加缓蚀剂后的表观活化能高于未添加缓蚀剂的,表明缓蚀剂主要发生物理吸附[9];相反,如果添加缓蚀剂的表观活化能低于未添加缓蚀剂的,则表明缓蚀剂主要发生化学吸附[10]。然而,用表观活化能来判断吸附的类型虽有一定的合理性,但并不具有决定性,因为在缓蚀体系中,除缓蚀剂外金属表面还存在其他物质的吸附,如溶液中水的吸附,酸根离子的吸附等,这些物质的吸附也会消耗表观活化能[11],导致表观活化能升高。Solmaz等[12]认为,有机缓蚀剂的吸附不能简单地归类为单纯的物理吸附或化学吸附。Moretti等[13]提出用表观活化能评判缓蚀剂的吸附类型时,最好结合其他参数来判断。
由表1可见,在HCl溶液中添加DAP后,表观活化能均会上升,但不能简单地认为DAP在冷轧钢表面的吸附类型为单纯的物理吸附,结合前述关于标准吸附Gibbs自由能的数据可知,DAP的吸附包含物理吸附和化学吸附。根据(4)式可知,欲使腐蚀速率趋于较低值,须使表观活化能具有较高值,而指前因子具有较低值。此体系中添加DAP后腐蚀速率的下降主要归因于活化能升高。
2.2 电化学试验
2.2.1 开路电位-时间曲线
由图6可见,冷轧钢的开路电位随时间的延长逐渐上升并且逐步趋于稳定,这与文献[14]报道的结果相一致。经2 h浸泡后,在添加和未添加10.0 mmol/L DAP的1.0 mol/L HCl溶液中,冷轧钢的开路电位分别稳定在-481.7 mV和-457.0 mV。由此可见,添加缓蚀剂后开路电位发生正移。

图6 在添加和未添加10.0 mmol/L DAP的1.0 mol/L HCl溶液中冷轧钢的开路电位-时间曲线Fig. 6 Curves of open circuit potential vs. time for cold rolled steel in 1.0 mol/L HCl solution added with and without 10.0 mmol/L DAP
2.2.2 动电位极化曲线
由图7可见,添加DAP对阴阳两极电化学反应产生了明显的抑制作用。图7中的阴极极化曲线均呈现出明显的Tafel直线区,这表明阴极析氢反应的机理主要为活化控制[15];添加DAP后,阴极极化曲线的Tafel直线与未添加时的平行,表明添加DAP后未改变H+得电子变成H2的机理[16]。由图7还可见,阳极极化曲线出现了3段特征区域:缓蚀Tafel区(I)、阳极脱附电位平台区(II)和脱附后无缓蚀作用区(III)[17]。在缓蚀Tafel区,随着腐蚀电流密度的不断增大,腐蚀电位升高较快,曲线的阳极Tafel斜率为ba1;当腐蚀电位升高到某一临界值后,腐蚀电位随腐蚀电流密度以极小的斜率ba2变化,即出现了相对变化较小的平台区(II)。平台区也可解释为缓蚀剂的吸附-脱附平衡区[17]。平台区所对应的电位为脱附电位值(Edes),当腐蚀电位到达Edes后,缓蚀剂在电极表面开始发生脱附。腐蚀电位超过Edes后,电极表面发生腐蚀的速率将急剧增大,即进入脱附后无缓蚀作用区,在此区域内腐蚀电位随阳极电流密度急剧上升,斜率为ba3。

图7 在添加不同浓度DAP的1.0 mol/L HCl溶液中冷轧钢的动电位极化曲线Fig. 7 Potentiodynamic polarization curves of cold rolled steel in 1.0 mol/L HCl added with different concentrations of DAP
对图7中的动电位极化曲线进行拟合,得到的拟合参数见表2。由表2可见,在HCl溶液中加入DAP后,自腐蚀电流密度Jcorr显著减小,且随DAP浓度的增大而减小,缓蚀率则随DAP浓度的增大而增大。在未添加DAP的1.0 mol/L HCl溶液中,Jcorr高达206.8 μA/cm2,表明冷轧钢的腐蚀程度较为严重。但添加10.0 mmol/L DAP后,Jcorr下降至13.2 μA/cm2,此时缓蚀率高达93.6%,表明DAP对HCl溶液中的冷轧钢具有良好的缓蚀作用。由文献[2]可知,在HCl溶液中添加10.0 mmol/L AP时,缓蚀率为90.1%。由此可见,在相同缓蚀剂浓度下,两种氨基嘧啶衍生物的缓蚀效果排序为:DAP>AP。加入DAP后,自腐蚀电位Ecorr并没有发生明显改变,说明DAP在HCl溶液中为混合抑制型缓蚀剂,并可推断其作用机理为“几何覆盖效应”[18]。HCl溶液中添加DAP后,Tafel斜率的数值发生了明显的改变,尤其是阳极Tafel斜率。
表2 在添加不同浓度DAP的1.0 mol/L HCl溶液中冷轧钢动电位极化曲线的拟合参数
Tab. 2 Fitted parameters of potentiodynamic polarization curves of cold rolled steel in 1.0 mol/L HCl added with different concentrations of DAP

cDAP/(mmol·L-1)Ecorr/mVJcorr/(μA·cm-2)-bc/(mV·dec-1)ba/(mV·dec-1)ηp/%0-458206.811757-2.0-45555.6967173.15.0-45620.2997490.210.0-46913.210913293.6
2.2.3 电化学阻抗谱
由图8可见,在不同条件下电化学阻抗谱的形状基本保持不变,均呈现单一半圆容抗弧,这表明添加DAP后未对腐蚀体系的腐蚀机理产生影响,且腐蚀主要由电荷传递控制。随DAP浓度的增大,容抗弧半径显著增大,故电极表面的阻抗值增大,腐蚀速率减慢,缓蚀效果增强。

图8 在添加不同浓度DAP的1.0 mol/L HCl溶液中冷轧钢的电化学阻抗谱Fig. 8 EIS of cold rolled steel in 1.0 mol/L HCl added with different concentrations of DAP
采用文献[1]中Rs(CPERt)的等效电路图对图8中的电化学阻抗谱进行拟合,见图9。其中,Rs为溶液电阻,Rt为电荷转移电阻,CPE为常相位角元件,拟合参数见表3。CPE一般由Qdl和n组成。n为弥散系数,表示电极表面的粗糙程度,如果其值等于1,代表电极/电解质溶液界面为理想的双电层电容。Qdl和双电层电容(Cdl)存在如下关系式[19]:
式中:fmax为Nyqutist图中虚轴(Zim)达到最大值时对应的频率。
由表3可见,溶液电阻Rs很小,这表明电解质溶液的IR降可以忽略;同时,随DAP浓度的增大,电荷转移电阻Rt显著增大,表现出良好的缓蚀作用。
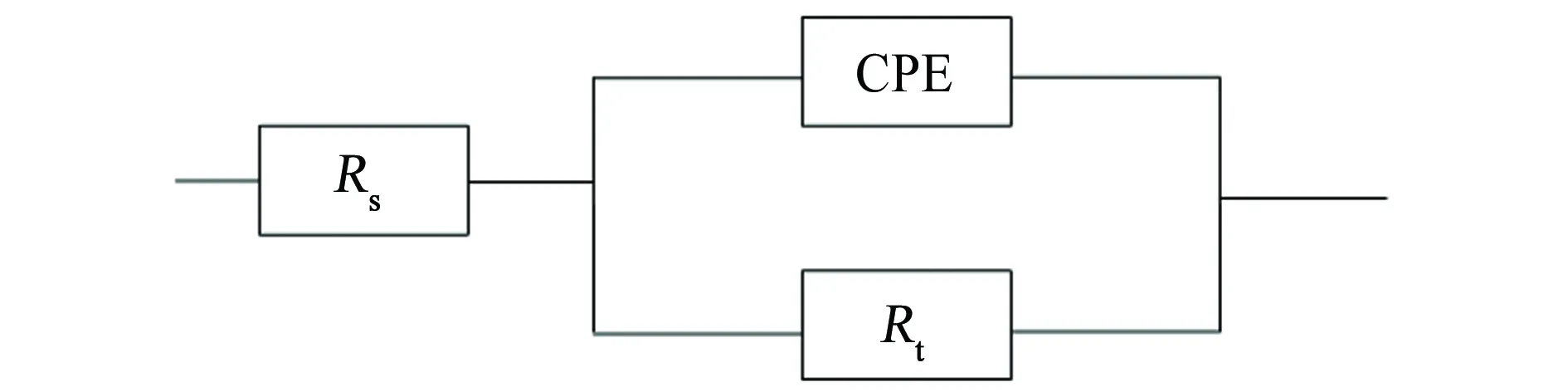
图9 拟合电化学阻抗谱的等效电路图Fig. 9 Equivalent circuit used to fit EIS

表3 在添加不同浓度DAP的1.0 mol/L HCl溶液中冷轧钢电化学阻抗谱的拟合参数Tab. 3 Fitted parameters of EIS of cold rolled steel in 1.0 mol/L HCl added with different concentrations of DAP
根据Helmholtz模型,双电层电容Cdl的表达式如式(6)所示[20]。
式中:ε0为真空介电常数;ε为电解质的介电常数;d为膜的厚度;S为电极表面的面积。
由表3还可见,与空白溶液相比,添加DAP后,Cdl减小,这是因为DAP吸附到冷轧钢表面时挤走了介电常数较大的水分子或使双电层的厚度增大[21];随着DAP浓度的增大,缓蚀率增大,当DAP浓度为10.0 mmol/L,缓蚀率最大,为90.6%,这表明DAP在1.0 mol/L HCl溶液中对冷轧钢具有优良的缓蚀作用。虽然由失重法、极化曲线法和EIS计算出的缓蚀率数据稍有差异,但变化规律一致。
2.3 扫描电子显微镜观察
图10为冷轧钢在HCl溶液中腐蚀后的表面腐蚀形貌。由图10可见,冷轧钢在1.0 mol/L HCl溶液中浸泡6 h后,表面被严重腐蚀,粗糙不平,腐蚀产物均匀分散在冷轧钢表面;添加10.0 mmol/L DAP后,冷轧钢表面较为平整,腐蚀程度大为减缓,这表明DAP对冷轧钢的腐蚀产生了明显的抑制作用。

(a) 1.0 mol/L HCl

(b) 1.0 mol/L HCl + 10.0 mmol/L DAP图10 在不同HCl溶液中浸泡6 h后冷轧钢表面的腐蚀形貌Fig. 10 Corrosion morphology of cold rolled steel after immersion in different HCl solutions for 6 h
3 结论
(1) DAP在1.0 mol/L HCl溶液中对冷轧钢具有良好的缓蚀作用,缓蚀率随缓蚀剂浓度增大而增大;在20 ℃,DAP浓度为10.0 mmol/L时,缓蚀率最大,为94.8%。
(2) DAP在HCl溶液中为混合抑制型缓蚀剂,其在冷轧钢表面的吸附服从Langmuir吸附模型,吸附过程包含了物理吸附和化学吸附。缓蚀率随温度升高而减小,添加DAP后表观活化能和指前因子均增大。
(3) DAP在HCl溶液中的电化学阻抗谱为单一容抗弧,添加DAP后,电荷转移电阻显著增加,但双电层电容减小; DAP能够有效抑制冷轧钢在HCl溶液中的腐蚀,起到了明显的缓蚀作用。
[1] 李向红,谢小光. 嘧啶衍生物对钢在盐酸溶液中的缓蚀作用[J]. 物理化学学报,2013,29(10):2221-2231.
[2] 李向红,邓书端,付惠. 2-氨基嘧啶在盐酸介质中对钢的缓蚀性能[J]. 应用化学,2012,29(2):209-215.
[3] AWAD H S,ABDEL G S. Mechanism of inhibition of iron corrosion in hydrochloric acid by pyrimidine and series of its derivatives[J]. Anti-Corrosion Methods and Materials,2005,52:328-336.
[4] ABDALLAH M,HELAL E A,FOUDA A S. Aminopyrimidine derivatives as inhibitors for corrosion of 1018 carbon steel in nitric acid solution[J]. Corrosion Science,2006,48(7):1639-1654.
[5] MASOUND M S,AWAD M K,SHAKER M A,et al. The role of structural chemistry in the inhibitive performance of some aminopyrimidines on the corrosion of steel[J]. Corrosion Science,2010,52:2387-2396.
[6] LI X H,XIE X G. Adsorption and inhibition effect of two aminopyrimidine derivatives on steel surface in H2SO4solution[J]. Journal of the Taiwan Institute of Chemical Engineers,2014,45:3033-3045.
[7] ASHASSI-SORKHABI H,MAJIDI M R,SEYYEDI K. Investigation of inhibition effect of some amino acids against steel corrosion in HCl solution[J]. Applied Surface Science,2004,225(1/4):176-185.
[8] TANG L B,MU G N,LIU G H. The effect of netural red on the corrosion inhibition of cold rolled steel in 1.0 M hydrochloric acid[J]. Corrosion Science,2003,45:2251-2262.
[9] BENPOUR M,GHOREISHI S M,SOLTANI N,et al. The inhibitive effect of some bis-N,S-bidentate Schiff bases on corrosion behaviour of 304 stainless steel in hydrochloric acid solution[J]. Corrosion Science,2009,51:1073-1082.
[10] BENTISS F,LEBRINI M,LAGRENEE M. Thermodynamic characterization of metal dissolution and inhibitor adsorption processes in mild steel/2,5-bis(n-thienyl)-1,3,4-thiadiazoles/hydrochloric acid system[J]. Corrosion Science,2005,47:2915-2931.
[11] VRACAR L M,DRAZC D M. Adsorption and corrosion inhibitive properties of some organic molecules on iron electrode in sulfuric acid[J]. Corrosion Science,2002,44:1669-1680.
[12] SOLMAZ R,KARDAS G,YAZICI B,et al. Adsorption and corrosion inhibitive properties of 2-amino-5-mercapto-1,3,4-thiadiazole on mild steel in hydrochloric acid media[J]. Colloids and Surfaces A:Physicochemistry and Engineering Aspects,2008,312:7-17.
[13] MORETTI G,GUIDI F,GRION G. Tryptamine as a green iron corrosion inhibitor in 0.5 M deaerated sulphuric acid[J]. Corrosion Science,2004,46:387-403.
[14] TANG Y M,ZHANG F,HU S X,et al. Novel benzimidazole derivatives as corrosion of mild steel in the acidic media. Part I:Gravimetric,electrochemical,SEM and XPS studies[J]. Corrosion Science,2013,74:271-282.
[15] MARKHALI B P,NADERI R,MAHDAVIAN M,et al. Electrochemical impedance spectroscopy and electrochemical noise measurements as tools to evaluate corrosion inhibition of azole compounds on stainless steel in acidic media[J]. Corrosion Science,2013,75:269-279.
[16] QIAN B,WANG J,ZHANG M,et al. Synergistic effect of polyaspartic acid and iodide ion on corrosion inhibition of mild steel in H2SO4[J]. Corrosion Science,2013,75:184-192.
[17] 王佳,曹楚南,陈家坚,等. 缓蚀剂阳极脱附现象的研究I缓蚀剂阳极脱附现象[J]. 中国腐蚀与防护学报,1995,15(4):241-246.
[18] 曹楚南,张鸣镝,林海潮. 铁在盐酸中的缓蚀剂的两种作用类型的研究[J]. 腐蚀科学与防护技术,1992,4(1):1-8.
[19] BOMMERSBACH P,ALEMANY-DUMONT C,JEAN-PIERRE M,et al. Hydrodynamic effect on the behaviour of a corrosion inhibitor film: characterization by electrochemical impedance spectroscopy[J]. Electrochimica Acta,2006,51:4011-4018.
[20] SCHWEINSBERG D P,ASHWORTH V. The inhibition of the corrosion of pure iron in 0.5 M sulphuric acid by n-alkyl quaternary ammonium iodides[J]. Corrosion Science,1988,28:539-545.
[21] LAGRENEE M,MERNARI B,BOUANIS M,et al. Study of the mechanism and inhibiting efficiency of 3,5-bis(4-metylthiophenyl)-4H-1,2,4-triazole on mild steel corrosion in acidic media[J]. Corrosion Science,2002,44:573-588.
欢迎订阅《腐蚀与防护》纸质/电子期刊
《腐蚀与防护》杂志创刊于1980年,为上海市腐蚀科学技术学会的会刊,也是国内创办最早的腐蚀专业杂志之一,由上海材料研究所主办。
《腐蚀与防护》杂志定价为每期15元,全年180元,各地邮局均可订阅,订阅代号:4-593,也可向本刊编辑部订阅。
为了倡导环保理念,本刊同时推出电子期刊,采用PDF格式用E-Mail形式发送给读者。全年订阅70元,半年40元,费用低且比邮局发行快10天左右。如需订阅,请您登录www.mat-test.com网站填写订阅信息,并把订阅款项打入指定银行或邮局,收到款后我们会及时将电子期刊发送给您。
联系电话:021-65527634;E-mail:wm@mat-test.com;联系人:王敏
Corrosion Inhibition of 2,4-Diaminopyrimidine to Cold Rolled Steel in HCl Solution
LI Xiang-hong1,2, XIE Xiao-guang2
(1. Faculty of Science, Southwest Forestry University, Kunming 650224, China;2. School of Chemical Science and Technology, Yunnan University, Kunming 650091, China)
The corrosion inhibition of 2,4-diaminopyrimidine (DAP) to cold rolled steel (CRS) in 1.0 mol/L HCl solution was studied through immersion test, electrochemical test and scanning electron microscopy (SEM). The results show that DAP was a good inhibitor for CRS in HCl solution. The inhibition efficiency increased with the increase of the concentration of DAP, and the maximum inhibition efficiency could reach as high as 94.8% when the concentration of DAP was 10.0 mmol/L. DAP acted as a mixed-type inhibitor and the adsorption of DAP on the surface of cold rolled steel obeyed Langmuir adsorption isotherm. As the temperature rose, the inhibition efficiency decreased.
cold rolled steel; HCl solution; 2,4-diaminopyrimidine (DAP); corrosion inhibition; adsorption
2015-08-02
国家自然科学基金项目(51361027); 西南林业大学科研启动基金项目(111435); 云南省中青年学术和技术带头人后备人才项目(2015HB049)
李向红(1981-),副教授,博士,从事缓蚀剂研究,18987172120,xianghong-li@163.com
10.11973/fsyfh-201612001
TG174.42
A
1005-748X(2016)12-0949-07
