PCB电镀铜添加剂作用机理研究进展
2016-12-23肖定军
彭 佳, 程 骄,王 翀, 肖定军, 何 为
(1.电子科技大学 应用化学系,四川 成都 610054; 2.广东光华科技股份有限公司,广东 汕头 515061)
PCB电镀铜添加剂作用机理研究进展
彭 佳1,2, 程 骄2,王 翀1,2, 肖定军2, 何 为1,2
(1.电子科技大学 应用化学系,四川 成都 610054; 2.广东光华科技股份有限公司,广东 汕头 515061)
添加剂是PCB镀铜溶液中的重要组成部分,在电镀过程中发挥着不可替代的作用。添加剂能有效改善电镀过程中的电流分布,提高镀液的均镀能力,控制铜离子从溶液本体到反应界面的运输与电结晶过程,从而影响PCB板面微观凹处和微观凸处的电化学沉积速率。然而添加剂的作用并不是单一组分添加剂所发挥作用的简单叠加,它们之间存在着复杂的协同作用或对抗竞争作用。为了更好地指导电镀铜添加剂配方的研发,提高电镀工艺水平,结合目前国内外相关的文献报道对电镀工艺中添加剂间的相互作用进行分析和概述。其中包括氯离子、加速剂、抑制剂、整平剂之间的相互作用。
添加剂; 电镀铜; 作用机理; 印制线路板
引言
金属铜具有电阻率低、可靠性高及延展性好等特性,目前被广泛用作超大集成电路和PCB板制造中的互连材料。实现PCB层间电气互连主要有三种方式:盲孔、通孔和埋孔。而电镀铜工艺作为PCB制造中重要工序之一,常常用于电镀铜层加厚(通孔,图形电镀)或电镀盲孔填充,以实现PCB层间电气互连。添加剂是PCB电镀液中的重要组成部分,在电镀过程中发挥着不可替代的作用。添加剂能有效改善电镀过程中的电流分布,提高镀液的均镀能力,影响铜离子从溶液本体到反应界面的运输与电结晶过程,从而改变板面微观凹处和微观凸处的电化学沉积速率[1]。
PCB电镀铜添加剂一般包括氯离子、加速剂、抑制剂和整平剂。添加剂的作用效果并不是单一组分所发挥作用的简单叠加,它们之间存在着复杂的相互作用(协同作用或对抗竞争作用)。只有在特定种类添加剂组合及合适的配比下,才能实现电镀板面光亮、整平,且孔内电镀效果良好的目的[2]。因此,为了更好地指导电镀铜添加剂配方的研发,提高电镀工艺水平,本文结合目前国内外相关的文献报道对电镀工艺中添加剂及其间的相互作用进行分析和综述。
1 电镀添加剂作用
PCB电镀铜添加剂一般由氯离子、加速剂(accelerator)、抑制剂(suppressor)和整平剂(leveler)组成,其中加速剂、抑制剂、整平剂的典型结构类型如图1所示。
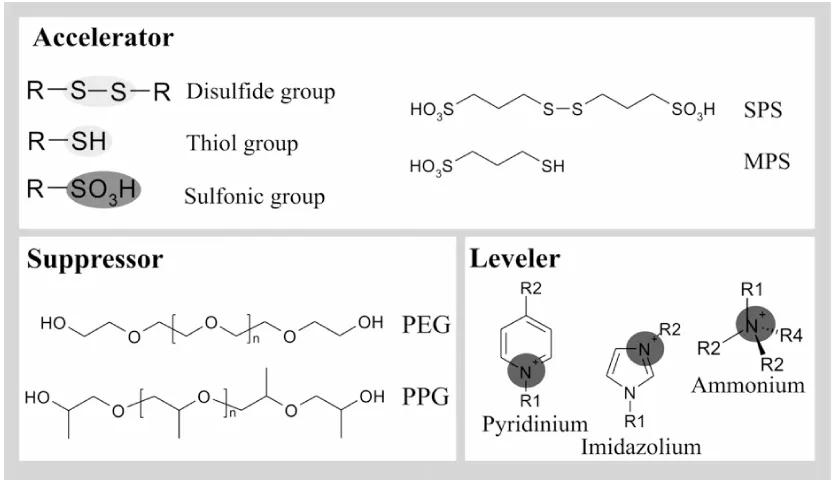
图1 镀铜添加剂结构简图
1.1 氯离子
氯离子是酸性镀铜液中必不可少的物质,通常以氯化钠或盐酸的形式添加到镀铜液中。氯离子在电镀过程中主要发挥三个方面的作用:1)作为铜离子与金属铜之间电子传递桥梁;2)适量的氯离子可以降低阴极极化,与有机添加剂相互作用,实现镀层的光亮、整平;3)提高阳极活性,在阳极表面形成一层均匀的阳极膜,帮助均匀溶解咬蚀磷铜球。
在无其他有机添加剂存在时,氯离子能表现出一定的加速性能,但它能与亚铜离子络合,形成不溶性“Cu(Ⅰ)-chloride”络合物薄膜,该络合物薄膜将会沉积在铜表面从而阻碍铜沉积过程。此时铜电镀沉积过程可以用四个基元步骤来表示[如反应(1)~(4)]。而有其他有机添加剂的加入时,它将与各添加剂相互作用,形成更复杂的络合物以实现盲孔的超共形填充。
Cu2++2Cl-+e-→CuCl2-
(1)
CuCl2-+e-→Cu2++2Cl-
(2)
Cu++Cl-→CuCl
(3)
CuCl+Cl-→CuCl2-
(4)
1.2 加速剂
加速剂通常是小分子脂肪族含硫有机物。在电镀过程中,加速剂有利于晶核的形成,发挥着细化晶粒的作用,使晶核分布致密,促使镀铜层变得平滑并得以反光。但单独使用时其不能起到加速的作用,反而会阻化金属铜的沉积。加速剂只有在复合添加剂中才能发挥加速效果。其典型功能化官能团有二硫键(—S—S—)、磺酸基团(—SO3—)以及巯基(—SH)。目前研究较多的光亮剂为聚二硫二丙烷磺酸钠(SPS)和3-巯基丙烷磺酸钠(MPS)。有研究表明在电镀铜的电位范围内,SPS分子本身的化学特性和电化学特性都不活泼,其在电镀反应过程中所发挥的加速作用主要是由于SPS分子中的二硫键在电场作用下发生裂解,形成MPS;而MPS则曾被认为是电镀过程中真正的加速剂[3]。DOW等[4]认为MPS或是SPS能加速电镀铜沉积是因为MPS或是SPS利用其硫醇官能基吸附在阴极铜面上,然后其末端的磺酸根阴离子会捕捉镀液中被水合的铜离子,使其先破水合作用,然后再与吸附在阴极表面上的氯离子产生交互作用,让电子透过氯离子传递给被磺酸根阴离子捕捉的铜离子,因而可以大幅提升铜离子的电化学还原速率。相关具体吸附模型及作用机制如图2所示。

图2 MPS加速作用机理及迁移作用机制[4]
1.3 抑制剂
整体上可把抑制剂分为两种类型,如图3所示。type Ⅰ是第一类抑制剂,是典型的抑制剂。在氯离子协同作用下,抑制剂在阴极表面吸附,最终达到抑制板面金属铜沉积的作用。同时,使高低电流区的差异降低(亦即增加极化电阻),让电镀铜能均匀的持续沉积。抑制剂可充当润湿剂,降低界面的表面张力(降低接触角),让镀液更容易进入孔内而增加传质效果。研究表明,抑制剂的抑制性能取决于它在铜/电解液界面上形成的那一层致密聚合物膜,在电镀过程中,此致密聚合物膜不会被大量并入到沉积铜层里,而是持续一个吸附-解吸过程(从旧铜层上解吸,到新铜层上吸附),从而不断吸附在新沉积的铜层表面,以作为一扩散阻挡层限制铜离子到铜表面的扩散。抑制剂的抑制效果归因于其或由其产生的中间产物在阴极表面吸附而产生“堵塞效应”(blocking effect),导致铜沉积活性位点的堵塞。目前研究最多的典型的抑制剂为聚醚类有机高分子,如聚乙二醇(PEG)、聚丙二醇(PPG)以及环氧已烷(EO)与氧化丙烷(PO)的三嵌段聚合物(EPE)。抑制剂的抑制效果与它们自身分子结构有关。一般来说,抑制剂的抑制效果会随着聚合物链中PO重复单元比例的增加而增加。但是作为一种疏水性基团,长PO链将会使聚合物分子不溶于水,因此常需要一些EO基团来增加其亲水性。有研究发现[5],抑制剂链中EO与PO的比值将直接决定其在电镀过程中的抑制效果大小。
type Ⅱ是第二类抑制剂,是通常说的整平剂。它是一种含氮的有机单体或者是聚合物,带有很强的正电性,包括多胺以及胺类与环氧烷或氯代醇衍生物的合成产物。整平剂表现出来的作用也是抑制作用。抑制剂类型Ⅰ(如PAG)有选择性形成有效阻挡铜扩散膜的特性,从而阻挡亚铜离子扩散到铜表面。抑制剂类型Ⅱ(如PEI)则没有选择性,但因其本身带有正电荷,基于阴阳离子对效应,它会与所有化学吸附在铜面上的阴离子相互作用。目前也有另一种抑制剂的合成,该抑制剂同时兼具抑制剂类型Ⅰ和抑制剂类型Ⅱ的功能团,如图3中抑制剂IBDGE。

图3 不同类型抑制剂基本结构
2 电镀添加剂间的相互作用
添加剂在电镀过程中发挥的作用各不相同,通常描述的添加剂的加速能力或抑制能力都不只是它们自身的固有能力,而是添加剂相互作用的结果,单一添加剂所发挥作用的简单叠加也并不能达到良好的电镀效果。有研究表明[6]各添加剂之间存在着相互作用,它们间的协同作用或对抗作用将导致它们在反应界面上形成更多、更复杂的分子络合物,而这些复杂的分子络合物才是使它们发挥加速效果或抑制效果的原因。而各添加剂活动行为之间的相互作用具有时间依赖性,不同的时间段它们间的作用模式也会不同[7]。
2.1 氯离子与加速剂间的作用
氯离子与加速剂之间存在着协同作用。研究证明[8],吸附物与基质间存在强烈的相互作用,当SPS或MPS单独加入电镀槽液中时,加速剂作为一种吸附物质将强烈吸附在铜表面,吸附的硫醇(RSH)分子将会改建最表面一层(M)的基质,形成不溶性的硫醇-铜络合物(RS-M)薄膜[反应式(5)],这种不溶性络合物薄膜将起到抑制作用,阻化铜沉积过程。而氯离子的加入,则将SPS或MPS由这种具有微弱抑制特性的抑制剂变为温和的加速剂[9],因为氯离子的存在不但能有效阻止硫醇-铜络合物沉淀的产生,而且能与亚铜离子、加速剂形成更稳定的、溶于水的配位复合体[Cu(Ⅰ)-Cl-thiolate]-[反应式(6)]。Vereecken等[10]研究认为,这种稳定后的亚铜离子络合物能够加速电镀铜沉积过程。
2Cu+SPS→2Cu(Ⅰ)(thiolate)
(5)
CuCl+SPS→CuCl(thiolate)-+H+
(6)
CuCl+SPS→Cu(Ⅰ)(thiolate)+Cl-+H+
(7)
如反应式(7)所示,氯离子与加速剂之间也存在着竞争吸附作用。因铜表面的吸附位点有限,SPS与氯离子在铜表面的吸附存在竞争吸附的关系,这种竞争吸附会引起化学吸附在金属铜表面的阴离子层发生变化,能使抑制剂(典型抑制剂,如PAG)失去活性。首先提出这种竞争吸附关系的是Bae等[11],他们认为氯离子形成的c(2×2)-Cl点阵结构能够有效阻挡SPS的吸附。他们用氯修饰后的铜(100)晶面作为模型基质,再加入SPS,但STM观察发现最先吸附形成的c(2×2)-Cl表面结构没有发生明显变化。而Moffat等[12]揭示了大多数情况下SPS的吸附构型,他们发现在完整的c(2×2)-Cl晶格点阵上存在一横向移动的SPS物理吸附层,当改变电极电位使其接近或超过c(2×2)-Cl结构断裂电位范围时,SPS将会吸附在裸露的铜表面,吸附分解后形成p(2×2)-MPS层。而这一SPS物理吸附层Bae等是没有观察到的。Hai等[13]也同意此竞争状态的存在,他们认为在无反应发生时,氯离子比SPS更快地在铜(100)晶面吸附、排序,形成c(2×2)-Cl吸附层,有效地阻挡了SPS的吸附。此时,游离SPS如要在铜面上吸附,就需要在氯离子距阵基体上产生缺陷位点。而在有反应发生时,不断沉积的铜表面使得阴离子不断重复着快速吸附/解吸/吸附过程,此过程就将导致氯离子吸附层上产生缺陷位点,而缺陷位点一旦产生,SPS将会吸附在裸露的铜表面,其在铜表面的分解产物MPS就会与氯离子共吸附在铜表面形成混合的、有更多缺陷位点的c(2×2)Cl-MPS吸附层。
2.2 氯离子与抑制剂间的作用
2.2.1 氯离子与典型抑制剂间的相互作用
在电镀过程中,氯离子作为一种必不可少的成分,极大地影响着抑制剂的抑制效果。它能够与抑制剂和亚铜离子交互作用形成Cu+-抑制剂-Cl-络合物,如反应式(8)所示。
nCuCl+HO((CH2)XO)yH→
HO((CH2)xOCuCl)n((CH2)XO)y-nH
(8)
该络合物将吸附在阴极表面,产生堵塞钉扎效应,阻挡铜离子或亚铜离子扩散到铜板面,从而抑制铜离子的还原。当基本镀液中缺少氯离子时,抑制剂仅能靠静电作用力或范德华力吸附在阴极表面,但这种吸附强度是很弱的,以致不能有效地抑制铜沉积[14]。有大量文献对聚醚类抑制剂与氯离子在铜电极表面上的合作吸附关系进行了报道,认为聚醚类抑制剂与氯离子的这种合作吸附作用能够增加铜电极表面的过电位。因为氯离子的存在为抑制剂的吸附提供强的结合位点[15],刚开始沉积铜时,氯离子首先快速特性吸附在铜表面[16],化学吸附后的氯离子作为配位结合的离子[8,17],再与抑制剂进行配位。Xiao N等[18]提出了EPE2900具体吸附作用模型,如图4所示,此模型揭示了目前大多数聚醚类抑制剂的作用机制。Feng Z V等[19]用表面增强拉曼光谱等分析手段证明Cl-Cu-PEG络合物确实存在于电极表面,此外,他们通过理论计算与详细的推理过程发现在这种复杂的络合物中,铜除与一个Cl配位外,还与PEG中的两个氧原子O进行配位。

图4 EPE2900在阴极表面可能存在的吸附模型
2.2.2 氯离子与整平剂间的相互作用
氯离子作为一种阴离子,可通过阴阳离子对效应与带有正电荷的整平剂发生静电耦合作用。从电化学的观点来看,整平剂是一种不会被加速剂去活化的抑制剂。因此,类似于氯离子与抑制剂间的相互作用,氯离子与整平剂间也存在着协同作用,最大限度的增加过电位,使电镀填孔后板面得以整平。
2.3 加速剂与抑制剂间的作用
在盲孔电镀的过程中,光亮剂作为一种去极化剂,主要分布在盲孔的底部,降低该位置的铜还原过电位,从而加速盲孔底部铜沉积。有研究发现随着光亮剂浓度的增加,其降低阴极铜还原电位的能力也持续增加[20]。但随着加速剂浓度越来越大,阴极电位会增加到一个最大值,意味着加速剂在阴极上达到了饱和吸附的状态,这时再增加其浓度对阴极电位没什么影响。此外,阴极电位越大并不意味着盲孔填充效果越好,Lu X等[21]证明了一定范围内的光亮剂含量增加,能增大盲孔填充率,但过高的光亮剂含量会影响抑制剂对板面铜沉积的抑制效果,从而使填充率下降。
2.3.1 光亮剂与典型抑制剂的相互作用
典型的抑制剂如第一类抑制剂与光亮剂之间存在对抗作用。加速剂作为抑制剂的去活化剂,对抑制剂有去极化作用,即灭活作用。Joshua W等[22]在研究不同抑制剂条件下SPS的加速效果时,发现无加速剂存在时抑制剂的抑制效果更强。
抑制剂的作用功效主要在板面上,而加速剂的贡献主要体现在盲孔底部,因为某些物理原因及电镀液强制对流等因素的差异,抑制剂与加速剂在铜表面上存在竞争吸附的关系。相对于加速剂,抑制剂先在板面上特性吸附形成一层CuCl-抑制剂薄膜,随后加速剂吸附在板面上,与抑制剂产生竞争吸附关系,部分抑制剂吸附位点就会被加速剂吸附取代。如反应式(9)所示。
HO((CH2)xOCuCl)n((CH2)xO)y-nH+nMPS→HO((CH2)xO)yH+nCl-+nCu(Ⅰ)(thiolate)
(9)
目前,已建立各种关系模型来描述加速剂与抑制剂之间的这种相互作用。Hebert等[23]利用加速剂与抑制剂之间的竞争吸附关系来描述于循环伏安测试过程中出现的迟滞现象,认为一旦铜表面从抑制剂形成的膜中裸露出来,加速剂就会在裸露的铜面吸附形成Cu(Ⅰ)(thiolate)ad膜,阻止CuCl的形成。而CuCl络合物对于抑制剂重新吸附是至关重要的[24][反应式(4)],CuCl的减少将影响抑制剂的吸附过程,最终导致滞后现象的发生。Huynh等[25]用表面覆盖模型来描述加速剂与抑制剂的这种相互作用,他认为有效表面覆盖度等于抑制剂或其中间体所覆盖的受抑制部分区域减去因加速剂作用而恢复到无抑制效果的区域。也有研究[26]认为SPS在氯点阵的表面的物理吸附将空间阻挡抑制剂与氯离子的相互作用。同时,氯作为抑制剂与铜表面的链接剂,物理吸附上一层加速剂后,将会造成抑制剂复合产物的瓦解。而这种瓦解作用,有研究[27]认为是游离MPS通过络合抑制剂络合物中的Cu(Ⅰ)而在结构上瓦解PAG-Cu(Ⅰ)-Cl抑制剂薄膜,因为阴离子MPS对Cu(Ⅰ)具有很强的络合能力。Tan M等[28]用示意图5来描述SPS对PAG-Cu(Ⅰ)-Cl抑制剂薄膜的灭活作用,此模型目前已被大多数人所认同接受。
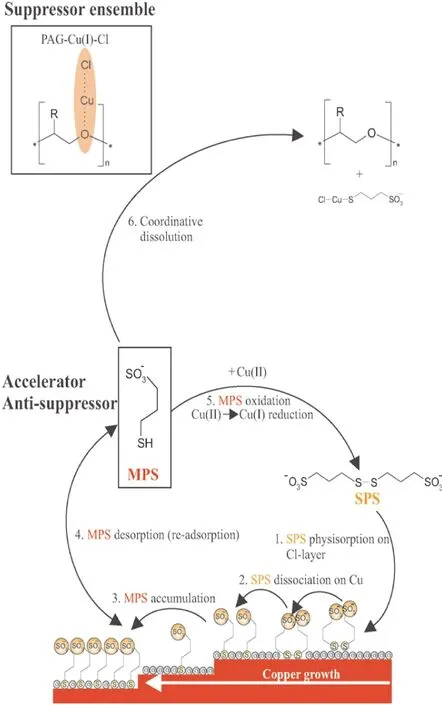
图5 SPS结构上瓦解PAG-Cu(Ⅰ)-Cl抑制剂薄膜反应机理示意图[28]
除此之外,加速剂对抑制剂还存在一定的性能依赖性。之前已经提到加速剂和氯离子的交互作用能加速铜沉积速率,但Moffat T等[29]在研究中发现无抑制剂存在时,即使有氯离子加入,小浓度的SPS仍起抑制效果,而无加速作用。目前已有大量的实验事实证明Hung的研究发现是正确的,在无抑制剂存在的条件下,加速剂没有明显的加速效果。为解释该现象产生的原因,有研究发现[30]抑制剂的加入能够增加加速剂的吸附量。他们认为加速剂的吸附具有电位依赖性,而抑制剂的加入会导致电位转移,过电位的增加将引起加速剂吸附量的增加。同时,抑制剂的加入也将使得加速剂并入消耗速率减小。
2.3.2 光亮剂与整平剂(抑制剂类型Ⅱ)的相互作用
整平剂含有带正电的氮阳离子,加速剂拥有带负电的磺酸基团,他们之间可通过静电吸引而产生离子对间的相互作用。作为另一种抑制剂类型(typeⅡ),整平剂不会被SPS光亮剂灭活(相对于SPS对PAG典型抑制剂的灭活作用)。Dow W P等[31]在研究十二烷基三甲基溴化铵(DTAC)控制“bump”形成的作用效果时认为,DTAC通过离子对效应对SPS具有减活化作用。Broekmann等[8]发现在往含有整平剂的电镀液中加入SPS时,电极过电位有了不可忽视的增大。这说明,不同于与典型抑制剂间的相互作用,加速剂与整平剂之间存在着协同作用而无对抗作用。随后Tan M等[28]也同样发现和聚乙烯亚胺(PEI)与SPS间的协同作用,为此他们提出了可能的理论模型来解释此协同作用机制,如图6所示。
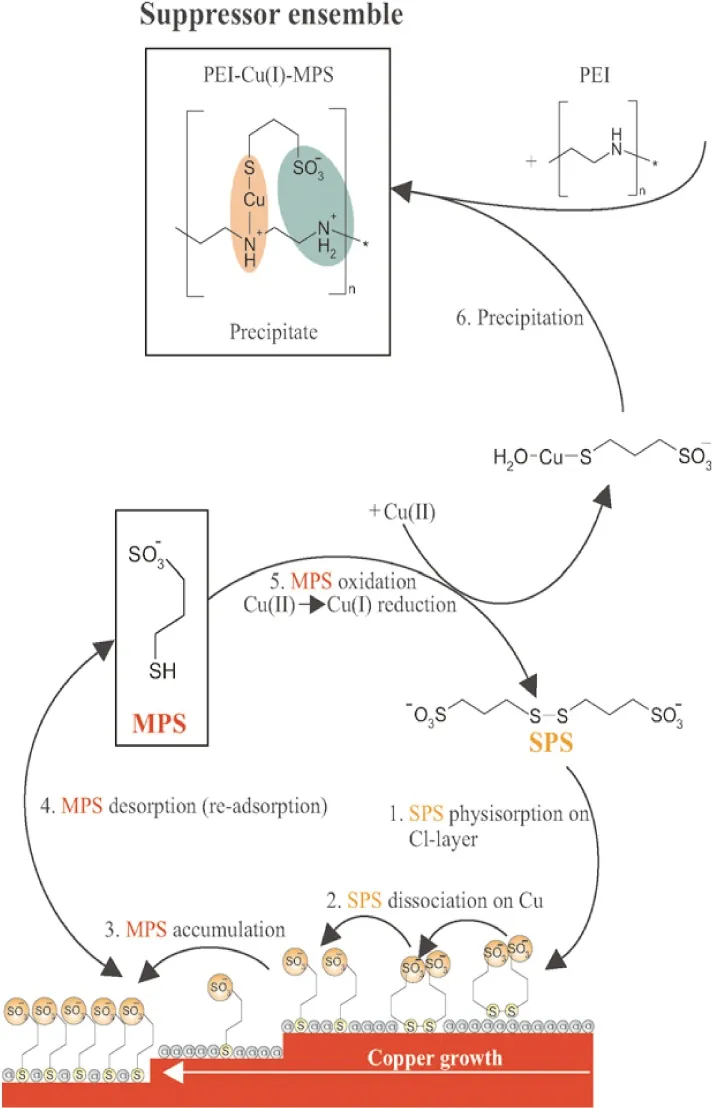
图6 SPS与整平剂PEI间协同作用生成PEI-Cu(Ⅰ)-MPS抑制剂反应机理示意图[28]
同时,加速剂与整平剂间也存在着竞争吸附的关系,这种竞争吸附作用很大程度上取决于对流强度,因为整平剂具有“convection-dependent”的特性。一般来说,在低流速下,起主导作用的主要是光亮剂,而在高转速下,整平剂将发挥其主导作用,取代光亮剂吸附于金属表面。Kim等[32]对此竞争吸附关系进行了解释。
2.4 整平剂与抑制剂间的相互作用
Dow W P等[31]认为整平剂JGB与抑制剂PEG间存在协同作用,形成一复合抑制剂,这种复合抑制剂对铜沉积的抑制效果比PEG和JGB的作用效果更强,并强调该协同作用的强度与对流有关。也有文献报道了一种以胆碱为基础、含有两个季铵结构的整平剂,在强对流条件下,此整平剂能与抑制剂共吸附在金属表面,该共吸附作用(也可称协同抑制作用)能有效增强对铜沉积的抑制效果。
3 结 论
本文结合目前国内外相关的文献报道对PCB电镀工艺中添加剂间的相互作用进行分析和综述。添加剂之间的相互作用复杂且多变。目前关于这方面的研究有很多,但还没有完全的定论。随着添加剂的不断开发,特别是多功能化添加剂的合成,添加剂间的作用将会更多样化,其在电镀过程中的作用机理也将会更复杂。
[1] Pasquale M A,Gassa L M,Arvia A J.Copper electrodeposition from an acidic plating bath containing accelerating and inhibiting organic additives[J].Electrochimica Acta,2008,53(20):5891-5904.
[2] Andricacos P C,Uzoh C,Dukovic J O,et al.Damascene copper electroplating for chip interconnections[J].IBM Journal of Research and Development,1998,42(5):567-574.
[3] Broekmann P,Mayer D.Function through structure:An atomistic view on the additive action at copper/electrolyte interfaces[C].2010 IEEE International Interconnect Technology Conference.IEEE,2010:1-3.
[4] Dow W P,Chiu Y D,Yen M Y.Microvia filling by cu electroplating over a au seed layer modified by a disulfide[J].Journal of The Electrochemical Society,2009,156(4):D155-D167.
[5] Gallaway J W,Willey M J,West A C.Acceleration kinetics of PEG,PPG,and a triblock copolymer by SPS during copper electroplating[J].Journal of The Electrochemical Society,2009,156(4):D146-D154.
[6] Akolkar R,Landau U.Mechanistic analysis of the "bottom-up" fill in copper interconnect metallization[J].Journal of The Electrochemical Society,2009,156(9):D351-D359.
[7] Moffat T P,Wheeler D,Edelstein M D,et al.Superconformal film growth:Mechanism and quantification[J].IBM Journal of Research and Development,2005,49(1):19-36.
[8] Broekmann P,Fluegel A,Emnet C,et al.Classification of suppressor additives based on synergistic and antagonistic ensemble effects[J].Electrochimica Acta,2011,56(13):4724-4734.
[9] Chen H M,Parulekar S J,Zdunek A.Interactions of chloride and 3-mercapto-1-propanesulfonic acid in acidic copper sulfate electrolyte[J].Journal of The Electrochemical Society,2008,155(5):D349-D356.
[10] Vereecken P M,Binstead R A,Deligianni H,et al.The chemistry of additives in damascene copper plating[J].IBM Journal of Research and Development,2005,49(1):3-18.
[11] Bae S E,Gewirth A A.In situ ec-stm studies of mps,sps,and chloride on cu (100):Structural studies of accelerators for dual damascene electrodeposition[J].Langmuir,2006,22(22):10315-10321.
[12] Moffat T P,Yang L Y O.Accelerator surface phase associated with superconformal Cu electrodeposition[J].Journal of The Electrochemical Society,2010,157(4):D228-D241.
[13] Hai N T M,Huynh T T M,Fluegel A,et al.Competitive anion/anion interactions on copper surfaces relevant for Damascene electroplating[J].Electrochimica Acta,2012,70:286-295.
[14] Kelly J J,West A C.Copper deposition in the presence of polyethylene glycol I.Quartz crystal microbalance study[J].Journal of The Electrochemical Society,1998,145(10):3472-3476.
[15] Healy J P,Pletcher D,Goodenough M.The chemistry of the additives in an acid copper electroplating bath:part I.Polyethylene glycol and chloride ion[J].Journal of Electroanalytical Chemistry,1992,338(1):155-165.
[16] Suggs D W,Bard A J.Scanning tunneling microscopic study with atomic resolution of the dissolution of Cu (100) electrodes in aqueous chloride media[J].The Journal of Physical Chemistry,1995,99(20):8349-8355.
[17] Kelly J J,West A C.Copper deposition in the presence of polyethylene glycol II.Electrochemical impedance spectroscopy[J].Journal of The Electrochemical Society,1998,145(10):3477-3481.
[18] Xiao N,Li D,Cui G,et al.Adsorption behavior of triblock copolymer suppressors during the copper electrodeposition[J].Electrochimica Acta,2014,116:284-291.
[19] Feng Z V,Li X,Gewirth A A.Inhibition due to the interaction of polyethylene glycol,chloride,and copper in plating baths:a surface-enhanced Raman study[J].The Journal of Physical Chemistry B,2003,107(35):9415-9423.
[20] Qin Y,Li X H,Xue F,et al.Effect of additives on shape evolution during electrodeposition -III.Trench infill for on-chio interconnects[J].Journal of The Electrochemical Society,2008,155(3):D223-D233.
[21] Lu X,Yao L,Ren S,et al.A study of bottom-up electroplated copper filling by the potential difference between two rotating speeds of a working electrode[J].Journal of Electroanalytical Chemistry,2014,712:22-32.
[22] Gallaway J W,Willey M J,West A C.Acceleration kinetics of PEG,PPG,and a triblock copolymer by SPS during copper electroplating[J].Journal of The Electrochemical Society,2009,156(4):D146-D154.
[23] Hebert K R.Analysis of current-potential hysteresis during electrodeposition of copper with additives[J].Journal of The Electrochemical Society,2001,148(11):C717-C732.
[24] Teerlinck I.Electrochemical Copper Deposition in IC Manufacturing[D].Ph.D.Thesis,Universiteit Gent in collaboration with IMEC,Leuven,Belgium,2002,Chapter 5.
[25] Huynh T M T,Weiss F,Hai N T M,et al.On the role of halides and thiols in additive-assisted copper electroplating[J].Electrochimica acta,2013,89:537-548.
[26] Hai N T M,Kramer K W,Fluegel A,et al.Beyond interfacial anion/cation pairing:The role of Cu(I) coordination chemistry in additive-controlled copper plating[J].Electrochimica Acta,2012,83:367-375.
[27] Hung C C,Lee W H,Chang S C,et al.Suppression effect of low-concentration bis-(3-sodiumsulfopropyl disulfide) on copper electroplating[J].Journal of The Electrochemical Society,2008,155(2):D133-D136.
[28] Tan M,Harb J N.Additive behavior during copper electrodeposition in solutions containing Cl-,PEG,and SPS[J].Journal of The Electrochemical Society,2003,150(6):C420-C422.
[29] Moffat T,Kim S K,Josell D.Control of overfill bumps in damascene cu electrodeposition[J].ECS Transactions,2007,2(6):93-106.
[30] Moffat T P,Wheeler D,Kim S K,et al.Curvature enhanced adsorbate coverage model for electrodeposition[J].Journal of The Electrochemical Society,2006,153(2):C127-C132.
[31] Dow W P,Huang H S,Yen M Y,et al.Influence of convection-dependent adsorption of additives on microvia filling by copper electroplating[J].Journal of The Electrochemical Society,2005,152(6):C422-C434.
[32] Kim M J,Seo Y,Kim H C,et al.Galvanostatic bottom-up filling of TSV-like trenches:Choline-based leveler containing two quaternary ammoniums[J].Electrochimica Acta,2015,163:174-181.
Research Progress of the Interactions among the Additives of Copper Electroplating in PCB Manufacturing
PENG Jia1,2, CHENG Jiao2, WANG Chong1,2, XIAO Dingjun2, HE Wei1,2
(1.Department of Applied Chemistry,University of Electronic Science and Technology of China,Chengdu 610054,China; 2.Guangdong Guanghua Sci-Tech Co.,Ltd.,Shantou 515061,China)
As the important components in copper electroplating solution for PCB manufacturing,additives play irreplaceable roles in the electroplating process.The additives can effectively improve the current distribution in the electroplating process,increase the throwing power of the plating solution and control the electrical transportation of copper ions and the crystallization process from plating solution to reaction interface,which will affect the electrochemical deposition rate in micro concave and micro convex of the PCB panel.But the additive function is not a simple sum of the function of each additive,there are complex synergistic and antagonistic interplay existed between them.For the sake of better guidance of copper electroplating additive formulation research and development,and improving the level of electroplating process,combined with the related literatures both at home and abroad,the interactions between the additives in the electroplating process are analyzed and summarized in this paper.
additives; copper electroplating; interaction; PCB
2016-06-06
2016-07-05
广东省引进创新科研团队计划(项目编号201301C0105324342);国家自然科学基金会资助(No. 61474019)
10.3969/j.issn.1001-3849.2016.12.004
TQ153.14
A
