非心脏手术患儿围术期死亡的危险因素分析和预警系统建立
2016-12-22黄葱葱杜垚强连春微田心毅李军
黄葱葱 杜垚强 连春微 田心毅 李军
非心脏手术患儿围术期死亡的危险因素分析和预警系统建立
黄葱葱 杜垚强 连春微 田心毅 李军
目的 探讨非心脏手术患儿围术期死亡的危险因素,建立预测死亡的风险评分系统。方法 选择2008年1月至2013年12月0~14岁非心脏手术围术期死亡患儿(57例)及非死亡患儿(114例)的临床资料,对其年龄、BMI、ASA分级、是否早产、手术方式、手术类别、体温、血氧饱和度(SpO2)、是否饱胃、手术时间、手术次数、WBC、是否贫血、是否低白蛋白、是否凝血功能异常及是否血电解质异常共17项可能的风险因素进行多因素和单因素分析,确定死亡危险因素,建立预测评分系统。结果 多因素回归确定非心脏手术患儿围术期死亡的危险因素为:年龄>1岁,BMI<15kg/cm2、ASA≥3级、SpO2<96%、饱胃、凝血功能异常(均P<0.05)。非心脏手术患儿围术期死亡发生的风险评分系统如下:年龄<1岁(14分),BMI<15 kg/cm2(17分),ASA≥3级(30分),SpO2<96%(22分),饱胃(16分),凝血异常(27分)(P<0.05或0.01)。根据方程绘制ROC曲线,所对应的非心脏手术患儿发生死亡的风险得分为30.5分,灵敏度为98.2%,特异度为89.5%。如患儿得分>30.5分,则围术期死亡的发生率大大增加。结论 非心脏手术患儿围术期死亡的预警评分系统简单易行,结果可靠,可为围术期死亡的早期发现和干预提供帮助。
小儿 围术期死亡 危险因素 评分系统
死亡是手术患者围术期最为严重的并发症。近十年国外数据显示围术期小儿的病死率有增长趋势[2-3],虽然国内暂无此方面的数据统计,但是围术期安全问题仍不容忽视。本研究收集近些年本院非心脏手术患儿的临床资料,并进行统计分析,筛选出非心脏手术患儿围术期死亡的危险因素,并初步建立预测风险的预警评分系统,现报道如下。
1 对象和方法
1.1 对象 收集2008年1月至2013年12月温州医科大学附属第二医院非心脏手术患儿(年龄≤14岁)围术期死亡(无论何种原因导致术后30d内出现的死亡)的所有病例,同时病案系统电脑随机抽样抽取同一时间段2倍于死亡数量的未死亡患儿作为病例对照分析,最终纳入死亡病例57例(死亡组),男27例,女30例,年龄0~12(1.77±3.24)岁;其中发生于胸外科15例,脑外科17例,骨科34例,普外科88例,泌尿外科17例。对照组114例,男101例,女70例,年龄0~14(3.95±4.66)岁。排除标准:重复登记、资料不完整的病例;家属无法配合进行随访;因手术并发症需再次手术。
1.2 方法
1.2.1 潜在危险因素的入选 低龄(年龄<1岁)、低BMI(<15kg/cm2)、ASA增高(≥3级)、早产(孕周<37周)、手术方式(脑外、胸外手术)、手术类别(3~4类手术)、体温异常(肛温>37.5℃或腋温>37℃)、低血氧饱和度[SpO2(吸空气时SpO2<96%)]、饱胃(禁饮、禁食时间为:固体食物、配方奶、母乳及清饮等分别不足8、6、4、2h)、手术时间(22:00pm~8:00am)、手术次数(再次手术)、WBC异常(>10×109/L)、贫血(<90g/L)、低白蛋白(<35g/L)、凝血功能异常 [APTT延长>10s或PT延长>3s]、血电解质异常(血钾>5.5mmol/L或<3.5mmol/L)。1.3 统计学处理 采用SPSS17.0统计软件。单因素分析采用χ2检验,并以logistics回归对单因素分析中有意义的危险因素进行多因素分析。预测评分模型的效能检验采用ROC曲线,AUC越接近于1,提示诊断效果越好。
2 结果
2.1 非心脏手术患儿围术期死亡危险因素的单因素分析 见表1。
由表1可见,非心脏手术患儿围术期死亡的可能相关因素为性别、年龄、BMI、ASA分级、早产、剖宫产、急诊、SpO2、意识状态、饱胃、手术时间、凝血功能及电解质异常(均P<0.05)。
2.2 非心脏手术患儿围术期死亡危险因素的多因素分析 对单因素分析结果有统计学意义的13个术前因素进行二元logistic回归分析,详见表2。
由表2可见,年龄<1岁,BMI<15kg/cm2、ASA≥3级、SpO2<96%、饱胃、凝血功能异常为非心脏手术患儿围术期死亡相关的独立危险因素(P<0.05或0.01)。
2.3 概率模型 根据logistic分析结果,建立非心脏患儿围术期死亡的预测模型:P概率=exp(LogitP)/(1+exp(LogitP),LogitP=-4.724+1.398×年龄+1.726×BMI+ 2.192×(SpO2<96%)+2.998×ASA+1.631×饱胃+2.714×凝血异常。根据此函数,在各个病例不同危险因素存在时,可计算死亡发生的可能性P值。根据logistic回归模型的特点,对各危险因素进行赋值:年龄<1岁为14,≥1岁为0;BMI<15kg/cm2为17,≥15kg/cm2为0;SpO2<96%为22,≥96%为0;ASA≥3级为30,<3级为0;饱胃为16,非饱胃为0;凝血异常为27,无异常为0。
2.4 评分系统的初步建立 根据171例患儿的相应方程预测率,绘制评分系统预测围术期死亡发生率的ROC曲线,计算不同预测值的特异度和敏感度(图1),AUC为0.977,约登指数为0.877,该方程预测值对应的最佳评分分界点为30.5。根据以上结果,初步建立的非心脏手术患儿围术期死亡的风险预测评分系统如下:年龄<1岁(14分),BMI<15kg/cm2(17分),SpO2<96%(22分),ASA≥3级(30分),饱胃(16分),凝血异常(27分)。如患者得分>30.5分,则围术期死亡的发生率大大增加。
3 讨论
围术期安全问题一直是困扰各大医院的重大医疗问题,全球每年约有2亿患者接受手术[4],术后约有5%~10%的患者合并有严重并发症,甚至死亡[5]。随着医疗技术及设备的发展,小儿围术期病死率总体呈明显下降趋势[6],由1954年的188.9/10 000例降至2006年的1.41/10 000例。然而,2007年美国的一项研究发现,手术室内及麻醉恢复室内的患儿病死率高达6.8/10 000例[2];澳大利亚的一项研究发现,术后24h患儿的病死率高达13.4/10 000例[3]。显然,各项研究在方法学、地域及外科水平等方面存在一定的差别,但小儿围术期病死率是否一直有下降趋势,仍存在争议。相反,不容忽视的是病死率可能存在回升趋势。如何提高围术期安全性,早期识别可能的潜在风险因素,完善术前准备,及早预防和避免不良事件发生,降低围术期病死率是外科和麻醉医师需要重视的问题。小儿麻醉有其独特的生理、心理、解剖和药理学特点以及存在麻醉操作管理等的特殊性,应认识到小儿麻醉的重要性和目前在我国的迫切性[7]。
目前国外对小儿死亡危险评分有小儿风险死亡评分[8](pediatric risk of mortality score,PRISM),新生儿急性生理评分[9]以及小儿并发症预测模型[10]等,前两者是短期病死率的风险评估体系,后者是1年病死率的风险评估体系。本研究尝试建立一个死亡风险预测评分系统以便指导临床工作,对存在高风险的围术期患儿,积极完善各项术前准备,努力纠正各项生理异常,寻求最佳的手术时机,为患儿提供更优质、更完善的围术期管理,最终达到降低围术期病死率的目的。绝大多数围术期死亡都伴随着呼吸系统和循环系统不良事件,而心脏手术作为围术期死亡的高危手术,病死率可达127/10 000例[11],为非心脏手术的20倍。考虑小儿先天性心脏病手术的特殊性,本文仅针对非心脏手术进行回顾性分析。本研究单因素分析结果发现,性别(女)、年龄<1岁,BMI<15kg/cm2、ASA≥3级、SpO2<96%、早产、剖宫产史、急诊、意识模糊、饱胃、手术时间(晚上)、凝血功能异常及血钾异常为小儿非心脏手术围术期死亡的相关危险因素;通过对上述相关危险因素进行多因素分析发现,仅年龄<1岁,BMI<15kg/cm2、ASA≥3级、SpO2<96%、饱胃、凝血功能异常为其独立危险因素。ASA分级是公认的术前麻醉危险分级,其值越高,代表病情越危重,本研究中ASA≥3级被证实为最主要的独立危险因素,与既往研究结果一致[1,11-12]。SpO2作为呼吸循环的重要生理指标,是导致外科术后严重并发症的危险因素[13]。国外研究亦发现ASA≥3级、SpO2<96%为围术期外科手术术后严重并发症的独立危险因素。低龄、低出生体重患儿,尤其是新生儿,常合并发育不良,对麻醉和手术耐受力较差,围术期风险明显增加,与既往研究结果一致[14-16]。本研究中单因素分析有意义的潜在风险因素中,部分在进行logistic回归时被剔除,分析原因可能与样本量不大,手术类型分布不均等相关。虽然ROC曲线下面积显示本评分系统具有较好的准确性,但是单中心、疾病类型、外科水平、样本数量以及地域的差异均有可能成为影响其准确性的重要因素。

表1 非心脏手术患儿围术期死亡危险因素的单因素分析[例(%)]
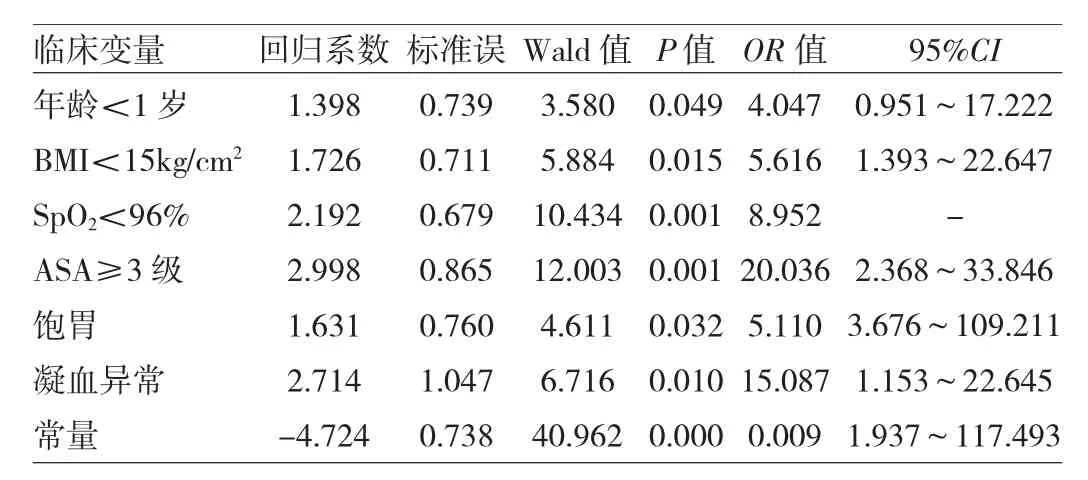
表2 非心脏手术患儿围术期死亡危险因素的多因素分析

图1 围术期死亡发生率的ROC曲线
综上所述,非心脏手术患儿围术期死亡与年龄<1岁,BMI<15kg/cm2、ASA≥3级、SpO2<96%、饱胃和凝血功能异常密切相关,其建立的预警评分系统简单易行,给围术期死亡的早期发现和干预提供了一定的帮助。
[1]Gonzalez L P,Pignaton W,Braz L G,et al.Anesthesia-related mortality in pediatric patients:a systematic review [J].Clinics, 2012,67(4):381-387.
[2]Flick R P,Sprung J,Hanson A C,et al.Perioperative cardiac arrests in children between 1988 and 2005 at a tertiary referral center:a study of 92,881 patients[J].Anesthesiology,2007,106(2): 226-237.
[3]van der Griend B F,Lister N A,Sheppard S J,et al.Postoperative mortality in children after 101,885 anesthetics at a tertiary pediatric hospital[J].Anesth Analg,2011,112(6):1440-1447.
[4]Devereaux P J,Guyatt G,Sigamani A,et al.Characteristics and short-term prognosis of perioperative myocardial infarction in patients undergoing noncardiac surgery:a cohort study[J].Ann intern med,2011,154(8):523-528.
[5]Vincent C,Moorthy K,Sarker S K,et al.Systems approaches to surgical quality and safety:from concept to measurement[J].Ann Surg,2004,239(4):475-482.
[6]Braz LG,Braz D G,Cruz D S,et al.Mortality in anesthesia:a systematic review[J].Clinics,2009,64(10):999-1006.
[7]连庆泉,上官王宁.小儿麻醉现状与展望 [J].浙江医学,2008,30(12): 1281-1284.
[8]Pollack MM,Ruttimann U E,Getson P R.Pediatric risk of mortality (PRISM)score[J].Crit Care Med,1988,16(11):1110-1116.
[9]Richardson D K,Gray J E,Goldmann D A,et al.Score for NeonatalAcute Physiology:a physiologic severity index for neonatal intensive care[J].Pediatrics 1993,91(3):617-623.
[10]Tai D,Dick P,ToT,et al.Development of pediatric comorbidity prediction model[J].Arch Pediatr Adolesc Med,2006,160(3): 293-299.
[11]van der Griend B F,Ragg P G,Sheppard S J,et al.Postoperative mortality in children after 101,885 anesthetics at a tertiary pediatric hospital[J].Anesth Analg,2011,112(6):1440-1447
[12]Biboulet P,Aubas P,Capdevila X,et al.Fatal and non fatal cardiac arrests related to anesthesia[J].Can J Anaesth,2001,48(4): 326-332.
[13]Weinberg A C,Huang L,Retik A B,et al.Perioperative risk factors for major complications in pediatric surgery:a study in surgical risk assessment for children[J].J Am Coll Surg,2011,212 (5):768-778.
[14]BhartiN,Batra YK,Kaur H.Paediatric perioperative cardiac arrest andits mortality:database of a 60-month period from a tertiary care paediatric centre[J].Eur J Anaesthesiol,2009,26(6): 490-495.
[15]BunchungmongkolN,Punjasawadwong Y,Vasinanukorn M,et al. Anesthesia-related cardiac arrest in children:the ThaiAnesthesia Incidents Study(THAI Study)[J].J Med Assoc Thai,2009,92 (4):523-530.
[16]Tremblay A,Bandi V.Impact of body mass index on outcomes following criticalcare[J].Chest,2003,123(4):1202-1207.
Risk factors of perioperative mortality in children with non-cardiac surgery and establishment of a risk scoring system
HUANG Congcong,DU Benqiang,LIAN Chunwei,et al.Department of Anesthesiology,The Second Affiliated Hospital of Wenzhou Medical University,Wenzhou 325027,China
【 Abstract】 Objective To analyze the preoperative risk factors of perioperative mortality in children with non-cardiac surgery and to establish a risk scoring system. Methods Total 171 children aged 0~14,who underwent non-cardiac surgery from January 2008 to December 2013 of non-cardiac surgery in the Second Affiliated Hospital of Wenzhou Medical University, were enrolled in the study,including 57 cases who died perioperatively and 114 cases who survived.The clinical data including age,body mass index(BMI),ASA classification,premature birth,category and types of operations,body temperature,oxygen saturation,full stomach,duration of surgery,number of operations,white blood cell count(WBC),anemia,albumin levels, electrolyte imbalance were retrospectively analyzed.Univariate and multivariate logistic regression analysis was used to determine the independent preoperative risk factors. Results Logistic regression analysis identified that low BMI,ASA classification,SpO2<96%,full stomach and coagulation abnormality were independent risks factors of perioperative mortality in children with non-cardiac surgery(P<0.05).The scoring system was set:age<1y as 14,BMI<15 as 17,ASA≥3 as 30,SpO2<96%as 22,full stomach as 16 and coagulation abnormality as 27.For children with total score>30.5,the incidence of perioperative mortality increased significantly.The ROC of risk scores was used in predicting repioperative mortality,and taking 30.5 as cut-off value the sensitivity was 0.982 and specificity was 0.895. Conclusion The risk scoring system can effectively predict the perioperative mortality for pediatric patients with non-cardiac surgery.
Children Perioperative mortality Risk factors Score system
2016-04-29)
(本文编辑:马雯娜)
浙江省医药卫生平台骨干人才项目(2012ZDA036)
325027 温州医科大学附属第二医院麻醉科(黄葱葱、连春微、田心毅、李军);温州医科大学检验医学院、生命科学学院(杜垚强)
李军,E-mail:lijun0068@163.com
