PEDV疫苗株与野毒株RT-PCR鉴别诊断方法的建立及临床应用
2016-12-21宋予震梁中涛
宋予震 , 董 青 , 梁中涛 , 霍 军
(1.河南牧业经济学院 , 河南郑州450011 ; 2.雏鹰农牧集团 , 河南三门峡472100)
PEDV疫苗株与野毒株RT-PCR鉴别诊断方法的建立及临床应用
宋予震1, 董 青1, 梁中涛2, 霍 军1
(1.河南牧业经济学院 , 河南郑州450011 ; 2.雏鹰农牧集团 , 河南三门峡472100)
根据猪流行性腹泻病毒(PEDV)疫苗株和野毒株在ORF3基因上的差异,我们设计了一对引物用于建立PEDV疫苗株和野毒株的RT-PCR鉴别诊断方法,其中疫苗株PCR扩增产物长度为213 bp,野毒株为262 bp。特异性试验结果表明,该引物对猪传染性胃肠炎病毒、猪轮状病毒、猪瘟病毒、猪伪狂犬病病毒和猪繁殖与呼吸综合征病毒的扩增均为阴性。2014年3月至2015年4月期间利用该方法对河南省51家猪场的581份腹泻样本进行检测,结果发现,PEDV总阳性率为54.9%(391/581),其中野毒株阳性率84.9%(332/391),疫苗株阳性率为15.1%(59/391),说明当前腹泻样本中的PEDV检出率依然较高,且在这些PEDV阳性病料中以野毒感染为主。
猪流行性腹泻病毒 ; 鉴别诊断 ; 临床应用
猪流行性腹泻(PED)是由猪流行性腹泻病毒(PEDV)引起的以仔猪腹泻、呕吐和脱水为主要症状的一种急性、高度接触性肠道传染病。2010年底,猪腹泻疫情在我国大范围流行,给养殖户带来严重的经济损失。PED的广泛流行使得猪场大范围高强度使用腹泻苗进行免疫预防,目前国内主要使用的PED 疫苗既有灭活苗也有弱毒苗,但存在一次免疫后保护期短、抗体效价不高,以及母猪防疫时保定不到位等缺陷,需要多次免疫才能产生足够的抗体。PED疫苗的高强度免疫接种以及接种过程中造成的散毒等情况对PEDV 野毒是一种免疫压力,但同时也是激发PEDV 野毒进行基因重组、遗传变异的刺激因素。本研究旨在建立一种可以区分PEDV 野毒株与疫苗株的RT-PCR 方法,并通过对临床样品进行检测,为PEDV 的诊断提供快速、简便、有效的方法,同时调查PEDV 在免疫压力的情况下疫苗株与野毒株的共存情况。
1 材料与方法
1.1 毒株 猪流行性腹泻疫苗株(CV777株)与猪流行性腹泻野毒株(CH/ZZ/11株)以及两个毒株的相关pMD-ORF3质粒、猪瘟病毒、猪繁殖与呼吸综合征病毒、猪传染性胃肠炎病毒、猪轮状病毒、猪伪狂犬病病毒均由本实验室保存。
1.2 临床样本 581份腹泻样品(粪便或小肠组织及内容物)。
1.3 主要试剂 QIAamp Viral RNA Mini Kit,购自Qiagen公司;RNA酶抑制剂、dNTP Mix ture、反转录酶、随机引物等,均购自宝生物工程(大连)有限公司;2×PCR Reagent,购自天根生化科技(北京)有限公司;其他常用试剂,购自Sigma公司。
1.4 引物设计与合成 根据GenBank上的猪流行性腹泻疫苗株以及野毒株ORF3基因序列,利用Primer Primier7.0软件设计一对特异性引物P1和P2。上游引物P1:5′-CTTGTCTGTGGATGCTGTCCA-3′,下游引物P2:5′-GACTCAACAAAGCCTGCCAAT-3′,预期疫苗株的目的基因大小为213 bp,野毒株目的基因大小为262 bp,引物由宝生物工程(大连)有限公司合成。
1.5 样品处理以及病毒RNA的提取 取适量粪便病料使用PBS(0.01 mol/L,pH值7.2)10倍稀释,小肠组织及内容物加适量PBS后研碎后制备成10%混悬液,将病料混悬液涡旋震荡后,10 000 r/min(4 ℃)离心15 min,收集上清,按照QIAamp Viral RNA Mini Kit说明书进行RNA提取,所提取的RNA置于-20 ℃保存备用。
1.6 cDNA的合成和PCR 参考鼠源反转录酶(M-MLV)说明书合成cDNA,20 μL体系:RNase free ddH2O 11 μL,RNA模板2 μL,5×PrimeScriptBuffer 4 μL,dNTP Mix ture(10 mmol each)1 μL,随机引物(20 pmol/μL)1μL,RNase抑制剂(40 U/μL)0.5 μL,M-MLV(200 U/μL)0.5 μL。反应条件为:42 ℃ 1 h,95 ℃ 5 min。
PCR体系为20 μL:2×PCR Reagent10 μL,cDNA1 μL,上下游引物各1 μL,ddH2O 7 μL。反应条件为:95 ℃ 5 min;然后94 ℃ 1 min,55 ℃ 1 min,72 ℃ 30 s,30个循环;72 ℃ 10 min。
1.7 特异性试验 分别取CSFV、PRRSV、TGEV、PoRV、PRV的cDNA或DNA为模板,以PEDV疫苗株和PEDV野毒株为阳性对照,以灭菌ddH2O作为阴性对照,PCR反应体系及条件同1.6。
1.8 敏感性试验 测定疫苗株和野毒株的pMD-ORF3质粒浓度,调整为统一浓度后按1∶1体积进行混合,并使用灭菌ddH2O对质粒进行连续的10倍稀释,使用稀释的质粒作为模板按照1.6的PCR反应程序进行反应,以灭菌ddH2O作为阴性对照,确定本方法的敏感性。
1.9 稳定性试验 在不同时间,使用不同的已知PEDV阳性和阴性的病料或疫苗进行重复检测,阴性样本与阳性样本各20份,检验本方法的重复性与稳定性。
1.10 临床样本检测 对河南省郑州、新乡、驻马店、信阳、许昌、三门峡、周口、漯河、洛阳9个地区51家猪场进行调查采样,2014年3月至2015年4月共采集腹泻仔猪样本581份,对这些病料使用本方法进行PEDV检测,统计病料中PEDV疫苗株和野毒株所占的比例。
2 结果
2.1 PCR扩增条件的优化 本研究建立的PCR方法由于采用随机引物以及2×PCR Reagent,因此主要对退火温度和时间、延伸时间、P1和P2引物浓度进行摸索和优化。最终确定引物浓度为20 pmol/μL,添加剂量为1 μL,最佳PCR反应条件为:95 ℃ 5 min;然后94 ℃ 1 min,55 ℃ 1 min,72 ℃ 30 s,30个循环;72 ℃ 10 min。所建立的RT-PCR方法能扩增出疫苗株213 bp大小的片段,也能扩增出野毒株262 bp大小的片段,与预期目的基因大小一致(图1)。
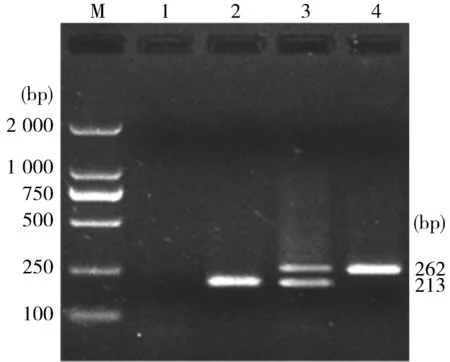
图1 目的基因的RT-PCR扩增
M:DL-2 000 DNA Marker;1:阴性对照;2:PEDV疫苗株扩增产物;3:PEDV疫苗株和野毒株混合物扩增产物;4:PEDV野毒株扩增产物
2.2 敏感性试验结果以灭菌ddH2O做阴性对照,用10倍稀释的混合pMD-ORF3质粒做模板进行PCR扩增,结果表示,本方法可以检测出20.6 pg/μL的混合pMD-ORF3质粒(两种质粒添加到PCR反应体系中各10.3 pg),并且该方法对两种质粒的敏感性相当(图2)。
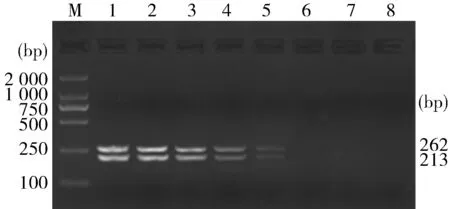
图2 RT-PCR敏感性试验
M:DL-2 000 DNA Marker;1:121 ng;2:20.6 ng;3:2.06 ng;4:206 pg;5:20.6 pg;6:2.06 pg;7:0.206 pg;8:ddH2O
2.3 特异性试验结果 利用本方法对CSFV、PRRSV、TGEV、PoRV、PRV的cDNA或DNA进行PCR扩增,结果对这些病毒的扩增均为阴性,表示本方法特异性良好(图3)。
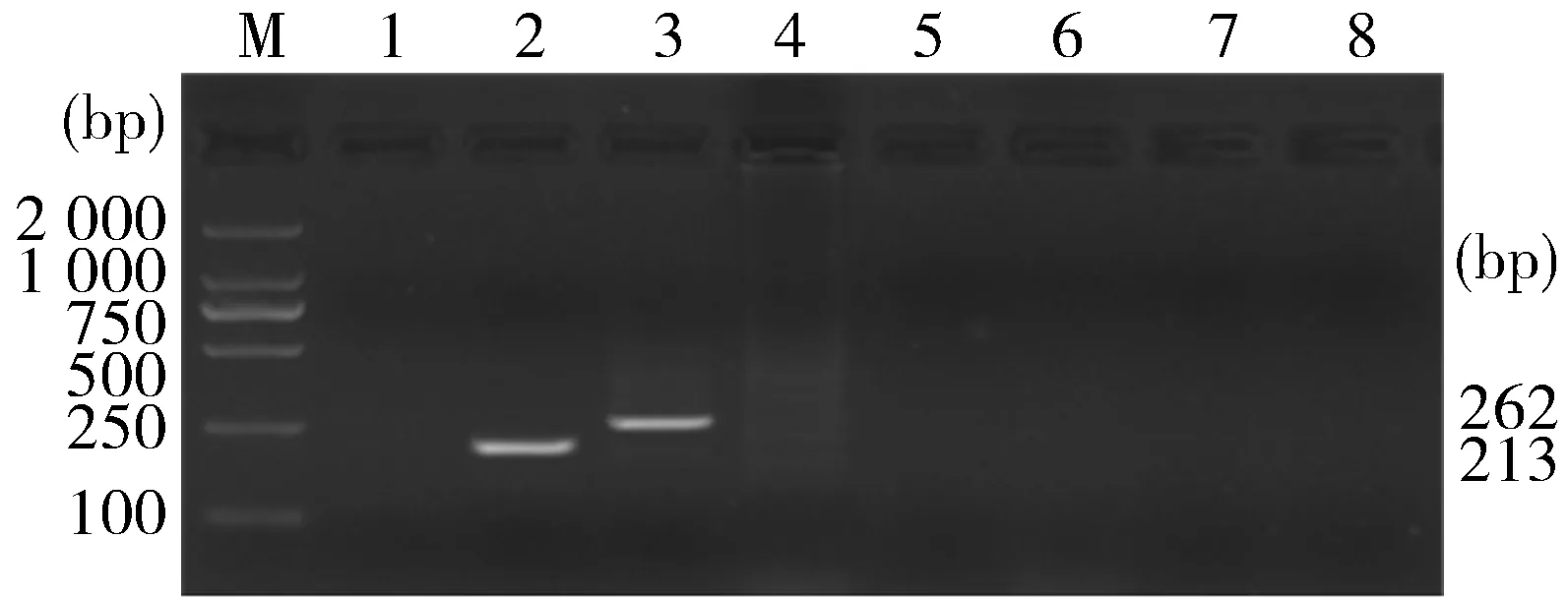
图3 RT-PCR特异性试验
M:DL-2 000 DNA Marker;1:阴性对照;2:PEDV疫苗株;3:PEDV野毒株;4:猪瘟病毒;5:猪繁殖与呼吸综合征病毒;6:猪传染性胃肠炎病毒;7:猪轮状病毒;8:猪伪狂犬病病毒
2.4 稳定性试验 不同时间使用本方法对20份PEDV阴性样本、20份PEDV阳性样本(5份疫苗株或疫苗株传代细胞毒、15份野毒株病料样本)重复检测3次,3次检测结果均一致,表示本方法重复性和稳定性均好。
2.5 临床样品检测结果 对采集的51家猪场581份腹泻样本使用本方法进行检测,结果显示,51家猪场全部为PEDV阳性场,猪场阳性率为100%,581份样本的PEDV阳性率为54.9%(391/581),391份PEDV阳性样本中野毒株阳性率84.9%(332/391),疫苗株阳性率为15.1%(59/391)二者均为阳性的样本2份,占PEDV阳性病料的0%(2/391)。
3 讨论
2010年10月份开始,PED在我国呈现暴发流行,给我国养猪产业带来巨大经济损失,我国各地市均有腹泻疫情报道[1-2]如Sun等[3]报道,中国南方10省暴发的PED疫情导致超过100万头仔猪死亡。2013年美国和古巴也陆续开始流行PED[4-5],PED的流行对生猪及相关产业的贸易交流带来诸多不便。
ORF3基因编码223个或224个氨基酸,是PEDV惟一的附属基因。Wang等[6]的研究表明,ORF3能够编码一种离子通道蛋白,该离子通道的功能对病毒的感染性和致病性有重要影响。ParkS等[7]研究表明,ORF3基因是PEDV毒力的决定性因素之一。对GenBank中PEDV疫苗株与野毒株的ORF3基因序列进行比对分析,发现弱毒株在ORF3基因中存在连续数十个碱基的缺失,但是不同毒株之间ORF3基因的相似性在97.8%以上,周兵强[8]等对ORF3的基因进行分群后发现2010年以后国内流行的绝大多数毒株的同源性高,同属于基因3群,疫苗株CV777株属于基因2群。ORF3基因在疫苗株和野毒株之间的差异性以及ORF3基因的相对保守性为本研究提供良好的理论基础。
由于RNA聚合酶缺乏矫正功能,所以RNA病毒容易发生变异和重组,自从SARS暴发后,人们开始越来越关注冠状病毒的变异情况。基于ORF3的基因分型结果,一般认为与CV777株在同一亚群的毒株为疫苗株演化而来,为人为或者自然情况下野毒株与疫苗株发生基因重组或基因缺失导致。2010年以来,绝大多数猪场采用腹泻疫苗进行免疫预防,相当一部分发生过PED疫情的猪场在使用腹泻疫苗免疫的同时,使用腹泻仔猪病料进行返饲或制备自家灭活苗,高强度的疫苗毒株与野毒株同时存在加速了PEDV的演化,同时也加速了野毒株与疫苗株之间的基因重组。
本研究中疫苗株的阳性率较李长龙等[9]建立的野毒株与疫苗株鉴别PCR方法检测的临床样本中疫苗株比例略高(15/2),除收集病料的地区不同外,推测主要原因为李长龙等收集的是2013年的腹泻病料,本研究收集的为2014年初至2015年初的病料,随时间推进,腹泻样本中疫苗株的阳性率有上升趋势。
本次采集样品的51家猪场中,34家为基础母猪数大于500头的中大型猪场,17家为基础母猪数在100~500头之间的小型猪场。34家中大型猪场采集的387份腹泻病料样品中PEDV阳性病料为299份,病料阳性率76.5%(299/391),PEDV阳性病料中疫苗株阳性48份,占全部疫苗株病料比例的81.4%(48/59)。17家小型猪场采集的131份腹泻病料样品中PEDV阳性病料92份,病料阳性率23.5%(92/391),PEDV阳性病料中疫苗株阳性11份,占全部疫苗株病料比例的18.6%(11/59)。检测出的2份既有疫苗毒又有野毒的病料来源于1家大型猪场。结合这些猪场PED免疫情况,产生这种结果的主要原因与规模化猪场强化PED疫苗免疫有关。规模化猪场在疫苗免疫、抗PEDV抗体制备、自家苗制备、PED治疗等措施方面优于小型猪场;同时PED具有潜伏期长、周期流行性,PED疫苗具有一次免疫后效果差、需要多次加强免疫的特点。导致规模化猪场PEDV疫苗毒和流行毒共存时间长,因此规模化猪场腹泻病料中PEDV阳性率低于小型猪场,但是疫苗株的阳性率高于小型猪场。同一病料中检测出疫苗毒和野毒,表示两者可同时感染。
本方法可区分PEDV疫苗株和野毒株,具有简便、快捷、高效的特点。随着分子诊断在规模化猪场的普及,本方法不仅可应用于科研单位进行大规模流行病学调查,还可应用于规模化猪场临床诊断,对PEDV的免疫和强毒感染情况区分具有重要意义。
[1] 朱良强,占松鹤,何长生,等.安徽部分地区冬春仔猪腹泻的流行病学调查与分析[J].畜牧与兽医,2013,45(8):36-38.
[2] 沈永恕,陈陆,皇甫和平,等.2011 年河南省猪流行性腹泻病毒流行株的遗传进化分析[J].中国预防兽医学报,2011,35(8):672-674.
[3] SUN R Q,CAI R J,CHEN Y Q,etal.Outbreak of porcine epidemic diarrhea in suckling piglets,China[J].Emerg Infect Dis,2012,18(1):161-163.
[4] Chen Q,Li G,Stasko J,etal.Isolation and characterization of porcine epidemic diarrhea viruses associated with the 2013 disease outbreak among swine in the United States[J].Acta Biochimicaet Biophysica Sinica,2014,52(1):234-243.
[5] Rodriguez P Y,Maritin L O.Several enteropathogens are circulating in suckling and newly weaned piglets suffering fron diarrhea in the province of villa clara[J].Trop Anim Health Prod,2013,45(2):435-440.
[6] WANG K,LU W,CHEN J,etal.PEDV ORF3 encodes an ionchannl protein and regulates virus production[J].FEBS Lett,2012,586(4):384-391.
[7] PARK S,MOON H,LUO Y,etal.Cloning and further sequence analysis of the ORF3 gene of wild and attenuated type porcine epidemic diarrhea viruses[J].Virus Genes,2008,36(1):95-104.
[8] 周兵强,吴志明,闫若潜,等.2012-2014 年河南省猪流行性腹泻病毒M 基因和ORF3 基因的遗传变异分析[J].中国兽医科学,2014,44(12):1236-1243.
[9] 李长龙,陈建飞,张鑫,等.猪流行性腹泻病毒野毒株/疫苗株PT-PCR 鉴别诊断方法的建立[J].中国兽医杂志,2014,50(6):6-8.
Development and Clinical Application of RT-PCR Differential Diagnosis Method for Vaccine Strains and Wild Strains of PEDV
SONG Yu-zhen1, DONG Qing1, LIANG Zhong-Tao2, HUO Jun1
(1.Henan University of Animal Husbandry and Economy,Zhengzhou 450011,China;.Truein Agro-Pastoral Group,Sanmenxia 472100,China)
Based on the genetic differences of ORF3 of the pig epidemic diarrhea virus(PEDV)vaccine strains and wild strains,we designed a pair of primers to establish a RT-PCR method for the differential diagnosis of PEDV vaccine strains and wild strains,of which the PCR amplification product length of the vaccine strains was 213 bp,and the wild strains was 262 bp.Specific test results showed that the amplification reactions of the primers to the pig infectious gastroenteritis virus,porcine rotavirus,swine fever virus,pig pseudo rabies virus and porcine reproductive and respiratory syndrome virus were negative.We used this method to test 581 diarrhea samples from 51 pig farms of Henan province during the period of March 2014 to April 2015,and the results showed that the total positive rate of PEDV was 54.9%(391/581),of which the positive rate of wild strains was 84.9%(332/391),and the vaccine strains was 15.1%(59/391).All of these results indicate that the detection rate of PEDV in the current diarrhea sample is still high,and the PEDV positive samples mainly are wild strain infections.
Porcine Epizootic Diarrhea(PED) ; Differential Diagnosis ; Clinical Application
HUO Jun
2015-10-14
河南牧业经济学院——雏鹰农牧经济技术研发中心研究项目(CYXYXM201401)
宋予震(1979-),男,副教授,硕士,从事预防兽医研究工作,E-mail:zzmzsong@163.com
霍军,E-mail:huojun@tom.com
S852.65
A
0529-6005(2016)10-0006-03