小金牛草质量控制方法研究
2016-12-19李建晨翟海峰段志清
李建晨,冉 云,翟海峰,哈 婧,段志清
(1.河北科技大学化学与制药工程学院,河北石家庄 050018;2.北京大学中国药物依赖性研究所,北京 100191;3.河北医科大学第一医院,河北石家庄 050051)
小金牛草质量控制方法研究
李建晨1,冉 云1,翟海峰2,哈 婧1,段志清3
(1.河北科技大学化学与制药工程学院,河北石家庄 050018;2.北京大学中国药物依赖性研究所,北京 100191;3.河北医科大学第一医院,河北石家庄 050051)
为了建立小金牛草药材的定性定量检测方法,为其质量评价提供依据,采用薄层色谱法对其进行定性鉴别;自制Telephenone B对照品,以芒果苷为参照物,建立芒果苷与Telephenone B间的相对校正因子,采用HPLC结合一测多评的方法进行含量测定,并将外标法测定的结果与计算值进行比较,评价所建立的一测多评方法的准确性和可行性。结果表明,薄层色谱斑点清晰,易于判断。芒果苷和Telephenone B分别在0.2~1.4 μg(r=0.999 9)和0.13~0.91 μg(r=0.999 4)范围内线性关系良好。所建立的相对校正因子重现性良好,采用相对校正因子计算的含量值与外标法的实测值之间没有显著性差异。该方法准确可行,可用于小金牛草的质量控制。
中药化学;小金牛草;质量控制;薄层色谱法;一测多评;相对校正因子
小金牛草来源于远志科植物小花远志PolygalatelephioidesWilld.的全草。小花远志分布于中国南方,主产地为华南地区,为一年生草本,秋季采收,干燥后全草入药[1]。小金牛草有活血散瘀、止痛、镇咳的功效,用于治疗胸痛咳嗽、百日咳、小儿麻痹后遗症[2],《中药志》记载小金牛草“性平,味辛,解毒破血,治风痰隔气,解罂粟毒”[3]。近年来,小金牛草作为一种戒毒中药,大量用于阿片类成瘾的戒断治疗,致使其资源日趋紧张,药材价格也已涨至每千克千元左右,掺杂使假及超前采集现象严重,药材的质量控制面临挑战。而对其质量标准的研究,目前只有《上海市中药材标准》(1994)收载了小金牛草品种,但该标准中只有性状鉴别项,难以有效地反映和评价小金牛草药材的质量[4]。随着小金牛草应用的不断扩大,尽快建立切实有效的药材标准,开展其质量控制和评价的必要性也愈加紧迫。
本文对小金牛草中针对性组分Telephenone B和芒果苷进行含量测定,在自制Telephenone B对照物的基础上,以芒果苷为对照品[5],尝试用一测多评(QAMS)的方法测定上述2个成分的含量,实现在对照品缺乏的情况下对小金牛草指标成分的定量控制;同时,建立了小金牛草的薄层色谱鉴别方法,为小金牛草的质量控制提供方法依据。
1 仪器与试药
LC-2010高效液相色谱仪(日本岛津公司提供);LC solution工作站(日本岛津公司提供);Agilent 1200高效液相色谱仪(美国Agilent公司提供);ChemStation for LC Systems工作站(美国Agilent公司提供);AL204电子天平,UV-2600酸度计(梅特勒-托利多仪器有限公司提供);KQ5200DE型数控超声波清洗器(昆山市超声仪器有限公司提供);Merck硅胶60 F254薄层板(德国Merck公司提供);聚酰胺(160~250 μm(60~90目),长丰化工有限公司提供)。
收集市售小金牛草样品5批,经河北省药品检验研究院段吉平主任药师鉴定为小金牛草,样品存放于河北科技大学。
芒果苷(批号4773-96-0)购自上海源叶生物科技有限公司,纯度≥98%;Telephenone B对照品由本实验室分离纯化。
试剂:乙腈(色谱纯),娃哈哈纯净水,均经0.45 μm滤膜过滤;甲醇、乙醇、磷酸二氢钠和磷酸,均为分析纯。
2 方法与结果
2.1 薄层鉴别
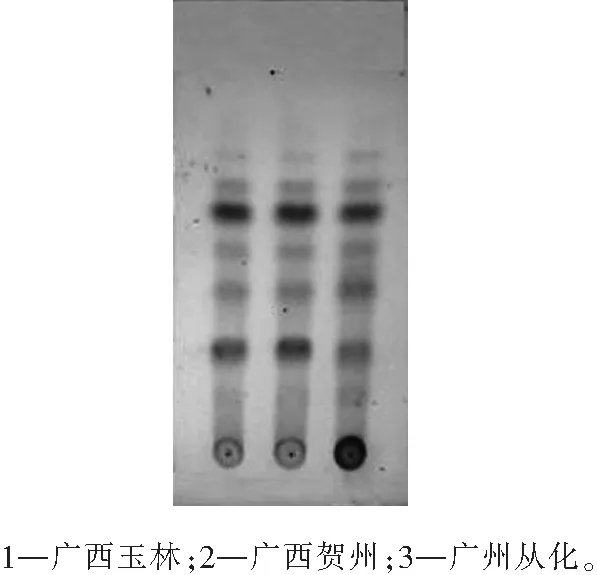
图1 小金牛草薄层色谱图Fig.1 TLC of Polygala telephioides herba
取小金牛草粉末0.5 g,加乙醇25 mL,超声处理30 min,过滤,将滤液蒸干,加水1 mL使残渣溶解,过聚酰胺柱(内径为1.5 cm,高度为8 cm)。依次用15 mL水及30%(体积分数,下同)乙醇30 mL洗脱,取30%乙醇洗脱液,蒸干,加甲醇2 mL使残渣溶解,作为供试品溶液。按照薄层色谱法(《中华人民共和国药典》(2015年版)(四部)通则0502)试验。吸取上述溶液各2 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(三者体积比为8∶2∶0.2)为展开剂,展开,取出,晾干,喷以10%(体积分数,下同)硫酸乙醇溶液,在105 ℃加热至斑点显色清晰。结果见图1。
2.2 Telephenone B对照物的制备与标定
2.2.1 Telephenone B对照物的制备[6-7]
取小金牛草药材,适当碎断,加乙醇回流提取,过滤,减压回收乙醇。将得到的浸膏依次通过大孔树脂柱、硅胶柱、Chromatorex ODS柱等柱色谱分离,再经HPLC纯化,得到单一物质Telephenone B。
2.2.2 Telephenone B对照物的纯度检查
薄层色谱:选用硅胶G薄层板(烟台康必诺化学试剂厂提供),点样量95 μg,分别以三氯甲烷-甲醇-水(三者体积比为7∶3∶0.5)、乙酸乙酯-甲醇(体积比为6∶4)、丙酮-水(体积比为9∶1)为展开剂展开,先在紫外(254 nm,365 nm)下检视,再喷以10%硫酸乙醇溶液,105 ℃加热至斑点清晰。结果均只有1个主斑点,未见其他斑点。
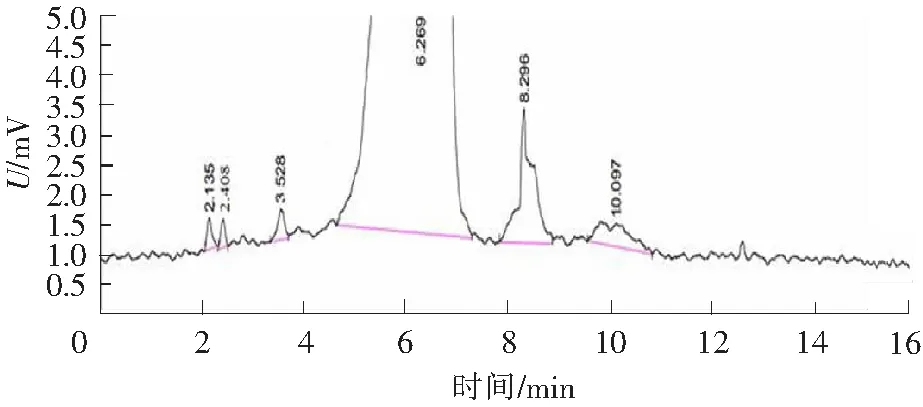
图2 纯度检测HPLC图谱Fig.2 HPLC spectra for purity test
HPLC测定:蒸发光散射检测器;色谱柱Agilent HC-C18(4.6 mm×250 mm,5 μm);流动相为甲醇-水(体积比为33∶67),流速为1.0 mL/min,柱温为25 ℃,进样量为20 μg。测得其纯度为99.2%(见图2)。
2.3 一测多评法测定含量
2.3.1 色谱条件
Agilent HC-C18色谱柱(4.6 mm×250 mm,5 μm),流动相为体积比15∶85的乙腈-磷酸二氢钠溶液(0.05 moL/L,用体积分数为1%的磷酸溶液调节pH值至2.5),流速为1.0 mL/min,柱温为25 ℃,检测波长为206 nm。
2.3.2 对照品溶液的制备
取芒果苷和Telephenone B对照品适量,精密称定,加甲醇制成质量浓度分别为100 μg/mL和65 μg/mL的混合对照品溶液,即得。
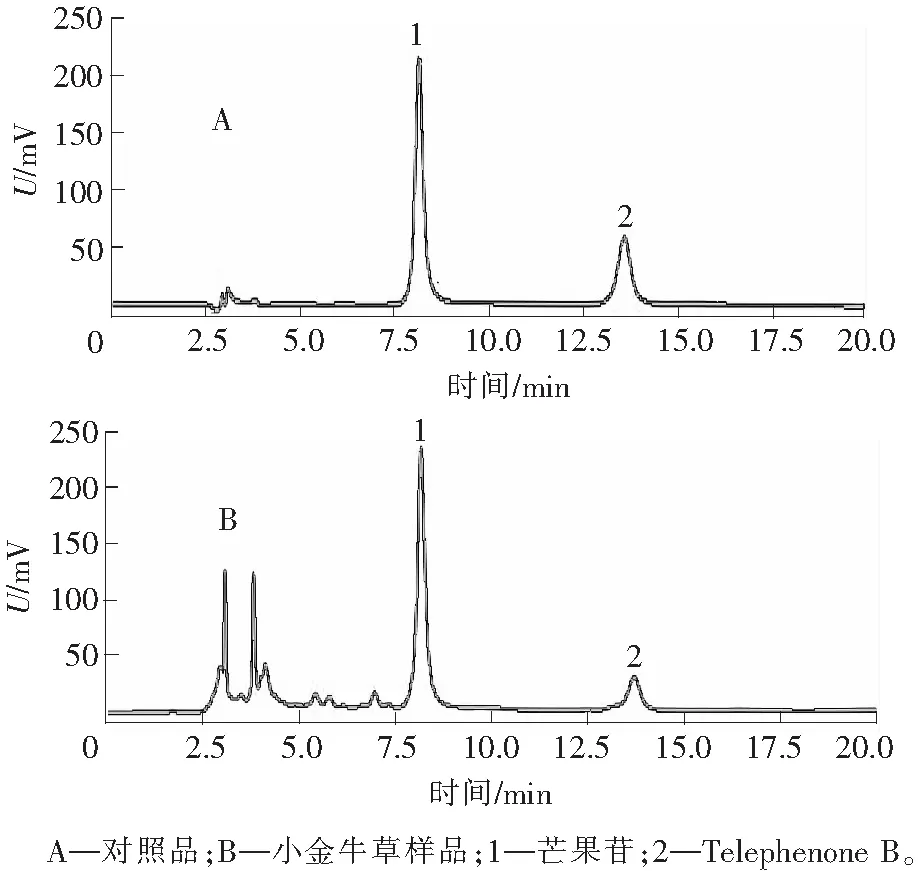
图3 对照品及小金牛草药材的HPLC图谱Fig.3 HPLC spectrums of the reference and sample
2.3.3 供试品溶液的制备
取小金牛草药材粉末(过3号筛)约0.25 g,精密称定,置具塞三角瓶中,精密加入40%甲醇50 mL,称定质量;超声提取30 min,放冷,再称定质量,用40%甲醇补足减失的质量,摇匀,过滤,取续滤液,即得。
对照品及样品的HPLC图谱见图3。
2.3.4 线性范围考察
精密吸取上述混合对照品溶液2,4,6,8,10,12,14 μL进样分析,以进样量对峰面积进行回归处理,得到芒果苷和Telephenone B的回归方程:y=3 890 644x+4 526(r=0.999 9),y=2 516 730x+23 495(r=0.999 4)。两者分别在0.2~1.4 μg和0.13~0.91 μg呈良好的线性关系。
2.3.5 精密度试验
精密吸取混合对照品溶液10 μL,连续进样6次,记录峰面积,芒果苷和Telephenone B峰面积的RSD值分别为0.69%和0.54%,表明仪器的精密度良好。
2.3.6 稳定性试验
精密吸取同一供试品溶液10 μL,在0,1,2,4,8,12 h分别进样分析,记录峰面积,芒果苷和Telephenone B的RSD值分别为0.43%和0.81%,表明12 h内供试品溶液的稳定性良好。
2.3.7 重复性试验
称取同一批小金牛草药材粉末约0.25 g,精密称定,平行6份,按照供试品溶液处理方法制备样品,测定,芒果苷和Telephenone B的平均质量分数分别为2.01%和0.53%,RSD值分别为0.32%和0.97%,表明该方法的重复性良好。
2.3.8 加样回收率试验
称取已知含量的小金牛草药材粉末约0.12 g,精密称定,平行6份,分别将药材-对照品按质量比1∶1加入一定量的对照品溶液,按供试品溶液处理方法制备样品,测定并计算各成分的加样回收率以及RSD值。结果发现,芒果苷和Telephenone B的平均回收率分别为98.36%和96.70%,RSD值分别为1.03%和1.42%,表明该方法的准确度良好。
2.3.9 相对校正因子的计算
以芒果苷为内标,按fkm=fk/fm=(Wk×Am)/(Wm×Ak)(式中Ak和Wk为芒果苷的峰面积和浓度,Am和Wm为Telephenone B的峰面积和浓度)[8-13]计算芒果苷对Telephenone B的相对校正因子f(芒果苷)/f(Telephenone B)=0.661,见表1。
2.3.10 不同仪器和色谱柱校正因子的重现性
分别考察LC-2010和Agilent 1200高效液相色谱系统与Agilent HC-C18(4.6 mm×250 mm,5 μm),YMC-Pack ODS-A(4.6 mm×250 mm,5 μm),Kromasil 100-5-C18(4.6 mm×250 mm,5 μm),COSMOSIL(4.6 mm×250 mm,5 μm)4种色谱柱对相对校正因子的影响。结果发现,Telephenone B

表1 相对校正因子
与内参物芒果苷间的相对校正因子重现性良好,RSD值<5%,见表2。
2.3.11 一测多评法对待测组分色谱峰的定位
一测多评法通常采用保留时间差或相对保留值等方法对待测组分色谱峰的准确定位[14-16]。本实验分别考察了保留时间差和相对保留值在不同品牌的仪器和不同型号的色谱柱之间的重现性。发现保留时间差RSD值>5%,相对保留值RSD值<5%。因此选用相对保留值对待测组分的色谱峰进行定位,其平均值r(Telephenone B)/r(芒果苷)=1.660。见表3。
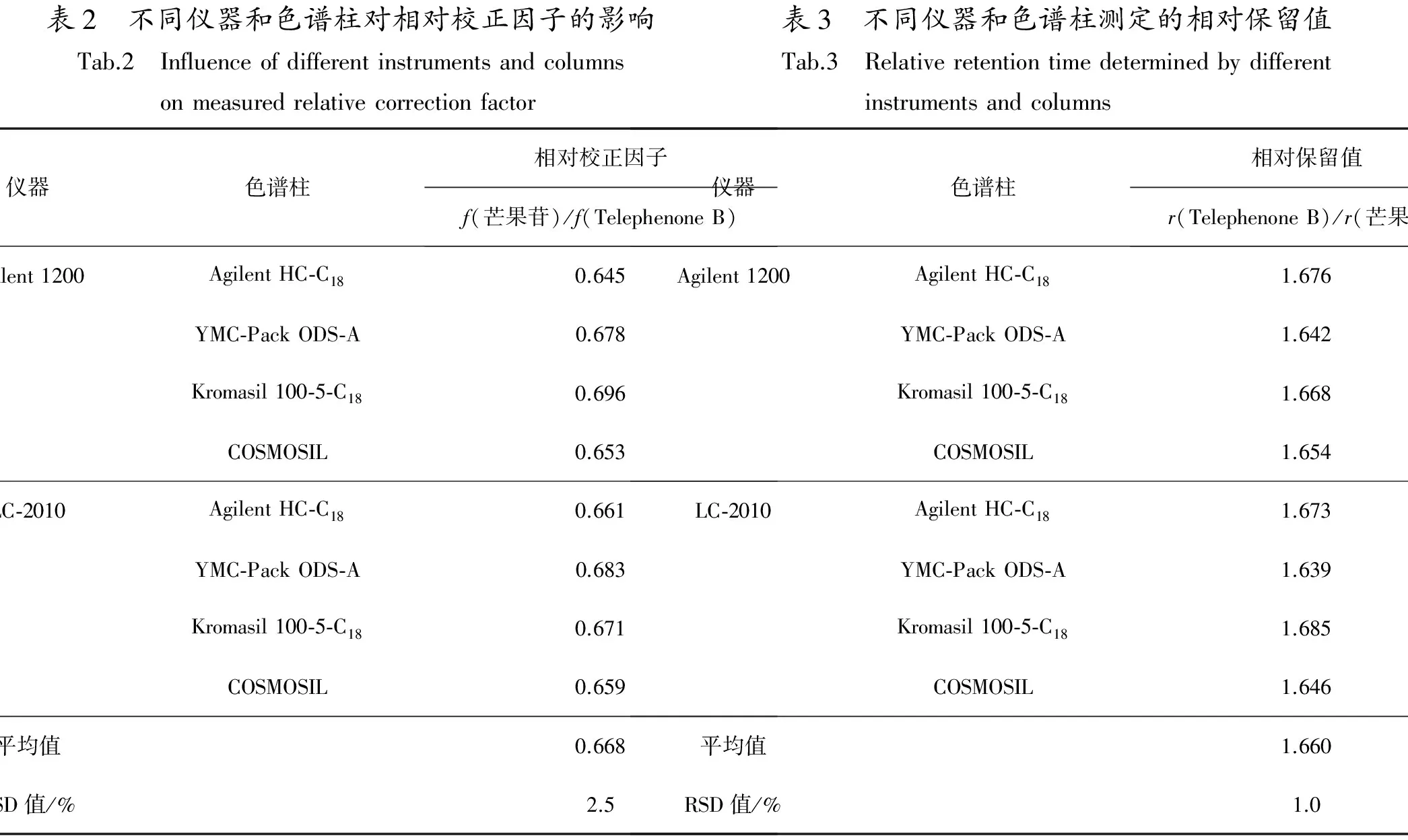
表2 不同仪器和色谱柱对相对校正因子的影响Tab.2 Influenceofdifferentinstrumentsandcolumnsonmeasuredrelativecorrectionfactor仪器色谱柱相对校正因子f(芒果苷)/f(TelephenoneB)Agilent1200AgilentHC⁃C180.645YMC⁃PackODS⁃A0.678Kromasil100⁃5⁃C180.696COSMOSIL0.653LC⁃2010AgilentHC⁃C180.661YMC⁃PackODS⁃A0.683Kromasil100⁃5⁃C180.671COSMOSIL0.659平均值0.668RSD值/%2.5表3 不同仪器和色谱柱测定的相对保留值Tab.3 Relativeretentiontimedeterminedbydifferentinstrumentsandcolumns仪器色谱柱相对保留值r(TelephenoneB)/r(芒果苷)Agilent1200AgilentHC⁃C181.676YMC⁃PackODS⁃A1.642Kromasil100⁃5⁃C181.668COSMOSIL1.654LC⁃2010AgilentHC⁃C181.673YMC⁃PackODS⁃A1.639Kromasil100⁃5⁃C181.685COSMOSIL1.646平均值1.660RSD值/%1.0
2.3.12 一测多评法和外标法测定结果的比较
取5批小金牛草药材粉末约0.25 g,精密称定,按2.3.3操作,测定。采用外标法和一测多评法计算小金牛草中芒果苷和Telephenone B的含量,2种方法测定结果的相对偏差小于5%,表明所建立的方法可信度良好。见表4。
3 讨 论
前期的成分研究发现,从结构类型上区分,小金牛草主要含有低聚糖酯和酮类两大类成分[6-7],其中芒果苷含量较高,且化学性质稳定,对照品易得[17-19],故作为一个指标成分。芒果苷在天然植物中分布较多,专属性较差,仅仅测定其单一含量不够充分。Telephenone B属二苯甲酮苷类化合物,是小金牛草含有的一个特异性的主要成分,目前未有在其他植物中的报道。根据正在进行的动物实验的结果,Telephenone B对于吗啡依赖症状具有比较明显的轻减作用,因此本文首选芒果苷和Telephenone B两种酮类成分作为定量检测的指标[20]。

表4 一测多评法和外标法测定小金牛草中芒果苷和Telephenone B成分含量
芒果苷和Telephenone B在波长206 nm和320 nm附近均有较强吸收,考虑到Telephenone B的含量相对较低,最终选择其最强吸收的206 nm作为检测波长。
实际工作中,中药的定量评价受到标准品短缺的严重制约,本文通过自制对照品并结合一测多评法,对于没有市售对照品提供的指标成分的定量工作提供了一条现实可行的路径。实验结果表明,一测多评法的计算结果与外标法测定值之间没有显著性差异,能够实现在Telephenone B对照品缺乏的情况下,同时进行Telephenone B和芒果苷的定量控制[21-22]。
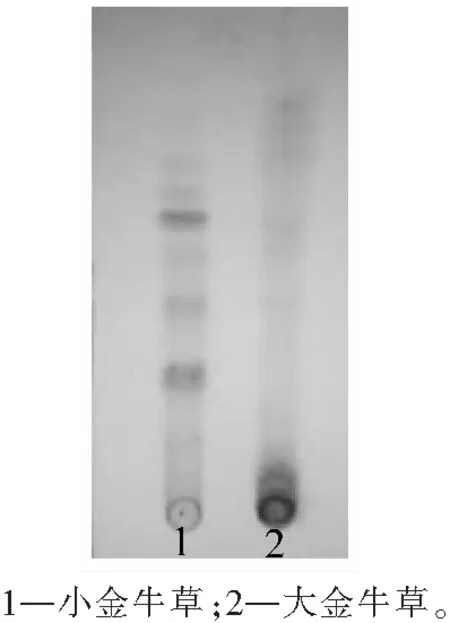
图4 薄层色谱辨别小金牛草与大金牛草Fig.4 TLC identification of Polygala telephioides herba and Polygala chinensis herba
薄层色谱是中药定性鉴别的重要手段[23],本文以极性较低的低聚糖酯类为主要目标成分,与定量检测的酮类成分互为补充,有效地增加了小金牛草鉴定和质量评价的信息量。考察了二氯甲烷和三氯甲烷作为展开剂时的展开情况,二氯甲烷作为展开剂时,需要在低温条件下进行薄层检测,最后确定用三氯甲烷作为展开剂。用所建立的方法将小金牛草与易混淆品种大金牛草[24]同时点样,结果如图4所示,表明所建立的方法专属性好,可用于其与混淆品的区分。
本文建立的小金牛草鉴别和含量测定方法,简单易行,重复性和适用性良好,完善了小金牛草的质量标准,可为小金牛草的质量控制提供依据。
[1] 李建晨, 冯丽, 戴敬, 等. 小花远志的化学成分研究[J]. 中国中药杂志, 2009, 34(4): 402-405. LI Jianchen, FENG Li, DAI Jing, et al. Chemical constituents fromPolygalatelephioides[J]. China Journal of Chinese Materia Medica, 2009, 34(4): 402-405.
[2] 中药大辞典编纂委员会. 中药大辞典[M]. 2版. 上海: 上海科学技术出版社, 2006: 367-368.
[3] 唐英. 中药戒毒初探[J]. 实用中医药杂志, 2004, 20(5): 268-269. TANG Ying. Detoxification of traditional Chinese medicine[J]. Journal of Practical Traditional Chinese Medicine, 2004, 20(5): 268-269.
[4] 曾利杰, 陈晓坚, 陈丽斯, 等. 小金牛草的质量标准研究[J]. 今日药学, 2014, 24(4): 240-242. ZENG Lijie, CHEN Xiaojian, CHEN Lisi, et al. Quality standard ofPolygalaarvensisWilld.[J]. Pharmacy Today, 2014, 24(4): 240-242.
[5] CHANG Haitao, TU Pengfei. New oligosaccharide esters and xanthone C-Glucosides fromPolygalatelephioides[J]. Helvetica Chimica Acta, 2007, 90(5): 944-950.
[6] LI Jianchen, TOSHIHIRO N. Benzophenone C-Glucosides fromPolygalatelephioides[J]. Pharmaceutical Society of Japan, 2000, 48(9): 1354-1355.
[7] NOBUAKI E, LI Jianchen, AI M, et al. Antagonistic effects of methanolic extract ofPolygalatelephioideson morphine responses in mice[J]. Journal of Ethnopharmacology, 2006, 104: 193-198.
[8] 王智民, 高慧敏, 付雪涛, 等. “一测多评”法中药质量评价模式方法学研究[J]. 中国中药杂志, 2006, 31(23): 1925-1928. WANG Zhimin, GAO Huimin, FU Xuetao, et al. Multi-components quantitation by one marker new method for quality evaluation of Chinese herbal medicine[J]. China Journal of Chinese Materia Medica, 2006, 31(23): 1925-1928.
[9] 喻华达. 无纯样色谱校正因子的测定[J]. 化学世界, 1992(7):816-818. YU Huada. Determination of no pure sample chromatographic correction factors[J]. Chemical World, 1992(7):816-818.
[11]李聪. 紫外检测器定量校正因子的性质与实用性探讨[J]. 色谱, 1990, 8(4): 254-256. LI Cong. The calculation and application of correction factors of UV detector[J]. Chinese Journal of Chromatography,1990,8(4):254-256.
[12]陆兔林, 石上梅, 蔡宝昌, 等. 基于一测多评的中药多成分定量研究进展[J]. 中草药, 2012, 43(12): 2525-2529. LU Tulin, SHI Shangmei, CAI Baochang, et al. Advances in studies on multi-component determination of Chinese material madica by QAMS[J]. Chinese Traditional and Herbal Drugs, 2012, 43(12): 2525-2529.
[13]张红伟, 张振凌. “一测多评”法在中药质量控制中的研究进展[J]. 海峡药学, 2010, 22(11): 88-89. ZHANG Hongwei, ZHANG Zhenling. Progress of QAMS in quality control of traditional Chinese medicine[J]. Strait Pharmaceutical Journal, 2010, 22(11): 88-89.
[14]王智民, 钱中直, 张启伟, 等. 一测多评法建立的技术指南[J]. 中国中药杂志, 2011, 36(6):657-658. WANG Zhimin, QIAN Zhongzhi, ZHANG Qiwei, et al. Technical guidelines established by QAMS[J]. China Journal of Chinese Materia Medica, 2011, 36(6): 657-658.
[15]王超群, 贾秀虹, 陈季, 等. 中药三七“一测多评”质量控制方法的系统研究[J]. 中国中药杂志, 2012, 37(22): 3438-3445. WANG Chaoqun, JIA Xiuhong, CHEN Ji, et al. Systematic study on QAMS method for quality control ofPanaxnotoginseng[J]. China Journal of Chinese Materia Medica, 2012, 37(22): 3438-3445.
[16]何兵, 刘艳, 田吉, 等. 指纹图谱结合一测多评模式在中药鱼腥草质量评价中的应用研究[J]. 中国中药杂志, 2013, 38(16): 2682-2689. HE Bing, LIU Yan, TIAN Ji, et al. Study on quality control ofHouttuyniacordata, a traditional Chinese medicine by fingerprint combined with quantitative analysis of multi-components by single marker[J]. China Journal of Chinese Materia Medica, 2013, 38(16): 2682-2689.
[17]邓家刚, 郑作文, 曾春晖. 芒果苷的药效学实验研究[J]. 中医药学刊, 2002, 20(6): 802-803. DENG Jiagang, ZHENG Zuowen, ZENG Chunhui. Pharmacodynamic studies on mangiferin[J]. Chinese Archives of Traditional Chinese Medicine, 2002, 20(6): 802-803.
[18]赵建国, 曲伟红. 远志化学成分分析方法研究进展[J]. 时珍国医国药, 2009, 20(12): 3114-3115. ZHAO Jianguo, QU Weihong. Advances on the analytical technologies of chemical components in Radix Polygalae[J]. Lishizhen Medicine and Materia Medica Research, 2009, 20(12): 3114-3115.
[19]宋成芝, 吴章康, 华燕. 远志属药用植物化学成分和生物活性研究进展[J]. 中国民族民间医药, 2008(3):28-29. SONG Chengzhi, WU Zhangkang, HUA Yan. Advances in study on chemical constituents and pharmacological activities of Polygala[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy, 2008(3):28-29.
[20]杨申明, 王振吉, 徐成东, 等. 重齿鳞毛蕨中总黄酮的含量测定[J]. 河北工业科技, 2014, 31(1): 48-52. YANG Shenming, WANG Zhenji, XU Chengdong, et al. Content determination of total flavonoids inDryopterisjuxtaposita[J]. Hebei Journal of Industrial Science and Technology, 2014, 31(1): 48-52.
[21]杨菲, 王智民, 张启伟, 等. “一测多评”法测定丹参酚酸类成分的含量[J]. 中国中药杂志, 2011, 36(17): 2372-2379. YANG Fei, WANG Zhimin, ZHANG Qiwei, et al. A quantitative method for simultaneous assay of five ingredients with one marker inSalviamiltiorrhiza[J]. China Journal of Chinese Materia Medica, 2011, 36(17): 2372-2379.
[22]ZHU Jingjing, WANG Zhimin, MA Xinyu, et al. A quantitative method for simultaneous determination of four anthraquinones with one marker inRheiRadixetRhizoma[J]. Chinese Herbal Medicines, 2012, 4(2): 157-163.
[23]冯海燕, 李向军, 胡瑞省, 等. 超声法提取萹蓄总黄酮正交试验研究[J]. 河北科技大学学报, 2011, 32(6): 611-614. FENG Haiyan, LI Xiangjun, HU Ruisheng, et al. Orthogonal test in extration of total flavonoids fromPolygonumaviculareby ultrasonic method[J]. Journal of Hebei University of Science and Technology, 2011, 32(6): 611-614.
[24]郝培培. 大金牛草的成分研究及远志醇制备工艺的优化[D]. 石家庄: 河北科技大学, 2011. HAO Peipei. Study on Constituent from Polygala Chinensis and Optimum Preparation Process of Polygalitol[D]. Shijiazhuang: Hebei University of Science and Technology, 2011.
Quality control method of Polygala telephioides herba
LI Jianchen1, RAN Yun1, ZHAI Haifeng2, HA Jing1, DUAN Zhiqing3
(1.School of Chemical and Pharmaceutical Engineering, Hebei University of Science and Technology, Shijiazhuang, Hebei 050018, China; 2.National Institute on Drug Dependence, Peking University, Beijing 100191, China; 3.The First Hospital of Hebei Medical University, Shijiazhuang, Hebei 050051, China)
In order to control the quality of Polygala telephioides herba, a method is established for the qualitative and quantitative analysis of the herba. Firstly, a TLC method is developed for qualitative detection of Polygala telephioides. Then, with home-made Telephenone B as comparison product and Mangiferin as the reference substance, the relative correlation factor (RCF) of Telephenone B and Mangiferin is determined. The contents are determined by HPLC combined with the quantitative analysis of multi-components by single-marker (QAMS), and the calculated value of QAMS is compared with the measured result to verify the veracity and feasibility of the QAMS method. The results show that the TLC spots are clear and easy to judge. Mangiferin and Telephenone B show good linear relationship in the range of 0.2~1.4 μg (r=0.999 9), 0.13~0.91 μg (r=0.999 4), respectively. The established relative correlation factor shows good reproducibility, and there is no significant difference between the content result calculated by RCF and the content result determined by external standard method. This method is accurate, feasible, and can be used for the quality control of Polygala telephioides herba.
Chinese medicine chemistry; Polygala telephioides herba; quality control; TLC; quantitative analysis of multi-components by single-marker (QAMS); relative correlation factor (RCF)
1008-1542(2016)06-0581-06
10.7535/hbkd.2016yx06009
2016-04-27;
2016-06-02;责任编辑:王海云
国家“十二五”科技重大专项(2014ZX09304-307-02);河北省自然科学基金(H2014208164)
李建晨(1964—),男,河北肃宁人,副教授,博士,主要从事天然药物方面的研究。
哈 婧教授。E-mail:hajing02@163.com
TQ46;R932
A
李建晨,冉 云,翟海峰, 等.小金牛草质量控制方法研究[J].河北科技大学学报,2016,37(6):581-586. LI Jianchen, RAN Yun, ZHAI Haifeng, et al.Quality control method of Polygala telephioides herba[J].Journal of Hebei University of Science and Technology,2016,37(6):581-586.
