不同种类人工心脏瓣膜的比较及其生物学评价
2016-12-14崔永春刘晓鹏张宏张冬吴爱丽唐跃心血管植入材料临床前研究评价北京市重点实验室心血管疾病国家重点实验室国家心血管病中心中国医学科学院北京协和医学院阜外医院动物实验中心北京100037
崔永春 刘晓鹏 张宏 张冬 吴爱丽 唐跃 心血管植入材料临床前研究评价北京市重点实验室,心血管疾病国家重点实验室,国家心血管病中心,中国医学科学院,北京协和医学院,阜外医院,动物实验中心 (北京 100037)
不同种类人工心脏瓣膜的比较及其生物学评价
崔永春 刘晓鹏 张宏 张冬 吴爱丽 唐跃 心血管植入材料临床前研究评价北京市重点实验室,心血管疾病国家重点实验室,国家心血管病中心,中国医学科学院,北京协和医学院,阜外医院,动物实验中心 (北京 100037)
近年来,国内大部分人工心脏瓣膜是从欧美等国家进口,国产率较低。随着科学技术的快速发展,尤其是生物医学材料科学和组织工程学的发展,为国内人工心脏瓣膜的开发研究与临床应用提供了新机遇。本文将对现有不同种类的心脏瓣膜的结构功能特点及其生物学评价进行阐述,为国内人工心脏瓣膜的研发或改良提供资料支持。
人工心脏瓣膜 机械瓣 生物瓣 介入瓣 生物评价
0.引言
人工心脏瓣膜是一种治疗心脏瓣膜疾病或缺损的心脏植介入医疗器械。1960年人工心脏瓣膜首次应用于临床,之后经历了机械瓣、生物组织瓣、介入瓣等阶段[1,2],目前已成为心血管治疗领域一种非常重要的医疗器械,是先天性畸形及风湿性心脏病、心脏退化以及细菌感染等疾病所造成的后天性心脏瓣膜疾病引发的心脏瓣膜功能异常的重要治疗手段[3~7]。当前国内心脏瓣膜病患者约占心脏病患者的30%,每年有大量的患者需要进行心脏换瓣手术,因此开展人工心脏瓣膜的研制工作不仅具有科学意义,而且具有巨大的经济价值和社会意义[8]。
本文将分别对现有不同种类的心脏瓣膜的结构、功能特点及其生物学评价进行描述。
1.机械瓣
机械瓣膜是由人工材料制成的可植入心脏内代替心脏瓣膜,使血液单向流动,并具有天然心脏瓣膜功能的的人工器官。机械瓣由坚硬材料(支架)、弹性材料(阻塞体)和织品类材料(瓣环)三部分组成。
常用的坚硬材料:①钴铬镍合金,是一种相当坚硬的金属,可植入与体内长期不变并可高度抛光;②钛,它优于钴铬镍 合金,不必铸造,可以机械加工,非常惰性且能高度抛光。③delrin,是一种聚缩醛树脂,缺点是轻度吸水;④Teflon,软而缺乏结构强度;⑤超高密度聚乙烯和聚丙烯都可以加压消毒且极稳定,但需用浇铸技术制造。
常用弹性材料:美国Dowcorning公司特别制造的硅橡胶是最令人满意的弹性体,1961年Storr-Ed-wards用它制造成球型瓣膜。
织品:涤纶长丝编织而成,用涤纶线牢固地扎在瓣架的凹槽内,具有不皱不缩,不变形,尺寸稳定等特点,被周围组织包埋后,更能使其牢固地固定。
机械瓣就其造型来讲,自诞生之日起先后经历了球笼瓣和笼碟瓣、斜碟瓣、双叶瓣四代里程碑式变革[9~12]。

表1. 不同人工机械瓣膜比较
2.生物组织瓣
现市场占有率较大的另一类人工心脏瓣膜为生物组织瓣,与全部用人造材料制成的机械瓣比较,生物组织瓣全部或部分用生物组织制成。通常具有良好的生物相容性和血流动力学特性,在临床中应用广泛。生物组织瓣分为同种生物瓣和异种生物瓣两种。材料来源分为:(1)同种同体组织:阔筋膜、肺动脉;(2)同种异体组织:动脉瓣、硬脑膜、阔筋膜;(3)异种异体组织:猪主动脉瓣、牛心包、牛主动脉瓣。生物瓣中以猪主动脉瓣最为常见,牛心包瓣是仅次于猪主动脉瓣用得较多的生物瓣。国内1972年由中国医学科学院阜外医院率先研制成功,1976年应用于临床。人工心脏瓣膜重大事件,见表3。牛心包组织与人类心包组织相似,其胶原纤维排列呈多向性,并呈波浪状结构,具有较好的生物学特性。现代表产品有LS瓣、Lonescu-Shiley低架瓣、EdwardsPericardial瓣、HancokePericardial瓣、MedicalMitroflow瓣等。
生物瓣的优点:(1)抗凝血性好,不易形成血栓和栓塞,术后抗凝治疗6个月即可,不必再服用抗凝血药物;(2)置换后接近正常的血液动力学特征,即瓣口流道中流体的中心流特征,由于没有阻塞体,血栓形成的可能性非常低,并且不会对血液有形成分产生破坏;(3)制作瓣膜的材料有很好的血液相容性,不会产生凝血、溶血以及形成血栓等良好特性,能维持长期组织学上与功能的完整性。缺点是强度较差,瓣膜耐久性比机械瓣短,预期使用寿命一般是15~20年。
目前阻碍生物组织瓣推广应用的最主要问题是瓣膜钙化问题。为攻克该瓶颈,人们一直在不懈地研究,发现钙化原因如下:
(1)无完整内皮细胞覆盖的生物瓣由于不能控制血浆成分的渗入,可能是引起组织钙化和衰坏的条件;(2)血流动力学状况不良的情况下,会产生血流滞流区易引起血栓形成,这种血栓极易促使钙盐的沉积形成钙盐沉积区,又产生血栓再形成,如此形成恶性循环,而导致生物瓣钙化失灵;(3)血中钙磷离子是荷电粒子,瓣膜表面电荷的变化,对钙、磷离子的沉积有很大影响。根据实验可知,材料表面负电荷占优势时,钙离子沉积的可能性较大。随着人们对钙化机制认识的不断深入,相信不久将来会找到解决问题的方案。
另一种未来最有希望得到大规模利用的性能优异的心脏瓣膜是组织工程人工心脏瓣膜[15,16](tissue engineered heart valve:TEHV),它是美国波士顿市生物科学家们开发的一种前所未有的新方法,即利用病人自身细胞经人工培育后成为新的心脏瓣膜,用于置换损坏的心脏瓣膜。其方法是将自体细胞(包括成纤维细胞核内皮细胞)在体外先后种植于生物可降解材料的支架上,形成成纤维细胞和内皮细胞层,移植后,随着支架的降解吸收,自体瓣膜可建立。由于瓣膜完全来自于自体细胞,有完整的内细胞层,因此无免疫原性、无须抗凝、具有可以生长、可以修复自身的损伤和较好的耐久性等优点,是一种新型的理想的人工生物心脏瓣膜。TEHV的在体实验研究尚处于动物实验阶段,近期效果比较明显,但是仍然有许多技术和临床问题需要解决。
3.介入瓣

图1. 典型的介入支架瓣膜结构
20世纪,对于瓣膜植入治疗,公认的金标准为外科开胸行二尖瓣成形或置换术。随着介入心脏病学的迅速发展,2002年,Cribier等报道了世界上第一例经导管植入主动脉瓣膜的人体试验的结果[17],引起广泛关注。经导管瓣膜介入治疗方法的出现开创了经导管瓣膜置换的新时代[18]。相对于外科手术,支架瓣膜介入治疗对人体的创伤微小、术后恢复快、不留疤痕,造福很多患者。现在介入心瓣技术已经不止用于危重病人的治疗,还可以作为外科手术治疗的替代方案用于普通病人的治疗。目前常用的支架瓣膜如图1所示,其性能见表2。

表2. 不同介入支架瓣膜的比较
4.人工心脏瓣膜生物学评价
虽然现有瓣膜已经取得了不错的临床效果,但同时亦存在诸多不足。为最大限度确保产品质量,帮助外科医生选择人工心脏瓣膜,便于手术台上操作,我国2008年颁发国标《心血管植入物人工心脏瓣膜》,明确规定了人工心脏瓣膜上市前需要进行体外实验、临床前体内评价和临床评价的过程。体外实验主要包括流体力学试验(包括静态前向流试验、稳态泄露试验、脉动流试验)和疲劳试验,以评价心脏瓣膜的耐久性和破坏性。为了获得动物体内反映人工心脏瓣膜预知性能及不可预知的副作用资料,需要进行动物体内实验[39]。
动物实验一般要求:(1)瓣膜植入至少一个预期使用的解剖位置;(2)实验瓣膜和对照瓣膜应具有和临床使用瓣膜相同的设计和尺寸;(3)所有人工心脏瓣膜植入应使用相同的外科技术,详细记录手术过程,包括缝合方法、瓣膜放置方位和手术并发症。
实验动物的选择:考虑到动物体型大小及术后看护,大部分国内外心脏瓣膜植入实验均用羊作为实验动物,而且要求同性别、同月龄的,数量要求是至少有6只动物存活20周以上。另外,至少应该有2只动物植入对照瓣膜。每个植入人工心脏瓣膜的动物都应该进行死后检查,要保留所有动物的试验数据;包括20周中存活和没有存活的动物。统计动物的死亡率时,应该基于术中及术后30天内实验动物存活情况。记录实验前动物的健康情况以及动物存活阶段使用的药物名称和剂量(例如,抗生素或止血药)[40]。
动物实验需要评价的内容包括:
(1)主要器官的大体和显微病理结果,包括最短植入期内死亡的动物;心脏瓣膜植入位置的形态以及主要器官是否发生血栓情况;如果动物不是处死的,应记录动物的死亡原因。
(2)取出的人工心脏瓣膜外观:包括直观形象记录和瓣膜结构改变评价。
(3)描述并记录所有血液试验研究结果,包括植入后各时间点的溶血评价、血液学评价和血液化学评价。
(4)20周后或20周中血液动态性能评价,包括测量在心脏指数约是3L/(min·m2)时的跨瓣压差(kPa或mmHg)、心率、平均主动脉压、心输出量(L/min)、3个心动周期内的返流量,瓣周泄漏量和瓣叶运动情况。
(5)瓣膜结构发生的任何变化:明显的损坏、材料的降解、变形和钙化。
5.展望
心脏瓣膜疾病是一类危及人类健康和生命的疾病,严重影响患者的工作和生活质量。随着我国经济的快速发展,医疗保障体系的逐步完善,我国心脏瓣膜替换病人的数量将会逐渐增加,这将为我国国产心脏瓣膜发展带来机遇。心脏是一个高精密组织结构器官,完全模拟其功能的人工心脏是极不容易的,需要医学、生物物理、工程学、电子学等多学科的综合应用和相当长时期的研究。由于人工心脏瓣膜是移植在人体心脏内的一种人工器官,长期和活的心肌组织、血液接触,可能会产生一系列复杂的反应,造成溶血、凝血,引起细胞的畸变和免疫排斥反应等,从而影响其完善性,易造成新的疾病或痛苦。因此,理想的人工心脏瓣膜除了能完成其特定的功能外,还必须具有很好的生物相容性。心脏瓣膜行业市场急需结构设计合理、性能稳定、安全、有效的抗凝血、抗感染的新型人工心脏瓣成品。因此,开展人工心脏瓣膜的研制工作不仅具有科学意义,而且具有巨大的经济价值和社会意义。虽然现有的人工心瓣还有很大的改进和提高空间,但对广大患者来说,在不久的将来更加高级和先进的人工心脏瓣膜还是非常值得期待的。
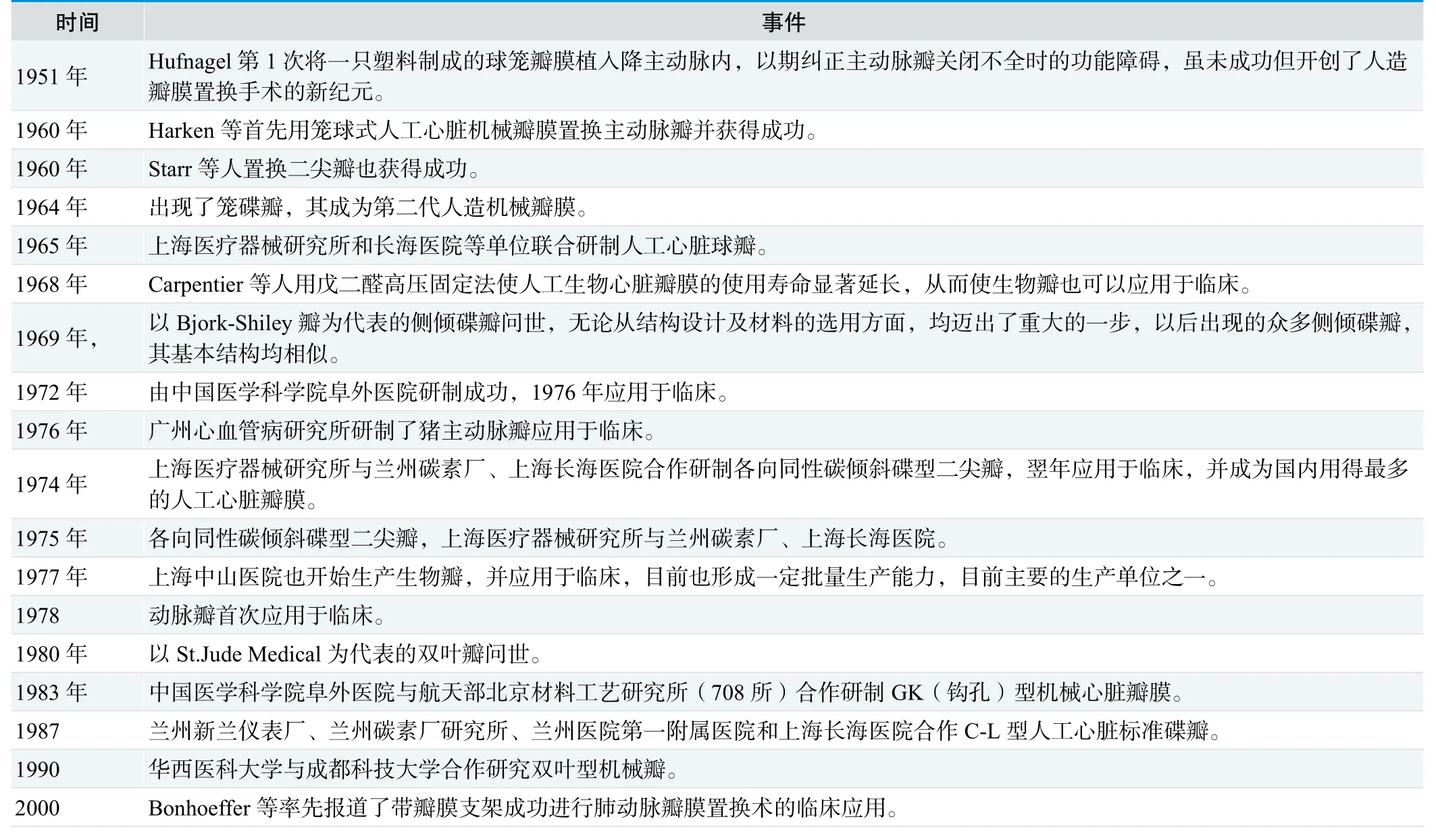
表3. 人工心脏瓣膜重大事件表
参考文献
[1] Harken D E,Soroff H S,Taylor W J,et ak Partial and complete prostheses in aortic insufficiency[J].J Thorac Cardiovasc Surg,1960,40:744~ 762.
[2] Starr A,Edwards M L.Mitral replacement clinical experience with a ball valve prosthesis[J].Ann Surg,1961,154:726.
[3] Rodes-Cabau J, Webb JG, Cheung A, et al. Transcatheter aortic valve implantation for the treatment of severe symptomatic aortic stenosis in patients at very high or prohibitive surgical risk: acute and late outcomes of the multicenter Canadian experience. Journal of the American College of Cardiology. 2010;55(11):1080-1090.
[4] Zahn R, Gerckens U, Grube E, et al. Transcatheter aortic valve implantation: first results from a multi-centre real-world registry. European heart journal. 2011;32(2):198-204.
[5] Moat NE, Ludman P, de Belder MA, et al. Long-term outcomes after transcatheter aortic valve implantation in high-risk patients with severe aortic stenosis: the U.K. TAVI (United Kingdom Transcatheter Aortic Valve Implantation) Registry. Journal of the American College of Cardiology. 2011;58(20):2130-2138.
[6] Smith CR, Leon MB, Mack MJ, et al. Transcatheter versus surgical aortic-valve replacement in high-risk patients. The New England journal of medicine. 2011;364(23):2187-2198.
[7] Abdel-Wahab M, Zahn R, Horack M, et al. Aortic regurgitation after transcatheter aortic valve implantation: incidence and early outcome. Results from the German transcatheter aortic valve interventions registry. Heart. 2011;97(11):899-906.
[8] 罗乐,许贤玉,郭慧尔,等. 人工心脏瓣膜的研究进展. 合肥工业大学学报 2008;31(2):305-308
[9] 董爱强,陈如坤.张昌铭.等国产全热解碳双叶瓣的动物实验.浙江大学学报:医学版,2000,29(4):162-164
[10] 杜微云,吴戴红.不同类型机械瓣对二尖瓣置换术患者血流动力学的影响[J].中国基层医药,2005,12(1):47-49.
[11] 唐跃,胡盛寿,孟亮,等.国产双叶二尖瓣植入绵羊体内的慢性实验研究[J] 中国循环杂志,2003,18(4):303.305.
[12] 王强, 肖明第,袁忠祥,等.胸腔镜主动脉瓣和二尖瓣双瓣膜置换术的动物实验研究及临床应用[J].中国微创外科杂志,2066,6("):845.846.
[13] Rippel RA1, Ghanbari H, Seifalian AM. Tissue-engineered heart valve: future of cardiac surgery. World J Surg. 2012 Jul;36(7):1581-91.
[14] Karen mendelson and Frederick J. schoen. Heart Valve Tissue Engineering Concepts, Approaches, Progress, and Challenges. Annals of biomedical engineering.2006: 34(12):1799-1819.
[15] Houstrop S P,Kadner A,Melnitchouk S,et a1.Tissue engineering of functional trileaflet heart valves from human marrow stroma cells[J].Circulation,2002,106(Suppl I):143— 150.
[16] Houstrop S P,Sodian R,Daebritz S,et a1.Functional living trileaflet heart valve grown in vitro[J].Circulation,2000,102(SupplⅢ):44—49.
[17] Cribier A, Eltchaninoff H, Bash A, et al. Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description. Circulation. 2002;106(24):3006-3008.
[18] Bourantas CV, Farooq V, Onuma Y, et al. Transcatheter aortic valve implantation: new developments and upcoming clinical trials. EuroIntervention : journal of EuroPCR in collaboration with the Working Group on Interventional Cardiology of the European Society of Cardiology. 2012;8(5):617-627.
[19] Treede H, Mohr FW, Baldus S, et al. Transapical transcatheter aortic valve implantation using the JenaValve system: acute and 30-day results of the multicentre CE-mark study. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 2012;41(6):e131-138.
[20] Rodes-Cabau J. Transcatheter aortic valve implantation: current and future approaches. Nature reviews Cardiology. 2012;9(1):15-29.
[21] Kempfert J, Rastan AJ, Beyersdorf F, et al. Trans-apical aortic valve implantation using a new self-expandable bioprosthesis: initial outcomes. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 2011;40(5):1114-1119.
[22] Kempfert J, Treede H, Rastan AJ, et al. Transapical aortic valve implantation using a new self-expandable bioprosthesis (ACURATE TA): 6-month outcomes. European journal of cardio-thoracic surgery : official journal of the European Association for Cardio-thoracic Surgery. 2012.
[23] Treede H. Safety and efficacy outcomes from the multicenter CE Mark study using the JenaValve second generation transcatheter aortic valve implantation (TAVI) system. 25th Annual Meeting of the European Association for Cardio-Thoracic Surgery. Lisbon, Portugal. 1-5 October 2011
[24] Falk V, Walther T, Schwammenthal E, et al. Transapical aortic valve implantation with a self-expanding anatomically oriented valve. European heart journal. 2011;32(7):878-887.
[25] Schofer J, Schluter M, Treede H, et al. Retrograde transarterial implantation of a nonmetallic aortic valve prosthesis in high-surgical-risk patients with severe aortic stenosis: a first-in-man feasibility and safety study. Circulation Cardiovascular interventions. 2008;1(2):126-133.
[26] Treede H, Tubler T, Reichenspurner H, et al. Six-month results of a repositionable and retrievable pericardial valve for transcatheter aortic valve replacement: the Direct Flow Medical aortic valve. The Journal of thoracic and cardiovascular surgery. 2010;140(4):897-903.
[27] Bijuklic K, Tuebler T, Reichenspurner H, et al. Midterm stability and hemodynamic performance of a transfemorally implantable nonmetallic, retrievable, and repositionable aortic valve in patients with severe aortic stenosis. Up to 2-year follow-up of the direct-flow medical valve: a pilot study. Circulation Cardiovascular interventions. 2011;4(6):595-601.
[28] Buellesfeld L, Gerckens U, Grube E. Percutaneous implantation of the first repositionable aortic valve prosthesis in a patient with severe aortic stenosis. Catheterization and cardiovascular interventions : official journal of the Society for Cardiac Angiography & Interventions. 2008;71(5):579-584.
[29] Willson AB, Rodes-Cabau J, Wood DA, et al. Transcatheter aortic valve replacement with the St. Jude Medical Portico valve: first-in-human experience. Journal of the American College of Cardiology. 2012;60(7):581-586.
[30] Mylotte D, Piazza N. Transcatheter mitral valve implantation: a brief review. EuroIntervention. 2015 Sep; 11 Suppl W:W67-70.
[31] Mack M. Presentation at TransCatheter Therapeutics 23rd Annual Scientific Symposium, November 7–11, 2011, San Francisco.
[32] Taramasso M, Maisano F. Transcatheter mitral valve interventions: pathophysiological considerations in choosing reconstruction versus transcatheter valve implantation. EuroIntervention. 2015 Sep; 11 Suppl W:W37-41.
[33] Bapat V, Buellesfeld L, Peterson MD, etal. Transcatheter mitral valve implantation (TMVI) using the Edwards FORTIS device. Eurolntervention, 2014, 10:U120-128.
[34] Bapat V1, Lim ZY, etal. The Edwards Fortis transcatheter mitral valve implantation system. EuroIntervention. 2015 Sep;11 Suppl W:W73-5.
[35] Banai S, Verheye S, Cheung A, etal. Transapical Mitral Implantation of the Tiara Bioprosthesis. JACC: Cardiovascular Interventions, 2014, Vol.7(2):154-162.
[36] Verheye S1, Cheung A, etal. The Tiara transcatheter mitral valve implantation system. EuroIntervention. 2015 Sep;11 Suppl W:W71-2
[37] Perpetua EM1, Reisman M. The Tendyne transcatheter mitral valve implantation system. EuroIntervention. 2015 Sep;11 Suppl W:W78-9.
[38] Abdelghani M, Onuma Y, etal. The Sino Medical AccuFit transcatheter mitral valve implantation system. EuroIntervention. 2015 Sep;11 Suppl W:W84-5.
[39] Nishimura RA,Otto CM, etal. 2014 AHA/ACC guideline for the management of patients with valvular heart disease.J Am Coll Cardiol. 2014,63:e57-e185.
[40] 徐秀林,张京航,梁伟,等人工心脏瓣膜质量及安全性评价[J].中国医疗器械杂志,2004,28(5):359—362.
The Comparison of Different Types of Artificial Heart Valves and Their Biological Evaluation
CUI Yong-chun LIU Xiao-peng ZHANG Hong ZHANG Dong WU Ai-li TANG Yue Peking Key Laboratory for Pre-clinical Evaluation of Cardiovascular Implant Material. State Key Laboratory of Cardiovascular Disease, National Center for Cardiovascular Diseases, Animal Experimental Center, Fuwai Hospital, Chinese Academy of Medical Sciences and Peking Union Medical College (Beijing 100037)
In recent years, most of the artificial heart valves are imported from Europe and the United States. The rapid development of science and technology, especially in biomedical materials and tissue engineering science, provide new opportunities for the development and clinical application of domestic artificial heart valves. This article compared the structural and functional characteristics of existing different kinds of heart valves, and dwelled on their biological evaluation to provide data support for the research, development or improvement of domestic artificial heart valves.
artificial heart valves, mechanical valve prosthesis, biovalve, in valve, biological evaluation
1006-6586(2016)01-0001-06
R318.11
A
2015-11-24
崔永春,医学博士,副研究员
