胡敏酸、富里酸对土壤-地下水系统中BDE-47迁移的影响
2016-12-12王春蕾刘路马腾陈柳竹蔡鹤生
王春蕾,刘路,马腾,,陈柳竹,蔡鹤生
1.中国地质大学(武汉) 环境学院,武汉 430074 2. 生物地质与环境地质国家重点实验室,中国地质大学,武汉 430074
胡敏酸、富里酸对土壤-地下水系统中BDE-47迁移的影响
王春蕾1,2,刘路1,2,马腾1,2,,陈柳竹1,2,蔡鹤生1,2
1.中国地质大学(武汉) 环境学院,武汉 430074 2. 生物地质与环境地质国家重点实验室,中国地质大学,武汉 430074
多溴联苯醚(polybrominated diphenyl ethers, PBDEs)是土壤-地下水系统中广泛存在的有机污染物,研究土壤组分对其迁移行为的影响是解决土壤-地下水系统中多溴联苯醚归趋问题的关键。以典型多溴联苯醚同系物2,2',4,4'-四溴联苯醚(2,2',4,4'-tetrabromodiphenyl ether, BDE-47)为研究对象,选取胡敏酸(humic acid, HA)、富里酸(fulvic acid, FA)2种代表性土壤有机组分,配制不同浓度的FA、HA溶液(150 mg·L-1、50 mg·L-1),分别对不同浓度的BDE-47(100 μg·g-1、10 μg·g-1)污染土壤进行土柱淋滤实验,探讨FA、HA对土壤-地下水系统中BDE-47迁移的影响。结果表明,HA作用下,实验组下层土壤中BDE-47的残留比例分别为0.62%和0.40%,分别低于对照组的0.72%和3.36%;FA作用下,实验组下层土壤中BDE-47的残留比例分别为6.40%和6.71%,分别高于对照组的0.72%和3.36%。结合HA和FA的元素组成和结构特征分析可知,疏水性强的HA能够促进BDE-47随水流迁移进入地下水系统;亲水性强的FA促进BDE-47在土壤系统中的分布,阻滞了土壤系统中BDE-47进入地下水系统。本文为评估HA、FA对土壤-地下水系统中BDE-47迁移的影响提供依据。
BDE-47;胡敏酸;富里酸;迁移;淋滤;土壤;地下水
Received 28 November 2015 accepted 30 December 2015
多溴联苯醚(polybrominated diphenyl ethers,PBDEs)作为一种新兴的持久性有机污染物,因其高毒性、生物累积性以及随水和空气的长距离迁移性近年来引起研究界的热议[1-4]。多溴联苯醚共有209种同系物[5],因其亲脂性的差异以不同形式在大气、地表水体、土壤/沉积物、地下水和生物体内被检出[6-11]。2,2,4,4-四溴联苯醚(2,2,4,4-polybrominated diphenyl ethers, BDE-47)较其他同系物而言,在土壤/沉积物和地下水中检出较多[12-13]。作为代表性四溴联苯醚,BDE-47毒性明显高于高溴代联苯醚,并且由于较低的辛醇-水分配系数,其更易在水中溶解并随水流迁移[5]。
土壤-地下水系统是一个复杂的水-岩相互作用系统[14],也是一个固-液-气-生相互依赖、相互作用、相互影响的特殊黑箱系统。以生态学角度,土壤-地下水系统可以作为依赖地下水生态系统(groundwater dependent ecosystems,GDEs)的背景地貌单元[15],而模型概化也必须考虑其复杂性而视作多孔介质与连续流体介质的耦合[16]。土壤-地下水系统是支持植物生长和进行光合作用的基本生境[17],是微生物、有机质等最发育的地质层位[18],同时也是最直接、最频繁地受到人类活动的影响的区域之一。土壤-地下水系统对进入环境的污染物有着极强的净化能力[19-20],对阻截污染物进入深层地下水环境起着至关重要的作用[21]。土壤作为土壤-地下水系统的第一道净化屏障,可被视为土壤-地下水系统的“皮肤”。因此,探究BDE-47在土壤中的迁移行为是评估其对土壤-地下水系统污染风险的前提。
腐植酸是土壤中较为典型的一类高分子有机化合物,以胡敏酸(humic acid,HA)、富里酸(fulvic acid,FA)为代表[22]。胡敏酸相较富里酸含有较多的芳香基团,不饱和程度高[23];而富里酸的脂肪链结构大于胡敏酸,饱和程度高[24]。二者元素组成中的O/C越高者极性越强,具有更强的亲水性[25]。由于BDE-47具有低水溶性及高脂溶性,预示着其进入土壤-地下水系统的过程中,迁移受土壤颗粒影响的同时,易与胡敏酸和富里酸结合,发生一系列复杂的吸附/解吸过程。因此,胡敏酸、富里酸是影响BDE-47在土壤中迁移的不可忽视的关键因素。已有学者指出在土壤胶体及高浓度的HA影响下PBDEs更易在地表水和地下水中迁移[26]。同样有研究表明,BDE-47在土壤中的解吸过程可用线性吸附等温线和Freundlich吸附等温线来描述,SOM分数(如胡敏酸(HA)、富里酸(FA))在低液相浓度下呈单点系数对应关系[27]。继“有机质是影响BDE-47在土壤体系吸附行为的关键组分”的观点提出后[28],土壤及其主要吸附组分和生物炭对BDE-47的吸附能力大小也逐步被探明[29]。然而,胡敏酸和富里酸在分子尺度对BDE-47迁移的影响仍需深入解译,二者与BDE-47在随地下水于土壤中迁移过程的相互作用机制有待进一步阐明。
本研究采用淋滤实验,以土壤-地下水为介质,探究胡敏酸和富里酸对BDE-47动态迁移行为的影响,以期为PBDEs的环境归趋及污染治理工作提供理论依据。
1 材料与方法 (Materials and methods)
1.1 实验材料与制备
1.1.1 实验试剂与材料
BDE-47标准溶液(50 μg·g-1,美国AccuStandard公司);PCB-141标准溶液(40 μg·g-1,美国AccuStandard公司);BDE-47粉末(97%+,武汉凯美克化学科技有限公司);正己烷(99.5%,美国TEDIA公司)、二氯甲烷、丙酮(农残级,美国J.T.Baker公司)[11];硅胶(100~200目)、氧化铝(100~200目);氯化汞(HgCl2);腐植酸粉末(88.0%+,上海科达化工有限公司);富里酸粉末(90%+,上海晶纯生化科技股份有限公司)。
所用供试土壤取自湖北省武汉市新洲区徐沙湾村农地,取样深度为地表以下10~50 cm,自然风干、剔除大颗粒后,过60目的多孔筛。将一定量的BDE-47溶于甲醇中,加入供试土壤样品中搅拌、混匀,并在通风厨中待甲醇完全挥发,得到本次试验所使用的BDE-47污染土壤。
1.1.2 HgCl2-胡敏酸、HgCl2-富里酸溶液的制备
称取一定质量的腐植酸粉末,按1:50的固液比(w:v)加入0.1 mol·L-1NaOH溶液中,搅拌至完全溶解,静置12 h。用1:1 HCl将pH调节至1.5左右,12 000 r·min-1离心5 min,弃上清液,沉淀用1 mol·L-1NaOH溶液溶解,并将pH调节至8左右,用0.45 μm的滤膜过滤,得到分离纯化后的胡敏酸溶液。
将富里酸粉末和超纯水按1:50的固液比(w:v)混合振荡2 h后,12 000 r·min-1离心5 min,上清液过0.45 μm的滤膜,得到富里酸溶液。
采用Multi N/C 3100 TOC/TN分析仪测试溶解性有机碳浓度(DOC, mg·L-1)以表征上述制备的胡敏酸、富里酸溶液浓度。最终,利用去离子水调整HgCl2-胡敏酸溶液中HgCl2百分含量为2%,胡敏酸浓度分别为150 mg·L-1和50 mg·L-1;同样调节HgCl2-富里酸溶液中HgCl2百分含量为2%,富里酸浓度分别为150 mg·L-1和50 mg·L-1。配制完成的溶液置于4 ℃冰箱储存备用。
1.2 实验方法
预处理后的供试土壤装入玻璃柱中(内径4.5 cm,高度25 cm),在土壤的顶层和底层铺设厚度达1 cm左右的石英砂(20目),底端用200目的尼龙纱布作为反滤层。使土柱系统排水顺畅,同时防止土壤颗粒随淋滤液向下流动堵塞出水通道。分段向玻璃柱中填充供试土壤,充填过程中均匀夯实供试土壤,保证土壤容重恒定。填充高度18 cm,从下到上依次为:15 cm无污染原状土壤(纯净土壤)+3 cm BDE-47人工污染土壤,避光。实验装置如图1所示。
利用蠕动泵自土柱下端注入去离子水,以驱除土柱中气泡,待土柱顶端出现水层时,即土柱达到饱水状态。饱水后用0.2% HgCl2作为抑菌渗透液对土柱从顶端渗透。1.2.1 不同初始浓度的BDE-47污染土壤淋滤实验
A柱中填充的污染土壤BDE-47浓度为100 μg·g-1,B柱中填充的污染土壤BDE-47浓度为10 μg·g-1。

图1 实验装置图Fig. 1 Schematic diagram of experimental setup
利用0.2% HgCl2溶液作为淋滤液分别淋溶土柱A和土柱B,分5次每次加入300 mL,达到拟定淋滤量1 500 mL后,停止淋滤,放置3 d使柱内水分排至接近自然状态。土柱内水分排至自然状态后拆分土柱,每3 cm取样,冷冻干燥后,称取1 g用索氏抽提法测定其中BDE-47浓度。
1.2.2 胡敏酸、富里酸溶液淋滤BDE-47污染土壤实验
C柱和D柱中填充的污染土壤BDE-47浓度为100 μg·g-1,E柱和F柱中填充的污染土壤BDE-47浓度为10 μg·g-1。0.2% HgCl2-HA溶液(HA浓度150 mg·L-1)作为淋滤液淋溶土柱C;0.2% HgCl2-FA溶液(FA浓度150 mg·L-1)作为淋滤液淋溶土柱D;0.2% HgCl2-HA溶液(HA浓度50 mg·L-1)作为淋滤液淋溶土柱E;0.2% HgCl2-FA溶液(FA浓度50 mg·L-1)作为淋滤液淋溶土柱F。各土柱中每次加入300 mL相应的淋滤液,达到拟定淋滤量1 500 mL后,停止淋滤,放置3 d使柱内水分排至接近自然状态。土柱内水分排至自然状态后拆分土柱,每3 cm取样,冷冻干燥后,称取1 g用索氏抽提法测定其中BDE-47浓度。实验方案设置如表1所示。

表1 土柱淋滤实验方案设置
1.3 分析测试方法
1.3.1 胡敏酸、富里酸的表征方法
采用varioELcube型元素分析仪,分析本实验所用胡敏酸(HA)和富里酸(FA)的元素组成以及4种主要元素(C、H、O、N)的原子数目比。
采用Nicolet 6700 FT-IR型傅里叶红外光谱仪,用KBr法制样,得到本实验所用胡敏酸(HA)和富里酸(FA)的红外光谱。
1.3.2 土壤样品预处理方法
土壤样品经冷冻干燥后,称取1 g待测土样,添加20 μL PCB141(2 000 μg·L-1)作为回收率指示物于土壤中,2层滤纸包裹,置于索氏抽提装置,在圆底烧瓶中加入150 mL体积比为1:1的丙酮和正己烷,连接装置,萃取24 h。萃取后的溶液进行旋转蒸发至2 mL后转移到多级复合层析柱内进行净化,层析柱自下而上为:6 cm氧化铝、2 cm中性硅胶、5 cm碱性硅胶、2 cm中性硅胶、8 cm酸性硅胶和2 cm无水硫酸钠。再用70 mL正己烷和二氯甲烷混合液(1:1,体积比v:v)洗脱层析柱,洗脱液旋转蒸发后氮吹并定容至1 mL,转移到2 mL棕色顶空进样瓶,备测。
称取1 g供试土壤样品,利用上述步骤进行土壤样品预处理,备测供试土壤中BDE-47本底值。
1.3.3 GC测试分析
BDE-47采用GC-μECD法测定。色谱柱采用HP-5毛细管色谱柱(30 m×0.32 mm,0.25 μm);柱升温程序如下:初始温度85 ℃,保持2 min,以18 ℃·min-1升温至320 ℃,保持3 min;进样口温度:280 ℃;载气:高纯氮气(≥99.99%),流量:3 mL·min-1;不分流进样,进样量:1 μL;检测器温度:320 ℃,尾吹气流量:25 mL·min-1。气相压力精度 0.001 psi。
样品的定量分析采用外标法,配制BDE-47标准溶液,浓度依次为10、20、50、100、400 μg·L-1。利用PCB141作为回收率指示物,同样配置梯度浓度的标准溶液,浓度依次为10、20、100、500 μg·L-1。建立浓度X-峰面积Y的定量曲线(图2),其中BDE-47标准曲线R2= 0.99962,PCB141标准曲线R2= 0.99999。计算得到样品的回收率为92.91%~106.44%。
2 结果与讨论 (Results and discussion)
2.1 胡敏酸、富里酸的元素组成及结构特性
胡敏酸和富里酸元素含量以及4种主要元素(C、H、O、N)的原子数目比值如表2所示,以文献报道中HA和FA各元素百分含量范围作为参照。
腐植酸的C元素比例可以反映其成熟度,比例越高,成熟度越高。根据测试结果,胡敏酸的C元素比例(59.46%)高于富里酸的C元素比例(45.45%),表明本研究所使用的胡敏酸成熟度大于富里酸。
H/C值可以反映物质的饱和程度,该值越大,饱和程度越高,物质含有越多的脂肪链结构和越少的芳香基团。根据测试结果,胡敏酸的H/C值(0.404)小于富里酸的H/C值(0.644),表明本研究所使用的胡敏酸的饱和程度低于富里酸,胡敏酸的脂肪链结构少于富里酸,而其芳香基团多于富里酸。
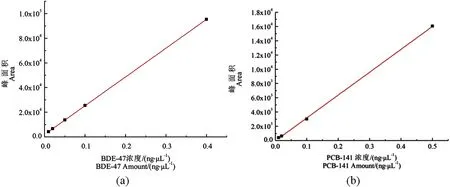
图2 BDE-47与PCB-141标准曲线Fig. 2 The standard curves of BDE-47 and PCB-141
O/C值可以反映物质的极性,该值越大,极性越强。水是一种极性物质,根据相似相溶原理,极性越强,亲水性越强。根据测试结果,胡敏酸的O/C值(0.436)小于富里酸的O/C值(0.826),表明本研究所使用的富里酸极性强于胡敏酸,具有更强的亲水性。
腐殖酸的C/N值越小,腐殖化程度越高。根据测试结果,胡敏酸的C/N值(23.05)小于富里酸的C/N值(44.94),表明本研究所用的胡敏酸腐殖化程度高于富里酸。
胡敏酸和富里酸红外光谱如图3所示。3 500~3 100 cm-1为O-H伸缩振动区间,结合1 100 cm-1处吸收峰判断-OH结构属于羧酸或是酚类:若1 100 cm-1处有明显的吸收峰,则3 500~3 100cm-1处宽吸收带为羧酸中的羟基;反之,则3 500~3 100 cm-1处宽吸收带与酚羟基有关。如图3所示,HA和FA在3 500~3 100 cm-1存在强宽峰,而在1 100 cm-1处没有明显的吸收峰,表明本研究所使用的HA和FA中均存在酚羟基。

图3 胡敏酸和富里酸的FTIR红外光谱图Fig. 3 FTIR infrared spectrum of HA and FA
3 000~2 800 cm-1为脂肪烃中甲基或亚甲基的C-H伸缩振动区间。若3 000~2 800 cm-1处有明显的吸收峰,则分子中脂肪链结构较多,芳香基团较少。如图3所示,HA在3 000~2 800 cm-1处没有明显吸收带,而FA在2 924 cm-1处存在弱吸收峰,表明本研究所使用的HA所含的脂肪链结构少于FA,而其所含芳香基团多于FA。
1 900~1 600 cm-1为羰基的伸缩振动区间。由于羰基与苯环共轭,1 900~1 600 cm-1处的吸收峰会偏移至低波数段。如图3所示,HA和FA在此区间是强吸收峰分别在1 637 cm-1和1 591 cm-1处,且HA的吸收峰低于FA的吸收峰,表明本研究所使用的HA的羧基丰度低于FA。
1 300~1 000 cm-1为C-O-C的伸缩振动区间。C-O-C的丰度越高,则物质含有越多的含氧基团,极性越高。如图3所示,FA在1 300~1 000 cm-1处出现吸收峰,而HA在该区间无吸收峰,表明本研究所使用的FA中含氧基团多于HA,极性更高,该结果与上述元素分析结果一致。
2.2 胡敏酸、富里酸对土壤中BDE-47迁移的影响
对供试原状土壤中BDE-47本底值测试的结果表明,其中BDE-47含量为0 μg·g-1。因此,供试土壤本底值对实验结果的影响可以忽略不计。
2.2.1 无HA、FA影响下土壤中BDE-47纵向分布特征解析
以0.2% HgCl2溶液为淋滤液,淋滤量达1 500 mL后,土柱A(表层污染土壤BDE-47浓度为100 μg·g-1)和土柱B(表层污染土壤BDE-47浓度为10 μg·g-1)中BDE-47的纵向分布对比如图4所示。
土柱A和土柱B中,BDE-47浓度均随深度的增加而减少,二者的纵向变化趋势一致。土柱A和土柱B的表层土壤(0~3 cm)中BDE-47残留含量分别为63.45 μg·g-1和5.42 μg·g-1;而两土柱的下层土壤(3~18 cm)中BDE-47累积含量分别为0.46 μg·g-1和0.19 μg·g-1,分别占土柱中BDE-47残留总量的0.72%和3.36%,表明大部分BDE-47残留在表层土壤中。同时,表层污染土壤BDE-47浓度高(100 μg·g-1)的土柱A中,下层土壤的BDE-47残留比例低;相反,表层污染土壤BDE-47浓度低(10 μg·g-1)的土柱B中,下层土壤的BDE-47残留比例高。

表2 胡敏酸和富里酸的元素组成
注:*O的含量等于总量减去C、H、N、S四种元素含量之和。
Note: *O concentration equals to the difference between total concentration of all the elements and the sum concentration of C, H, N, and S.

图4 土壤中BDE-47浓度纵向分布Fig. 4 Vertical distribution of BDE-47 concentration in soil columns
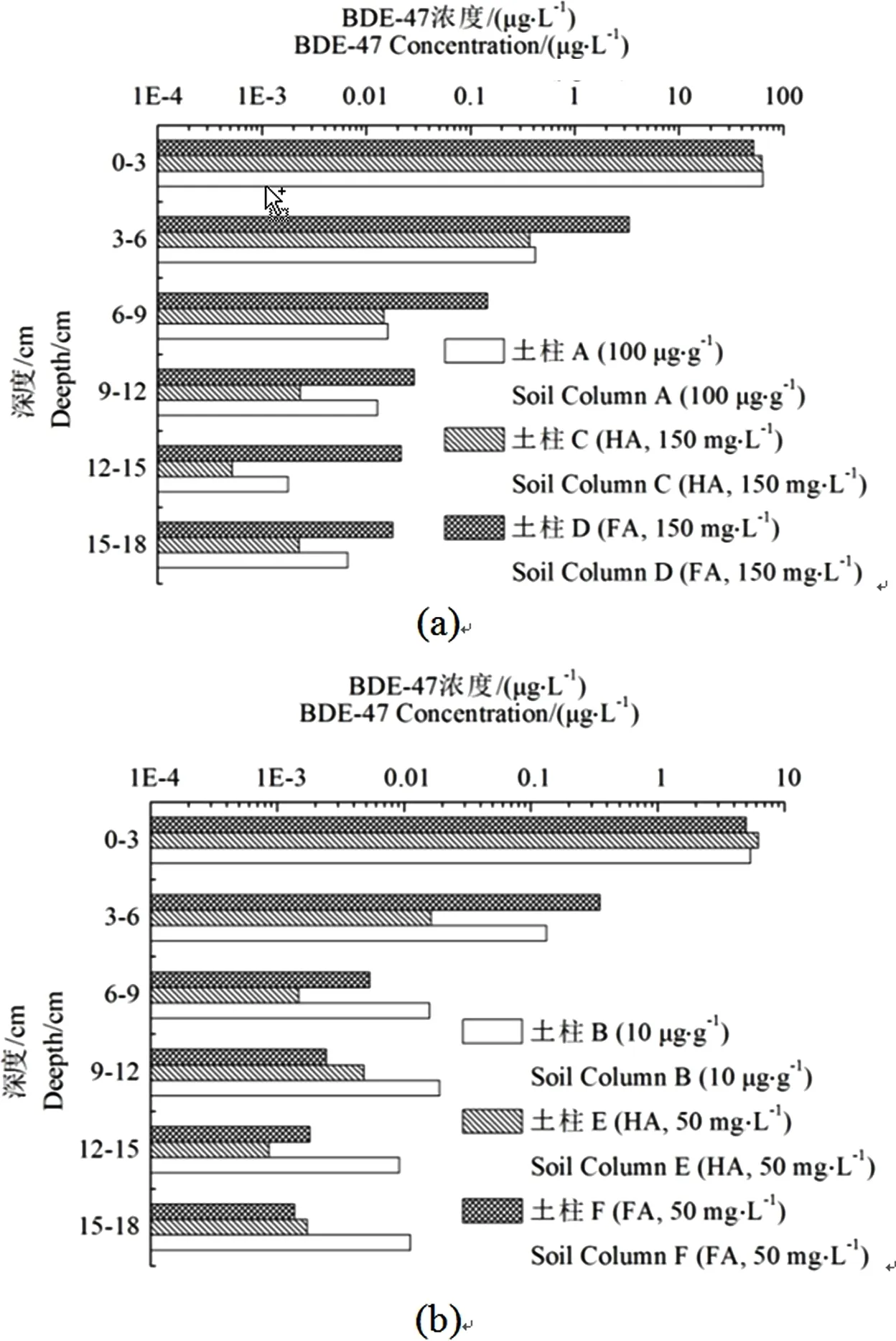
图5 HA、FA作用下土壤中BDE-47浓度纵向分布Fig. 5 Vertical distribution of BDE-47 concentration in soil columns under the influence of HA and FA
根据土柱A和土柱B淋滤前后表层污染土壤中BDE-47的浓度变化,计算其表层污染土壤中BDE-47淋失率,公式(1)如下:
(1)
得出土柱A和土柱B表层土壤中BDE-47淋失率分别为36.55%和45.80%。
土柱A的表层土壤中BDE-47淋失率(36.55%)低于土柱B(45.80%),表明土壤-地下水系统中BDE-47在其低浓度区更易被解吸,从土壤表面脱附下来,并随水流下行,因而更具纵向迁移性。土柱A表层土壤中所含的BDE-47被淋溶进入淋滤液并随淋滤液流入下层土壤的总量(36.55 μg·g-1)高于土柱B(4.58 μg·g-1),而土柱A的下层土壤BDE-47残留比例(0.72%)低于土柱B(3.36%),表明供试土壤对BDE-47的吸附点位一定,吸附能力有限,水流速度恒定的条件下,当水中的BDE-47含量超出土壤本身的吸附能力时,过量的BDE-47便无法再吸附于土壤表面,从而继续随水流向下流动,进入地下水系统。
2.2.2 HA、FA作用下土壤中BDE-47纵向分布特征解析
胡敏酸、富里酸溶液淋滤条件下BDE-47在土壤中的纵向分布如图5所示。其中,土柱A作为土柱C和土柱D的对照,土柱B作为土柱E和土柱F的对照。
实验结果表明,各土柱中BDE-47浓度均随深度的增加而减少,趋势一致。具体分析如下:
(1)HA作用下,土柱C和土柱E的下层土壤(3~18 cm)中BDE-47累积含量分别为0.39 μg·g-1和0.03 μg·g-1,分别低于对照组(土柱A和土柱B)下层土壤中BDE-47的累积含量(0.46 μg·g-1和0.19 μg·g-1);土柱C和土柱E下层土壤(3~18 cm)中BDE-47的残留比例分别为0.62%和0.40%,同样分别低于对照组下层土壤中BDE-47的残留比例(0.72%和3.36%)。该结果表明,在HA的影响下,BDE-47虽然会随水流向土壤深层迁移,但较少在土壤中残留,即HA作用下BDE-47更易随地下水流迁移而不易吸附残留于土壤表面。
(2)FA作用下,土柱D和土柱F的下层土壤(3~18 cm)中BDE-47累积含量分别为3.54 μg·g-1和0.36 μg·g-1,分别高于对照组(土柱A和土柱B)下层土壤中BDE-47的累积含量(0.46 μg·g-1和0.19 μg·g-1);土柱D和土柱F下层土壤(3~18 cm)中BDE-47的残留比例分别为6.40%和6.71%,同样分别高于对照组下层土壤中BDE-47的残留比例(0.72%和3.36%)。该结果表明,在FA的影响下,BDE-47不仅会随水流向土壤深层迁移,并且会增强土壤对其的吸附以使其更易残留在土壤中,即FA作用下BDE-47随地下水流的迁移被阻滞,吸附残留于土壤表面。
HA和FA是复杂的高分子有机物,其分子结构中既含有疏水性基团(脂肪链、苯环等),也含有亲水性基团(羧基、酚羟基、羰基等),因此其对于BDE-47在土壤-地下水系统中的迁移影响是双重的:一方面,芳香基团(疏水性基团)是腐殖酸结合多环芳烃的核心官能团,芳香基团与多环芳烃之间以分子间π-π电子给体/受体作用为主要结合方式,疏水性基团的存在使得BDE-47易与HA和FA结合;另一方面,亲水性基团的存在能够增强与FA和HA的BDE-47在土壤-地下水系统中的迁移性。本研究所使用的HA和FA的元素组成和结构特征表明,HA含有较多的芳香基团,成熟度、腐殖化程度较高,具有较强的疏水性;FA极性较强,具有较强的亲水性。结合淋滤实验结果,分析可知:HA与BDE-47分子之间π-π共轭作用强烈,使得BDE-47更易与淋滤液中的HA相结合并随其流动在土壤-地下水系统中迁移,因而淋滤液中的HA会促进BDE-47随地下水流的迁移,使得BDE-47更易进入地下水系统,污染地下水;反之,FA与BDE-47分子之间π-π共轭作用较弱,该作用会使表层污染土壤中的BDE-47解吸并随含有FA的淋滤液向下迁移,然而却未能维持BDE-47随含FA的淋滤液长距离迁移,以致BDE-47更易吸附于下层土壤表面而非随含FA的淋滤液流出土壤系统,因而淋滤液中的FA会阻滞BDE-47进入地下水系统。
在胡敏酸(HA)的影响下,表层土壤中的BDE-47易随水流纵向迁移而非残留在土壤表面,增加了其进入地下水系统并对其造成污染的风险。富里酸(FA)促进了BDE-47在土壤系统中的分布,阻滞了土壤系统中BDE-47进入地下水系统。由于不同土壤的有机组分存在差异,而腐殖质又是土壤的重要有机组分之一,明确胡敏酸和富里酸对土壤-地下水系统中BDE-47迁移的影响,通过对土壤有机组分的分析来评估BDE-47的潜在污染风险具有极其重要的现实意义。
致谢:感谢中国地质大学(武汉)环境学院王亚芬副教授在文章修改中给予的帮助。感谢审稿专家和编辑在文章评审中提出的宝贵意见。
[1] Darnerud P O. Toxic effects of brominated flame retardants in man and in wildlife [J]. Environment International, 2003, 29(6): 841-853
[2] Jansson B, Asplund L, Olsson M. Brominated flame retardants-ubiquitous environmental pollutants [J]. Chemosphere, 1987, 16(10): 2343-2349
[3] Mcdonald T A. A perspective on the potential health risks of PBDEs [J]. Chemosphere, 2002, 46(5): 745-755
[4] Frederiksen M, Vorkamp K, Thomsen M, et al. Human internal and external exposure to PBDEs-A review of levels and sources [J]. International Journal of Hygiene and Environmental Health, 2009, 212(2): 109-134
[5] World Health Organization (WHO). Brominated Diphenyl Ethers [M]. Geneva: WHO, 1994: 347
[6] Mai B X, Chen S J, Luo X J, et al. Distribution of polybrominated diphenyl ethers in sediments of the Pearl River Delta and adjacent South China Sea [J]. Environmental Science & Technology, 2005, 39(10): 3521-3527
[7] Han W, Feng J, Gu Z, et al. Polybrominated diphenyl ethers in the atmosphere of Taizhou, a major e-waste dismantling area in China [J]. Bulletin of Environmental Contamination and Toxicology, 2009, 83(6): 783-788
[8] Li Y, Jiang G, Wang Y, et al. Concentrations, profiles and gas-particle partitioning of PCDD/Fs, PCBs and PBDEs in the ambient air of an E-waste dismantling area, southeast China [J]. Chinese Science Bulletin, 2008, 53(4): 521-528
[9] Zou M, Ran Y, Gong J, et al. Polybrominated diphenyl ethers in watershed soils of the Pearl River Delta, China: Occurrence, inventory, and fate [J]. Environmental Science &Technology, 2007, 41(24): 8262-8267
[10] Yogui G T, Sericano J L. Polybrominated diphenyl ether flame retardants in the US marine environment: A review [J]. Environment International, 2009, 35(3): 655-666
[11] 单慧媚, 马腾, 杜尧, 等. 多溴联苯醚在河套农灌区土壤和水体中的分布特征[J]. 环境科学与技术, 2013, 36(6): 37-41
Shan H M, Ma T, Du Y, et al. Distribution of PBDEs in soil and water from hetaoagriculture irrigation area [J]. Environmental Science & Technology, 2013, 36(6): 37-41 (in Chinese)
[12] Cai Z, Jiang G. Determination of polybrominated diphenyl ethers in soil from e-waste recycling site [J]. Talanta, 2006, 70(1): 88-90
[13] Zhao G, Wang Z, Dong M H, et al. PBBs, PBDEs, and PCBs levels in hair of residents around e-waste disassembly sites in Zhejiang Province, China, and their potential sources [J]. Science of the Total Environment, 2008, 397(1-3): 46-57
[14] 单慧媚. 污灌区土壤—地下水系统中PBDEs地球化学行为及其原位测试新技术[D]. 武汉: 中国地质大学(武汉), 2014: 65-68
Shan H M. Geochemical behavior of PBDEs and their in situ measurement in soil-groundwater system in the Sewage Irrigation area [D]. Wuhan: China University of Geosciences (Wuhan), 2014: 65-68 (in Chinese)
[15] Sinclair Knight Merz Pty. Ltd. Environmental Water Requirements to Maintain Groundwater Dependent Ecosystems [M]. Australia: Environment Australia, 2001: 140
[16] 李喜林. 铬渣堆场渗滤液对土壤—地下水系统污染规律研究[D]. 阜新: 辽宁工程技术大学, 2012: 19-20
Li X L. Study on pollution laws of leachate of chromium slag site for soil-groundwater system [D]. Fuxin: Liaoning Technical University, 2012: 19-20 (in Chinese)
[17] Murray B B R, Zeppel M J, Hose G C, et al. Groundwater-dependent ecosystems in Australia: It's more than just water for rivers [J]. Ecological Management & Restoration, 2008, 4(2): 110-113
[18] Cornelissen G, Gustafsson O, Bucheli T D, et al. Extensive sorption of organic compounds to black carbon, coal, and kerogen in sediments and soils: Mechanisms and consequences for distribution, bioaccumulation, and biodegradation [J]. Environmental Science & Technology, 2005, 39(18): 6881-6895
[19] 马爱军. 水溶性有机物和土壤胶体对草萘胺环境行为的影响[D]. 南京: 南京农业大学, 2005: 62-74
MaA J. Effects of dissolved organic matter and soil colloid on napropmide environmental behavior in soil system [D]. Nanjing: Nanjing Agricultural University, 2005: 62-74 (in Chinese)
[20] Jerez J, Flury M. Humic acid-, ferrihydrite-, and aluminosilicate-coated sands for column transport experiments [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006, 273(1-3): 90-96
[21] 商书波. 包气带中的土壤可移动胶体及对重金属迁移影响的研究[D]. 长春: 吉林大学, 2008: 95-137
Shang S B. Study on the impact of soil colloid on heavy metals migration in vadose zone [D]. Changchun: Jilin University, 2008: 95-137 (in Chinese)
[22] 牛育华, 李仲谨, 郝明德, 等. 腐殖酸的研究进展[J]. 安徽农业科学, 2008, 36(11): 4638-4639
Niu Y H, Li Z J, Hao M D, et al. Research development of humic acid [J]. Journal of Anhui Agricultural Science, 2008, 36(11): 4638-4639 (in Chinese)
[23] Qin X, Liu F, Wang G. Fractionation and kinetic processes of humic acid upon adsorption on colloidal hematite in aqueous solution with phosphate [J]. Chemical Engineering Journal, 2012, 209: 458-463
[24] Tatzber M, Stemmer M, Splegel H, et al. FTIR-spectroscopic characterization of humic acids and humin fractions obtained by advanced NaOH, Na4P2O7, and Na2CO3extraction procedures [J]. Journal of Plant Nutrition and Soil Science, 2007, 170(4): 522-529
[25] Ellerbrock R H, Hohn A, Gerke H H. Characterization of soil organic matter from a sandy soil in relation to management practice using FT-IR spectroscopy [J]. Plant and Soil, 1999, 213(1-2): 55-61
[26] Yu S, Zou P, Zhu W, et al. Effects of humic acids and microorganisms on decabromodiphenyl ether, 4,4’-dibromodiphenyl ether and anthracite transportation in soil [J]. Science China Chemistry, 2010, 53(4): 950-968
[27] Liu W, Cheng F, Li W, et al. Desorption behaviors of BDE-28 and BDE-47 from natural soils with different organic carbon contents [J]. Environmental Pollution, 2012, 163: 235-242
[28] Xin J, Liu R, Fan H, et al. Role of sorbent surface functionalities and microporosity in 2,2',4,4'-tetrabromodiphenyl ether sorption onto biochars [J]. Journal of Environmental Sciences (China), 2013, 25(7): 1368-1378
[29] 刘锐龙. 生物质炭对BDE-47在土壤中吸附和解吸行为的影响[D]. 北京: 清华大学, 2013: 74-75
Liu R L. The effects of bio-char on sorption and desorption behavior of BDE-47 in natural soil [D]. Beijing: Tsinghua University, 2013: 74-75 (in Chinese)
[30] Rice J A, MacCarthy P. Statistical evaluation of the elemental composition of humic substances [J]. Organic Geochemistry, 1991, 17(5): 635-648
◆
Effects of Humic Acid and Fulvic Acid on the Transportation of BDE-47 in Soil-Groundwater System
Wang Chunlei1,2, Liu Lu1,2, Ma Teng1,2,*, Chen Liuzhu1,2, Cai Hesheng1,2
1. School of Environmental Studies, China University of Geosciences at Wuhan, Wuhan 430074, China 2. State Key Laboratory of Biogeology and Environmental Geology, China University of Geosciences, Wuhan 430074, China
Polybrominated diphenyl ethers (PBDEs), as a kind of persistent organic pollutants, have been pervasively detected in the soil-groundwater systems. Determining the effects of soil composition on the transportation behaviors of PBDEs is the key of tracing their fate in the soil-groundwater system. The transportation of 2,2',4,4'-tetrabromodiphenyl ether (BDE-47), a typical congener of PBDEs, was examined within soil columns containing agricultural soil amended with BDE-47 (100 μg·g-1and 10 μg·g-1) at the surface layer, using humic acid (HA) and fulvic acid (FA) (150 mg·L-1and 50 mg·L-1) as the leaching solutions, respectively. Results showed that in the soil below the surface layer, the residual ratios of BDE-47 with initial concentrations at 100 μg·g-1and 10μg·g-1were 0.62% and 0.40% in the HA leaching groups, lower than that in the control groups of 0.72% and 3.36%, respectively. However, in the soil below the surface layer, the residual ratios of BDE-47 in the FA leaching groups were 6.40% and 6.71%, higher than that in the control groups, respectively. Combined with the element component analysis and structure feature analysis of HA and FA, HA of strong hydrophobicity could promote the migration of BDE-47 with the water into the groundwater system, while the hydrophilic FA promoted the dispersion of BDE-47 in soil system, but could retard BDE-47 to enter the groundwater system. This work provided fundamental evidence for evaluating the effects of HA and FA on the transportation of BDE-47 in the soil-groundwater system.
BDE-47; humic acid; fulvic acid; transportation; leach
10.7524/AJE.1673-5897.20151128001
国家自然科学基金(面上项目)资助(41372252)
王春蕾(1991-),女,硕士研究生,研究方向为微生物地球化学、环境同位素,E-mail: carolinell321@yeah.net
*通讯作者(Corresponding author), E-mail: mateng@cug.edu.cn
2015-11-28 录用日期:2015-12-30
1673-5897(2016)2-501-08
X171.5
A
简介:马腾(1972—),男,博士,教授,主要研究方向地下水污染与防治、地下水与环境变化。
王春蕾, 刘路, 马腾, 等. 胡敏酸、富里酸对土壤-地下水系统中BDE-47迁移的影响[J]. 生态毒理学报,2016, 11(2): 501-508
Wang C L, Liu L, Ma T, et al. Effects of humic acid and fulvic acid on the transportation of BDE-47 in soil-groundwater system [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 501-508 (in Chinese)
