吉西他滨联合顺铂治疗晚期三阴乳腺癌的疗效观察
2016-11-29柏峰方献英宋波张宇
柏峰方献英宋波张宇
作者单位:464000信阳河南省信阳市中心医院肿瘤内科
临床经验
吉西他滨联合顺铂治疗晚期三阴乳腺癌的疗效观察
柏峰方献英宋波张宇
作者单位:464000信阳河南省信阳市中心医院肿瘤内科
目的评价吉西他滨联合顺铂(GP方案)治疗晚期三阴乳腺癌(triple negative breast cancer,TNBC)的疗效和不良反应。方法回顾性分析晚期TNBC患者37例,采用顺铂(DDP)25 mg/m2静脉滴注,d1~d3;吉西他滨(GEM)1 000 mg/m2静脉滴注,d1、d8;21 d为1个周期,分析临床疗效和不良反应。结果完全缓解(CR)1例、部分缓解(PR)16例、疾病稳定(SD)12例、疾病进展(PD)8例,治疗有效率(RR)为45.9%。中位无进展生存时间(PFS)为5.5个月,中位总生存时间(OS)为15.5个月,主要不良反应为骨髓抑制和消化道反应。结论GP方案治疗晚期TNBC疗效确切,耐受性较好,可作为解救方案。
乳腺肿瘤;三阴乳腺癌;吉西他滨;顺铂;化疗
三阴乳腺癌(triple negative breast cancer,TNBC)是乳腺癌的一种亚型,主要特征为雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)和人类表皮生长因子受体-2(human epidemic growth factor receptor 2,HER-2)均表达阴性,与其他亚型相比复发转移率高,预后不良。TNBC不适合内分泌治疗和针对HER-2阳性的曲妥珠单抗靶向药物治疗,化疗是主要治疗手段[1]。TNBC早期化疗多已应用蒽环类和紫杉类药物,因此对耐药晚期TNBC化疗方案的选择成为临床治疗中的难题。吉西他滨联合顺铂(GP方案)在各种晚期肿瘤治疗中疗效明显[2],为探讨GP方案治疗晚期TNBC的临床可行性,本研究回顾性分析我科应用GP方案治疗37例晚期TNBC患者的临床疗效和不良反应。现报道如下。
1 资料与方法
1.1一般资料
收集我院2010年7月至2015年2月收治的37例晚期TNBC临床资料。患者既往均行乳腺癌根治术并经病理检查证实为TNBC,辅助化疗或姑息化疗中均接受蒽环类和紫杉类药物化疗失败或有效但缓解期小于6个月。患者年龄31~72岁,中位47岁。绝经前23例,绝经14例。浸润导管癌35例,浸润小叶癌1例,髓样癌1例。肺转移17例,骨转移14例,肝转移11例,脑转移7例,局部复发无远处转移6例。
1.2化疗方案
采用GP方案:顺铂(DDP)25 mg/m2静脉滴注,d1~d3;吉西他滨(GEM)1 000 mg/m2静脉滴注,d1、d8;21 d为1个周期,至少化疗2个周期。
1.3疗效评价和不良反应评估
根据实体肿瘤疗效评价标准(RECIST 1.0),每2周期评价疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),有效率(RR)为CR+ PR。根据美国国立癌症研究所毒性分级标准(3.0版),每2周期化疗后评估不良反应。
1.4随访
治疗结束后每2~3个月电话随访1次,随访至2016年1月,随访5~35个月,失访1例,死亡26例,至今存活10例。
1.5统计学方法
采用SPSS 19.0软件处理数据,计数资料比较采用Fisher确切概率法,无进展生存时间(PFS)和总生存时间(OS)采用Kaplan-Meier法分析,log-rank检验比较生存差异。以P<0.05为差异有统计学意义。
2 结果
2.1近期疗效
每例患者至少完成2个周期化疗,37例患者均可评价疗效,共完成127个周期化疗,平均3.43个周期。获CR 1例,PR 16例,SD 12例,PD 8例,RR为45.9%。各亚组疗效分析结果见表1。

表1 GP方案治疗晚期TNBC的疗效[n(%)]
2.2生存分析
37例患者中位PFS为5.5个月(95%CI:4.3~6.6),中位OS为15.5个月(95%CI:10.6~20.3)。亚组分析:转移部位个数≤1个组患者中位PFS为6.8个月,高于>1个组的4.5个月,但差异无统计学意义(P=0.138)(图1);术后PFS≤2年组患者中位PFS为4.8个月,低于>2年组的5.8个月,差异亦无统计学意义(P=0.583)(图2)。

图1 不同转移部位个数患者中位PFS的生存曲线
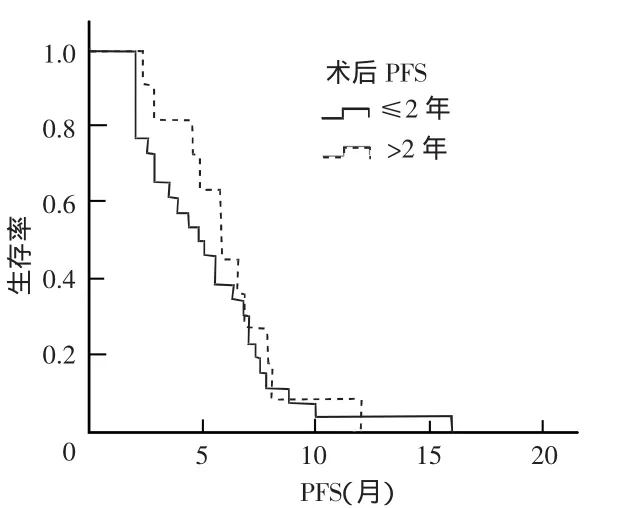
图2 不同术后中位PFS患者的生存曲线
2.3不良反应
主要不良反应为骨髓抑制和消化道反应,无化疗相关性死亡。中性粒细胞减少23例(62.2%),Ⅲ级以上8例(21.6%);血小板减少19例(51.4%),Ⅲ级以上10例(27%),经粒细胞集落刺激因子或重组人白介素-11治疗后骨髓抑制均可恢复;血红蛋白减少21例(56.8%),Ⅲ级以上4例(10.8%);恶心呕吐22例(59.5%),Ⅲ级以上4例(10.8%),予以对症止吐治疗后均可缓解;乏力14例(37.8%),Ⅲ级以上6例(16.2%)。见表2。

表2 GP方案治疗晚期TNBC的不良反应[n(%)]
3 讨论
2000年Perou等[3]应用基因微阵列技术将乳腺癌分成Luminal A、Luminal B、HER-2过表达型、基底细胞样型和正常乳腺样型五种不同的分子亚型,其中基底细胞样型预后较差,而80%的TNBC为基底细胞样型[4]。TNBC作为乳腺癌的一种亚型,与其他亚型相比预后不良,大多在3年内复发转移[5]。对一线治疗后复发转移的TNBC患者,目前二线治疗没有标准方案。
TNBC多伴乳腺癌易感基因(BRCA-1)突变,而BRCA-1参与DNA损伤修复,BRCA-1表达下调或缺失时,提示DNA损伤类药物铂类治疗有效[6]。吉西他滨是嘧啶类抗代谢药物,属于周期特异性药物,可杀灭S期细胞,并阻止G1期向S期过渡,在晚期乳腺癌中有确定的临床疗效[7]。与顺铂联合具有协同作用。因此,GP方案成为二线治疗TNBC的一个可选方案,其疗效在临床中陆续得到证实[8~10]。
O′Shaughnessy等[11]应用吉西他滨联合卡铂治疗转移性TNBC,结果一线治疗有效率为57%,二三线治疗有效率为43%,中位PFS为4.1个月,中位OS为11.1个月;最常见的Ⅲ级或Ⅳ级不良反应包括中性粒细胞减少(53%)、贫血(22%)、血小板减少(24%)和白细胞减少(15%)。Koshy等[12]应用GP方案治疗17例晚期TNBC患者,结果中位PFS为5.3个月。Ozkan等[13]回顾性分析用GP方案治疗的33例蒽环类和紫杉类药物耐药的晚期TNBC患者,结果中位PFS为5个月,中位OS为14个月;最常见的Ⅲ级和Ⅳ级不良反应分别为中性粒细胞减少(27.7%)和血小板减少(24.9%)。刘娜等[14]应用GP方案治疗32例对蒽环类和紫杉类耐药的晚期乳腺癌患者,有效率为34.4%,中位PFS为5.2个月,主要不良反应为骨髓抑制和消化道反应,Ⅲ级和Ⅳ级中性粒细胞和血小板减少发生率分别为33%和19%。本研究的有效率为45.9%,中位PFS为5.5个月,中位OS为15.5个月,与上述研究结果相似。
本研究亚组分析显示:术后PFS≤2年组有效率为34.6%,明显低于>2年组的72.7%(P=0.069)。转移部位个数≤1个组有效率为75%,高于>1个组有效率的32%,但两组差异无统计学意义,有待进一步研究。
综上,GP方案治疗晚期TNBC具有较好的疗效和耐受性,可作为晚期TNBC蒽环类和紫杉类耐药后解救方案的一种选择。由于本研究属于回顾性研究且例数较少,有关结论仍需进一步证实。
[1]Yagata H,KajiuraY,Yamauchi H.Current strategy for triple-negative breast cancer:appropriate combination of surgery,radiation,and chemotherapy[J].Breast Cancer,2011,18(3):165-173.
[2]张定清.吉西他滨联合铂类化疗方案治疗晚期恶性肿瘤的临床观察[J].中国癌症防治杂志,2015,7(1):49-51.
[3]Perou CM,Sørlie T,Eisen MB,et al.Molecular portraits of human breast tumours[J].Nature,2000,406(6797):747-752.
[4]Foulkes WD,SmithIE,Reis-FilhoJS.Triple-negativebreast cancer[J]. N Engl J Med,2010,363(20):1938-1948.
[5]Dent R,Trudeau M,Pritchard KI,et al.Triple-negative breast cancer:clinical featuresandpatternsofrecurrence[J].Clin Cancer Res,2007,13(15 Pt 1):4429-4434.
[6]Byrski T,Gronwald J,Huzarski T,et al.Pathologic complete response rates in young women with BRCA1-positive breast cancers after neoadjuvant chemotherapy[J].J Clin Oncol,2010,28(3):375-379.
[7]农先胜,黄显实.卡培他滨单药或联合用药治疗复发/转移性乳腺癌的疗效观察[J].中国癌症防治杂志,2012,4(4):336-339.
[8]Erten C,Demir L,Somali I,et al.Cisplatin plus gemcitabine for treatment of breast cancer patients with brain metastases;a preferential option for triple negative patients?[J].Asian Pac J Cancer Prev,2013,14(6):3711-3717.
[9]Maisano R,Zavettieri M,Azzarello D,et al.Carboplatin and gemcitabine combination in metastatic triple-negative anthracycline-and taxane-pretreated breast cancer patients:a phaseⅡstudy[J].J Chemother,2011,23(1):40-43.
[10]Zhang J,Wang Z,Hu X,et al.Cisplatin and gemcitabine as the first line therapy in metastatic triple negative breast cancer[J].Int J Cancer,2015,136(1):204-211.
[11]O'Shaughnessy J,Schwartzberg LS,Danso MA,et al.A randomized phase III study of iniparib(BSI-201)in combination with gemcitabine/carboplatin(G/C)in metastatic triple-negative breast cancer(TNBC)[J].J Clin Oncol,2011,29(15-suppl):1007.
[12]Koshy N,Quispe D,Shi R,et al.Cisplatin-gemcitabine therapy in metastatic breast cancer:Improved outcome in triple negative breast cancer patients compared to non-triple negative patients[J].Breast 2010,19(3):246-248.
[13]Ozkan M,Berk V,Kaplan MA,et al.Gemcitabine and cisplatin combination chemotherapy in triple negative metastatic breast cancer previously treated with a taxane/anthracycline chemotherapy;multicenter experience[J].Neoplasma,2012,59(1):38-42.
[14]刘娜,马天江,支卫国,等.吉西他滨联合顺铂治疗三阴性晚期乳腺癌的临床观察[J].现代肿瘤医学,2015,23(16):2308-2310.
[2016-06-14收稿][2016-09-12修回][编辑江德吉]
临床经验
R737.9;R730.53
A
1674-5671(2016)05-03
10.3969/j.issn.1674-5671.2016.05.10
