钨掺杂介孔TiO2微球紫外光下降解罗丹明B的研究
2016-11-17郑健田颖程国伟
郑健,田颖,程国伟
(大连交通大学 环境与化学工程学院,辽宁 大连 116028)*
钨掺杂介孔TiO2微球紫外光下降解罗丹明B的研究
郑健,田颖,程国伟
(大连交通大学 环境与化学工程学院,辽宁 大连 116028)*
以钛酸四异丙酯为钛源,钨酸铵为钨源,通过水热法制备了W掺杂介孔TiO2微球.所得样品用X射线衍射(XRD)、扫描电镜(SEM)、氮吸附、紫外可见漫反射等测试方法表征.以罗丹明B为目标降解物,考察了钨掺杂介孔TiO2在紫外光下对罗丹明B的催化活性.结果表明,TiO2微球平均孔径10 nm左右.钨掺杂对TiO2微球结构与晶型没有影响,但是缩小了二氧化钛的光吸收范围,适量掺杂钨离子后,TiO2吸收边产生蓝移,吸收波长从384 nm缩短为378 nm.钛钨摩尔比为0.2%的钨掺杂TiO2活性最好,对罗丹明B降解率较未掺杂TiO2提高约30%.
介孔二氧化钛微球;钨掺杂;水热合成;光催化活性
0 引言
自从1972年Fujishima和Honda 发现TiO2在紫外光照射下能持续发生水的氧化还原反应,并产生氢气,揭开了TiO2作为光催化材料发展的序幕[1].Frank等人于1977年将光催化技术应用于污染物在水体系中的降解并取得突破性进展,引领了光催化氧化技术在污染物治理方面的应用[2].近年来,TiO2以其无毒、稳定、高效等性质成为了半导体光催化材料在环境治理应用领域的典型代表.但是较大的禁带宽度以及较高的电子-空穴复合率极大地限制了其在实际生产中的应用[3].大量的研究发现,在TiO2中掺杂一定量的金属离子可以抑制光生电子和空穴的复合,这是由于金属离子可以有效地捕获光生电子,从而提高光生电子空穴对的分离效率.Choi等发现掺杂Fe3+、Ru3+、V4+、Mo5+、Os3+、Re5+和Rh3+等离子可以提高TiO2紫外光降解CHCl3的活性[4].Chen等研究表明,掺杂Fe或Ni离子后,TiO2的紫外光
催化活性提高.也有研究表明通过对TiO2进行离子掺杂,缩短其能带间隙,扩展其光响应范围,增强其可见光催化活性.Ni等采用溶液燃烧法制备了Cu2+、Mn2+、Ce3+和Sn4+离子掺杂的TiO2光催化剂,发现所制样品在可见光区的吸收明显增强[5].过渡金属元素W6+与Ti4+有相似的原子半径(0.61Å和0.62 Å)使W6+取代Ti4+成为可能[6].另外W6+较Ti4+冗余的两个正电荷可作为电子受体,抑制光生电子的复合从而提高光催化活性[7-8].
另一方面,形貌和微观结构对TiO2的光催化性能也有很大的影响.介孔结构的二氧化钛材料由于具有密度低、比表面积大和光吸收效率高等优点,引起了研究者的普遍关注[9-11].同时介孔能够成为通道,有利于大分子有机物进入到微球内部[12-14].本文以钛酸四异丙酯为钛源,以钨酸铵为钨源通过水热法制备了介孔TiO2微球,并研究了该光催化剂的可见光光催化活性.
1 实验部分
1.1 催化剂的制备
以钛酸四异丙酯为钛源,钨酸铵为钨源,参照文献合成钨掺杂二氧化钛[15].室温下,将无水乙醇、十六胺、钛酸四异丙酯、去离子水、氯化钾和钨酸铵以物质的量之比为236.5∶0.5∶6∶0.005 5∶1∶x依次加入500 mL烧杯中,以400 r/min匀速搅拌5 min,静止沉淀18 h.洗涤、过滤,将所得沉淀转移至100 mL聚四氟乙烯水热釜,依次加入40 mL乙醇、20 mL水,于160℃保温16 h.待水热釜冷却后,将沉淀用乙醇和水分别清洗3次,再将沉淀在80℃下干燥1 h.将所得前驱体至于马弗炉中升温至500℃灼烧2 h得到最终产物.以钛钨物质的量之比命名催化剂,如当钨钛的物质的量之比为n(W)∶n(Ti)=0.2%时,则材料命名为TiO2∶W-0.2at%.
1.2 实验设备及表征方法
用日本Rigaku公司生产的Miniflex600型X射线粉末衍射仪对样品进行X射线(XRD)图谱测定.工作条件为:用Cu Ka为辐射源,扫描速率为1°/min,加速电压和应用电流分别为40 kV和15 mA.采用日本Hitachi U-3900型紫外-可见分光光度计测定样品的可见光(UV-Vis)漫反射光谱,扫描范围200~800 nm,以标准BaSO4作为参比.样品形貌使用日本JSM-7800F型场发射扫描电子显微镜测定.催化剂的比表面积用ASAP 2420型氮吸附/脱附仪测定.
1.3 光催化活性分析
在室温下通过降解罗丹明B水溶液来评价光催化活性.在直径为4.5 cm的定制容器中加入50 mL浓度为15 mg/L的罗丹明B水溶液,循环水用以维持反应体系温度恒定,再将0.05 g催化剂分散在溶液中,于暗处搅拌60 min后在可见光照射下进行光催化实验,以氙灯(PLS-SXE300)为光源,紫外光照射下反应开始后每隔20 min取1 mL反应溶液离心分离,再用紫外-可见吸收光谱仪测定反应溶液中的RhB浓度.
2 实验结果与讨论
2.1 催化剂的晶型和形貌
图1为W掺杂TiO2粒子的SEM图片,1(a)为未掺杂的TiO2的形貌,从图中可以看出未掺杂TiO2为规则球体,单分散性较好,TiO2前驱体在160℃的乙醇和水的混合液中水热18h得到了介孔结构.介孔球平均直径在0.5 um左右.TiO2∶W-0.2at%、TiO2∶W-1at%、TiO2∶W-4at%样品分别如图1(b)、(c)、(d)所示,钨掺杂的样品维持了介孔微球的形状,具有良好的分散性.可以看出钨离子的掺杂没有对TiO2的形貌造成影响,这与钨的较低掺杂量有关.介孔结构的存在大大增加了TiO2催化剂的比表面积,有利于有机物在催化剂表面吸附,对提高光催化效率有重要作用.

(a)

(b)

(c)

(d)
图2为样品的XRD谱图.由图可见,水热法合成的TiO2样品在2θ= 25.3°、37.8°和48.0°处出现明显的衍射峰, 分别对应于锐钛矿(101)、(004)和(200)面(JCPDS 65-5714),钨掺杂改性后的样品保持了原有的锐钛矿结构.说明钨的掺杂对TiO2的晶型没有产生影响.在钛钨摩尔比n(W)∶n(Ti)=4%时,XRD仍没有探测到WO3的衍射峰的存在,这说明钨原子可能进入TiO2晶格,形成了W-O-Ti或者分散在TiO2表面[16].
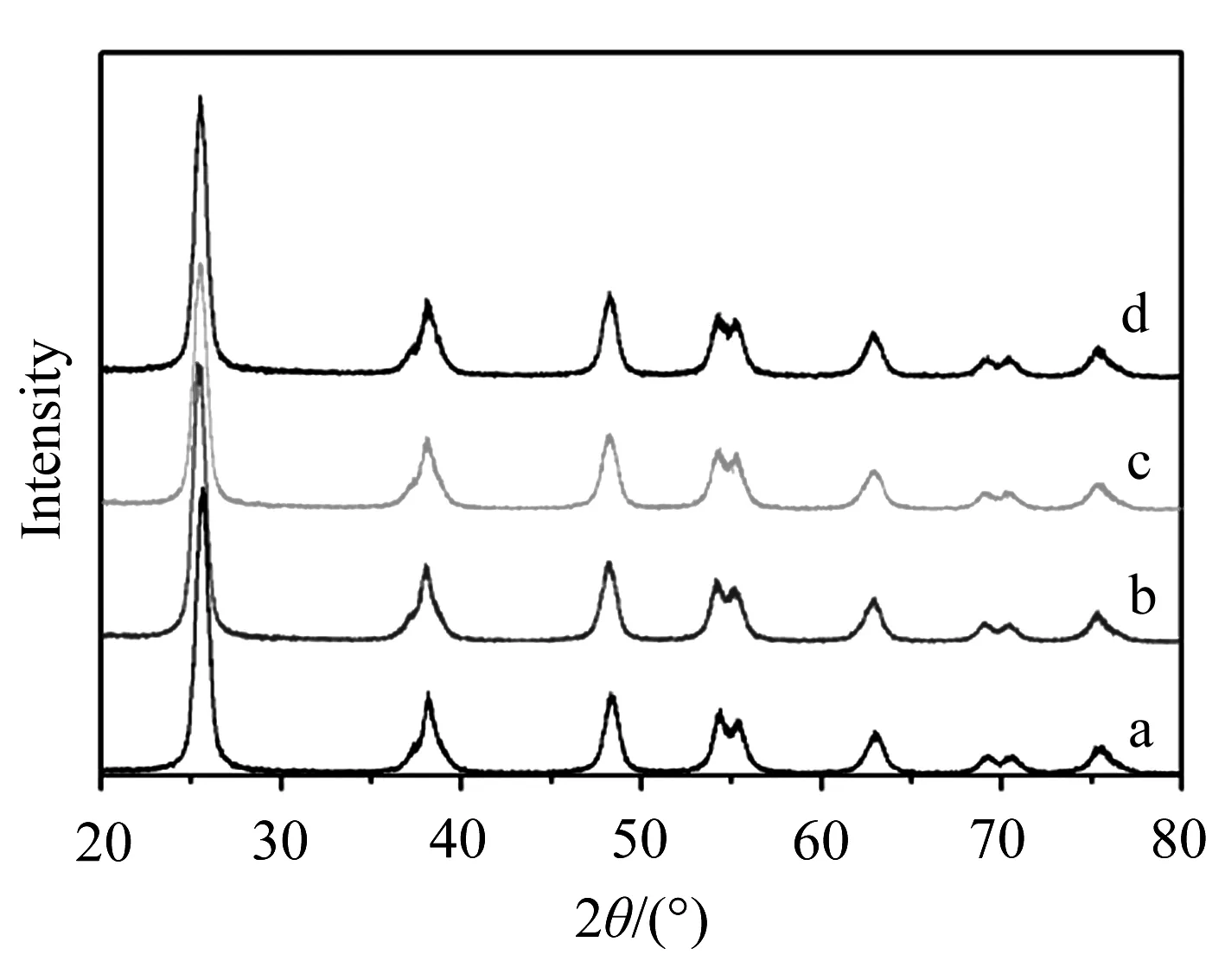
图2 TiO2(a),TiO2∶W-0.2at%(b),TiO2∶W-1at%(c),TiO2∶W-4at%(d)的XRD图谱
2.2 紫外-可见漫反射光谱分析
图3(a)为样品的UV-vis DRS谱图,从图中可以看出,钨的掺杂对二氧化钛的本征吸收产生了影响,与未掺杂的二氧化钛相比,TiO2∶W-0.2at%、TiO2∶W-1at%吸收边明显蓝移,吸收波长分别从384 nm移动到378 nm和377 nm,这与Zhang等人报道相一致[17-18].根据Burstein-Moss效应,对TiO2半导体进行重电子掺杂,费米能级进入导带,杂质能级与导带中能级发生杂化,有效光学带隙增大,本征光吸收边向短波长方向移动,这说明吸收边的蓝移是由钨离子的掺杂造成.TiO2∶W-4at%没有观察到明显的蓝移,说明适当浓度的钨掺杂对TiO2本征吸收有重要影响.
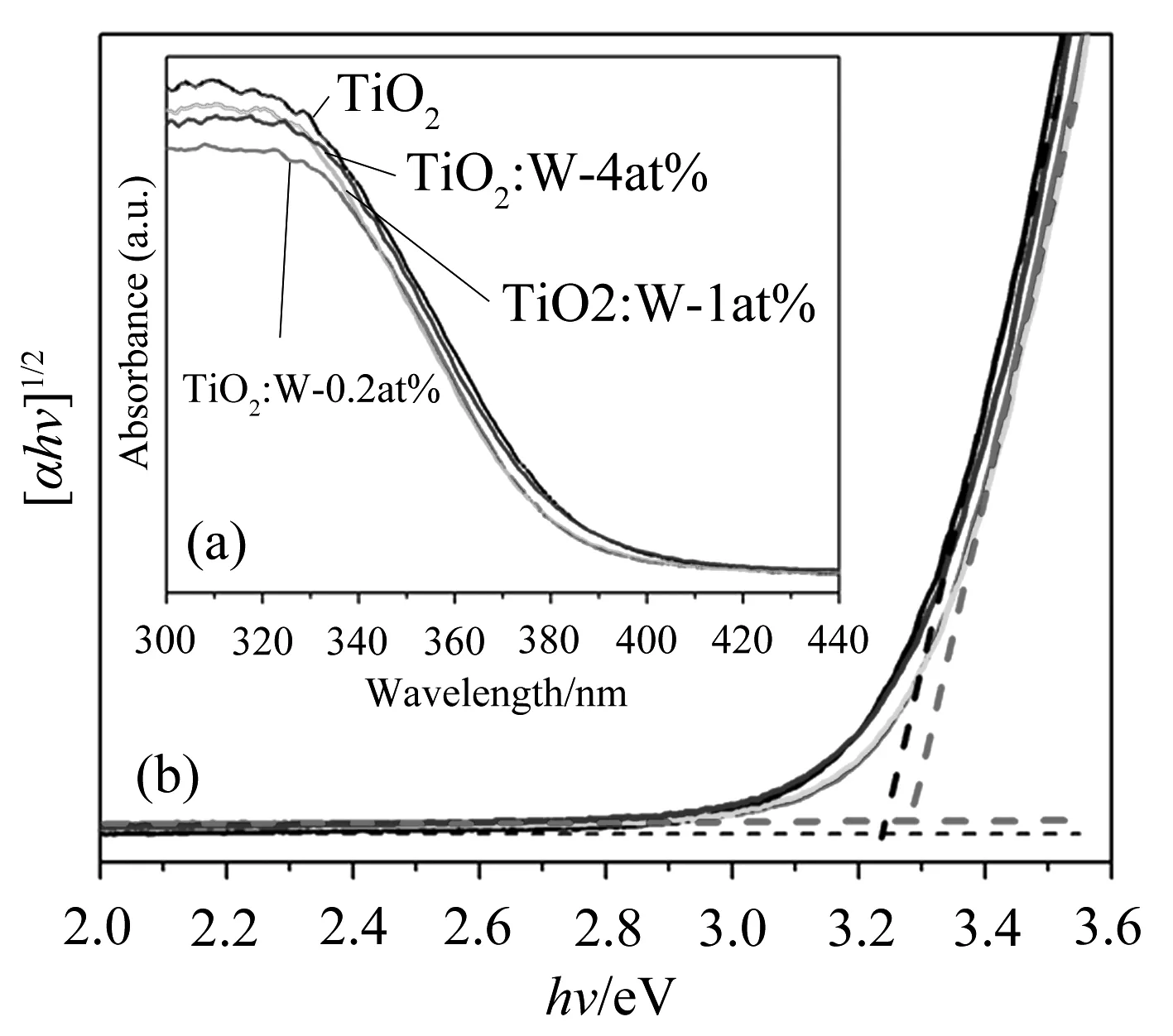
图3 TiO2和W掺杂TiO2UV-vis DRS光谱和能带图
TiO2为间接带隙半导体.根据半导体表观光学带隙与UV-Vis吸收系数的关系α=c(hv-E)/hv(c为吸收常数,α为吸收系数)绘制(αhv)1/2-hv曲线[19].取该曲线中直线部分截距可以得到催化剂的禁带宽度Eg[20].图3(b)以TiO2和TiO2∶W-0.2at%为例表示了禁带宽度计算示意图.计算得到的TiO2禁带宽度为3.23 eV,TiO2∶W-0.2at%禁带宽度为3.28 eV,与未掺杂的TiO2相比,TiO2∶W-0.2at%能隙增大,而TiO2∶W-4at%能带没有明显变化,这与紫外可见吸收光谱所得结果相一致.根据半导体的光吸收阈值λg与禁带宽度Eg的关系方程所得吸收阈值λg见表1.
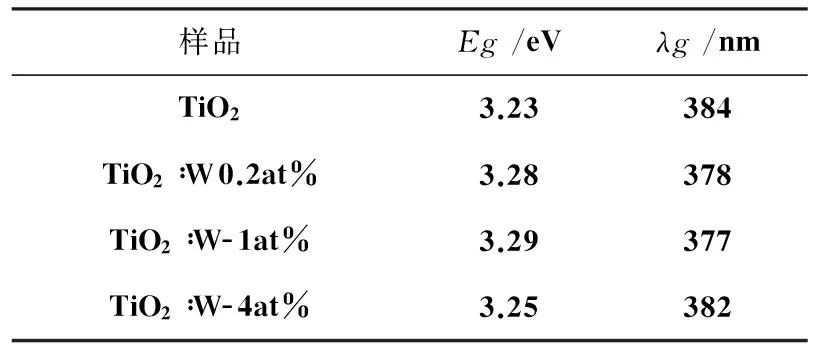
表1 TiO2和W掺杂TiO2的带隙能和吸收波长
从表中可以看出较低钨浓度的掺杂(0.2%,1%)扩展了TiO2的禁带宽度,吸收波长范围变窄,而较高钨浓度的掺杂(4%)并未对TiO2的禁带宽度和吸收边产生明显影响.
2.3 光催化活性分析
图4为紫外光辐照下不同掺钨量TiO2催化剂对RhB的光催化降解曲线.紫外光催化降解120 min,光催化活性顺序为:TiO2∶W-0.2at%>TiO2∶W-1at%>TiO2∶W-4t%>TiO2.钨离子作为电子的受体,提高了光生电子的分离效率从而提高光催化活性.TiO2∶:W-0.2at%和TiO2∶W-1at%在80 min内完全降解RhB.但是,TiO2∶W-4at%和未掺杂TiO2光催化活性相似,80 min降解率约为83%和77%,这是由于过高浓度的钨离子掺杂产生正电荷成为了新的光生电子-空穴的复合中心,从而减弱了光催化活性,这说明钨的掺杂浓度对提高TiO2光催化活性非常重要.TiO2∶W-0.2at%和TiO2∶W-1at%禁带宽度大于TiO2和TiO2∶W-4at%,却有着较高的光催化效率,说明介孔二氧化钛的光催化活性强烈依赖于带隙、介孔结构、吸收带边,但这些因素的影响并不是相互独立的,光催化活性相互作用机制的进一步还需要进一步探讨.

图4 紫外光辐照下不同掺钨量TiO2催 化剂对RhB的光催化降解曲线
3 结论
以钛酸四异丙酯为钛源,钨酸铵为钨源通过水热法制备了介孔TiO2微球,所制备的样品吸收波长产生明显变化,不同钨掺杂量样品紫外光区活性差异较大,其中当钨钛摩尔比n(W)∶n(Ti)=0.2%时合成的TiO2粒子活性最好,在80 min内完全降解RhB,相比未掺杂样品降解率明显提高.
[1]FUJISHIMA A,HONDA K.Electrochemical photolysis of water at a semiconductor electrode[J].Nature,1972,238(5358):37-38.
[2]FRANK S N,BARD A J.Heterogeneous photocatalytic oxidation of cyanide and sulfite inaqueous solutions at semiconductor powders[J].Journal of Physical Chemistry,1977(81):1484-1489.
[3]HUANG L H,SUN C,LIU Y L.Pt/N-codoped TiO2nanotubes and its photocatalytic activityunder visible light[J].Applied Surface Science,2007,253(17):7029-7035.
[4]CHOI W,TERMIN A,HOFFMANN M R.The role of metal ion dopants in quantum-sized TiO2:correlation between photoreactivity and charge carrier recombination dynamics[J].Journal of Physical Chemistry,1994,98(51):13669-13679.
[5]NI Y H,ZHU Y,MA X.A simple solution combustion route for the preparation of metal-doped TiO2nanoparticles and their photocatalytic degradation properties[J].Dalton Transactions,2011,40,3689-3694.
[6]ARCHANA P S,ARUNAVA G,MASHITAH M,et al.Tungsten doped titanium dioxide nanowires for high efficiency dye-sensitized solar cells[J].Physical Chemistry Chemical Physics,2014,16,7448-7454.
[7]范晓星,于涛,邹志刚.介孔TiO2的材料合成及其在光催化领域的应用[J].功能材料,2006,37(1):6-9.
[8]GAO B,MA Y,CAO Y,et al.Great Enhancement of Photocatalytic Activity of Nitrogen-Doped Titania by Coupling with Tungsten Oxide[J].Journal of Physical Chemistry B,2006,110(29):14391-14397.
[9]LI H,BIAN Z,ZHU J,et al.Mesoporous Titania Spheres with Tunable Chamber Stucture and Enhanced Photocatalytic Activity[J].Journal of the American Chemical Society,2007,129(27):8406-8407.
[10]YU J G,LIU S W,YU H G.Microstructures and photoactivity of mesoporous anatase hollow microspheres fabricated by fluoride-mediated self-transformation[J].Journal of Catalysis,2007,249(1):59-66.
[11]SYOUFIAN A,SATRIYA O H,NAKASHIMA K.Photocatalytic activity of titania hollow spheres:Photodecomposition of methylene blue as a target molecule[J].Catalysis Communications,2007,8(5):755-759.
[12]YANG G Z,JIANG H,SHI T XIAO,et al.Preparation of highly visible-light active N-doped TiO2photocatalyst[J].Journal of Materials Chemistry,2010,20:5301-5309.
[13]ZHANG Y H,A WEIDENKAFF,A RELLER.Mesoporous structure and phase transition of nanocrystalline TiO2[J].Materials Letters,2002,54(5-6):375-381.
[14]姬平利,王金刚,孔祥正.Ag掺杂型空心TiO2纳米微球的制备与表征及其光催化性能[J].物理化学学报,2012,28(9):2155-2161.
[15]CHEN D H,CAO L,HUANG F Z,et al.Synthesis of Monodisperse Mesoporous Titania Beads with Controllable Diameter,High Surface Areas,and Variable Pore Diameters (14-23 nm)[J].Journal of the American Chemical Society,2010,132(12):4438-4444.
[16]SAJJAD A K,SHAMAILA S,TIAN B,et al.One step activation of WOx/TiO2nanocomposites with enhanced photocatalytic activity[J].Applied Catalysis B,2009,91(1-2):397-405.
[17]ZHANG J,QIAN L S,FU W,et al.Alkaline-Earth Metal Ca and N Codoped TiO2with Exposed {001} Facets for Enhancing Visible Light Photocatalytic Activity[J].Journal of the American Ceramic Society,2014,97(8):2615-2622.
[18]ZHANG J,XI J H,JI Z G.Mo+N Codoped TiO2sheets with dominant {001} facets for enhancing visible-light photocatalytic activity[J].Journal of Materials Chemistry,2012,22:17700-17708.
[19]杨华博,李翔,王安杰.MoO3改性的TiO2在可见光下催化降解亚甲基蓝[J].催化学报,2014,35(1):140-147.
[20]ELDER S H,COT F M,SU Y,et al.The Discovery and Study of Nanocrystalline TiO2-(MoO3) Core Shell Materials[J].Journal of the American Chemical Society,2000,122(21):5138-5146.
Enhanced Photocatalytic Degradation of Rhodamine B under Ultraviolet Light Irradiation on Mesoporous Anatase TiO2Beads by Doping with W
ZHENG Jian,TIAN Ying,CHEN Guowei
(School of Environmental Science and Chemical Engineering,Dalian Jiaotong University,Dalian 116028,China)
Eesoporous anatase TiO2beads were prepared via hydrothermal and calcination processes with addition of W source for doping W. All the samples were characterized by X-ray diffraction (XRD),scanning electron microscopy (SEM),nitrogen adsorption,and UV-visible(UV-Vis) diffuse reflectance spectroscopy.RhB (rhodamine B) aqueous solution is used as a target degradation to investigate the photocatalytic activity of the W doped mesoporous TiO2beads.The doped mesoporous TiO2beads achieves a relatively narrow pore size distribution centered at 10.0 nm.All the samples are of anatase phase,which implies no variation of crystal phase generation in the W-doping process.The band edge absorption blue shifts from 384 nm to 378 nm with a moderate amount of W doping.TiO2beads have a higher photocatalytic activity when the mole ratio of Ti to W is 0.2%.Photocatalytic degradation of RhB on TiO2:W-0.2at% is increased to 30% of that on pure TiO2beads.
mesoporous TiO2beads;W doping;hydrothermal method;photocatalytic property
1673-9590(2016)04-0105-05
2014-01-11
中华环保基金会辽宁环境科研教育“123工程”资助项目(CEPF2013-123-2-20)
郑健(1989-),男,硕士研究生;田颖(1969-),女,教授,博士,主要从事水处理技术和材料的研究E-mail:931434391@qq.com.
A
