饲料级金霉素新品的制备
2016-11-16涛杨旭郭红伟李书至
伍 涛杨 旭郭红伟李书至*
(1重庆市畜牧科学院,重庆 402460;2重庆大学,重庆 400044;3驻马店华中正大有限公司,河南驻马店 463000)
饲料级金霉素新品的制备
伍 涛1杨 旭2郭红伟3李书至3*
(1重庆市畜牧科学院,重庆 402460;2重庆大学,重庆 400044;3驻马店华中正大有限公司,河南驻马店 463000)
本文介绍了一种以金霉素为原料,在有机溶剂中合成金霉素锌盐、镁盐、铜盐和钴盐4个金霉素金属盐的制备方法,并采用滴定、紫外-可见光谱、红外光谱等分析法对制备的配合物进行了表征。以期通过合成这几种金霉素金属盐,改善传统饲料级金霉素在胃肠道的释药特征和吸收,促进和拓展新型饲料级金霉素的生产与销售。
饲料级金霉素;新品;制备
在当前饲料级金霉素生产工艺中,金霉素是以金霉素钙盐的形式存在[1,2],而金霉素作为四环素类药物,在动物胃肠道内会与钙、镁、铝、铁等不同的金属离子形成络合能力不同的螯合盐而导致不同的吸收模式。本试验设计了一条为金霉素配体引入更多具有药学活性金属元素的合成路线,制备了锌盐、镁盐、铜盐和钴盐4个金霉素金属盐,拟考察不同金属离子对金霉素释药特征的影响。
1 制备方法
1.1 试剂与仪器
盐酸金霉素(含量92%,购自驻马店华中正大有限公司);六水合氯化镁、五水合硫酸铜、七水合硫酸锌、六水合氯化钴(含量>99.5%,购自重庆川东化工集团公司);金霉素等对照品(购自中国药品生物制品检定所)。其他试剂均为分析纯试剂。
紫外可见光谱仪(购自日本岛津公司,型号:UV 2450);红外光谱仪(购自北京第二光学仪器厂,型号:WQF-510A);液相色谱仪(美国waters 515型液相色谱仪)。
1.2 制备工艺流程
取盐酸金霉素4.5 g,在低温条件下,加入甲醇水溶液搅拌溶解,抽滤,去除金霉素甲醇溶液中的不溶性杂质,继续低温搅拌溶解,用NH3·H2O∶CH3OH(V∶V =1∶1)体系调节反应pH值于适宜范围,反应20分钟。然后向反应体系中加入1当量的M2+金属离子的甲醇水溶液(M代表Zn、Mg、Cu和Co其中之一),搅拌反应20分钟。最后将溶液的pH值回调,反应30分钟,至溶液变浑浊,有沉淀生成。常压过滤,固体经水洗、甲醇洗后真空干燥48小时得到饲料级金霉素新品。制备的金霉素锌盐、镁盐、铜盐和钴盐的收率分别为88.31%、96.28%、66.87%和90.51%。
2 表征试验
2.1 配位比
产物中配体的含量采用高效液相色谱测定,金属元素含量采用EDTA滴定法测定。
2.1.1 色谱条件
色谱柱为C8柱(250×4.6 mm,5μm),流动相为高氯酸-二甲基亚砜-水(8∶525∶467,pH<2.0),柱温45℃,检测波长280 nm,进样量20μL[3]。
2.1.2 溶液的制备
精密称取适量盐酸金霉素和差向金霉素等对照品及样品,用0.01 mol/L盐酸溶液溶解定量稀释成每1 m L中分别含1mg的溶液。采用外标一点法进行金霉素含量的测定。然后称取适量样品于600℃马弗炉中煅烧4小时,煅烧后的残渣用于EDTA滴定分析,确定金属含量。
2.1.3 检测结果
检测结果见图1、表1和表2。

图1 金霉素和杂质色谱图

表1 液相含量的测定结果 (折合干物质) (%)

表2 金霉素盐的离子滴定结果
2.1.4 结果分析
试验结果表明在摩尔比1∶1(M∶L)的条件下,根据元素含量推测金霉素与镁离子、锌离子、钴离子反应得到的配合物的配合比为1∶1,而铜离子与金霉素反应得到的配合物配合比为2∶1。
2.2 紫外-可见吸收光谱分析
2.2.1 试验条件
用0.5%的二甲亚砜(DMSO)溶解盐酸金霉素以及4种合成的金属配合物,制成适宜浓度的溶液,调节测定波长为200~500 nm区间,测定紫外吸收光谱[4]。
2.2.2 试验结果
配体与配合物的UV-Vis光谱数据见图2,盐酸金霉素和金霉素配合物的紫外吸收波长见表3。

图2 配体与配合物的UV-Vis光谱图

表3 盐酸金霉素和金霉素配合物的紫外吸收波长对比表 (nm)
由图2和表3可知,金霉素在275、368、228 nm处有3个最大吸收峰,其中368 nm、275 nm是最主要的两个吸收峰;与不同金属离子结合后,金霉素的紫外吸收峰发生了不同程度的红移,其中以金霉素铜和金霉素锌的程度较大,分别从368 nm红移至382 nm和377 nm。而钴盐和镁盐在此处的最大吸收峰发生微小红移,约3~4 nm。对于在275 nm处的最大紫外吸收,除了铜盐发生了5 nm的红移外,其他3种盐均没有明显改变。这可能是由于金霉素与金属离子形成配合物后,分子中电子的离域程度增大,加之金属离子具有一定的吸电子能力,使得电子从基态跃迁至激发态(n→π*或者π→π*)所需要能量减小,从而导致吸收峰发生了不同程度的红移。金属元素兼并d轨道,与电子供体配位后,可使兼并的d轨道分裂成不同的能级,吸收电磁波能量后,电子可由低能级的d轨道跃迁到高能级的d*轨道,在可见光区产生吸收谱带。因此上述结果可以证明金霉素和金属离子间发生了配位。
2.3 红外光谱分析 (FT-IR)
2.3.1 试验条件
采用KCl压片法,在400~4 000 cm-1范围内对盐酸金霉素以及4种金属配合物进行红外光谱扫描。
2.3.2 试验结果
盐酸金霉素和4个金霉素盐的红外光谱分析见表4。
由表4可知,金霉素酰胺基的1 671 cm-1处的峰移至1 640~1 650 cm-1,1 520 cm-1移至1 504 cm-1左右,而在1 250 cm-1和1 226 cm-1处的伸缩振动在配合物中变为了单峰1 210~1 220 cm-1之间,说明酰胺基参与了金霉素盐的配位,而A环的C=O在1 604 cm-1处的伸缩振动没有变化,说明C1位的C=O没有参与反应,而铜盐C环C=O的位于1 578 cm-1吸收峰转移至1 558 cm-1处的强峰,说明C环的C=O发生了配位。而金霉素盐在560 cm-1处均发现了金属M-O键的振动[5-7],而此处峰在金霉素的红外图谱中未发现,进一步证明了金属离子确实和金霉素发生了配位反应。
3 金霉素新品的可能结合位点
由于金霉素分子结构中存在着羟基、氧和氮等不同的给电子体,金霉素的这种性质使它和不同的金属离子产生不同的结合方式和能力,其配合物的组成和结构取决于试验条件和金属离子性质。金霉素结构中含有三个易解离出质子的官能团,一个是A环上的环戊二烯三羰基甲烷体系(C1-C3),另一个是酚二酮体系(C10-C12),还有一个是A环上的二甲胺基体系(C4),其pka分别为3.5、7.7和9.5[8]。由于金霉素结构中含有羟基、羰基、氨基等含有氮氧的基团,因此溶液的pH值会影响金霉素与金属离子的配位能力。通过紫外、红外表征发现,金霉素确实与金属离子发生了配位,且配位的位置应该是环戊二烯三羰基甲烷体系(C1 C3)和酚二酮体系(C10-C12),通过金属离子滴定法确定了金属离子与金霉素的配位比例分别为1∶1和2∶1,这一点与相关文献得出的结论一致[9,10]。
Mg2+最外层电子为 3s03p0,钴最外层电子为3p63d7,与金霉素作用时,金霉素中的-OH、C=O中的孤对电子对转移到Mg2+空轨道上,同时Mg2+的3s、3p亚层上以及Co2+的3d亚层的空轨道发生sp3杂化,形成了4个能量相等的杂化轨道,使原轨道形状改变,进一步增强了镁、钴接受电子的能力,使其与金霉素分子形成牢固的配合物。
Zn2+最外层电子是3d104s0,Cu2+最外层电子分别3d94s0,配位时,3d亚层中的1个电子被激发到了4p轨道上,能量相近的1个3d、1个4s和2个4p轨道发生dsp2杂化,形成4个能量相等的空轨道,从而接受孤对电子,形成配合物。
因此,4种金霉素新品的可能结合位点见图3~6。
4 小结
长期以来,饲料级金霉素凭借其安全、高效、低成本的优势被广泛应用,市场需求量不断扩大,根据内蒙古饲料工业协会统计,2007年、2008年和2009年我国金霉素的消费量分别为2.47万吨、2.99万吨和3.45万吨,增长了39.68%。预计在未来较长一段时间内,金霉素仍是药物饲料添加剂的主力产品之一。此外,人口数量的增加以及人们对肉禽蛋需求的增加将推动畜牧业进一步发展,从而也将带动饲料级金霉素需求量的增加。本试验制备的锌盐、镁盐、铜盐和钴盐4个金霉素金属盐,以期通过改善金霉素在胃肠道的释药特征和吸收,进一步减少传统饲料级金霉素的耐药特征,促进和拓展新型饲料级金霉素的生产与销售。

表4 盐酸金霉素和4个金霉素盐的红外光谱分析对比表

图3 金霉素锌的可能结合位点
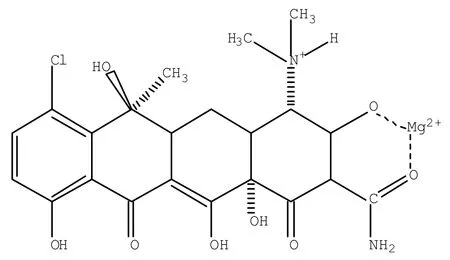
图4 金霉素镁的可能结合位点

图5 铜配合物的可能结结合位点

图6 钴配合物的可能结合位点
[1]Chopra I,Roberts M.Tetracycline Antibiotics:Mode of Action,Applications,Molecular Biology,and EpidemiologyofBacterialResistance[J].Microbiologyand MolecularBiology Reviews,2001,65(2):232-60.
[2]Scholar E.Chlortetracycline A2-Enna,S.J [M].New York: The Comprehensive Pharmacology Reference.Elsevier,2007:1-5.
[3]中国兽药典委员会.中华人民共和国兽药典[M].2010版.北京:中国农业出版社,2010:207-208.
[4]Silva PP,Guerra W,Silveira JN,et al.Two New Ternary Complexes of Copper(II)with Tetracycline or Doxycycline and 1,10-Phenanthroline and Their Potential as Antitumoral:Cytotoxicity and DNA Cleavage[J].Inorganic Chemistry,2011,50(14):6414-6424.
[5]ChenWR,HuangCH.Adsorptionand transformationoftetracycline antibioticswithaluminum oxide[J].Chemosphere,2010,79(8):779-785.
[6]Guerra W,Azevedo EDA,Monteiro ARDS,et al.Synthesis,characterization,and antibacterial activity of three palladium(II)complexes of tetracyclines[J].Journal of Inorganic Biochemistry,2005,99(12):2348-2354.
[7] GuerraW,Silva IR,Azevedo EA,et al.Three new complexes of platinum(II)with doxycycline,oxytetracycline and chlortetracycline and their antimicrobial activity[J].Journal of the Brazilian Chemical Society,2006,17(8):1627-1633.
[8]Jin L,Amaya-Mazo X,Apel ME,et al.Ca2+and Mg2+bind tetracycline with distinct stoichiometries and linked deprotonation[J]. Biophysical Chemistry,2007,128(2-3):185-196.
[9]Carlotti B,Cesaretti A,Elisei F.Complexes of tetracyclineswith divalent metal cations investigated by stationary and femtosecondpulsed techniques[J].Electronic supplementary information(ESI)available,2011,14(2):823-34.
[10]文美琼,高云涛,罗永刚,等.四环素-铜(Ⅱ)配合物与DNA相互作用的吸收光谱研究[J].感光科学与光化学,2005,23(1):71-78.
S816.7
B
1673-4645(2016)10-0068-04
2016-01-07
2014年重庆市农发资金项目(14417)
伍涛(1982-),重庆荣昌人,硕士,助理研究员,研究方向为兽药制剂,Tel:023-46791139*
