外周药物球囊在猪体内的药代动力学研究
2016-11-14谢琦宗宋精忠卢金华龙汉王刚张贵先健科技深圳有限公司广东深圳58057
谢琦宗宋精忠卢金华 龙汉 王刚 张贵 先健科技(深圳)有限公司 (广东 深圳 58057)
外周药物球囊在猪体内的药代动力学研究
谢琦宗1宋精忠1卢金华 龙汉 王刚 张贵 先健科技(深圳)有限公司 (广东 深圳 518057)
内容提要: 目的:将外周药物球囊在健康猪模型体内扩张后,通过LC/MS检测靶血管、脏器和血浆中药物含量,计算靶血管组织、主要器脏的药代动力学参数,以评估外周药物球囊产品的药效,局部和全身可耐受性。方法:用载药密度为2μg/mm2的药物球囊在健康猪髂/股动脉扩张后,分别在术后2h、7d、28d、90d时,取药物球囊治疗段、治疗段近端、治疗段远端的血管检测含药量;取重要生命器官(心、肺、肝、脾、肾)检测药物浓度;另在治疗后30min、2h、6h、12h、1d、3d、7d取血液,检测血浆中的药物浓度。结果:靶血管部位在T=2h时,药物含量到达峰值,达130μg/g以上,7D时8.59μg/g,28D时有约3.43μg/g,90D时仍有0.09μg/ g,均高于最低治疗剂量0.047μg/g。其他组织和器官药物含量均非常低,未发现任何由药物涂层引起的不良事件,产品在局部和全身对紫杉醇是可耐受。结论:紫杉醇在靶血管的分布远大于主要脏器和血液,呈主要分布,在局部和全身对紫杉醇是可耐受。
药物球囊 药代动力学 再狭窄
1.研究背景
外周动脉疾病(Peripheral arterial disease,PAD)又称为下肢动脉闭塞性病变,是指下肢血管的动脉粥样硬化而导致的动脉狭窄、闭塞、下肢远端组织缺血坏死[1]。目前裸球囊导管、裸支架、药物支架是主要治疗手段[2]。裸球囊扩张后,再狭窄率高,产品有效性难以令人满意;金属裸支架的植入虽有70~80%的通畅率,但有金属物质永久留于人体内,再狭窄后难以处理;载药支架具有很好的有效性,但同样有金属物质永久留于人体内[3],且由于涂层含有高分子物质,晚期血栓风险较高。
先健药物洗脱外周球囊导管是在PTA裸球囊导管的球囊表面涂覆了一层药物。将药物洗脱外周球囊导管通过导引导管和导丝输送到病灶处并定位,液体加压使导管末端球囊扩张,球囊表面药物涂层与病灶血管壁紧密接触,使药物迅速释放并粘附于病灶血管壁上,被病灶血管组织吸收,从而抑制平滑肌细胞增生,进而使血管畅通以及减少再狭窄的发生。
2.材料和方法
2.1测试样品
先健科技(深圳)有限公司药物洗脱外周球囊导管,规格为:4.0×40mm、5.0×40mm、6.0×40mm;载药密度为2μg/mm2。
2.2设备和手术耗材
Innova 2100IQ数字成像系统
介入和辅助耗材(康德莱生产的7F血管穿刺鞘套装,批号:20131216;Medtronic 0.018ʺ×300cm导引导丝,批号:0007062968;Cordis 6F MPA1导引导管,批号:15932165)
球囊扩张压力泵(康德莱生产,型号为IN-30,批号:20140108)
非离子型造影剂(泛影葡胺注射液,批号:LF120801)
2.3实验设计
共选用8头健康家猪(约3个月大,30kg左右,雌性不限),将载药密度为2μg/mm2的先健外周药物球囊,借助导管和导丝,经过右侧或左侧颈总动脉血管通路分别送达左右髂/股动脉或其主要分支动脉血管内预定位置[4]。球囊扩开直径与靶血管直径的比例在1.1:1到1.3:1之间。共有4个随访时间点:2h(n=2)、7D(n=2)、28D(n=2)、90D(n=2);在到达随访时间点时,对动物进行安乐死,迅速分离出靶血管,以及心、肝、脾、肺、肾脏组织,用少量生理盐冲洗,于LC/MS检测组织药物含量;另在观察时间为7D(n=2)和28D(n=1)的动物分别在以下时间点:0min,30min,2h,6h,12h,24h,3D和7D取血,于LC/ MS检测血浆药物含量[5]。实验分组和研究内容如下表1所示。
2.4实验程序
实验动物3个月大小的实验家猪或小型猪,从上海南汇华新特种动物养殖场采购,在手术操作开始之前,通过静脉给予肝素钠注射液(150U/kg),监测凝血时间(ACT),确保手术过程中ACT值大于300。手术过程中,实时监测实验动物的血流动力学、ECG、血氧饱和度等。
药物球囊治疗手术在汇智赢华医疗科技研发(上海)有限公司实施,按照汇智赢华标准操作规程操作。先放好导引导管和导丝的位置,球囊经导引导管和0.018导丝引导球囊经颈总动脉入路进入血管,到达髂动脉及其主要分支动脉血管药物球囊治疗目标位置,用球囊扩张压力泵以适当压力扩开球囊,使药物球囊充分贴附于血管壁上。保压120秒后撤除球囊压力,然后将球囊撤出体外。药物球囊治疗完成后血管造影评价治疗段血管情况,手术结束,从实验动物体内撤除一切器械、设备。麻醉复苏后,实验动物继续观察饲养到指定的存活时间点。
实验动物观察期结束时,被再次麻醉,经静脉给予肝素钠注射液12500U,造影复查,观察外周药物球囊治疗血管的情况。复查结束后,实验动物在深麻状态下经静脉注射过量氯化钾溶液实施安乐死,依据汇智赢华标准操作规程(SOP317病理操作程序-尸检及样本处理)实施尸体解剖,检查胸腔、腹腔及各脏器情况并取样。取出的所有测含药量的组织样本立即放入干冰盒中保存。收集的所有样本都于取样后由实验发起方运送到指定的化学分析机构保存。每头实验动物所采样本有:治疗段血管、治疗段近端血管、治疗段远端血管、及部分心脏、肺、脾脏、肝脏、肾脏组织样本等。
2.5样本分析
实验样本运送到澎立生物医药技术(上海)有限公司通过LC/MS进行药物含量分析检测。
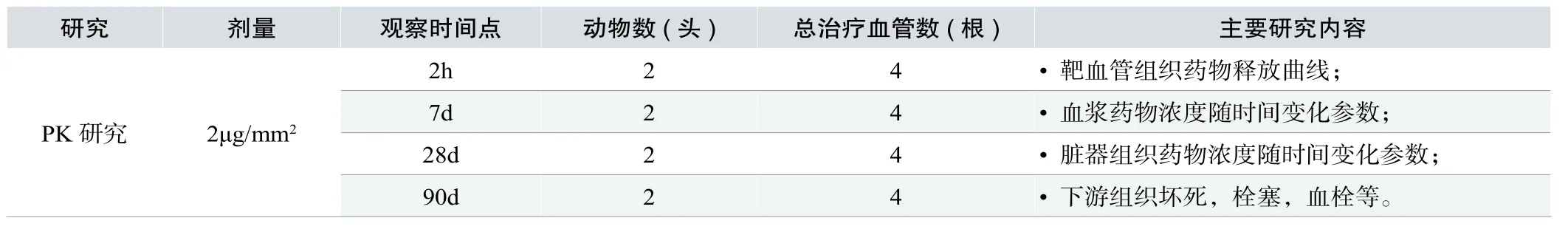
表1. 实验分组和研究内容

图1. 先健外周药物球囊猪体内球扩段血管紫杉醇浓度-时间曲线图
3.结果
3.1实验动物总体健康状况和解剖发现
(1)实验动物总体健康状况
在本研究的实施过程中,所有实验动物在手术时和术后观察阶段均没有出现不利的临床征象。
(2)大体尸检观察
对纳入本研究中的8只实验动物实施了大体解剖,所有实验动物胸腔、腹腔、及其主要脏器、治疗段血管周围组织在尸检中均没有发现异常。
(3)治疗血管血流情况评价
实验动物所有的治疗血管经药物球囊治疗后血管造影评价发现部分血管在治疗后血管出现轻微的痉挛现象,但血管内腔通畅。随访发现治疗段血管基本恢复正常,血流正常。
3.2治疗血管血流情况评价
载药量为2μg/mm2的先健外周药物球囊,在靶血管球扩段的药物含量随时间变化血线见下图1。
紫杉醇在靶血管不同部位和心脏、肝脏、脾脏、肺、肾组织中的主要药代动力学参数见下表2。
另外,所有血浆样本中紫杉醇浓度均不超过1.29ng/mL。
4.讨论
先健科技(深圳)有限公司开发的外周药物球囊在猪体内髂/股动脉治疗后,即刻血管造影评价发现部分动物血管出现轻微痉挛现象,随访时发现血管痉挛全部缓解。动物在观察饲养阶段未出现任何异常情况,大体解剖未见任何异常组织。所有动物均存活到设定的时间点,没有发现异常临床征象。所有的经药物球囊治疗的血管均是开放的,未发现血管夹层、动脉瘤、血管影像充盈缺损、过度狭窄、血栓、闭塞等异常现象。主要药代动力学研究结果:
(1)紫杉醇在血管中的总AUClast值为36994693 ng*hr/g,在脏器组织中总AUClast值为1725448 ng*hr/g,在血管中的总分布量是主要脏器组织中总分布量的21.4倍,呈现主要分布;
(2)靶血管部位在Tmax=2h时,药物含量到达峰值,达130μg/g以上。之后迅速下降,7D时8.59μg/g。此后含量则平缓降低,28D时有约3.43μg/g,并在90D时仍有0.09μg/g。整个释放和吸收过程,无论短期还是长期药物含量均远高于文献报道的最低有效剂量0.047μg/g[5];
(3)90天时,除肺组织(约100ng/g)以外,其他组织的药物含量下降到低于定量限,这表明,紫杉醇在主要脏器(心、肝、脾、肺、肾)组织中很快代谢并消除;血浆中药物在12小时之后就已消失;
(4)未见任何组织相关毒性,以及药物副作用等并发症。

表2. 紫杉醇在组织分布的药代动力学参数
5.结论
实验结果显示,先健科技(深圳)有限公司的药物洗脱外周球囊导管,通过在猪体内药代动力学研究,获得了更全面药物释放特征,均达到了研究终点,表明产品是可以起到有效药物作用的,且产品在局部和全身对紫杉醇是可耐受的。
[1]A Pletea,C Plesa,CN Neacsu,et al. Peripheral Arterial Disease in People With Diabetes[J], Diabetes Care, 2003, 26(12):3333-41
[2]Jude EB, Eleftheriadou I, Tentolouris N. Peripheral arterial disease in diabetes-a review[J]. Diabet Med, 2010,27(1):4-14.
[3]Carrozza JP, Kuntz RE, Levine MJ, et al. Angiographic and clinical outcome of intracoronary stenting: Immediated and long-term results from a large single-center experience[J].Journal of the American College of Cardiology, 1992,20(2):328-37
[4]Thomas Albrecht, MD, FRCR, Ulrich Speck, PhD, Claudia Baier, MD, et al. Reduction of Stenosis Due to Intimal Hyperplasia After Stent Supported Angioplasty of Peripheral Arteries by Local Administration of Paclitaxel in Swine[J]. Investigative Radiology, 2007, 42(8):579-85
[5]Saami K. Yazdani PhD.Vascular, Downstream, and Pharmacokinetic Responses to Treatment with a Low Dose Drug-Coated Balloon in a Swine Femoral Artery Model[J]. Catheterization and Cardiovascular Interventions, 2014, 83(1):132-40
Intravascular Drug Release Kinetics Dictate Arterial Drug for Peripheral Atery Disease Drug Coated Balloon Catheter
Xie Qi-zong1Song Jing-zhong1Lu Jing-hua Long Han Wang Gang Zhang Gui Lifetech Scientific (Shenzhen) Co., LTD. (Guangdong Shenzhen 518057)
Objective: To evaluate the were Product efficacy, local and systemic tolerability, the peripheral drug balloon was inflated in a healthy pig model, and the drug concentration of the target vessels, organs and plasma were tested by LC/MS/MS, then calculated the pharmacokinetic parameters. Methods: The peripheral drug balloon(2μg/mm2)was inflated in a healthy pig iliofemoral artery model, Retrieve the treatments, proximal and distal section of the vascular and test drug content; the vital organs samples (heart, lung, liver, spleen, kidney) was examined for the distribution of the drug. Blood samples were retrieved at 30min,2h, 6h, 12h, 1d, 3d, 7d after treatment, and the drug concentration in plasma was measured. Results: At the time of 2h after treatment, the drug content reached a peak value of 130μg/g, 8.59μg/g at 7D, 3.43μg/g at 28D and 0.09μg / g at 90D, all were higher than the lowest therapeutic dose of 0.047μg / g. Other tissues and organs
very low drug content, not drug-induced adverse events were finded . the paclitaxel is tolerable in the local and systemic .Conclusion: Paclitaxel was mainly distributed in the target vessel, which is much larger than the main organs and blood, paclitaxel in the local and systemic is tolerable.
drug coated balloon, pharmacokinetic, restenosis
1006-6586(2016)05-0001-03
R965
A
1这些作者对本文的贡献相同。
深圳市科技创新委员会战略性新兴产业(生物产业发展)专项资金,项目编号:CXZZ20140813102720940,本项目进入国家食药监总局创新医疗器械特别审批绿色通道。创新医疗器械特别审批申请项目编号:2015061,审查结果公示(2016年第2号)。
