超声辅助Fe3O4活化过一硫酸盐降解酸性红B
2016-11-12刘丽艳孙至柔叶文博谭蔚
刘丽艳,孙至柔,叶文博,谭蔚
(天津大学化工学院,天津 300354)
超声辅助Fe3O4活化过一硫酸盐降解酸性红B
刘丽艳,孙至柔,叶文博,谭蔚
(天津大学化工学院,天津 300354)
含偶氮型染料废水色度高、降解困难,对环境危害大,采用传统水处理方法难以达到严格的工业废水排放要求。本文选取典型偶氮染料酸性红B为研究对象,采用超声辅助Fe3O4活化过一硫酸盐的高级氧化方法进行处理。以酸性红B染料废水的色度去除率为指标,研究Fe3O4投加量、PMS投加量、超声功率、超声频率、初始染料浓度、溶液初始pH等参考对降解效果的影响规律及该法的适用范围。实验获得最优的酸性红B处理条件为Fe3O41.0g/L,PMS 60mmol/L,超声频率50kHz,超声功率80W。结果表明,该法可在pH为3.5~8.5范围中适用,能处理初始浓度1g/L酸性红B溶液。实验还研究了催化剂循环利用性能,发现重复3次的时候色度去除率仍然可以保持在95%以上。该研究结果可为偶氮型染料工业废水的处理提供技术指导。
过一硫酸盐;四氧化三铁;超声;酸性红B;高级氧化法
随着染料制备工业的发展,全世界每年随工业废水排放到环境中的染料约6万吨,染料废水由于其来源复杂、对环境及人体健康危害大,已经成为污染环境最严重的废水之一[1]。其中,偶氮染料占常用染料的70%以上,其色度高、COD值高、可生化性差,使用传统方法难以将其彻底降解[2]。
基于自由基反应的高级氧化技术因其反应条件温和、反应速率快逐渐成为研究热点[3-4]。由于传统Fenton试剂产生羟基自由基·OH的高级氧化技术在其使用过程中,对废水酸碱度要求较高、操作复杂、催化剂再生性差且产生二次污染等原因影响了其应用[5]。研究者进而转向研究非均相的Fenton氧化体系替代传统试剂,以铁氧化物代替Fe2+,不仅可以高效降解有机物,而且可以改善二次污染问题。Fe3O4广泛存在于自然界中,其具有顺磁性,极大简化了催化剂的分离回收步骤[6]。另外,在传统Fenton试剂中,氧化剂H2O2用量高,利用率低,常温下易分解,运输成本高且经济性差。近年来,基于硫酸根自由基SO4-·的高级氧化技术发展迅猛[7-8],其来源主要有过二硫酸盐(S2O82-,PS)和过一硫酸盐(HSO5-,PMS),其中过一硫酸盐主要以2KHSO5·KHSO4·K2SO4三盐化合物的形式存在,商品名称为Oxone。可通过过渡金属离子催化活化[9]、高温热解[10]或UV辐射[11]等方法产生SO4-·。在非均相体系中,常常引入超声作用来强化固液两相间的传质,从而提高反应速率和有机物的降解率。超声空化产生的瞬时局部高温高压可活化PMS产生SO4
-·,并且超声具有不受水质影响、不产生二次污染和能耗低等特点[12]。HOU等[13]成功将超声辅助Fe3O4活化过硫酸盐的方法用于降解四环素废水中。本文拟采用超声耦合Fe3O4活化过一硫酸盐方法处理染料酸性红B,探究Fe3O4及过一硫酸盐的投加量、超声频率及功率、初始染料浓度、溶液初始pH等对色度去除率的影响,为高级氧化技术在处理染料废水的工程应用提供参考。
1 实验材料和方法
1.1实验试剂及仪器
(1)实验试剂 酸性红B(分子式如图1所示),分析纯≥98%,上海萨恩化学技术有限公司;四氧化三铁,天津市江天化工技术有限公司;过一硫酸氢钾复合盐(Oxone,有效成分peroxymonosulfate,PMS),有效成分>42.8%,天津易创成医药技术有限公司;无水甲醇,分析纯≥99.5%,天津市江天化工技术有限公司。

图1 酸性红B结构式
(2)实验仪器 双频数控超声波清洗器KQ-100VDE,昆山市超声仪器有限公司;双频数控超声波清洗器KQ-100VDB,昆山市超声仪器有限公司;精密增力电动搅拌器JJ-1,金坛市城东新瑞仪器厂;紫外-可见分光光度计UV1000,上海天美科学仪器公司。
1.2实验方法
将一定量的Fe3O4粉末倒入200mL染料溶液中,用电动搅拌器以180r/min的转速搅拌20min,使溶液达吸附平衡;调节超声频率、功率至设定值,将锥形瓶置于超声槽中,加入一定量的PMS,开启超声电源并开始计时;每隔10min取样,加入无水甲醇淬灭自由基终止反应;用紫外分光光度计测定样品吸光度,进而得到相应的染料浓度;控制清洗槽内温度(25±2)℃。每次取3个样品测试,取平均值。
1.3测试方法
采用紫外-可见分光光度计对样品进行扫描,发现酸性红B在515nm处有最大吸收峰值。在515nm的最大吸收波长下测定不同浓度的酸性红B溶液的吸光度A,得到表征酸性红B溶液浓度的标准曲线。本文使用酸性红B的色度去除率DR作为实验的分析指标,见式(1)。
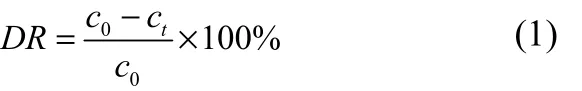
式中,c0为酸性红B初始浓度;ct为取样测定时酸性红B浓度。
2 结果与讨论
2.1PMS投加量对色度去除率的影响
设定酸性红B溶液浓度100mg/L,调节溶液初始pH为8.3,超声频率50kHz,超声功率80W,四氧化三铁投加量为1.0g/L,PMS投加量分别为10mmol/L、20mmol/L、40mmol/L、80mmol/L和100mmol/L。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图2所示。

图2 不同PMS投加量对色度去除率影响
当其他条件相同,PMS投加量由20mmol/L提高至60mmol/L时,酸性红B色度去除率越来越高。这是由于,PMS的浓度越大,产生的SO4-·数量就越多。在PMS投加量为60mmol/L时,降解效果最好,反应60min,降解率已经接近100%。当PMS的浓度超过60mmol/L时,继续增加用量,降解效果变差。文献报道硫酸根自由基之间可以相互作用生成S2O82-,淬灭生成的自由基,如反应式(2)所示;同时过量的硫酸根自由基来不及与酸性红B分子发生反应,就与过一硫酸氢根离子发生反应,式(3)为反应方程式,生成过硫酸根自由基活性低于硫酸根自由基,使降解效率降低[14]。

此外,一定量的Fe3O4具有固定数量的表面活性位点,能活化一定的HSO5-。同时超声空化也会活化过一硫酸盐产生过量的硫酸根自由基,与催化剂表面的Fe2+反应生成SO42-,进行如式(4)反应,不利于有机物分子降解和反应速率的提升[15]。因此选择PMS最优投加量为60mmol/L。
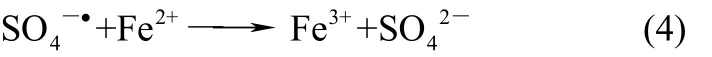
2.2Fe3O4投加量对色度去除率的影响
设定酸性红B溶液浓度100mg/L,调节溶液初始pH为8.3,超声频率50kHz,超声功率80W,PMS投加量为60mmol/L,Fe3O4投加量分别为0.5g/L、1.0g/L、1.5g/L和2.0g/L。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图3所示。

图3 不同Fe3O4投加量对色度去除率影响
Fe3O4是多价态的混合物,组成为FeO·Fe2O3,主要成分Fe2+,其作为PMS的活化剂,活化HSO5-产生SO4-·,实现酸性红B的降解[6]。根据图3可以看出,随着增大Fe3O4投加量,色度去除率有所提高,但是Fe3O4用量超过一定值时,酸性红B的降解速率会下降。虽然Fe3O4可以快速活化PMS产生硫酸根自由基,但是加入大量Fe3O4时迅速产生的SO4-·没有完全和目标污染物酸性红B发生反应。当Fe3O4浓度增大至过量时,溶液中产生过量的SO4-·。一方面,过量的SO4-·会发生自身淬灭反应消耗掉,另一方面,过量Fe3O4中的Fe2+也会与SO4-·发生反应。这两个副反应阻止SO4-·与酸性红B分子进一步接触,从而导致降解速率下降,因此选择1.0g/L为最佳Fe3O4投加量。
超声可以起到活化PMS的作用,设定酸性红B溶液浓度100mg/L,调节溶液初始pH为8.3,超声频率50kHz,PMS投加量为60mmol/L,Fe3O4投加量1.0g/L,超声功率分别为40W、60W、80W、100W。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图4所示。

图4 不同超声功率对色度去除率影响
根据图4可以看出,在非均相催化体系中,随着超声功率的增大,降解效率有所提高。这是因为随着功率增加,可以产生更多的热能,从而增加SO4
-·和˙OH的数量。随着超声波功率的增加,由于空化泡破裂产生微射流的作用,增强了固液两相间的传质。同时,超声的清洗作用保证了催化剂的活性位点与中间产物及时分离而不被其覆盖,防止催化剂失活。此外,当超声功率由80W提高到100W时,酸性红B的降解速率不升反而下降,超声表现了一定的抑制作用。这是由于当超声强度较高时,超声波所产生的空化泡的数量和大小成为影响降解速率的主要影响因素。超声功率过高时,导致声强过高产生大量无效气泡,增加散射衰减,形成声屏障,导致空化效率降低,从而降低酸性红B的降解效率[16]。
2.4超声频率对色度去除率的影响
超声可以起到活化PMS的作用,但是不同频率的超声,空化程度不同,对反应过程的影响也不同。此部分对不同超声频率下的酸性红B降解情况进行了研究。设定酸性红B溶液浓度100mg/L,调节溶液初始pH为8.3,超声功率80W,PMS投加量为60mmol/L,Fe3O4投加量1.0g/L,超声频率分别为20kHz、40kHz、50kHz、80kHz。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图5所示。

图5 不同频率超声对色度去除率影响
由图5可以看出,在其他条件相同的情况下,随着超声频率的增大,色度去除率呈现先增大后减小的趋势,在频率为50kHz达到最大值。低频时的降解效果总体上大于高频。因为随着频率降低,空化阈降低,在液体中发生空化越容易。频率较低时,液体受到的压缩和膨胀作用时间间隔长,空化泡生长所达到的最大半径增大,崩溃程度更加猛烈。但是频率过低时,气泡存活时间过长,空化泡内的自由基相互结合,导致活性降低,声化学产额下降,不利于有机物的降解[17]。实验中得到的最优值结果可以由CUM等[18]的研究中得到解释,假设声化学产额与频率的函数关系满足Gussian分布,如式(5)所示。

式中,y表示声化学产额;B为常数;fc为具有共振半径为R气泡核的共振频率;δ为分布曲线的半宽高度。
在授课过程中,有的教师基本依据教材,但会展开得比较丰富,这就需要我们在预习时对教材内容有一定的理解,并在此基础上有一定的分析;有的教师讲课则完全是对教材的展开、升华,那么,就要求我们在预习时要了解教材,分析教材,做读书笔记。这就告诉我们,预习不是盲目的,如果不根据教师的授课情况进行预习,那么,就可能收到事倍功半的效果。因此,教师应该指导学生进行有针对性的预习。
当超声频率f=fc时,超声与空化泡能达到最有效的能量耦合,此时声化学产额最高;f<fc时,f增大,空化增强;f>fc时,f增大,空化减弱。他们通过碘释放法得出fc在40~60kHz之间,与本文实验结果一致。因此,适合本文中的非均相体系降解酸性红B的最佳频率为50kHz。
2.5溶液初始pH对色度去除率的影响
实际染料废水pH范围较广,而传统Fenton试剂对溶液的酸碱度要求较苛刻,限制了其广泛应用,因此对本文中提出方法的酸碱度适用范围进行探究。设定酸性红B溶液浓度100mg/L,取超声频率50kHz,超声功率80W,PMS投加量为60mmol/L,Fe3O4投加量1.0g/L,溶液初始pH分别为3.5、7.0、8.5。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图6所示。

图6 不同pH对色度去除率影响
在酸性条件下,Fe3O4中的二价铁离子更利于参与PMS的活化,产生更多。随着溶液pH升高,酸性红B的降解速率随之下降。

此外,在反应进行过程中,由于生成有机酸类小分子物质使得反应液的pH随反应时间增加而降低,并且随着PMS在溶液中的溶解及反应式(7)的进行,会向溶液中释放更多的H+,导致溶液的pH降低。

由测得的反应后的溶液pH可知,即便溶液初始pH不同,经过90min后,最终的pH基本一致,分别为2.5、2.4、2.5。因此,不同初始pH条件下,反应后酸性红B的色度去除率最终基本相同。
2.6初始酸性红B浓度对色度去除率的影响
分别取浓度为100mg/L、200mg/L、400mg/L和500mg/L的酸性红B溶液200mL,取超声频率50kHz,超声功率80W,PMS投加量为60mmol/L,Fe3O4投加量1.0g/L,溶液初始pH分别为8.5。按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图7所示。

图7 初始酸性红B浓度对色度去除率影响
根据图7可以看出,当反应体系的其他条件相同时,随着染料初始浓度的增加,降解效率会逐渐降低。当PMS投加量,Fe3O4的投加量相等且其他氧化条件一定时,的产生量也是一定的。初始染料浓度的增加会降低染料分子与自由基的反应机率。另外,反应中生成的中间产物也与自由基发生氧化反应,导致了的消耗。尽管被消耗,但是在不同染料初始浓度下,色度去除率均达到90%以上,这表明反应90min后,在Fe3O4的催化下,60mmol/L的PMS分解产生的硫酸根自由基已经足够完全降解酸性红B。
2.7催化剂循环利用性能
催化剂的重复利用性能是考核其经济价值的重要方面之一。基于Fe3O4具有磁性这一特点,采用外加磁场对反应过后的Fe3O4进行回收,经过洗涤干燥等操作后重复使用。并对重复利用前后降解反应的脱色效果进行对比,检验催化剂的稳定性。回收前后反应条件均相同,PMS投加量为60mmol/L,Fe3O4投加量为1.0g/L,超声功率为80W,超声频率为50kHz,初始pH为8.3,初始染料浓度为100mg/L,按照前述降解实验获得溶液中酸性红B色度去除率随时间的变化,如图8所示。
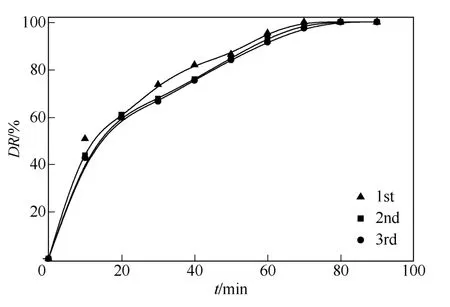
图8 催化剂循环利用性能对比
根据图8可以看出,随着催化剂使用次数的不断增加,降解效率略有所降低。催化剂Fe3O4中,Fe2+的溶出是导致其活性降低的主要因素。此外,文献[6]报道,在Fe3O4固体中Fe2+与Fe3+之间的相互转化,在催化剂表面形成三价铁氧化膜,阻碍了固体中的结构二价铁活化PMS产生自由基,降低了催化效率。由于本实验在非均相体系中引入超声,超声的清洗作用促进了反应中生成的中间产物与催化剂及时分离,防止其覆盖在催化剂表面使其中毒。综上所述,本文所选催化剂Fe3O4回收再利用的性能较好,能够有效节省由于催化剂损失所带来的成本,具有很好的经济性。
3 结 论
本文选取典型偶氮染料酸性红B作为目标污染物,采用超声辅助Fe3O4活化PMS方法对其进行降解,以色度去除率为指标对降解效果进行研究。结果表明,该方法可以有效降解酸性红B,且反应速率快,色度去除率达到90%以上。其实验优化条件为Fe3O4投加量1.0g/L,PMS投加量60mmol/L,超声频率50kHz,超声功率80W,初始pH影响较小,可降解较大浓度酸性红B溶液。本方法具有简单、成本低廉等特点。催化剂重复使用性能好,可利用外磁场对反应后溶液实现快速分离,具有良好应用前景。
[1] BANERJEE P,DAS GUPTA S,DE S,et al.Removal of dye from aqueous solution using a combination of advanced oxidation process and nanofiltration[J].Journal of Hazardous Materials,2007,140(1):95-103.
[2] 齐鲁青,汪晓军,徐绮坤,等.印染废水深度处理及回用[J].现代化工,2010,30(12):73-76.
[3] 叶林静,关卫省,李宇亮,等.高级氧化技术降解双酚A的研究进展[J].化工进展,2013,32(4):909-918.
[4] MUNTER R. Advanced oxidation processes-current status and prospects[J].Proc. Estonian Acad. Sci. Chem.,2001,50(2): 59-80.
[5] 包木太,王娜,陈庆国,等.Fenton法的氧化机理及在废水处理中的应用进展[J].化工进展,2008,27(5):660-665.
[6] DHAKSHINAMOORTHY A,NAVALON S,ALVARO M,et al.Metal nanoparticles as heterogeneous Fenton catalysts[J].Chem. Sus. Chem., 2012,5(1):46-64.
[7] 杨世迎,杨鑫,王萍,等.过硫酸盐高级氧化技术的活化方法研究进展[J].现代化工,2009,29(4):13-19.
[8] 王兵,李娟,莫正平,等.基于硫酸自由基的高级氧化技术研究及应用进展[J].环境工程,2012,30(4):53-57.
[9] LIANG C,LEE I L,HSU I Y,et al.Persulfate oxidation of trichloroethylene with and without iron activation in porous media[J].Chemosphere,2008,70(3):426-435.
[10] SNOOK M E,HAMILTON G A.Oxidation and fragmentation of some phenyl-substituted alcohols and ethers by peroxydisulfate and Fenton's reagent[J].Journal of the American Chemical Society,1974,96(3):860-869.
[11] YANG S,WANG P,YANG X,et al.Degradation efficiencies of azo dye Acid Orange 7 by the interaction of heat,UV and anions with common oxidants: persulfate,peroxymonosulfate and hydrogen peroxide[J].Journal of Hazardous Materials,2010,179(1):552-558.
[12] 范拴喜,江元汝.Fenton法的研究现状与进展[J].现代化工,2007,27(s1):104-107.
[13] HOU L,HUI Z,XUE X,et al.Ultrasound enhanced heterogeneous activation of peroxydisulfate by magnetite catalyst for the degradation of tetracycline in water[J].Separation & Purification Technology,2012,84(2):147-152.
[14] 丁耀彬.基于过渡金属氧化物催化活化过一硫酸盐高级氧化方法及其在有机污染物降解中的应用[D].武汉:华中科技大学,2013.
[15] HUIE R E,CLIFTON C L.Temperature dependence of the rate constants for reactions of the sulfate radical,SO4-·,with anions[J].Journal of Physical Chemistry,1990,94(23):8561-8567.
[16] LIU L Y,YANG Y,LIU P H,et al.The influence of air content in water on ultrasonic cavitation field[J].Ultrasonics Sonochemistry,2014,21(2):566-571.
[17] 刘丽艳,杨洋,刘芃宏,等.基于频谱分析方法的超声空化场三维重建及其分布[J].天津大学学报(自然科学与工程技术版),2014(11):962-966.
[18] CUM G,GALLI G,GALLO R,et al.Role of frequency in the ultrasonic activation of chemical reactions[J].Ultrasonics,1992,30(4):267-270.
[19] LAU T K,WEI C,GRAHAM N J D,et al.The aqueous degradation of butylated hydroxyanisole by UV/S2O82-:study of reaction mechanisms via dimerization and mineralization[J].Environmental Science & Technology,2007,41(2):613-619.
Degradation of Acid Red B with Fe3O4activated peroxymonosulfate with ultrasound irradiation
LIU Liyan,SUN Zhirou,YE Wenbo,TAN Wei
(School of Chemical Engineering & Technology,Tianjin University,Tianjin 300354,China)
Azo dyes,with high chromaticity,are difficult to degrade by traditional methods to meet the industrial emission standard,which become great threat to the environment. In this paper,Acid Red B,as a selected azo dye,was degraded with advanced oxidation process by Fe3O4activating peroxymonosulfate(PMS) with ultrasound irradiation. This study focus on the effect of parameters on the degradation rate such as the addition of Fe3O4,the concentration of PMS,the ultrasound power and frequency,the initial concentration of Acid Red B and the initial pH of the solution. The optimized operating parameters are Fe3O41.0g/L,PMS 60 mmol/L,ultrasound frequency 50kHz,ultrasound power 80W. This method can be applied in a wide range of pH from 3.5 to 8.5 and is capable of degrading high concentration of Acid Red B up to 1g/L. The study also investigated the reusability of the catalyst. The catalyst was recycled for 3 times and the decoloration rate still remained above 95%. These results can be applied to the industrial process of wastewater treatment of azo dyes.
peroxymonosulfate;Fe3O4;ultrasound;Acid Red B;advanced oxidation process
X 703.1
A
1000-6613(2016)11-3663-06
10.16085/j.issn.1000-6613.2016.11.042
2016-04-06;修改稿日期:2016-05-26。
刘丽艳(1977—),女,副教授,研究方向为非均相分离理论与技术。联系人:谭蔚,教授,研究方向为非均相分离理论与技术。E-mail wtan@tju.edu.cn。
