外用西罗莫司治疗儿童结节性硬化症血管纤维瘤的疗效及安全性研究
2016-11-06王森分王旭魏京海张建刘元香徐子刚
王森分 王旭 魏京海 张建 刘元香 徐子刚
100045北京,首都医科大学附属北京儿童医院皮肤科(王森分、刘元香、徐子刚),神经内科(王旭),药学部(魏京海、张建)
外用西罗莫司治疗儿童结节性硬化症血管纤维瘤的疗效及安全性研究
王森分 王旭 魏京海 张建 刘元香 徐子刚
100045北京,首都医科大学附属北京儿童医院皮肤科(王森分、刘元香、徐子刚),神经内科(王旭),药学部(魏京海、张建)
目的研究0.1%西罗莫司软膏治疗儿童结节性硬化症血管纤维瘤的临床疗效及安全性。方法自制0.1%西罗莫司软膏。选取结节性硬化症面部血管纤维瘤患儿20例,予0.1%西罗莫司软膏外用,每天2次。分别于治疗4周、12周时,记录面部血管纤维瘤严重程度指数(FASI评分)、皮损治疗满意度及不良反应等。治疗前、治疗12周时,检测西罗莫司血药浓度、血尿常规、凝血功能、血生化及免疫指标。结果治疗前、治疗4周、治疗12周时,20例患儿FASI评分分别为5.750±1.175、4.400± 1.284和2.975± 1.543,治疗4周、12周时的FASI评分均较治疗前显著下降(均P<0.000 1),且治疗12周时显著低于治疗4周时(P<0.000 1)。治疗12周时平均疗效指数(49.87%±22.08%)显著高于治疗4周时(24.43%±10.18%),差异有统计学意义(t=7.338,P<0.01)。治疗12周时,皮损颜色明显变淡,体积明显缩小,瘤体数量减少,2例皮损完全消退。治疗4周时,10例对红斑减淡程度满意,3例对皮损体积改善满意,3例对皮损面积改善满意。治疗12周时,家长的满意度均提高。20例患儿治疗前后西罗莫司血药浓度均低于1.0 μg/L,无严重系统及皮肤不良反应发生。结论0.1%西罗莫司软膏治疗结节性硬化症血管纤维瘤疗效显著,安全性好。
结节性硬化症;血管纤维瘤;西罗莫司;治疗结果
结节性硬化症(tuberous sclerosis complex,TSC)是一种常染色体显性遗传的神经皮肤综合征,其发病率一般为1/6 000~1/10 000,受累器官主要为神经系统、皮肤、心脏、肾脏等[1⁃3]。面部血管纤维瘤是TSC特征性损害,可见于约80%的TSC患者,具有损容性,对患者的身心健康造成极大的影响[1⁃4]。目前治疗面部血管纤维瘤的方法包括冷冻、磨削、激光和光动力等,这些治疗方法均为有创治疗,可能会遗留永久性瘢痕,且由于复发,患者需要反复治疗[1⁃3],故对儿童患者多采用随诊观察。有研究报道,口服或外用西罗莫司治疗结节性硬化症皮肤症状,取得一定疗效[2⁃3,5]。2015年3月以来,我们应用0.1%西罗莫司软膏治疗儿童TSC面部血管纤维瘤,获得较好疗效。
对象与方法
一、临床资料
1.纳入标准:符合2012更新版TSC诊断标准[4];患有面部血管纤维瘤;家长或法定监护人自愿签订本研究知情同意书,同意本治疗方案,能遵守试验规定、规范用药、定期随访。排除标准:合并免疫系统相关疾病,既往或目前口服西罗莫司治疗,正在参加另一项临床研究,依从性差或无法按照要求完成研究。
2.患者一般资料:2015年3-5月就诊于北京儿童医院皮肤科的20例TSC面部血管纤维瘤患儿纳入本研究,其中男12例,女8例,年龄4~13(7.750±2.221)岁,发病年龄0~ 9岁,中位年龄(P25~P75)为2.36(0.625~3)岁。面部血管纤维瘤严重程度指数(facial angiofibroma severity index,FASI)评分[6]:轻度9例,中度11例。其他皮损:卵圆形或条叶状白斑19例,鲨鱼皮样斑11例,甲周纤维瘤2例。12例有抽搐史。本研究通过北京儿童医院医学伦理委员会批准。
二、药物制备及载药率测定
1.仪器与试剂:Agilent 1260高效液相色谱仪(美国安捷伦科技有限公司);西罗莫司标准品(华北制药股份有限公司新药研发中心,批号:YNSN1501401),含量98.3%;乙腈、甲醇(美国Fisher公司);黄凡士林。
2.0.1%西罗莫司软膏制备方法:称取西罗莫司标准品1 g,置乳钵中研成80目的粉末。取黄凡士林1 000 g,置于恒温水浴箱加热溶解,当温度至60℃时,停止加热,在不断搅拌下,缓缓以细流加入西罗莫司粉末,边加边搅拌,使其充分分散。
3.西罗莫司含量测定:采用高效液相色谱法。
(1)色谱条件:色谱柱为ZORBAX SB⁃C18,4.6 mm(内径)×250 mm(柱长),填料内径5 μm,批号USCL044217;紫外检测器检测波长278 nm;进样量10 μl;流速1.0 ml/min;柱温40 ℃;流动相为乙腈(100%)。
(2)对照品溶液配制:秤取西罗莫司标准品25 mg,置25 ml容量瓶中,加乙腈适量,振荡使对照品溶解,配制成0.01、0.1、1.0、10、100、1 000 mg/L系列工作液。
(3)样品液的配制:秤取已制备的西罗莫司软膏1.040 3 g,置于5 ml样品管中,加入甲醇2.5 ml,60℃恒温水浴箱加热,搅拌振荡,置于冰袋迅速冷凝析出黄凡士林,待黄凡士林凝固后,收集样品管中液体;在残留凝固软膏的样品管中再加入甲醇2.5 ml,重复上述加热冷凝过程4次后,将收集的液体经中速定性滤纸过滤,收集滤液于离心管中,加入乙腈5 ml,振荡2 min,以1 110 ×g离心10 min,留取上清液待用。按照上述方法制备3份待测样品。
(4)求曲线方程和相关系数:不同浓度的对照品溶液各进样1次,记录色谱图,以峰面积的对数对对照品溶液浓度的对数进行线性回归,求得曲线方程和相关系数。
(5)计算西罗莫司含量:3份样品溶液各进样1次,记录峰面积,带入标准曲线方程,计算3份样品西罗莫司含量。
三、治疗观察
1.治疗方法:皮损处清洗后,外用0.1%西罗莫司软膏,每天2次。分别在治疗4周、12周时,记录FASI评分、皮损治疗满意度和不良反应。
2.FASI评分与临床疗效判定:FASI评分[6]由三部分评分相加组成,其中红斑0~3分,体积0~3分,受累面积2~3分,FASI≤5为轻度,FASI>5且<8为中度,FASI≥8为重度。由研究者以外的两位主治医师及以上资格的皮肤科医师进行FASI评分,取平均值。临床疗效判定:疗效指数(%)=[(治疗前FASI评分-治疗后FASI评分)/治疗前FASI评分]×100%。FASI25、FASI50、FASI75分别为疗效指数达25%、50%、75%的患者比例。
3.满意度评价:通过家长填写满意度调查表,评价面部血管纤维瘤外用0.1%西罗莫司软膏治疗后,红斑、皮损体积、受累面积较治疗前的改善程度。满意度评价定义为,不满意:疗效指数0~25%;一般:疗效指数26%~50%;满意:疗效指数51%~75%;非常满意:疗效指数76%~100%。
4.安全性指标:治疗前后西罗莫司血药浓度、血尿常规、血生化、凝血功能、免疫指标(T淋巴细胞数、辅助性T细胞数、抑制性T细胞数、CD4/CD8比值、B淋巴细胞数、自然杀伤细胞数)。记录治疗期间出现的系统不良反应(如发热、口腔溃疡、腹泻等)及皮肤不良反应(如红斑、瘙痒、疼痛、烧灼感、粉刺等)。
5.统计方法:应用SAS9.4及SPSS23.0软件进行数据分析。单组的重复测量数据采用单组重复测量方差分析,比较3个时间点之间的差异。首先进行球性假定检验,如果满足球性假定,采用单变量方差分析;如果不满足,则采用多变量方差分析。如果时间点之间差异有统计学意义,进一步采用contrast法比较治疗后2个时间点与治疗前的差异,并采用Bonferroni法校正P值,将检验水准设为0.05/2=0.025。同一受试对象两两时间点间的比较采用配对t检验,相关分析使用Pearson相关分析,P<0.05为差异有统计学意义。
结 果
一、0.1%西罗莫司软膏药物含量测定结果
采用高效液相色谱法测定自制0.1%西罗莫司软膏中西罗莫司含量,求得曲线方程y=0.978 6x+5.722 3和复相关系数R=0.999 7,决定系数R2=0.999 5,模型对数据拟合程度较好。检测西罗莫司软膏3个样本,含量分别为0.107 9%、0.107 6%、0.103 5%,平均含量为0.106 3%。
二、治疗效果
1.治疗前后临床疗效比较(表1):治疗前、治疗4周、治疗12周时,20例患儿FASI评分有随时间逐渐下降的趋势(F=80.132,P<0.000 1)。与治疗前相比,治疗4周、12周时的FASI评分均显著下降(均P<0.000 1),且治疗12周显著低于治疗4周时(P<0.000 1)。皮损红斑及面积FASI评分随治疗时间延长也有不同程度下降(F=361.042、17.403,均P<0.000 1)。治疗12周时,皮损颜色均明显减淡,体积明显缩小,瘤体数量减少,2例皮损完全消退。典型病例治疗前后疗效对比见图1。
治疗12周时平均疗效指数显著高于治疗4周时,差异有统计学意义(t=7.338,P<0.01)。治疗前FASI评分与治疗4周时疗效指数呈低度线性负相关(r=-0.446,P< 0.05),但与治疗12周时疗效指数无显著相关性(P=0.103)。患儿年龄与治疗前FASI评分、治疗4周、治疗12周时疗效指数均无明显相关性(均P>0.05)。治疗4周时8例达FASI25以上;治疗12周时,20例均达FASI25,8例达FASI50,2例达FAST75。
2.治疗4、12周时患儿家长满意度评价(表2):治疗4周时,20例中10例对红斑减淡程度满意,3例对皮损体积改善满意,3例对皮损面积改善满意;治疗12周时,家长的满意度均提高,满意和非常满意的评价居多,不满意的评价减少。
三、安全性评价
治疗12周时,20例患儿中15例西罗莫司血药浓度较治疗前升高,5例较治疗前降低。20例患儿平均西罗莫司血药浓度[(0.665±0.243)μg/L]高于治疗前[(0.366±0.263)μg/L],差异有统计学意义(t=3.823,P< 0.01),但治疗前后均低于1.0 μg/L。血尿常规、血生化、凝血功能、免疫指标无明显变化,在整个治疗和随访过程中亦未见其他系统不良反应发生。仅1例11岁男性患儿,在外用药1周后面部出现1~2个白头粉刺,反复4周,在外用药5周时症状消失,之后未再出现皮肤不良反应。

表1 外用0.1%西罗莫司软膏治疗20例结节性硬化症患儿面部血管纤维瘤不同时间面部血管纤维瘤严重程度指数(FASI)评分及疗效指数比较(x±s)
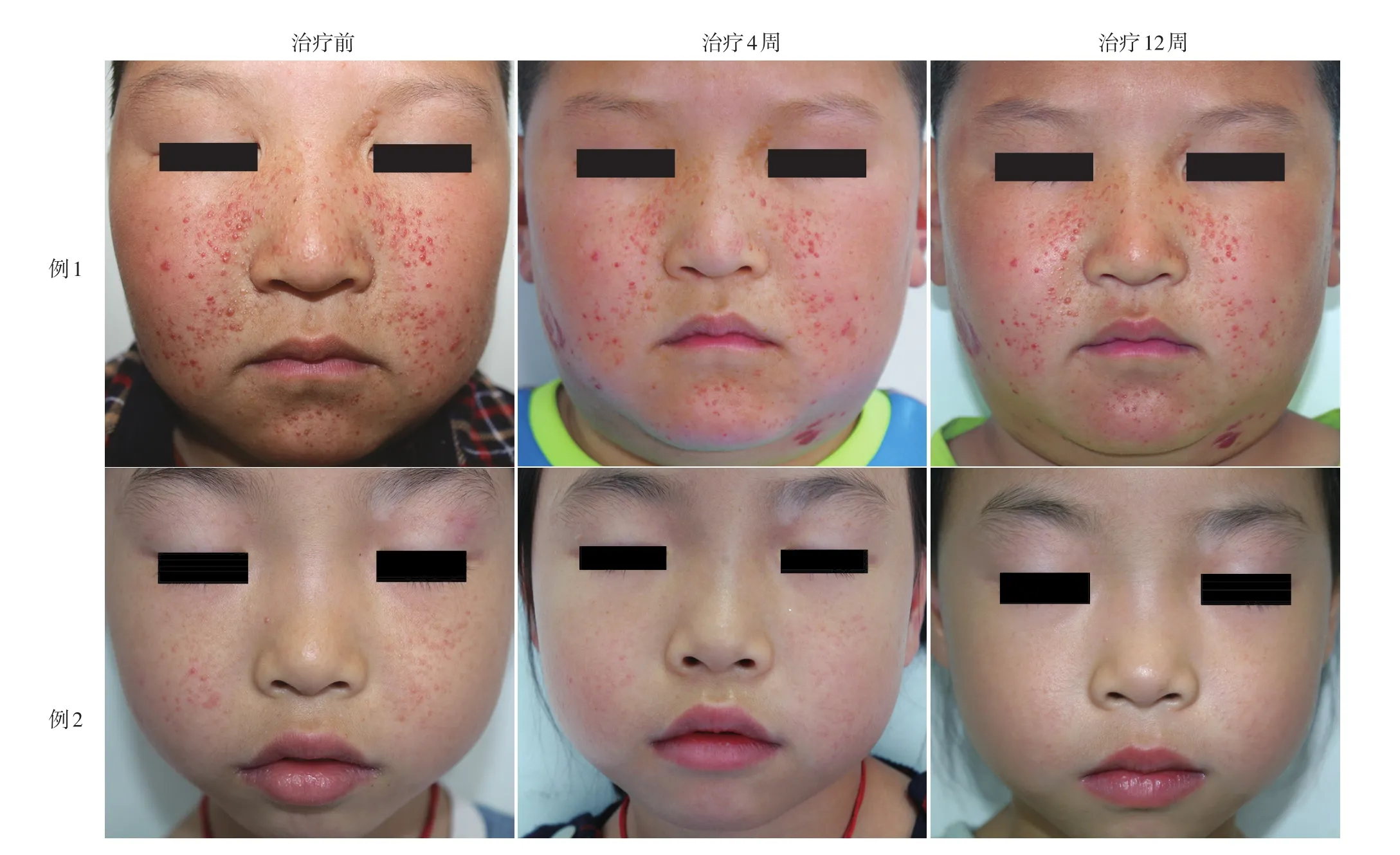
图1 2例结节性硬化症患儿面部血管纤维瘤外用0.1%西罗莫司软膏治疗前后比较 例1男,9岁,治疗后皮损明显缩小,颜色明显减淡,瘤体数量减少;例2女,6岁,治疗12周时面部血管纤维瘤完全消退
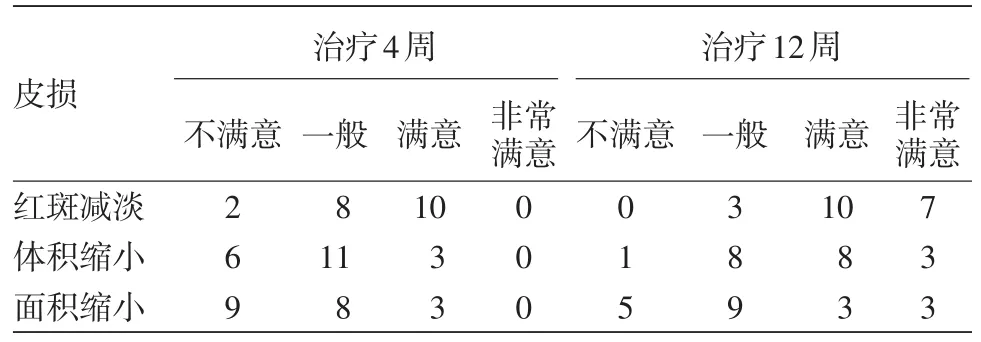
表2 外用0.1%西罗莫司软膏治疗20例结节性硬化症面部血管纤维瘤患儿4周及12周时家长满意度(例)
四、随访
治疗12周,面部血管纤维瘤完全消退的2例患儿,分别在停药2周、4周后复发,继续外用0.1%西罗莫司软膏仍有效。余18例皮损未消退患儿仍在治疗随访中。
讨 论
TSC为TSC1、TSC2基因突变导致的全身各系统均可受累的神经皮肤综合征[1,7⁃9]。皮肤受累主要表现为卵圆形或条叶状白斑、面部血管纤维瘤、鲨鱼皮样斑、甲周纤维瘤等[4,10]。约80%TSC患者会出现面部血管纤维瘤。不经治疗,面部血管纤维瘤不会自行改善或消退,随年龄增长其数量和体积也进行性增加[2⁃3,10]。TSC1和TSC2基因分别编码错构瘤蛋白和马铃薯球蛋白,从而抑制mTOR信号通路。mTOR信号通路通过其下游的靶蛋白核糖体蛋白S6激酶1(S6K1)和蛋白质翻译起始因子4E结合蛋白1(4EBP1),加快细胞从G1期到S期的转换,促进细胞生长和增殖,抑制细胞凋亡。而TSC1和TSC2基因突变可增强mTOR活动,导致细胞生长的调节异常和肿瘤发生[1,8⁃11]。TSC 患者血管纤维瘤中的成纤维细胞产生过多的表皮生长因子、上皮调节蛋白,刺激表皮增殖,使表皮增殖速度超过凋亡速度。同时,TSC患者血管内皮生长因子表达增多,两者共同导致面部血管纤维瘤的出现及持续增长[3,9,12]。
西罗莫司属于大环内酯类化合物,是mTOR特异性抑制剂,可抑制 mTOR 活性[1,3,7,10⁃11],阻断细胞由G1期至S期的细胞周期进程,抑制血管内皮生长因子的释放和内皮祖细胞、角质形成细胞的增殖[11⁃13]。目前已有大量文献报道其应用于皮肤科多种疾病的治疗,包括遗传性皮肤病(如TSC、Birt⁃Hogg⁃Dubé综合征、Cowden病、鲜红斑痣、血管瘤等)、皮肤肿瘤(如黑素瘤、非黑素瘤细胞性皮肤肿瘤、皮肤T细胞淋巴瘤、Kaposi肉瘤等)、自身免疫性或炎症性疾病(如系统性硬化病、慢性口腔扁平苔藓等)[2,14⁃16]。西罗莫司易溶于乙醇、氯仿、丙酮等有机溶剂,能够通过表皮吸收,并进入真皮深层[3,7,14]。我们以凡士林为基质,配制0.1%西罗莫司软膏,软膏中西罗莫司平均含量测定结果为0.106 3%,提示药物配制精准,符合本研究所需制剂要求。
我们外用0.1%西罗莫司软膏治疗20例TSC面部血管纤维瘤患儿12周,皮损颜色明显减淡,体积明显缩小,瘤体数量减少。治疗4、12周时,患儿FASI评分均显著下降。治疗12周时平均疗效指数达到49.87%,2例皮损完全消退。停药复发者,继续外用0.1%西罗莫司软膏仍有效。皮损红斑、体积、面积FASI评分结果及患儿治疗满意度调查提示,TSC患儿面部血管纤维瘤红斑消退时间早,速度快,但皮损体积和面积的改善速度相对较慢。本研究20例患儿年龄与治疗前FASI评分、治疗4周、治疗12周时疗效指数均无显著相关性,但未经治疗的TSC患者,随年龄增长面部血管纤维瘤数量和体积将进行性增加[3,10],故其FASI评分应随年龄增大而增大。已有文献报道,由于增生期的肿瘤在早期时增生成分更多,对西罗莫司更敏感,故应早期开始治疗[3],年龄小者治疗效果更好[14⁃15]。故患者年龄与面部血管纤维瘤的严重程度及疗效的相关性分析仍需大样本调查研究。
文献报道,西罗莫司的检测下限为 1.0 μg/L[7],提示本研究中5例患儿治疗12周时,西罗莫司血药浓度低于治疗前,可能由于受内源性因素影响,浓度在1.0 μg/L内的波动无临床意义。本研究20例患儿治疗前后西罗莫司血药浓度均低于1.0 μg/L,远低于口服西罗莫司治疗TSC需要维持的血药浓度(5 ~ 15 μg/L)[1,8,11],且20例患儿治疗12周期间血尿常规、血生化、凝血功能、免疫指标无明显变化,无发热、口腔溃疡、腹泻等系统不良反应发生。仅1例在外用药1周后面部出现1~2个白头粉刺,在外用药5周时消失,之后未再出现皮肤不良反应。该结果与既往报道外用西罗莫司治疗TSC面部血管纤维瘤安全性高是一致的[6⁃7,14⁃16]。
既往文献报道,外用西罗莫司浓度多为0.1%~1%[3,14⁃16],本研究入组患者均为儿童,故采用低浓度0.1%。我们的研究结果提示,0.1%西罗莫司软膏治疗儿童TSC血管纤维瘤效果显著,安全性好。
[1] Schwartz RA,Fernández G,Kotulska K,et al.Tuberous sclerosis complex:advances in diagnosis,genetics,and management[J].J Am Acad Dermatol,2007,57(2):189⁃202.DOI:10.1016/j.jaad.2007.05.004.
[2]Tu J,Foster RS,Bint LJ,et al.Topical rapamycin for angiofibromas in paediatric patients with tuberous sclerosis:follow up of a pilot study and promising future directions[J].Australas J Dermatol,2014,55(1):63⁃69.DOI:10.1111/ajd.12125.
[3]Vasani RJ.Facial angiofibromas of tuberous sclerosis treated with topical sirolimus in an Indian patient[J].Indian J Dermatol,2015,60(2):165⁃169.DOI:10.4103/0019⁃5154.152516.
[4]NorthrupH,KruegerDA,GroupITSCC.Tuberoussclerosiscomplex diagnostic criteria update:recommendations of the 2012 international tuberous sclerosis complex consensus conference[J].Pediatr Neurol,2013,49(4):243 ⁃254.DOI:10.1016/j.pediatrneurol.2013.08.001.
[5]Nathan N,Wang J,Li S,et al.Improvement of tuberous sclerosis complex(TSC)skin tumors during long⁃term treatment with oral sirolimus[J].J Am Acad Dermatol,2015,73(5):802⁃808.DOI:10.1016/j.jaad.2015.07.018.
[6] Salido⁃Vallejo R,Ruano J,Garnacho⁃Saucedo G,et al.Facial angiofibroma severity index(FASI):reliability assessment of a new tool developed to measure severity and responsiveness to therapy in tuberous sclerosis⁃associated facial angiofibroma[J].Clin Exp Dermatol,2014,39(8):888⁃893.DOI:10.1111/ced.12398.
[7] Koenig MK,Hebert AA,Roberson J,et al.Topical rapamycin therapy to alleviate the cutaneous manifestations of tuberous sclerosis complex[J].Drugs R D,2012,12(3):121⁃126.DOI:10.2165/11634580⁃000000000⁃00000.
[8]Sampson JR.Therapeutic targeting of mTOR in tuberous sclerosis[J].Biochem Soc Trans,2009,37(Pt 1):259⁃264.DOI:10.1042/BST0370259.
[9] Li S,Takeuchi F,Wang JA,et al.Mesenchymal⁃epithelial interactions involving epiregulin in tuberous sclerosis complex hamartomas[J].Proc Natl Acad Sci USA,2008,105(9):3539 ⁃3544.DOI:10.1073/pnas.0712397105.
[10]Darling TN.Hamartomas and tubers from defects in hamartin⁃tuberin[J].J Am Acad Dermatol,2004,51(1 Suppl):S9 ⁃11.DOI:10.1016/j.jaad.2004.01.009.
[11] Paghdal KV,Schwartz RA.Sirolimus(rapamycin):from the soil of Easter Island to a bright future[J].J Am Acad Dermatol,2007,57(6):1046⁃1050.DOI:10.1016/j.jaad.2007.05.021.
[12]Hofbauer GF,Marcollo⁃Pini A,Corsenca A,et al.The mTOR inhibitor rapamycin significantly improves facial angiofibroma lesions in a patient with tuberous sclerosis[J].Br J Dermatol,2008,159(2):473⁃475.DOI:10.1111/j.1365⁃2133.2008.08677.x.
[13]Del Bufalo D,Ciuffreda L,Trisciuoglio D,et al.Antiangiogenic potentialofthe mammalian targetofrapamycin inhibitor temsirolimus[J].Cancer Res,2006,66(11):5549 ⁃5554.DOI:10.1158/0008⁃5472.CAN⁃05⁃2825.
[14] Tanaka M,Wataya⁃Kaneda M,Nakamura A,et al.First left⁃right comparative study of topical rapamycinvs.vehicle for facial angiofibromas in patients with tuberous sclerosis complex[J].Br J Dermatol,2013,169(6):1314⁃1318.DOI:10.1111/bjd.12567.
[15] SalidoR,Garnacho⁃SaucedoG,Cuevas⁃AsencioI,etal.Sustained clinical effectiveness and favorable safety profile of topicalsirolimus fortuberous sclerosis⁃associated facial angiofibroma[J].J Eur Acad Dermatol Venereol,2012,26(10):1315⁃1318.DOI:10.1111/j.1468⁃3083.2011.04212.x.
[16]Fogel AL,Hill S,Teng JM.Advances in the therapeutic use of mammalian target of rapamycin(mTOR)inhibitors in dermatology[J].J Am Acad Dermatol,2015,72(5):879⁃889.DOI:10.1016/j.jaad.2015.01.014.
Efficacy and safety of topical sirolimus in the treatment of facial angiofibromas in children with tuberous sclerosis complex
Wang Senfen,Wang Xu,Wei Jinghai,Zhang Jian,Liu Yuanxiang,Xu Zigang Department of Dermatology,Beijing Children′s Hospital,Capital Medical University,Beijing 100045,China(Wang SF,Liu YX,Xu ZG);Department of Neurology,Beijing Children′s Hospital,Capital Medical University,Beijing 100045,China(Wang X);Department of Pharmacy,Beijing Children′s Hospital,Capital Medical University,Beijing 100045,China(Wei JH,Zhang J).
ObjectiveTo investigate the efficacy and safety of sirolimus 0.1%ointment in the treatment of facial angiofibromas in children with tuberous sclerosis complex.MethodsSirolimus 0.1%ointment was prepared.Twenty children with tuberous sclerosis complex who had facial angiofibromas were enrolled in this study.Facial angiofibromas were topically treated with the self⁃prepared sirolimus 0.1%ointment twice a day for 12 weeks.The facial angiofibroma severity index(FASI)was calculated,the degree of satisfaction with the treatment was evaluated,and adverse reactions were analyzed at weeks 4 and 12.Plasma sirolimus concentrations as well as blood biochemical and immunological parameters were measured,blood coagulation activity was evaluated,and routine blood tests as well as urine tests were performed at baseline and week 12.ResultsThe FASI of patients significantly decreased at weeks 4(4.400 ±1.284)and 12(2.975±1.543)compared with that at baseline(5.750 ± 1.175,bothP< 0.000 1),and was significantly lower at week 12 than at week 4(P<0.000 1).The efficacy index was 49.87% ± 22.08%at week 12,significantly higher than that at week 4(24.43% ±10.18%,t=7.338,P<0.01).The color,size and number of lesions significantly decreased in all the patients,and facial angiofibromas completely disappeared in 2 patients at week 12.At week 4,10 parents were satisfied with the improvement of erythema,3 parents with that of lesion volume,and 3 parents with that of lesion area.The degree of parent satisfaction increased at week 12 in all the cases.The blood concentration of sirolimus was lower than 1.0 μg/L both before and after the treatment.No severe systemic or local adverse reactions were noted in these patients.ConclusionSirolimus 0.1%ointment is markedly effective and safe for the treatment of facial angiofibromas in patients with tuberous sclerosis complex.
Tuberous sclerosis;Angiofibroma;Sirolimus;Treatment outcome
Xu Zigang,Email:zigangxu@yahoo.com
徐子刚,Email:zigangxu@yahoo.com
10.3760/cma.j.issn.0412⁃4030.2016.07.005
北京市科委“首都临床特色应用研究”专项课题(Z161100000516070);北京市医院管理局临床医学发展专项(ZYLX201601)
Fund programs:the Capital Clinical Characteristic Application Research Program of Beijing Municipal Science and Technology Commission(Z161100000516070);Beijing Municipal Administration of Hospitals Clinical Medicine Development of Special Funding Support(ZYLX201601)
2015⁃09⁃29)
(本文编辑:周良佳 颜艳)
