高硫煤还原硫化焙烧锡铁精矿脱锡
2016-11-01冯鑫洋桑秀丽
冯鑫洋,李 磊,于 勇,桑秀丽
高硫煤还原硫化焙烧锡铁精矿脱锡
冯鑫洋,李 磊,于 勇,桑秀丽
(昆明理工大学复杂有色金属资源清洁利用省部共建国家重点实验室冶金与能源工程学院,昆明 650093)
高硫煤对锡铁精矿进行还原硫化焙烧,可实现物料中锡的有效脱除。以热力学和动力学分析为基础,对锡铁精矿的高硫煤硫化焙烧脱锡机理和过程进行了研究。结果表明:在空气气氛下,高硫煤还原硫化锡铁精矿主要通过布多尔反应产物CO的还原作用和气化产物SO2的硫化作用实现。与传统黄铁矿硫化现象不同,高硫煤添加量由0.6增加至1.8,锡铁精的矿深度还原未造成锡脱除率的下降,是由于高硫煤气化产物SO2的气相硫化速率较快,使锡快速挥发,减少了硬头(锡铁合金)的生成;在空气流量10 mL/min、焙烧温度1473 K、保温时间60 min、高硫煤添加量1.8(高硫煤/锡铁精矿质量比)及添加粒度74 μm的条件下,处理后矿样锡含量降至0.066%,经进一步磁选处理物料锡含量最低可降至0.058%,达到高炉炼铁关于锡含量小于0.08%的要求,为高硫煤的清洁利用提供一种新途径。
高硫煤;锡铁精矿;还原硫化焙烧;脱锡;动力学
我国铁矿资源总量大,但难选矿和多组分共(伴)生矿所占比重大[1],合格铁矿石产量不能满足钢铁产业需求,需增加进口弥补供需缺口,导致我国钢铁行业对外依存度逐年上升[2],解决此问题需提高我国自身复杂铁矿资源的综合利用率。锡铁矿是一种典型的复杂难处理铁矿,储量丰富,集中分布于湖南、内蒙古和云南等地区,一般含铁30%~50%(质量分数),锡 0.13%~ 0.5%[3−4],选矿处理后精矿锡含量仍高于高炉原料低于0.08%的标准[5],不可直接用于炼铁,需进行脱锡预处理。
目前,国内外锡铁分离方法主要有还原挥发 法[6−7]、氯化挥发法[8−9]和硫化挥发法[9−10]。还原挥发法是指控制一定温度和还原气氛(焙烧温度1123~1348 K,CO体积浓度40%~50%)[6−7]将锡铁矿中含锡物相定向还原成SnO,利用SnO与铁氧化物蒸汽压的差别实现锡铁分离,陈丽勇[7]研究了还原挥发法的脱锡效果,发现焙烧温度1348 K、CO含量40%及焙烧时间大于30 min时,锡挥发脱除率高达98%。张元波等[10]在CO还原SnO2机理研究中发现,975~1100 ℃温度下,CO浓度由16.25%变化为20.00%时,SnO2还原物相中Sn含量变化较大,实现物料中锡的脱除,反应气氛需精确控制[10],导致该工艺规模化应用较难实现。氯化挥发法是通过加入氯化剂,将物料中锡转变为氯化物进行挥发,该方法可有效脱除锡,但氯气(或氯化氢)化学活性较强,对设备腐蚀性大,且容易造成环境污染,应用局限性较大。与还原法类似,硫化法则是利用SnS饱和蒸汽压与物料中其他组分硫化物区别较大的特点,通过添加硫化剂使锡铁矿中锡物相硫化成SnS进行锡的挥发脱除,此前应用及研究中主要用于富锡渣及锡中矿的处理[9, 11],其优点是锡物料适应性强,硫化剂可以和SnO2的还原产物发生作用,生产工艺简单,但方法中还原剂添加过量时硬头的产生将导致锡脱除率降低,还原剂添加量需精确控制。另外,邱在军等[12]以黄铁矿为硫化剂对锡铁精矿硫化焙烧脱锡工艺进行了研究,发现控制一定焙烧气氛和焙烧温度,矿样中锡含量由 0.65%可分别降 0.22%[3]和0.42%[12],锡脱除率相对有限,焙烧后物料不能满足高炉冶炼入炉矿石原料Sn含量低于0.08%的要求。同时,硫化焙烧过程中FeS2转化不彻底容易形成FeS而造成锡铁精矿中硫含量升高[13−14],不利于精矿中铁的回收,该硫化剂对处理锡铁矿适用性受限。
高硫煤赋存量约占我国煤炭资源总量的30%以上,对其利用前须进行脱硫预处理,然高效脱硫成本较高,经济脱硫预处理只能脱除其中无机硫,对含有机硫高的煤的硫脱除效果不显著[15]。结合硫化焙烧脱锡工艺特点,研究提出高硫煤为同时为还原剂和硫化剂对锡铁精矿进行焙烧新思路,充分利用其中有机硫和无机硫矿相实现锡的高效硫化脱除,并通过烟气收尘对锡资源进行回收,同时也为高硫煤的有效利用提供一种新途径。
1 实验
1.1 实验原料
实验所用锡铁精矿来自云南个旧某矿山,化学组成见表1。表1所列为锡铁精矿中锡含量为0.56%,远大于高炉炼铁要求,实现铁矿资源有效利用需将其脱除,同时其自身具备回收价值。另表1 中“Others”主要指元素氧,主要存在于铁氧化物中。图1显示锡铁精矿中含铁物相主要为Fe3O4和Fe2O3,脉石成分主要为Ca2SiO4和SiO2,锡物相含量少,XRD谱中无法显示,有研究表明其物相形式主要为SnO2[16]。实验所用高硫煤来自山西某煤场,工业分析结果如表2所示,表2所列为高硫煤中硫含量较高为3.47%,固定碳含量相对较低为31.43%。

图1 锡铁精矿XRD 谱
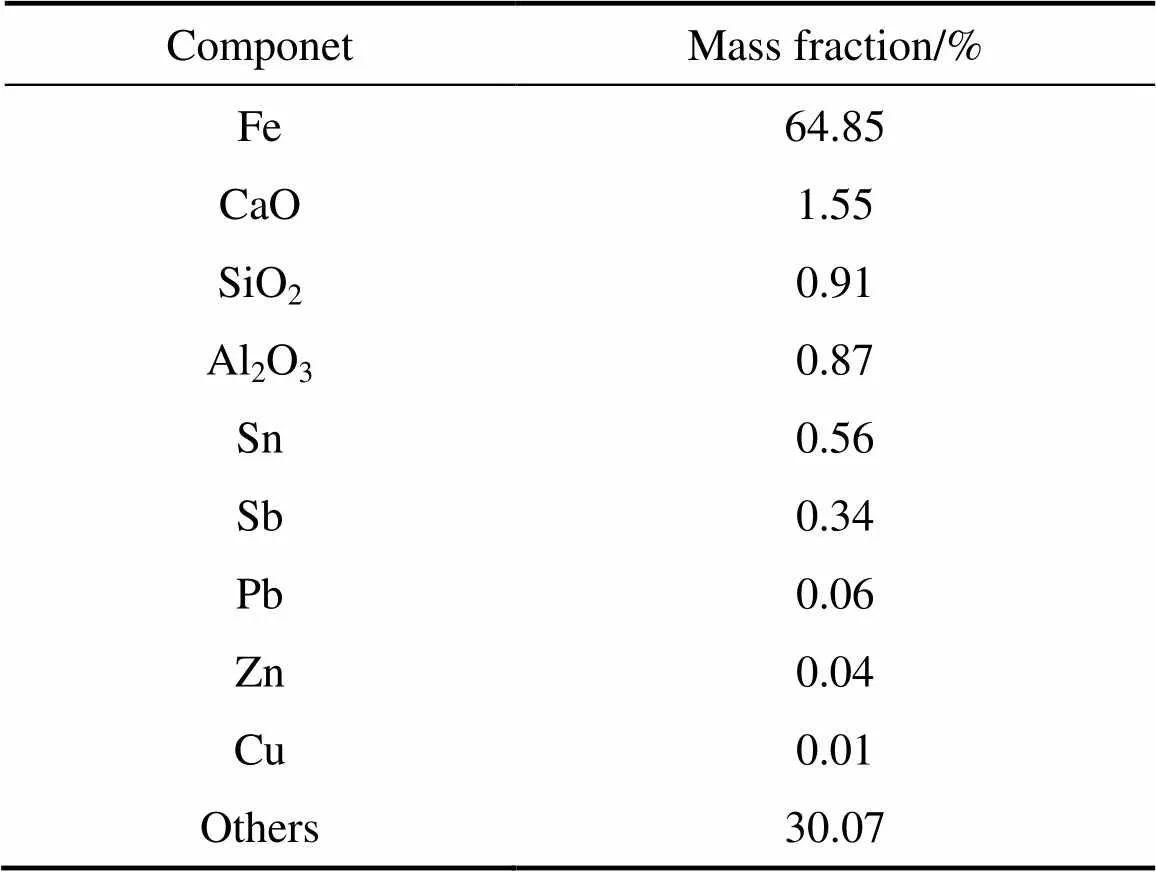
表1 锡铁精矿化学组分
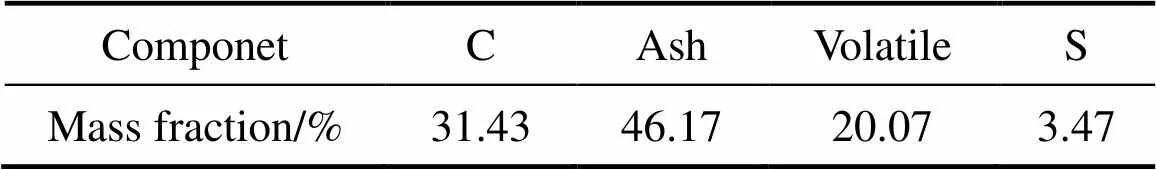
表2 高硫煤的工业分析组分
1.2 实验设备及方法
实验所用装置主要为管式电阻炉,炉膛尺寸 100 mm×1000 mm,加热元件为硅钼棒,可精确温度控制范围为1073~1873 K,控温精度±1 K,实验装置连接如图2所示。
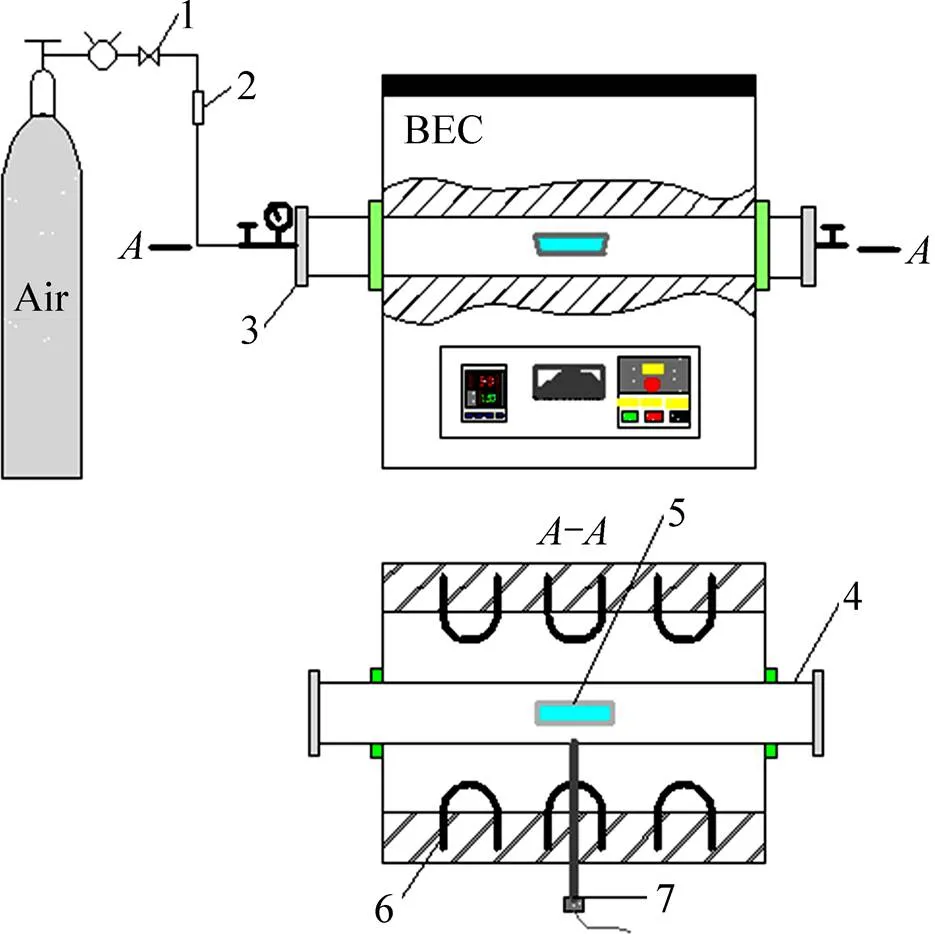
图2 实验装置图
高硫煤添加量由高硫煤(H)和锡铁精矿(T)质量比表示,研究主要探索焙烧温度、焙烧时间、高硫煤添加量及添加粒度四因素对锡铁精矿锡脱除效果的影响规律。实验方法为:锡铁精矿破碎至粒度小于74 μm 后与一定粒度高硫煤按比例混匀,之后装入长方体刚玉槽(100 mm×12 mm×9 mm)中,空气气氛下(空气流量10 mL/min)电阻炉升温至设定温度后,将刚玉槽置于炉内进行焙烧,保温一定时间,停炉降温取样分析。
研究中,锡脱除率定义如下:
=(00−11)/(00) (1)
式中:为锡脱除率;0为锡铁精矿加入质量;0为锡铁精矿中锡含量;1为焙烧后物料质量;1为焙烧后物料中锡含量。
2 高硫煤焙烧锡铁精矿脱锡机理
研究利用高硫煤对锡铁精矿进行焙烧将锡物相转变为SnS实现锡的挥发脱除。焙烧过程中,有氧条件下,高硫煤中固定碳发生布多尔反应,所产生CO起主要还原作用。CO作用下,SnO2被还原为Sn和SnO,铁物相则按照Fe2O3→Fe3O4→FeO→Fe方式被逐级还原[17−18]。与此同时,高硫煤气化所释放不同形态的硫对Sn和SnO起硫化作用。
2.1 锡物相还原机理
SnO和Sn与硫结合能力较SnO2强,硫化焙烧应在还原气氛中进行[16]。高硫煤对锡铁精矿进行焙烧时,空气环境中固定碳发生燃烧反应和布多尔反应(分别见式(2)和(3)),CO对物料还原起主要作用[19]。
C(s)+O2(g)=CO2(g) (2)
C(s)+CO2(g)=2CO(g) (3)
温度低于1313 K时,SnO不能稳定存在,或分解生成Sn和SnO2,或还原气氛下继续还原生成金属Sn,锡铁精矿中锡的还原以1313 K为界可分为以下两个阶段:
<1313 K时,
SnO2(s)+2CO(g)=Sn(l)+2CO2(g) (4)
1313 K<<1353 K,
SnO2(s)+CO(g)=SnO(s)+CO2(g) (5)
1353 K<<1473 K,
SnO2(s)+CO(g)=SnO(l)+CO2(g) (6)
2.2 锡还原物相硫化机理
高硫煤中硫以无机硫和有机硫形式存在。无机硫存在形式主要为黄铁矿硫(FeS2)、硫酸盐硫(主要是CaSO4和FeSO4等)和单质硫(S6、S7、S8等),有机硫则主要有脂肪族化合物(如醇、硫醚、二硫醚等)、芳香族化合物(如酚、硫醌、硫蒽等)和杂环硫化物(如噻吩类硫化物等)3种[20]。有氧环境中,高硫煤气化气体含硫组分主要为SO2,同时有少量COS、CS2等,H2S基本不释放。SO2主要由稳定有机硫和黄铁矿硫受热分解放出的单体硫氧化生成[13−14, 21−22],具体反应 如下:
噻吩类有机硫(热解)→S(7)
FeS2=FeS+1/S(8)
S+O2=SO2(9)
2FeS+3O2=2FeO+2SO2(10)
COS可由黄铁矿分解产生的硫与布多尔反应产物CO反应生成,亦可由黄铁矿自身与CO反应直接生成[13−14, 22−23],反应过程如下:
S+CO=COS (11)
FeS2+CO=FeS+COS (12)
CS2由高温下噻吩类有机硫热解、黄铁矿与C反应以及COS的二级反应生成,见式(12)~(14)[24]:
噻吩类有机硫(热解)→CS2(13)
2FeS2+C=CS2+2FeS (14)
2COS=CS2+CO2(15)
CO还原作用下,锡铁精矿中SnO2物相还原生成Sn和SnO[25],含硫气体SO2、COS和CS2等可将两者硫化生成SnS,实现锡的挥发脱除,具体反应如式(16)~(21),对应各反应吉布斯自由能DΘ随温度的变化见图3和4。图3和4所示为各反应吉布斯自由能均小于0,即在热力学上均可发生。
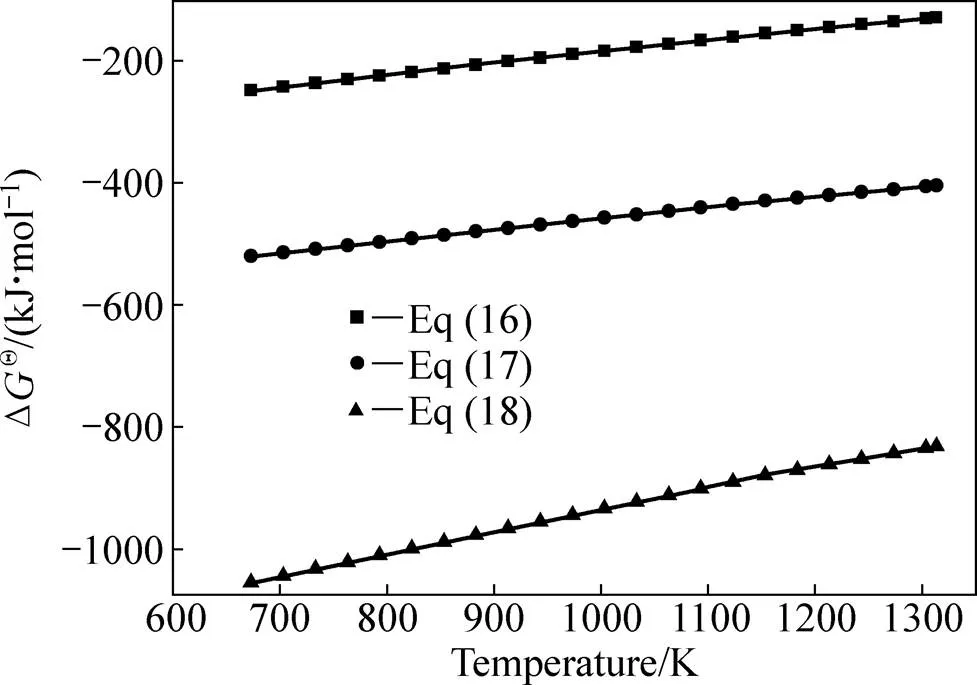
图3 反应(16)、(17)和(18)的DGΘ与温度的关系

图4 反应(19)、(20)和(21)的DGΘ与温度的关系
<1313 K:
Sn(l)+SO2(g)+2CO(g)=SnS+2CO2(g) (16)
Sn(l)+COS(g)+CO(g)+O2(g)=SnS+2CO2(g) (17)
2Sn(l)+CS2(g)+2CO(g)+2O2(g)=2SnS+3CO2(g) (18)
>1313 K:
1/3SnO+1/3SO2(g)+CO(g)=1/3SnS+CO2(g) (19)
SnO+COS(g)+2CO(g)+O2(g)=SnS+3CO2(g) (20)
2SnO+CS2(g)+2CO(g)+O2(g)=2SnS+3CO2(g) (21)
3 结果与讨论
不同实验条件下精矿锡脱除率和焙烧磁选后物料主要成分如表3和4所示。
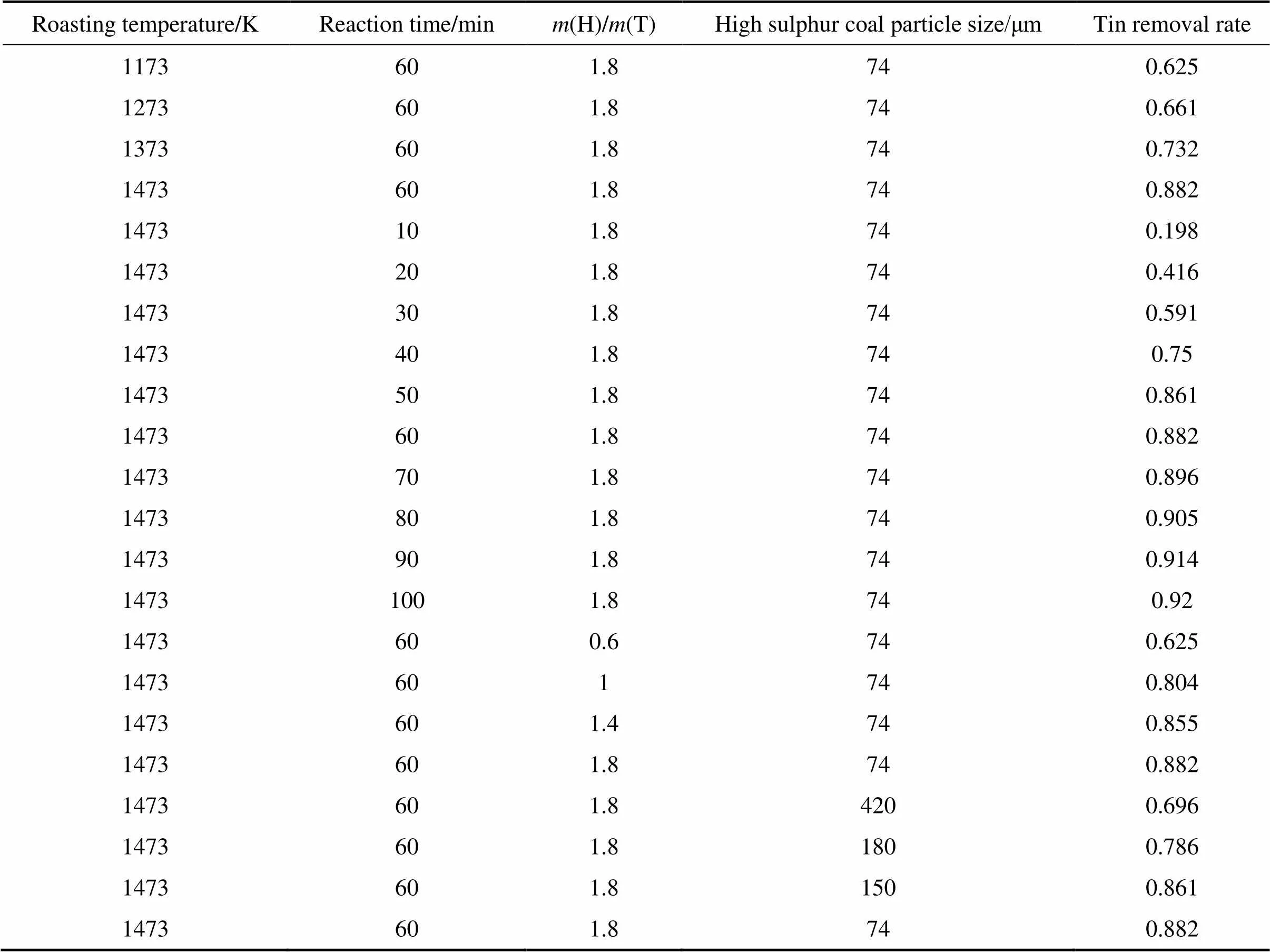
表3 不同实验条件下锡铁精矿锡脱除率

表4 焙烧磁选后物料元素组成
3.1 焙烧制度对锡铁精矿硫化焙烧脱锡效果的影响
空气流量10 mL/min、高硫煤添加量1.8及添加粒度74μm实验条件下,研究焙烧制度对锡铁精矿硫化焙烧脱锡效果的影响。焙烧温度升高,煤中黄铁矿等无机硫和噻吩硫等有机硫分解速度加快,硫化剂的生成和扩散传质速度提高,同时,锡物相(SnO2)还原活化能降低[26],反应速率常数增大,锡物相还原反应速率和硫化挥发速率加快,锡挥发脱除率随之增高。图5所示为焙烧温度从1173 K升高至1473 K时,锡脱除率由62.5%增至88.2%。图6显示焙烧时间由10 min延长至60 min时,锡脱除率由19.8%增至88.2%,焙烧时间继续延长,锡脱除率虽有所升高,但幅度较低。降低能耗并最大限度脱除锡铁精矿中锡,焙烧温度选择为1473 K,焙烧时间选择为60 min。

图5 焙烧温度对锡铁精矿锡脱除率的影响
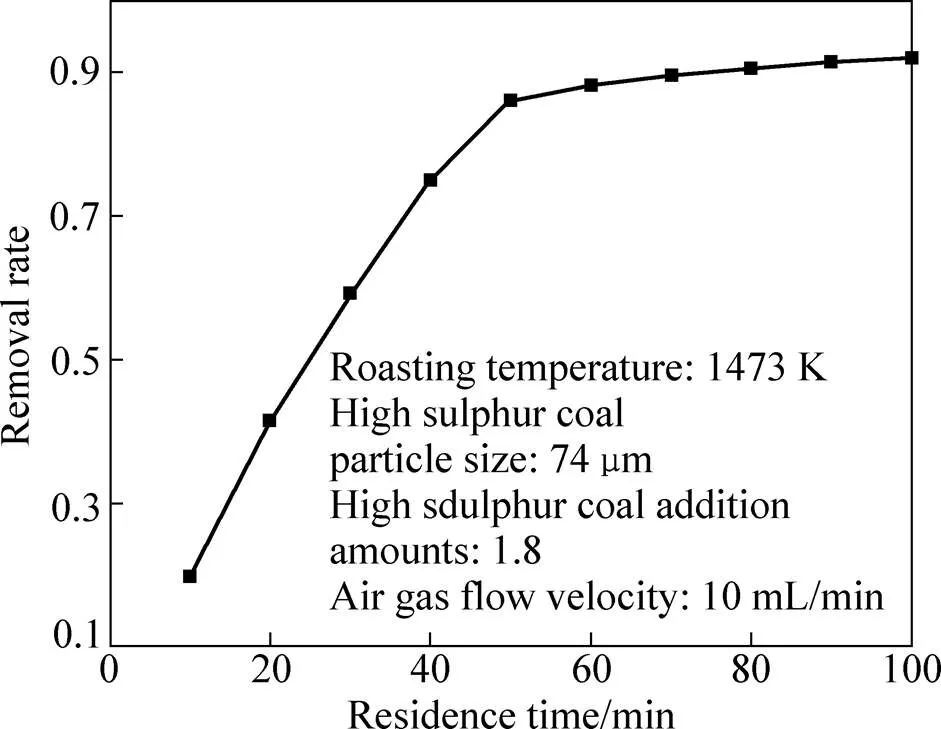
图6 保温时间对锡铁精矿锡脱除率的影响
在空气环境中,高硫煤对锡铁精矿进行硫化焙烧,气化产物SO2起主要硫化作用,总反应为
SnO2+4CO(g)+SO2(g)=SnS+4CO2(g) (22)
试样整体反应符合未反应收缩模型,过程包括外扩散、内扩散和界面反应三部分,可分为以下5个步骤[27−29]:
1) CO和SO2通过气相边界层扩散到反应物颗粒表面;
2) CO和SO2通过反应物颗粒缝隙扩散到气−固相化学反应界面;
3) CO和SO2在气−固相反应界面发生吸附,同时与锡物相发生界面化学反应,产物SnS和CO2脱附;
4) SnS和CO2通过反应物颗粒扩散到气相边界层;
5) SnS和CO2通过气相边界层扩散至外界气相。
反应速率取决于过程中最慢环节。实验中焙烧温度为1473 K、反应气体空气流速为10 mL/min,外扩散不会成为反应限速环节[30−31],反应由内扩散、界面化学反应或两者共同控制。限速环节不同,反应所对应动力学方程不同,具体如表5所示。表5中,=0/(0),02(2E0),1−/0(式中:指固体反应物密度,0指固体反应物颗粒半径,指反应速率常数,0指固体反应物颗粒表面气体浓度,E指扩散速度常数,1指界面化学反应比重权数,1指内扩散比重权数,0指固体反应物初始质量,指反应时间后固体反应物质量,指反应时间)。

表5 不同限速步骤时所对应动力学方程[28]
反应速率由表5中某一步骤控制时,对应动力学方程进行−关系作图,所得图像应趋近于直线。假设反应速率受界面化学反应控制,以为横坐标、[1−(1−)1/3]为纵坐标进行作图,图7所示为焙烧时间小于50 min时图像趋近于一条直线,此时反应速率受界面化学反应控制,50 min后,图像与直线偏离幅度较大,原因可能为后期反应物浓度下降,内扩散对反应速率的影响比重增加。假设50 min后,反应受内扩散和界面化学反应共同控制,对应动力学方程做简化处理,=1[1−(1−)1/3]−−[1−2/3−(1−)2/3]左右两边同除以1−(1−)1/3,简化得/[1−(1−)1/3]=1−1[1+ (1−)1/3−2(1−)2/3]。以/1−(1−)1/3为横坐标、1+ (1−)1/3−2(1−)2/3为纵坐标进行作图,图8显示所得图像趋近于一条直线,即50 min后反应速率由界面化学反应控制转变为界面化学反应和内扩散共同控制,其导致保温时间由50 min继续延长时锡脱除率增速减慢。

图7 保温时间和[1−(1−X)1/3]的关系

图8 t/[1−(1−X)1/3]和[1+(1−X)1/3−2(1−X)2/3]的关系
3.2 高硫煤添加量及添加粒度对锡铁精矿硫化焙烧脱锡效果影响
空气流量10 mL/min、焙烧温度1473 K和保温时间60 min实验条件下,研究高硫煤添加量及添加粒度对锡铁精矿硫化焙烧脱锡效果的影响。
图9显示高硫煤添加量由0.6增加到1.8,锡脱除率由62.5%增至88.2%。与图9中锡脱除率随高硫煤添加量(H/T)增加一直增高不同,一些研究发现黄铁矿为硫化剂时,锡脱除率随还原剂添加量增加呈先升高后下降趋势,原因为还原剂添加过量时锡铁精矿中锡、铁过度还原并结合生成硬头不利于锡的挥发脱除[3]。同时,另有研究发现,在不添加硫化剂情况下,CO为还原剂对SnO2还原,当CO在(CO+CO2)混合气体中的含量高于25%(体积分数)时,SnO2容易被还原为Sn[10],造成锡挥发脱除率下降。本研究中,高硫煤添加量增加时,系统CO分压和硫势升高,锡物相还原和硫化反应速率加快;同时,CO浓度过高虽使SnO2过还原生成Sn,然其可以通过反应(15)~(17)生成SnS而被有效脱除。研究中高硫煤的硫化作用主要通过SO2实现,其硫化锡物相的反应属气−固相反应,反应气体在固体表面被吸附时,其可使晶体表面的电子结构发生变化,可对固体的化学键产生影响,从而改变固体的化学反应性,使反应速率相对较快[32],物料中锡、铁过度还原生成硬头前即可实现大部分锡的有效脱除。提高锡脱除率,高硫煤添加量(H/T)选择为1.8。

图9 高硫煤添加量(H/T)对脱锡率的影响
针对硫组分硫化作用配煤量选择为1.8,远高于此锡铁精矿直接还原铁计算配煤量0.6(煤中碳与氧化铁中氧的摩尔比,通常稍大于1),过程中多余固定碳用以提供还原氛围,避免敞开系统中铁还原物相的再氧化。因实验所用高硫煤成本低廉,对比所回收锡资源,工艺具备经济性。
图10显示高硫煤粒度减小时锡铁精矿锡脱除率增大,原因是相同保温温度、保温时间和高硫煤添加量条件下,高硫煤粒度越小,反应物接触面积越大,锡物相的还原硫化反应速率和脱除率均增大。图10中,高硫煤粒度由420 μm减小至74 μm,锡脱除率由69.6%增至88.2%,提高锡铁精矿锡脱除效率;高硫煤添加粒度选择为74 μm时,锡铁精矿中锡含量降至0.066%,通过烟气收尘可实现精矿中锡资源的有效回收。
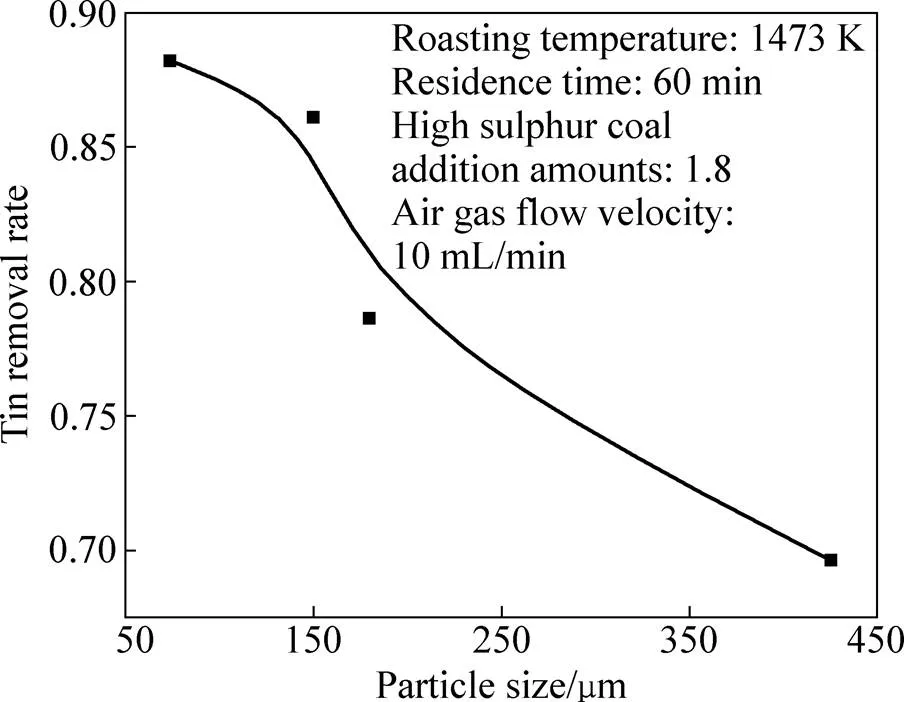
图10 高硫煤粒度对脱锡率的影响
磨矿粒度小于74 μm、磁场强度为0.3 T条件下,对焙烧后物料进行磁选。磁选后物料全元素分析如表4所示。表4显示焙烧实验中高硫煤粒度分别为150 μm和74 μm时,经磁选后物料锡含量可降至0.069%和0.058%,达到了高炉炼铁关于锡含量小于0.08%的要求。同时,磁选后物料含硫量约0.58%,炼铁工艺中需加强脱硫处理,物料铁含量最高可达88.93%,主要物相形式为金属铁(伴有少量Fe3O4,见图11),工艺可同步实现铁物相的深度预还原。

图11 焙烧磁选分离后物料XRD 谱
4 结论
1) 空气氛围下,高硫煤硫化锡铁精矿中锡主要通过布多尔反应产物CO的还原作用和气化产物SO2的硫化作用实现。
2) 在一定范围内,提高焙烧温度和延长焙烧时间有利于提高锡铁精矿中锡脱除效率。焙烧温度1473 K、高硫煤添加量1.8和添加粒度74 μm条件下,焙烧时间小于50 min时反应速率受界面化学反应控制,50 min后转为界面化学反应和内扩散共同控制。
3) 当高硫添加量由0.6增加至1.8时,锡铁精矿过度还原未造成锡脱除率下降,与传统黄铁矿硫化现象不同,原因可能是由于高硫煤的硫化作用主要通过SO2实现,其硫化锡物相反应属气−固相反应,反应速率相对较快,锡铁精矿过度还原生成硬头前即可实现大部分锡的有效脱除。
4) 在空气流量10 mL/min、焙烧温度1473 K、保温时间60 min、高硫煤粒度74 μm及添加量1.8试验条件下,锡铁精矿中锡含量可降至0.066%。磨矿粒度小于74 μm、磁场强度0.3 T条件下对焙烧后物料进行磁选,锡铁精矿中Sn含量可降至0.08%以下,达到了高炉炼铁关于锡含量的要求。
REFERENCES
[1] 崔立伟, 夏浩东, 王 聪. 中国铁矿资源现状与铁矿实物地质资料筛选[J]. 地质与勘探, 2012, 48(5): 894−905. CUI Li-wei, XIA Hao-dong, WANG Cong. Current status of iron-ore resources in China and screening of object iron-ore geological data[J]. Geology and Exploration, 2012, 48(5): 894−905.
[2] 朱庆山, 李红钟.难选铁矿流态化磁化焙烧研究进展与发展前景[J]. 化工学报, 2014, 65(7): 2437−2442.ZHU Qing-shan, LI Hong-zhong. Status quo and development prospect of magnetizing roasting via fluidized bed for low grade iron ore[J]. Journal of Chemical Industry and Engineering, 2014, 65(7): 2437−2442.
[3] 李 磊, 邱在军, 王 华, 魏永刚, 廖 斌, 桑秀丽. 锡铁矿硫化焙烧脱锡[J]. 中国有色金属学报, 2014, 24(2): 519−527.LI Lei, QIU Zai-jun, WANG Hua, WEI Yong-gang, LIAO Bin, SANG Xiu-li. Removing tin from tin-bearing iron concentrates with sulfidation roasting[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 519−527.
[4] 舒 波, 张仁杰, 廖 彬. 锡铁矿处理技术的研究进展[J]. 材料导报, 2013, 27(z2): 98−101. SHU Bo, ZHANG Ren-jie, LIAO Bin. Research progress in the treatment of tin-bearing iron ores[J]. Bin Materials Review, 2013, 27(z2): 98−101.
[5] CHEN Hong-sheng, ZHENG Zhong, SHI Wan-yuan. Investigation on the kinetics of iron ore fines reduction by CO in a micro-fluidized bed[J]. Procedia Engineering, 2015, 102: 1726−1735.
[6] 李光辉, 贾志鹏, 张元波, 姜 涛. 含锡铁精矿CO还原分离锡铁的行为研究[J]. 矿冶工程, 2012, 32(4): 83−86. LI Guang-hui, JIA Zhi-peng, ZHANG Yuan-bo, JIANG Tao. Research on separating tin and iron from tin-bearing iron concentrate by CO reduction[J]. Mining and Metallurgical Engineering, 2012, 32(4): 83−86.
[7] 陈丽勇. 含锡铁矿还原焙烧锡铁分离的基础研究[D]. 长沙: 中南大学, 2010: 8−12. CHEN Li-yong. Fundamental researches on tin separation from tin-bearing iron ores by reduction roasting[D]. Changsha: Central South University, 2010: 8−12.
[8] 李学鹏, 尹久发. 氯化挥发回收含锡尾矿中的有价金属[J]. 有色金属(冶炼部分), 2012, 9(4): 11−14. LI Xue-peng, YIN Jiu-fa. Valuable metals recovery from tin tailing with chlorination volatility process[J]. Nonferrous Metals (Extractive Metallurgy), 2012, 9(4): 11−14.
[9] 宋兴诚. 锡冶金[M]. 北京: 冶金工业出版社, 2011: 135−138. SONG Xing-cheng. Tin metallurgy[M]. Beijing: Metallurgical Industry Press, 2011: 135−138.
[10] ZHANG Yuan-bo, LIU Bing-bing, SU Zi-jian, CHEN Jun, LI Guang-hui, JIANG Tao. Volatilization behavior of SnO2reduced under different CO-CO2atmospheres at 975−1100℃[J]. International Journal of Mineral Processing, 2015, 144: 33−39.
[11] 戴永年. 含锡物料烟化过程的分析[J]. 有色金属(冶炼部分), 1965(1): 38−40. DAI Yong-nian. Tin material analysis of fuming process[J]. Nonferrous Metals (Extractive Metallurgy), 1965(1): 38−40.
[12] 邱在军, 李 磊, 王 华, 魏永刚, 廖 彬. 含锡铁精矿硫化焙烧脱锡的反应特征[J]. 过程工程学报, 2012, 12(6): 957−961. QIU Zai-jun, LI Lei, WANG Hua, WEI Yong-gang, LIAO Bin. Reaction characteristics study on the removal of tin from tinbearing iron concentrates by sulfidation roasting[J]. The Chinese Journal of Process Engineering, 2012, 12(6): 957−961.
[13] HUANG Fang, ZHANG Li-qi, YI Bao-jun, XIA Zuo-jun, ZHENG Chun-guang. Transformation pathway of excluded mineral pyrite decomposition in CO2atmosphere[J]. Fuel Processing Technology, 2015, 138: 814−824.
[14] LÜ Wei-zhi, YU Dun-xi, WU Jian-qun, ZHANG Lian, XU Ming-hou. The chemical role of CO2in pyrite thermal decomposition[J]. Proceedings of the Combustion Institute, 2015, 35: 3637−3644.
[15] 焦东伟, 胡廷学, 金会心, 王 振, 张 莹. 高硫煤脱硫技术及展望[J]. 能源与环境, 2010, 4: 55−58. JIAO Dong-wei, HU Ting-xue, JIN Hui-xin, WANG Zhen, ZHANG Ying. Development of coal desulfurization process[J]. Energy Engineering, 2010, 4: 55−58.
[16] 赖来仁, 李 艺. 矽卡岩锡矿石中锡的赋存状态与锡物相[J]. 矿产与地质, 1999, 13(2): 86−90. LAI Lai-ren, LI Yi. Ocurrence and phase of tin(Sn) contained in tin minerals of skarn[J]. Mineral Resources and Geology, 1999, 13(2): 86−90.
[17] ZHANG Yuan-bo, LI Guang-hui, JIANG Tao, GUO Yu-feng, HUANG Zhu-cheng. Reduction behavior of tin-bearing iron concentrate pellets using diverse coals as reducers[J]. International Journal of Mineral Processing, 2012, 110/111(18): 109−116.
[18] ROSMANINHOA M G, MOURAA F C C, SOUZAAL R, NOGUEIRAA R K, GOMESA G M, NASCIMENTOA J S, PEREIRAA M C, FABRISA J D, ARDISSONB J D, NAZZARROC M S, SAPAGC K, ARAUJOA M H, LAGOA R M. Investigation of iron oxide reduction by ethanol as a potential route to produce hydrogen[J]. Applied Catalysis B (Environmental), 2012, 45: 115−116.
[19] 廖 彬, 李 磊, 王 华, 胡建杭, 邱在军, 桑秀丽. 硫化焙烧锡铁矿脱锡[J]. 化工进展, 2013, 32(5): 1177−1182.LIAO Bin, LI Lei, WANG Hua, HU Jian-hang, QIU Zai-jun, SANG Xiu-li. Tin removal from tin-bearing iron ore with sulfidation roasting[J]. Chemical Industry and Engineering Progress, 2013, 32(5): 1177−1182.
[20] 王之正, 王利斌, 裴贤丰, 王 岩, 白效言. 高硫煤热解脱硫技术研究现状[J]. 洁净煤技术, 2014, 20(2): 76−79.WANG Zhi-zheng, WANG Li-bin, PEI Xian-feng, WANG Yan, BAI Xiao-yan. Desulfurization of high-sulfur coal through pyrolysis[J]. Clean Coal Technology, 2014, 20(2): 76−79.
[21] 张 成, 李婷婷, 夏 季, 陈 刚. 高硫煤不同气氛温和热解过程中含硫组分释放规律的实验研究[J]. 中国电机工程学报, 2011, 31(14): 24−31.ZHANG Cheng, LI Ting-ting, XIA Ji, CHEN Gang. Experimental research on the releasing characteristics of sulfur-containing gases in high-sulfur coal under different atmospheres during mild thermal upgrading[J]. Proceedings of the Chinese Society for Electrical Engineering, 2011, 31(14): 24−31.
[22] 李世光. 煤热解和煤与生物质共热解过程中硫的变迁[D]. 大连: 大连理工大学, 2006: 23−77. LI Shi-guang. Desulfurization of coal during pyrolysis and copyrolysis with biornass[D]. Dalian: Dalian University of Technology, 2006: 23−77.
[23] 赵丽红, 郭慧卿, 马青兰. 煤热解过程中气态产物分布的研究[J]. 煤炭转化, 2007, 30(1): 5−9.ZHAO Li-hong, GUO Hui-qing, MA Qing-lan. Study on gaseous products distributions during coal pyrolysis[J]. Coal Conversion, 2007, 30(1): 5−9.
[24] 段玉亲. 煤中形态硫在热解过程中的转化和迁移规律[D]. 太原: 太原理工大学, 2010: 6−14. DUAN Yu-qin. Form sulfur transformation during coal pyrolysis at various gas atmospheres[D]. Taiyuan: Taiyuan University of Technology, 2010: 6−14.
[25] 陶东平, 杨显万. 氧化亚锡歧化还原动力学和二氧化锡还原机理[J]. 中国有色金属学报, 1998, 8(1): 126−130. TAO Dong-ping, YANG Xian-wan. Kinetics of disproportionation and reduction of stannous oxide and mechanism of reduction of stannic oxide[J]. The Chinese Journal of Nonferrous Metals, 1998, 8(1): 126−130.
[26] LIU Shui-shi, GUO Yu-feng, QIU Guan-zhou, JIANG Tao, CHEN Feng. Solid-state reduction kinetics and mechanism of pre-oxidized vanadium titanium magnetite concentrate[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(10): 3372−3377.
[27] DANG J, ZHANG G H, CHOU K C. Kinetics and mechanism of hydrogen reduction of ilmenite powders[J]. Journal of Alloys and Compounds, 2015, 619: 443−451.
[28] MILSHTEIN J D, GERGEL D R, BASU S N, PAL U B GOPALAN S. Mixed ionic electronic conducting powder bed for grid level energy storage and release: A study of tungsten oxide reduction kinetics[J]. International Journal of Hydrogen Energy, 2015, 40(9): 3624−3632.
[29] 陶东平. 气体还原二氧化锡的非等温过程动力学[J]. 化工冶金, 1988, 9(4): 86−92. TAO Dong-ping. Non-isothermal process kinetics of the gaseous reduction of tin dioxide[J]. Engineering Chemistry & Metallurgy, 1988, 9(4): 86−92.
[30] GUO Da-bin, HU Mian, PU Cheng-xi, XIAO Bo, HU Zhi-quan, LIU Shi-ming, WANG Xun, ZHU Xiao-lei. Kinetics and mechanisms of direct reduction of iron ore-biomass composite pellets with hydrogen gas[J]. International Journal of Hydrogen Energy, 2015, 40(14): 4733−4740.
[31] ZHANG Yuan-bo, SU Zi-jian, ZHOU You-lian, LI Guang-hui, JIANG tao. Reduction kinetics of SnO2and ZnO in the tin, zinc-bearing iron ore pellet under a 20%CO-80%CO atmosphere[J]. International Journal of Mineral Processing, 2013, 124: 15−19.
[32] 华一新. 冶金过程动力学导论[M]. 北京: 冶金工业出版社, 2004: 313−314. HUA Yi-xin. Metallurgical process kinetics introduction[M]. Beijing: Metallurgical Industry Press, 2004: 313−314.
Tin removal from tin-bearing iron concentrates through reduction-sulfidation roasting using high sulfur coal
FENG Xin-yang, LI Lei, YU Yong, SANG Xiu-li
(Faculty of Metallurgical and Energy Engineering, State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming University of Science and Technology, Kunming 650093, China)
Through the reduction-sulfidation roasting process using high sulfur coal, tin can be removed efficiently from tin-bearing iron concentrates. According to thermodynamics and kinetics analysis, the mechanism and process of tin-bearing iron concentrates reduction-sulfidation roasting were studied. The results show that, under air atmosphere, the tin reduction-sulfidation is realized mainly through CO and SO2, which are respectively generated from the Boudouard reaction and the high sulfur coal gasification. Being different from the phenomena using pyrite as curing agent, deep reduction of tin-bearing concentrates does not cause tin removal rate decrease with the increase of high sulfur coal addition. The reason may be that curing rate of tin phases by the SO2is higher, and the formation of iron-tin alloy decreases. Tin content of the concentrates decreases to 0.066% under the conditions of air flow rate of 10 mL/min, roasting temperature of 1473 K, reaction time of 60 min, high sulfur coal addition amount of 1.8 (mass ration of high sulfur coal to tin-bearing iron concentrates) and particle size of 74 μm. It is further reduced to 0.058% after magnetic separation, which can meet the standard of BF iron making, requiring tin content in iron ores less than 0.08%. The work may provide a new approach for the clean use of high sulfur coal.
high sulfur coal; tin-bearing iron concentrates; reduction-sulfidation roasting; tin removal; kinetics
Project(51304092) supported by National Natural Science Fund for Distinguished Young Scholars
2015-06-29; Accepted date: 2016-01-20
LI Lei; Tel: +86-13987619187; E-mail: tianxiametal1008@163.com
1004-0609(2016)-09-1990-09
TF046
A
国家自然科学青年基金资助项目(51304092)
2015-06-29;
2016-01-20
李 磊,副教授,博士;电话:13987619187;E-mail:tianxiametal1008@163.com
(编辑 李艳红)
