新四联根除幽门螺旋杆菌的临床对比研究
2016-10-21惠增骞
顾 勇,杨 艳,王 兰,李 娜,惠增骞,段 炜
新四联根除幽门螺旋杆菌的临床对比研究
顾勇1,杨艳2,王兰1,李娜1,惠增骞1,段炜1
目的比较3种不同用药方法治疗幽门螺旋杆菌感染(helicobacter pylori ,Hp)的临床效果及其不良反应发生情况。方法选取420例Hp阳性患者,随机分成3组。A组标准四联组(埃索美拉唑+胶体果胶铋+阿莫西林+克拉霉素),B组新四联组(埃索美拉唑+胶体果胶铋+阿莫西林+环丙沙星),A、B两组用药疗程14d。C组序贯治疗组(埃索美拉唑+ 阿莫西林治疗5 d,随后埃索美拉唑+环丙沙星+替硝唑再治疗5 d)。比较3组患者Hp根除率,随访3、6个月的Hp再感染率及不良反应发生率。结果B组、C组Hp根除率分别为92.9%、95.7%,优于A组的85.0%(P<0.05),随访3个月A、B、C组再感染率分别为10.1%、6.2%、7.5%,3组比较差异无统计学意义。6个月A组Hp再感染率为26.9%,显著高于B、C两组的13.8%、11.9%(P<0.05)。不良反应发生率组间比较差异无统计学意义。结论以环丙沙星为基础的新四联及10d序贯疗法高效、复发率低、安全、患者依从性好,可推荐作为抗Hp治疗的一线标准治疗方案。
幽门螺旋杆菌;标准四联疗法;新四联疗法;序贯疗法
幽门螺旋杆菌(helicobacter pylori,Hp)能在强胃酸环境下持续生存。全世界约有一半以上的人群携有Hp。每年大约有74万人死于胃癌,权威研究证实,Hp感染是胃癌的主要触发因素,是一个重要的危险致癌病理因素[1,2]。另外,Hp不仅被公认与慢性胃炎、消化性溃疡、低度胃恶性黏膜相关淋巴组织淋巴瘤,以及早期胃癌术后等相关,近年来研究也发现,其在缺血性心脑血管疾病、脑出血、糖尿病、特发性血小板减少性紫癜、贝赫切特综合征、肝硬化及相关并发症、肝癌、宫颈癌等多种疾病的进展和转归中发挥一定的作用[3,4]。当前的根除治疗仍采用胃酸抑制药联合抗生素较为复杂的疗法。近年来Hp对克拉霉素和甲硝唑的耐药率明显增加,以此为基础的标准四联、三联疗法根除率越来越低。有多项研究显示,以喹诺酮类药物为基础的根除方案能够明显提高Hp根除率,目前逐渐被广泛应用于一线治疗[5,6]。本研究旨在探讨和评估标准四联、以环丙沙星为基础的新四联及10d序贯疗法对清除初治患者Hp感染的疗效。
1 对象与方法
1.1对象选择420例2012-01至2014-10门诊及住院的Hp阳性患者作为本课题研究对象。病例均为确诊的Hp相关性胃炎、消化性溃疡。经C13尿素呼气试验及胃黏膜组织快速尿素酶试验两项均为阳性,方可证实患者具有Hp感染。所有病例均为初次行Hp根除治疗。排除标准:(1)严重的心脑肾肺血管疾病;(2)意识障碍或其他严重的精神、神经系统疾病;(3)慢性肝肾功能不全;(4)治疗开始前6周曾口服质子泵抑制药、H2受体拮抗药、铋药、抗生素、肠道菌群调节药等能干预Hp根除疗效的药物;(5)恶性溃疡或疑似肿瘤并需进一步证实者;(6)曾有胃部手术史;(7)出现上消化道出血、穿孔、幽门梗阻等严重并发症;(8)妊娠期及哺乳期女性;(9)对口服的药物成分过敏以及不愿参加本研究试验的患者。所有患者均签署知情同意书。按随机数字表法分为3组,每组140例,采用不同药物、不同方法进行抗Hp治疗。A组:男82例,女58例;年龄21~68岁,平均(43.6±12.4)岁。B组:男76例,女64例;年龄18~70岁,平均(46.2±11.6)岁。C组:男77例,女63例;年龄20~66岁,平均(40.8±13.7)岁。3组患者在性别、年龄、身高、体重、病情、病程等一般资料无统计学差异(P>0.05,表1)。
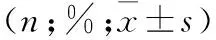
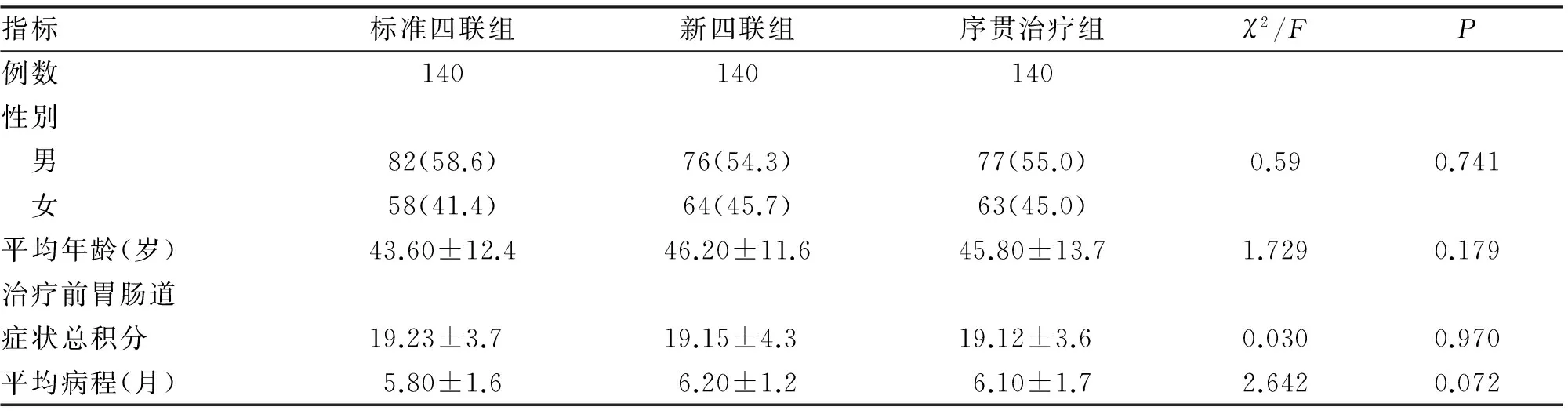
指标标准四联组新四联组序贯治疗组χ2/FP例数140140140性别 男82(58.6)76(54.3)77(55.0)0.590.741 女58(41.4)64(45.7)63(45.0)平均年龄(岁)43.60±12.446.20±11.645.80±13.71.7290.179治疗前胃肠道症状总积分19.23±3.719.15±4.319.12±3.60.0300.970平均病程(月)5.80±1.66.20±1.26.10±1.72.6420.072
1.2方法
1.2.1用药方案A组采用标准四联法:埃索美拉唑20 mg,胶体果胶铋200 mg,阿莫西林1000 mg,克拉霉素500 mg,2次/d。B组采用新四联法:埃索美拉唑20 mg+胶体果胶铋200 mg+阿莫西林1000 mg+环丙沙星250 mg,2次/d;A、B组用药疗程14 d。C组采用序贯治疗法:前5 d(埃索美拉唑20 mg+阿莫西林1000 mg),2次/d;后5 d埃索美拉唑20 mg+环丙沙星250 mg+替硝唑500 mg,2次/d。告知各组患者及其亲属用药的具体方法、剂量以及药物可能出现的不良反应,以充分提高患者依从性,使治疗顺利进行。治疗期间需严格禁用其他药物。
1.2.2疗效评价(1)用药规范疗程结束后28 d,行C13尿素呼气试验、胃组织快速尿素酶试验检测Hp,两项均为阴性方可判定Hp根除,并统计对比各组患者Hp根除率;(2)通过与患者或家属电话、短信、微信、调查样表等多种形式,详细记录患者服药期间能明显感受到的不适,最后进行综合分析各组不良反应发生情况;(3)治疗结束后随访6个月,3、6个月节点时行C13尿素呼气试验检测各组患者Hp,统计再次感染率。
1.2.3不良反应对3组患者在服药期间出现腹痛腹胀、恶心呕吐、头晕乏力、腹泻纳差、便秘口苦等不良反应发生情况进行统计,计算不良反应发生率。
1.3统计学处理采用SPSS17.0统计软件进行数据处理,多组之间率的比较采用χ2检验,进一步比较两个总体率采用χ2分割法。以P<0.05为差异有统计学意义。
2 结 果
2.1HP根除率及再感染率比较各组Hp根除率及再感染率比较见表2。420例均完成了治疗,达到随访要求。A组Hp根除率为85.0%,与B、C两组的92.9%、95.7%比较,差异有统计学意义(P<0.05) ,B、C两组比较差异无统计学意义。结合随访资料,A、B、C组3个月时检测Hp,再感染率分别为10.1%、6.2%、7.5%,3组比较差异无统计学意义 (P>0.05)。6个月时比较A组Hp再感染率总计为26.9%,显著高于B、C两组的13.8%和11.9%(P<0.05)。B、C两组比较差异无统计学意义。

表2 3组HP根除率及再感染率比较 (n=140;%)
注:标准四联组与新四联组与比较,①P<0.05;与序贯治疗组比较,②P<0.05
2.2不良反应各组分别在服药期间以相关不适为主要或较明显症状时做详细统计。A、B、C各组不良反应总发生率分别为15.8%、17.1%、22.2%,3组差异无统计学意义(P>0.05,表3)。
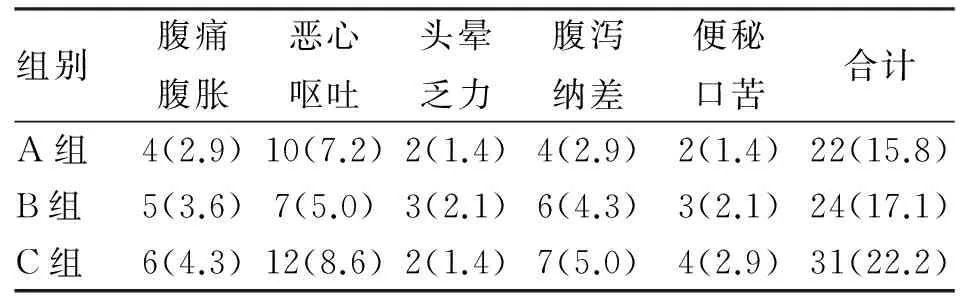
表3 3组不良反应比较例 (n=14;%)
3 讨 论
胃癌前状态是指胃黏膜萎缩和肠上皮化生。Hp相关性胃炎是胃癌发生的重要危险因素。1994年,Hp就被国际癌症研究机构(IARC)归类为Ⅰ类致癌原[7]。根除Hp后胃黏膜急慢性炎性反应可以快速或逐渐得到缓解,Hp相关的各类间接、直接分子事件也可逐渐逆转或消失,继之抑制甚至终止胃恶性病变发生和进展的级联反应[8]。多项研究表明根除Hp后,胃癌总体发病率降低[9]。
随着不同国家、不同地区Hp耐药率的明显升高,标准三联、四联根除疗法面临严峻挑战。在常用多种抗生素耐药的情况下,拓展提高Hp根除率的新路径、新方法已成为当今Hp相关研究的一个热点和焦点。已有研究证实克拉霉素耐药的幽门螺杆菌与23S核糖体RNA(rRNA)基因的点突变相关。来自韩国的研究小组通过聚合酶链反应对检出克拉霉素耐药变异的Hp感染患者行特定治疗方案根除率明显提高,显示基因检测或可为个体化根除Hp治疗提供基础和指导[10]。Rhode Island大学近期努力突破应用免疫信息方法鉴别HPHLAⅡ类抗原决定簇的人体免疫反应,这是首次涉及对Hp病原体的人类免疫反应的相关研究,结果显示幽门螺杆菌疫苗的使用指日可待[11]。新加坡癌症科学研究所科学家发现,胃细胞经由RUNX3释放 IL23A蛋白,可防御Hp感染以抑制胃癌的发生。这一发现为寻找开发防治胃癌的新靶标提供了可能性[2]。在我国目前针对Hp的治疗研究仍多为药物。2009年,全国进行了Hp对目前共识广泛使用的几种抗生素耐药率的多中心研究调查,结果显示对克拉霉素、甲硝唑的耐药率明显升高,尤其是甲硝唑耐药率高达70%、克拉霉素耐药率也达23%。经过两个疗程规范抗Hp治疗没有得到根除的患者,多数考虑对甲硝唑和克拉霉素双重耐药。
有研究指出,克拉霉素耐药几乎可降低所有抗Hp治疗方案的疗效,甲硝唑耐药则仅影响序贯疗法疗效[12]。本研究考虑采用新型抗生素组合,选择环丙沙星为基础用药,替硝唑更换甲硝唑。结果显示,环丙沙星为基础的新四联和序贯疗法Hp根除率分别为92.9%、95.7%,明显高于标准四联法的85.0%。B、C组两者虽然比较无明显差异,但C组根除患者所占比例要高于B组。随访3组统计Hp再感染率,6个月时A组总计为26.9%,显著高于B、C两组的13.8%、11.9%。组间比较不良反应或并发症发生率则无显著差异。笔者认为,以环丙沙星为基础的新四联及10 d序贯疗法,疗效均优于标准四联疗法且具有复发率低、安全、患者依从性好等特点,推荐作为抗Hp治疗的一线标准治疗方案。
喹诺酮类药可人工合成,易得价廉,已为抗感染广泛应用。其作用机制是干扰细菌细胞的DNA复制,当细菌出现耐药时,往往出现耐药靶位点突变,常在细菌染色体编码的DNA回旋酶和拓扑异构酶Ⅳ的基因突变[13]。环丙沙星主要与编码拓扑异构酶Ⅳ的ParC靶位结合。KanelladopoulouK研究认为环丙沙星与β-内酰胺类药(阿莫西林)联用对多重耐药的铜绿假单胞菌的分离菌株有协同作用[14],因此以环丙沙星为基础的新四联及序贯疗法根除Hp疗效好可能与此有关。序贯疗法中前5 d采用的阿莫西林不仅本身能够杀灭幽门螺杆菌,而且还能够减少患者的细菌负荷量,从而增加细菌对后5 d采用的环丙沙星的敏感性,使序贯疗法根治率明显提高。序贯疗法的具体作用机制还有待进一步研究。
综上所述,本研究发现,对根除HP方案的选择必须考虑抗生素过敏与敏感、耐药等多种因素,视不同患者不同病情进行个体化治疗。本项目组拟依据方案选择,继续深入对不同治疗方法的耐药性做验证试验,以确保疗效佳、不良反应低、效价比高等充分治疗目标的实现和发展,为临床医师提供更多选择的治疗方案。
[1]Strugatsky D,McNulty R,Munson K,etal.Structure of the proton-gated urea channel from the gastric pathogen Helicobacter pylori[J]. Nature ,2013,493(7431):255-258.
[2]Fukamachi H, Mimata A,Tanaka I,etal. In vitro differentiation of Runx3-/- p53-/- gastric epithelial cells into intestinal type cells[J].Cancer Sci, 2008, 99(4):671-676.
[3]Martinde Argila C, Boixeda D,Canton R,etal.High seroprevalence of Helicobacterpylori infection in coronary heart disease[J].Lancet,1995, 346(8970):310.
[4]Gasbarrini A,Franceschi F,Tartaglione R,etal.Regression of autoimmune thrombocytopenia after eradication of Helicobacter pylori[J].Lancet,1998 ,352(9131):878.
[5]Hirata Y,Ohmae T,Yanai A,etal.Sitafloxacin resistance in Helicobacter pylori isolates and sitafloxacin-based triple therapy as a third-line regimen in Japan[J].Int J Antimicrob Agents ,2012 ,39(4):352-355.
[6]Tay CY,Windsor HM,Thirriot F,etal. Helicobacter pylori eradication in Western Australia using novel quadruple therapy combinations[J]. Aliment PharmacolTher, 2012,36(11-12):1076-1083.
[7]IARC. schistosomes, liver flukes and Helicobacter pylori. IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Lyon, 7-14 June 1994 [J] . IARC MonogrEvalCarcinog Risks Hum,1994,61:1-241.
[8]Kokkola A, Sipponen P, Rautelin H,etal. The effect of Helicobacter pylori eradication on the natural course ofatrophic gastritis with dysplasia[J]. Alimentary Pharmacology and Therapeutics,2002,16:515-520.
[9]Venerito M,Malfertheiner P. Preneoplastic Conditions in the Stomach: Always a Point of No Return[J].Dig Dis,2015,33(1):5-10.
[10]Lee HJ,Kim JI,Cheung DY,etal.Eradication of Helicobacter pylori according to 23S ribosomal RNA point mutations associated with clarithromycin resistance[J]. J Infect Dis, 2013 ,208(7):1123-1130.
[11]Zhang S,DesrosiersJ,Aponte-Pieras JR,etal.Human immune responses to H. pylori HLA Class II epitopes identified by immunoinformatic methods[J].PLoS One,2014,9(4):e94974.
[12]Liou JM, Chen CC,Chen MJ,etal.Sequential versus triple therapy for the first-line treatment of Helicobacter pylori: a multicentre, open-label, randomised trial[J]. Lancet, 2013, 381(9862):205-213.
[13]Bago P1, Vcev A, Tomic M,etal. High eradication rate of H. pylori with moxifloxacin-based treatment: a randomized controlled trial [J]. Wien Klin Wochenschr,2007,119(11-12):372-378.
[14]Kwon AS, Park GC, Ryu SY,etal. Higher biofilm formation in multidrug-resistant clinical isolates of Staphylococcus aureus. [J]. Int J Antimicrob Agents, 2008, 32(1):33- 39.
(2015-11-11收稿2016-01-28修回)
(责任编辑张楠)
Clinical evaluation of new quadruplet therapy forHelicobacterpylorieradication
GU Yong1, YANG Yan2, WANG Lan1, LI Na1, XI Zengqian1, and DUAN Wei1.
1.Digestive System Department,Shaanxi Provincial Crops Hospital of Chinese People’s Armed Police Force, Xi’an Shaanxi 710054, China.2.Xijing Hospital of Digestive Diseases,Fourth Military Medical University,Xi’an,710032,China
ObjectiveTo compare the clinical efficacy and adverse events of three different therapies forHelicobacterpylori(H. pylori) eradication. MethodsFour hundred and twenty H. pylori positive patients were randomly assigned into three groups in this open-label, prospective, controlled study. Group A patients received 14-day standard quadruplet therapy (esomeprazole plus colloidal bismuth pectin, amoxicillin and clarithromycin). Group B received 14-day new quadruplet therapy (esomeprazole plus colloidal bismuth pectin, amoxicillin and ring ciprofloxacin). Group C received 10-day sequential therapy (esomeprazole plus amoxicillin for 5 days, followed by esomeprazole plus ciprofloxacin and tinidazole for 5 days). H. pylori eradication rate, reinfection rates and adverse events were assessed at three months and six months after treatment. ResultsH. pylori eradication rates in group B, group C were significantly higher than in the group A (92.9%, 95.7%vs85.0%,P<0.05). H. pylori reinfection rates were 10.1%, 6.2%, 7.5%, respectively, with no significant difference between the three groups,at three months after treatment. Six months after treatment, H. pylori reinfection rate in group A was 26.9%, which was significantly higher than in groups B, and C, with a 13.8% and 11.9%, respectively (P<0.05). The incidence rate of adverse events between the three groups was not significantly different. ConclusionsCiprofloxacin-based new quadruple therapy and 10-day sequential therapy are both efficient and safe, with a low reinfection rate and high patient compliance, and can be recommended as first-line anti-H. pylori therapy.
Helicobacterpylori;standard quadruplet therapy;new quadruplet therapy;sequential therapy
顾勇,博士,副主任医师。
1.710054西安,武警陕西总队医院消化内科;2.710032西安,第四军医大学西京消化病医院四科
杨艳,E-mail: yangygy@fmmu.edu.cn
R573
