OR-SON催化Fenton法深度处理工业废水研究
2016-10-20刘灵婕常臻王芬于雷
□文/刘灵婕 常臻 王芬 于雷
OR-SON催化Fenton法深度处理工业废水研究
□文/刘灵婕 常臻 王芬 于雷
采用OR-SON为催化剂,与H2O2形成分非均相Fenton试剂对天津某化工工业园区的综合工业废水进行深度处理试验。研究了反应时间、FeSO4·7H2O投加量对传统Fenton氧化处理效果影响;考察了pH、反应时间、催化剂用量、H2O2浓度对ORSON催化Fenton氧化能力的影响。结果表明:OR-SON催化剂具有强化H2O2氧化的作用,能够明显提高反应体系的反应速率和COD去除率,同时OR-SON催化Fenton体系的硫酸亚铁需要量仅为传统Fenton法投加量的1/10,该技术可大幅度减少铁泥的产生量;试验还发现该催化剂可在一定条件下重复多次使用。
深度处理;工业废水;催化氧化;OR-SON;非均相Fenton
Fenton氧化技术是一种常见的高级氧化技术,具有反应速度快、处理设备简单、成本低等优点[1]。但传统Fenton氧化法也有诸多不足,如铁离子的使用会使出水色度较高且反应过程中会产生大量铁泥,由此加大了处理成本[2]。由于上述诸多缺点,研究人员将目光锁定在对Fenton法的改进上,这其中非均相催化Fenton法已经成为人们研究的热点。
非均相Fenton法是将铁离子固定在合适的载体上或者以含铁的固体物质作为催化剂的多相Fenton体系,与均相Fenton相比,其具有催化剂易分离、回收,能循环利用等优点[3~4]。
近年来,诸多学者致力于非均相催化剂的制备以及催化效率提高的研究中。高真等[5]以Si-FeOOH作为非均相催化剂,利用催化Fenton法降解活性艳红MX-5B取得了较好的效果。窦晓文等[6]采用针铁矿作为非均相催化剂利用Fenton氧化法降解橙黄G,结果表明在pH为3,H2O2浓度为30 mmol/L,针铁矿用量1.0 g/L时,橙黄G降解率为99.6%。郭茂峰等[7]将铜铁复合层柱蒙脱石催化剂用于Fenton处理含酚废水,在催化剂浓度1 g/L,pH在3~9范围内,苯酚去除率均有较大提高。韦朝海等[8]还通过人造沸石固定Fenton反应中的高价铁复合物进行非均相光Fenton反应,催化降解硝基苯,其性能远高于普通Fe2+光催化性能。梁晓亮等[9]研究了天然钛钒磁铁矿非均相Fenton法降解酸性橙II的性能,结果表明天然钛钒磁铁矿催化降解酸性橙II能力明显强于人工合成的单相磁铁矿。
不难发现,研究人员仍然将精力放在寻找铁矿石或者负载铁的非均相催化剂上,虽然这种非均相Fenton法能在一定程度上解决均相Fenton法的不足,但其也存在催化效率不高、物理强度较差易破碎、难以重复利用、催化剂溶出铁等问题,这使得非均相催化Fenton的应用受到限制[5]。本研究根据非均相催化Fenton法机理,以日本三菱瓦斯化学株式会社生产的OR-SON为非均相催化剂,催化H2O2深度处理工业废水中的难降解有机物。从催化机理、催化剂性质等方面对OR-SON进行了研究并研究了不同条件下Fenton氧化的处理效果,得出了适于其反应的条件。
1 材料与方法
1.1原水水质
试验原水为天津某化工园区综合工业废水处理厂生化工艺后的二沉池出水,该废水的pH为7.5~8,COD和BOD5分别为100~120 mg/L和15~20 mg/L,NH3-N为15~20 mg/L,NO3--N为6~10 mg/L。
1.2试剂与仪器
试验所用药品均为分析纯。FeSO4·7H2O(天津市江天化工有限公司),H2O2(天津市风船化学试剂科技有限公司)质量分数为30%;OR-SON催化剂混合液(日本三菱瓦斯化学株式会社提供的样品)。
仪器:PT-10型pH计,北京市赛多利斯仪器系统有限公司;PB-700型六联搅拌器,美国PHIPPS&BIRD公司。
1.3试验方法
移取1 000 mL水样于1 L的烧杯中,用(1+1)硫酸调节pH至设定值,然后加入一定量的FeSO4·7H2O和OR-SON催化剂混合液,置于六联搅拌机上,再加入一定量H2O2溶液,计时反应。反应完成后,静置沉淀30 min后取上清液用10%NaOH调节pH至碱性,静置沉淀后将上清液通过真空抽滤机抽滤(0.45 μm滤膜),取滤后液进行水质分析。
2 结果与讨论
2.1Fe2+投加量对传统Fenton处理效果的影响
在初始pH为3,H2O2投加量50 mg/L,反应时间2 h的条件下,考察Fe2+投加量对Fenton氧化处理效果的影响,结果见图1。

图1 Fe2+投加量对传统Fenton处理效果的影响
由图1可知,FeSO4·7H2O投加量随着Fe2+/H2O2(摩尔比,本文以后提到该数值均指摩尔比)的增加而不断增加,出水COD先下降再上升,其中Fe2+/H2O2为2∶1时对COD的去除效果最好,此时出水COD为71 mg/L。分析原因是:当Fe2+浓度过高时,Fe2+会消耗已产生的·OH;而当Fe2+浓度过低时,体系产生的·OH速率较慢且会影响Fenton体系链式反应的延续,从而影响Fenton体系的氧化能力,因此,确定适宜的FeSO4·7H2O投加量为Fe2+/H2O2为2∶1。
2.2反应时间对传统Fenton处理效果的影响
在初始pH为3,H2O2投加量100 mg/L,Fe2+/H2O2为2∶1的条件下,考察不同反应时间对处理效果的影响,结果见图2。

图2 反应时间对传统Fenton处理效果的影响
由图2可知,Fenton氧化的起始反应速度较快,在0.5 h左右大部分COD得到去除,但随着反应时间的延长出水COD不断降低,在反应时间为2 h时COD的去除率达到最大,此时出水COD为55.4 mg/L,因此对于传统Fenton氧化反应时间选择为2 h。
2.3OR-SON催化剂吸附作用对处理效果的影响
2.3.1OR-SON投加量对吸附效果的影响
在初始pH为3,反应时间1 h的条件下,考察不同OR-SON催化剂混合液投加量对吸附效果的影响,结果见图3。

图3 OR-SON投加量对吸附效果的影响
对于非均相Fenton反应的机理何莼等[10]认为:有机物和H2O2首先扩散到催化剂表面的活性中心被吸附,然后H2O2分子通过Fenton反应产生羟基自由基并与有机物发生氧化降解反应,最后降解产生物从催化剂表面扩散到溶液中。由图3可知,OR-SON催化剂吸附效果明显,在初始COD为107 mg/L的情况下,随着OR-SON投加量的增加COD去除率不断提高,但超过一定量后处理效果趋于稳定。在投加量分别为3 mL/L和5 mL/L时出水COD可到达到51.8 mg/L和45.8 mg/L,COD去除率为51.6%和57.2%,因此对于吸附反应而言OR-SON投加量可选择3 mL/L。
2.3.2pH对OR-SON吸附作用的影响
在OR-SON投加量3 mL/L,反应时间1 h,考察不同pH值对OR-SON吸附作用的影响,结果见图4。

图4 pH对OR-SON吸附作用的影响
由图4可知,在初始COD为110 mg/L的情况下,当初始pH为3时,OR-SON吸附作用明显,出水COD为56.3 mg/L,去除率为48.8%。但随着pH值逐渐趋于中性,出水COD明显增大,其值为68 mg/L;当pH为9时,OR-SON的吸附作用急剧减弱,出水COD急剧增大,其值为84.6 mg/L。因此可以看出,pH对OR-SON的吸附作用影响明显,在酸性条件下其吸附作用得以发挥,因此选择pH为3作为反应条件。
2.3.3反应时间对OR-SON吸附作用的影响
在初始pH为3,OR-SON混合液投加量3 mL/L的条件下,考察不同反应时间对OR-SON吸附效果的影响,结果见图5。
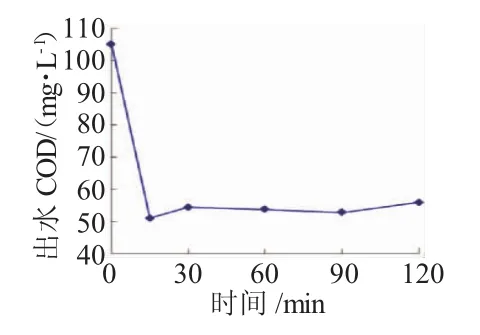
图5 反应时间对OR-SON吸附作用的影响
由图5可知,在OR-SON投加量一定时,其吸附反应速率相当快,反应15min后,吸附过程已经完成,在反应时间从15 min延长到120 min的过程中出水COD一直稳定在50~55 mg/L之间,COD去除率为48.6%~53.3%,此过程中并无有机物脱附的现象发生。从与图2的比较中也可以发现,OR-SON的投加可以明显降低反应时间,而在实际工程中,反应时间是影响建设和运行费用的因素之一,因此反应时间的降低十分重要。而考虑到投加H2O2后H2O2在OR-SON表面与有机物的反应过程,为使反应完全,反应时间设定为1 h。
2.3.4OR-SON投加量对Fenton处理效果的影响
为使对比效果更明显,选取初始条件:H2O2浓度25 mg/L,FeSO4·7H2O投加量按Fe2+/H2O2为0.2∶1计算,pH为3,反应时间1 h,结果见图6。

图6 OR-SON投加量对Fenton处理效果的影响
由图6可知,在初始COD为107 mg/L情况下,随着OR-SON投加量的逐渐增加,出水COD不断降低,在投加量从0.5 mL/L提高到5 mL/L时,出水COD从83.1 mg/L降低到36.6 mg/L,COD去除率从22.4%提高到65.8%,提高效果明显,与只投加OR-SON相比,出水COD从45.8 mg/L降低到36.6 mg/L。其原因可能一方面催化剂用量提高,吸附量提高,另一方面催化剂的使用使得H2O2吸附到其表面,进而能高效利用·OH降解污水中的难降解有机物。但由于H2O2投加量较小,H2O2的作用并不明显。
2.4OR-SON催化Fenton与传统Fenton氧化处理效果对比
1)传统Fenton的反应条件。废水初始COD=110mg/L,pH=3,Fe2+/H2O2(摩尔比)为2∶1,反应时间2 h,考察不同H2O2浓度对传统Fenton处理效果的影响。
2)OR-SON催化Fenton反应条件。废水初始COD=107 mg/L,pH=3,FeSO4·7H2O投加量按Fe2+/H2O2为0.2∶1计算,反应时间1 h,OR-SON混合液投加量5 mL/L,考察投加OR-SON后,H2O2浓度变化对处理效果的影响,结果见图7。
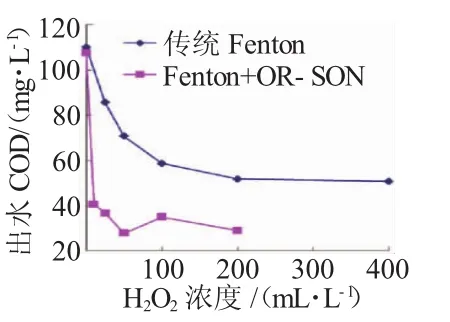
图7 OR-SON催化Fenton与传统Fenton氧化处理效果对比
由图7可知,对于传统Fenton而言,当H2O2浓度较低时,出水COD随着H2O2浓度的提高而降低,H2O2作为一种强氧化剂,在催化剂作用下产生大量·OH,可快速降解有机物,而在H2O2浓度达到一定限值后,出水COD稳定在50.7 mg/L,此时COD去除率为53.9%。这可能是由于[5]过量H2O2会使体系中OH-过多,·OH发生积聚反应:·OH+·OH-→H2O2;同时H2O2是·OH的捕获剂,过量的H2O2反而会使生成的OH-减少,不利于有机物降解·OH+H2O2→H2O+HO2·。
在传统Fenton氧化反应中投加OR-SON催化剂,能够明显提高对有机物的去除效果。由图7可见,在H2O2投加量为50 mg/L情况下,同时投加5 mL/L的OR-SON混合液时,反应后出水COD仅为27.8 mg/L,去除率达到74%。而传统Fenton氧化法在同样的H2O2投量和大10倍的FeSO4·7H2O投加量下,出水COD还有70.7 mg/L,去除率仅为36%。
2.5OR-SON催化剂的重复利用
1)单独OR-SON多次吸附试验。反应条件:废水初始COD=110 mg/L,初始pH为3,OR-SON投加量5 mL/L,反应时间1 h,考察连续使用OR-SON催化剂对其吸附性能的影响。在反应完毕后,将反应后的混合液用0.45 μm滤纸过滤,再将滤渣重新投加到1 L废水中,开始下一轮处理试验。如此多次重复试验,共进行6次,结果见图8。
2)Fenton-OR-SON多次催化氧化试验。反应条件:废水初始COD=110 mg/L,pH为3,H2O2投加量100mg/L,OR-SON投加量5 mL/L,FeSO4·7H2O投加量按Fe2+/H2O2为0.2∶1计算,反应时间1 h,考察OR-SON催化剂重复使用的效果。具体操作同上,共进行10次试验,结果见图8。

图8 OR-SON催化剂的重复使用效果
由图8可见,在只投加OR-SON情况下,第一次反应能使COD从110 mg/L降低到32.8 mg/L。在重复使用时其吸附性能明显下降,使用到第3次时出水COD上升到63.1 mg/L,去除率下降到42.6%,而使用到第6次出水COD为89.3 mg/L,去除率降低到18.8%。可见仅依靠OR-SON吸附作用,不能多次重复使用ORSON。
而在OR-SON催化Fenton反应体系中,虽然第2~4次重复使用OR-SON催化剂,出水COD呈明显上升趋势,但第4次重复使用后,其出水COD浓度稳定在65~70 mg/L,该值接近于投加100 mg/L H2O2的传统Fenton法去除效果,但FeSO4·7H2O投加量仅为传统Fenton法的1/10。这可能是由于在OR-SON吸附饱和后,其在反应体系中完全起到催化作用,虽然其催化性能与硫酸亚铁相比稍差,但是使用OR-SON催化剂能明显减少硫酸亚铁的用量,从而减少含铁泥的产生。
3 结论
1)OR-SON催化剂使用初期具有明显的吸附作用,在pH=3,OR-SON投加量为5 mL/L时,COD去除率为57.2%。而对于传统Fenton法,在pH=3,H2O2投加量达到200 mg/L后,COD去除率才达到53%。二者相比,可以发现OR-SON催化剂的吸附能力非常强。但其吸附性不能维持太长时间,因此单独使用OR-SON时其重复利用性不好,使用到第3次时COD去除率下降到42.6%,而使用到第6次COD去除率降低到18.8%。
2)OR-SON催化剂具有强化H2O2氧化的作用,能够明显提高反应体系的反应速率和COD去除率。在pH=3,OR-SON混合液投加量5 mL/L,H2O2投加量为50 mg/L条件下,反应1 h后出水COD仅为27.8 mg/L,去除率达到74%。而传统Fenton氧化法在同样的H2O2投量和大10倍的FeSO4·7H2O投加量下,反应1h后出水COD还有70.7 mg/L,去除率仅为36%。
3)在保障达到较好去除效果的前提下,OR-SON催化Fenton反应体系中的OR-SON催化剂可重复使用2~3次。如果为减少FeSO4·7H2O投加量,在处理效果与传统Fenton法相近的前提下,OR-SON催化剂可重复使用10次以上。
4)OR-SON催化Fenton体系的FeSO4·7H2O需要仅为传统Fenton法投加量的1/10,该技术可大幅度减少铁泥的产生量。
[1]赵晓亮,魏宏斌,陈良才,等.Fenton试剂氧化法深度处理焦化废水的研究[J].中国给水排水,2010,26(3):93-95.
[2]郑怀礼,谢礼国,胡鹏,等.非均相类Fenton反应催化氧化脱色降解直接桃红12B[J].光谱学与光谱分析,2010,30(6):1647-1651.
[3]龙明策,林金清,许庆清.非均相Fenton反应技术研究进展[J].环境污染治理技术与设备,2005,6(7):14-18.
[4]吴伟,吴程程,赵雅萍.非均相Fenton技术降解有机污染物的研究进展[J].环境科学与技术,2010,33(6):99-104.
[5]高真,雷国元,姜成春.Si-FeOOH非均相Fenton降解活性艳红MX-5B的效能研究[J].环境科学学报,2011,31(6):765-769.
[6]窦晓雯,林小琴,张华灵,等.非均相Fenton法降解水中橙黄G的研究[J].安徽农业科学,2011,39(9):5187-5190.
[7]郭茂峰,于少明,杨杰茹,等.铜铁复合层柱黏土的制备及其在含酚废水处理中的应用[J].工业催化,2007,15(7):56-61.
[8]韦朝海,陈传好,王刚,等.Fenton试剂催化氧化降解含硝基苯废水的特性[J].环境科学,2001,22(5):60-64.
[9]梁晓亮,何宏平,袁鹏,等.天然钒钛磁铁矿非均相Fenton法降解酸性橙II的研究[J].环矿物学报,2010,30(1):40-47.
[10]何莼,徐科峰,奚红霞,等.均相和非均相Fenton型催化剂催化氧化含酚废水[J].华南理工大学学报(自然科学版),2003,31(5):51-55.
□常臻/天津市排水管理处。
□王芬、于雷/天津大学环境科学与工程学院。
X703
C
1008-3197(2016)03-17-04
国家水体污染控制重大专项课题(2015ZX07203-011)
2016-03-08
刘灵婕/女,1992年,硕士在读,天津大学环境科学与工程学院,从事环境科学研究工作。
□DOI编码:10.3969/j.issn.1008-3197.2016.03.007
