不同化疗方案在晚期胃癌患者中的疗效对比
2016-10-18施英瑛王伟冯睿卜保国黎君陈新华陈晓光武警总医院消化内科检验科北京00039
施英瑛 王伟# 冯睿 卜保国 黎君 陈新华 陈晓光武警总医院消化内科,检验科,北京 00039
不同化疗方案在晚期胃癌患者中的疗效对比
施英瑛1王伟1#冯睿2卜保国1黎君1陈新华1陈晓光1
武警总医院1消化内科,2检验科,北京100039
目的比较SP与FOLFOX4两种化疗方案治疗晚期胃癌的临床疗效。方法选取84例晚期胃癌患者,按照随机数字表法分为SP组与FOLFOX4组,每组42例。SP组患者接受SP化疗方案,FOLFOX4组患者接受FOLFOX4化疗方案,比较两组患者的临床疗效、中位疾病进展时间、中位生存时间及两组患者化疗过程中出现的不良反应。结果SP组患者临床有效率为55.00%,FOLFOX4组患者临床有效率为46.15%,两组疗效比较差异无统计学意义(P>0.05);两组患者中位疾病进展时间及中位生存时间比较差异均无统计学意义(P>0.05);在不良反应发生方面,SP组白细胞减少、恶心呕吐、腹泻发生率低于FOLFOX4组,差异有统计学意义(P<0.05);贫血、手足综合征、肝功能异常、口腔黏膜炎等不良反应,两组比较差异无统计学意义(P>0.05)。结论SP方案与FOLFOX4方案在治疗晚期胃癌方面均具有较好的临床疗效,且SP方案患者白细胞减少、恶心呕吐、腹泻等不良反应发生率低,值得临床上进一步研究应用。
晚期胃癌;替吉奥;顺铂;化疗;不良反应
Oncol Prog,2016,14(4)
胃癌是全球发病率及病死率最高的恶性肿瘤之一。但其早期临床表现不典型,往往发病隐匿,人群普查较为困难,早期检出率低,60%患者确诊时已为晚期,失去手术切除的机会[1-2]。研究显示胃癌患者中位生存期为7~12个月,2年的生存率<10%[3]。目前,晚期胃癌的治疗主要为药物化疗。SP方案为替吉奥与顺铂联用,临床疗效优于两种药物单独使用[4-5];FOLFOX4为氟尿嘧啶、奥沙利铂与亚叶酸钙三种药物联用,也是临床常用的治疗晚期胃癌化疗方案。本研究主要对比SP与FOLFOX4两种化疗方案在治疗晚期胃癌患者的临床效果。
1 对象与方法
1.1研究对象
选取北京武警总医院消化内科自2012年9月至2014年9月收治的84例晚期胃癌患者,其中男性50例,女性34例;年龄35~82岁,平均年龄(59.8±5.9)岁;中分化腺癌44例,低分化腺癌22例,印戒细胞癌11例,黏液腺癌7例;Ⅲ期26例,Ⅳ期58例。入选标准:病理学检查证实为晚期胃癌患者,至少存在一个可评估病灶;肝肾功能及血常规检查正常,且无既往化疗史者。排除标准:患者预计生存期不足3个月;孕期(前3个月)除非中断妊娠;败血症患者;昏迷患者;严重心血管、肺功能障碍者;不能充分合作的病人;出现频繁呕吐、腹泻每日超过5次,白细胞<3×109,血小板<60×109的患者需停止化疗,并列入排除对象;未能完成电话随访的患者。按照随机数字表法随机分为SP组与FOLFOX4组,每组42例。SP组患者男性25例,女性17例;中分化腺癌22例,低分化腺癌11例,印戒细胞癌5例,黏液腺癌4例;Ⅲ期13例,Ⅳ期29例。FOLFOX4组男性25例,女性17例;中分化腺癌22例,低分化腺癌11例,印戒细胞癌6例,黏液腺癌3例;Ⅲ期13例,Ⅳ期29例。两组患者性别、年龄、病理分型、疾病严重程度等比较差异无统计学意义(P>0.05)。
1.2治疗方法
SP组:口服替吉奥胶囊,根据患者体表面积确定给药剂量,40 mg/m2,早晚各1次,连用15 d;顺铂30 mg/m2,溶于500 ml生理盐水,静脉滴注4 h,连用5 d,21 d为1个疗程。FOLFOX4组:亚叶酸钙200 mg/m2,静脉滴注2 h,连用5 d;5氟尿嘧啶400 mg/m2,静脉滴注2 h,连用2 d,5氟尿嘧啶600 mg/m2,持续泵入22 h,连用2 d;奥沙利铂85 mg/m2,静脉滴注2 h,第1天给药,28 d为1个疗程。两组患者均在给予3个疗程的化疗后,CT检测肿瘤组织大小的变化。化疗期间给予止吐、护肝、利尿等常规处理,定期复查血常规、肝肾功能等。
1.3评价标准
临床疗效评价标准参考RECIST标准[6]:完全缓解(CR):肿瘤组织完全消失;部分缓解(PR):肿瘤组织缩小50%以上;疾病稳定(SD):肿瘤组织缩小或者增大不超过20%且无新的肿瘤组织出现;疾病进展(PD):肿瘤组织增大20%。有效率(RR)=(CR+PR)例数/总病例数×100%。
对患者均进行电话随访,末次随访时间为2015年12月,记录两组患者中位疾病进展时间(MDFS)及中位生存时间(MST),其中5例患者因未能完成随访列入排除对象(SP组2例,FOLFOX4组3例)。参考WHO标准评价两组患者化疗过程中出现的不良反应。
1.4统计学方法
对所有数据采用SPSS19.0-统计软件进行分析,计量资料以均数±标准差(±s)表示,采用t检验;计数资料用率(%)来表示,采用χ2检验,有序分类变量采用秩和检验,生存率采用Kaplan-Meier法,组间比较采用Log-rank检验,以P<0.05为差异有统计学意义。
2 结果
2.1两组患者的临床疗效比较
SP组患者临床有效率为55.00%,FOLFOX4组患者临床有效率为46.15%,两组临床疗效比较差异无统计学意义(Z=1.170,P>0.05),详见表1。

表1 两组患者临床疗效
2.2两组患者中位疾病进展时间及中位生存时间比较
经Log-rank检验两组患者中位疾病进展时间及中位生存时间比较,差异均无统计学意义(χ2= 0.956、0.657,P>0.05),详见表2。
表2 两组-患者中位疾病进展时间及中位生存时间比较(月,±s)

表2 两组-患者中位疾病进展时间及中位生存时间比较(月,±s)
组别SP组(n=40)FOLFOX4组(n=39)中位疾病进展时间7.3±1.8 6.7±1.4中位生存时间12.7±2.7 13.5±3.1
2.3两组患者不良反应情况比较
SP组白细胞减少、恶心呕吐、腹泻不良反应发生率低于FOLFOX4组,差异有统计学意义(P<0.05);两组贫血、手足综合征、肝功能异常、口腔黏膜炎不良反应发生率比较差异无统计学(P>0.05),详见表3。
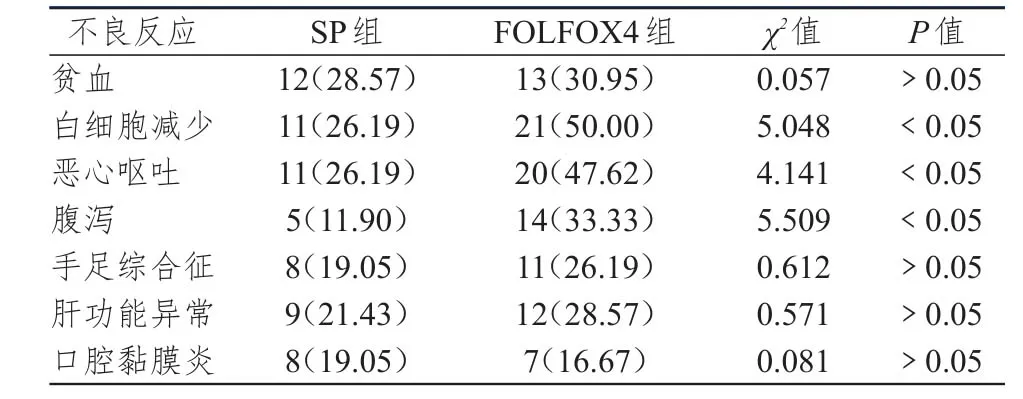
表3 两组患者不良反应发生情况比较[n(%)]
3 讨论
我国胃癌每年的新发患者数约为40万,直接或间接死于胃癌人数接近30万,给人们的生活造成极大的威胁[7]。但是,胃癌患者早期症状不典型,不易被发现,一旦确诊大多已为晚期,错过手术治疗的时期[8-9]。对于晚期胃癌患者,化疗是主要治疗方法之一。研究表明,与支持治疗相比,化疗可显著延长患者的生存时间[10]。由于晚期胃癌患者多为老年人,机体脏器功能下降,且伴有多发疾病,机体免疫力弱,对化疗药物的耐受性差,因此,如何在保证化疗疗效的前提下尽可能降低药物的不良反应成为治疗晚期胃癌患者的治疗方向。
SP方案为替吉奥与顺铂联用。替吉奥是一类新的氟尿嘧啶药物,其主要成分为替加氟、吉美嘧啶和奥替拉西钾,患者口服后替加氟在体内代谢为5-氟尿嘧啶,5-氟尿嘧啶能够抑制胸苷酸合成酶,进一步阻止脱氧鸟苷酸的甲基化,干扰DNA的合成,发挥其抗癌作用;吉美嘧啶则能抑制氟尿嘧啶在体内分解,从而维持其血药浓度,增强抗癌效果;奥替拉西钾通过阻断氟尿嘧啶的磷酸化,降低氟尿嘧啶的胃肠道毒性,减少不良反应的发生[11]。顺铂与氟尿嘧啶具有协同作用,共同杀伤癌症细胞,并对氟尿嘧啶耐药的肿瘤具有较好疗效,因此两种药物联合应用已成为新的趋势。FOLFOX4化疗方案为氟尿嘧啶、奥沙利铂与亚叶酸钙三种药物联用。氟尿嘧啶对增殖的各期肿瘤细胞均有杀伤作用,但对DNA合成期(S期)的肿瘤细胞杀伤作用最强,是S期特异的抗癌药物。奥沙利铂具有良好的抗癌效果,Koizumi等[12]研究表明,奥沙利铂联合替吉奥治疗晚期胃癌的有效率为59.1%,疾病的控制率为80.6%。习羽等[11]比较了SP方案与FOLFOX4方案治疗晚期胃癌的效果,结果发现SP方案总有效率为56%,对照组总有效率为44%,两组疗效差异无统计学意义,这与本研究结果SP组患者临床有效率55.00%,FOLFOX4组患者临床有效率46.15%,两组有效率比较差异无统计学意义结果类似。同时,本研究发现两组患者中位疾病进展时间及中位生存时间比较差异均无统计学意义;在不良反应发生方面,SP组白细胞减少、恶心呕吐、腹泻发生率低于FOLFOX4组,差异有统计学意义;两组贫血、手足综合征、肝功能异常、口腔黏膜炎不良反应发生率比较差异无统计学意义。
综上所述,SP化疗方案与FOLFOX4化疗方案在治疗晚期胃癌方面均具有较好的临床疗效,且SP方案患者白细胞减少、恶心呕吐、腹泻不良反应发生率低,值得临床上进一步研究应用。
[1]杨子鑫,刘巍.晚期胃癌内科治疗的研究进展[J].中华肿瘤防治杂志,2011,18(19):1572-1576.
[2]Bang YJ,Van Cutsem E,Feyereislova A,et al.Trastu-zumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer(ToGA):aphase 3,open-label,randomised controlled trial[J].Lancet,2010,376(42):687-697.
[3]Huang Z,Xie DH,Guo L,et al.The utility of MRI for preoperative T and N staging of gastric carcinoma:a systematic review and meta-analysis[J].Br J Radiol,2015,88(50): 1120-1130.
[4]Kim JG,Chung HY,Yu W.Recent advances in chemotherapy for advanced gastric[J].World J Gastrointest Oncol,2010,2(7):287-294.
[5]王程.PFC方案和FOLFOX4方案治疗晚期胃癌的疗效及对外周血淋巴细胞的影响[J].中国老年学杂志,2014(22): 6324-6326.
Efficacy of two chemotherapy regimens in patients with advanced gastric cancer
SHI Ying-ying1WANG Wei1#FENG Rui2BU Bao-guo1LI Jun1CHEN Xin-hua1CHEN Xiao-guang1
1Department of Gastroenterology,2Department of Clinical Laboratory,General Hospital of Chinese People's Armed Police Force,Beijing 100039,China
ObjectiveTo compare the clinical curative effect of two chemotherapy regimens,which are SP and FOLFOX4,in patients with advanced gastric carcinoma.Method84 patients with advanced gastric cancer were enrolled and randomized into SP group and FOLFOX4 group according to a random number table,with 42 cases in each.Patients in SP group received chemotherapy of SP,while those in FOLFOX4 group were treated with FOLFOX4 chemotherapy. The clinical curative effect,median time to disease progression,median survival time and adverse reactions of the two groups were compared.ResultsThe clinical response rate(RR)of SP group and FOLFOX4 group was 55.00%and 46.15%,respectively,with no significant difference observed(P>0.05).No significant difference was detected between the two groups in regard of median time to progression and median survival time(P>0.05).As for adverse reactions,the incidences of leucopenia,nausea,vomiting,diarrhea of SP group were significantly lower than those of FOLFOX4 group(P<0.05),while the incidences of anemia,hand foot syndrome,abnormal liver function,oral mucositis of the two groups were similar(P>0.05).Conclusion Both SP regimen and FOLFOX4 regimen are fairly effective in the treatment of advanced gastric cancer,and SP regimen is associated with less adverse reactions,such as leucopenia,nausea,vomiting,and diarrhea,which is clinically beneficial and practical.
advanced gastric cancer;S-1;cisplatin;chemotherapy;adverse reaction
R735.2
A
10.11877/j.issn.1672-1535.2016.14.04.23
(corresponding author),邮箱:licsyy@sina.com
