苯乙烯在H2O2/HBr条件下的多样性转化
2016-10-18闫鹏相翠满鹏程
闫鹏,相翠,满鹏程
(枣庄学院化学化工与材料科学学院,山东枣庄 277160)
苯乙烯在H2O2/HBr条件下的多样性转化
闫鹏,相翠,满鹏程
(枣庄学院化学化工与材料科学学院,山东枣庄277160)
本文主要探讨苯乙烯在H2O2/HBr体系中的反应情况.通过改变体系中的投料比、温度、溶剂、光照和pH值等条件,来比较1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮、1-苯基-2-溴乙醇的产率情况,从而找到合成这三种产物的最佳反应条件,并用红外光谱仪对产物进行表征.
苯乙烯;双氧水;氢溴酸①
0 引言
苯乙烯在过氧化氢和氢溴酸体系中,反应的产物主要有1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮、1-苯基-2-溴乙醇,这三种化合物都是非常重要的有机合成中间体[1-3]. 1,2-二溴-1-苯基乙烷在制药工程、农药和其他特殊化学品方面也有着广泛的应用[2-4].ω-溴代苯乙酮具有较高的活性,这使它能和很多亲核试剂发生反应,生成具有生物活性的化合物,在化学和生物医药方面都有着非常重要的价值[5-8],可以用于合成雌激素类药物的重要中间体[9].1-苯基-2-溴乙醇可以用来合成合成树脂、抗生素、抗氧化剂等,而且在农药和各种药物的合成中也有着重要的应用[3,10].
本文实验中通过改变苯乙烯在H2O2/HBr中的投料比、温度、溶剂等条件,比较产品中1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮、1-苯基-2-溴乙醇的产率,从而确定分别合成这三种化合物的最佳反应条件.
1 实验部分
1.1实验仪器及主要设备
实验所用仪器及主要设备如表1所示.
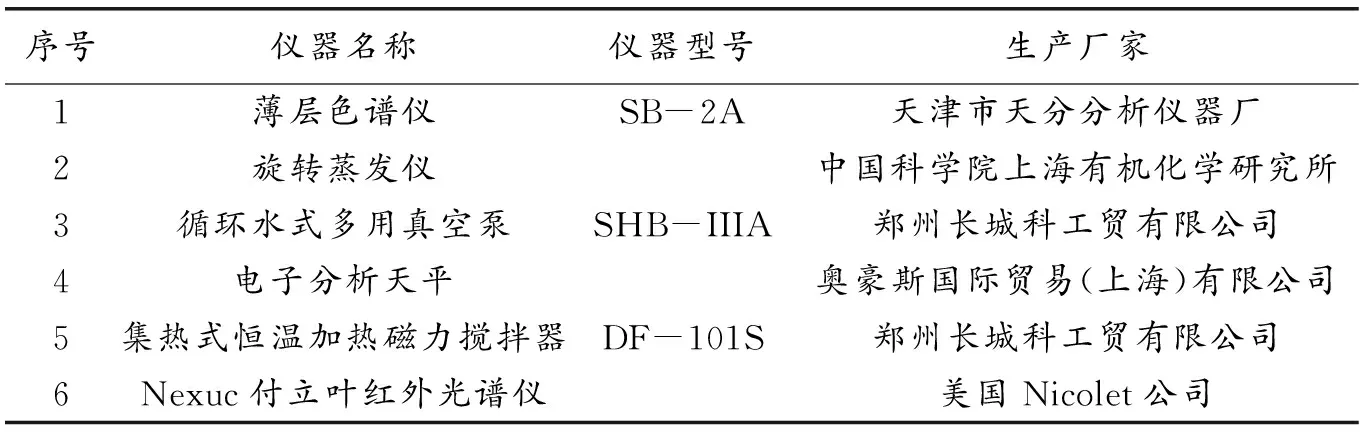
表1 主要仪器设备一览表
1.2实验药品
实验用主要试剂:苯乙烯、四氯化碳、石油醚、乙酸乙酯、硫酸镁等均为分析纯,双氧水浓度为30%,氢溴酸浓度为40%.
1.3实验方法
在100 mL的圆底烧瓶中加入30 mL水、10 mmol苯乙烯、10 mmol氢溴酸,在室温下不断搅拌.通过恒压漏斗逐滴加入10 mmol过氧化氢,搅拌5h,并不断通过TLC跟踪反应,直至反应结束.用20 mL乙酸乙酯萃取3次.对于萃取的有机相用无水硫酸镁干燥,然后过滤,旋蒸,从而得到粗产品.最后用乙酸乙酯:石油醚=1:10的展开剂对粗产品进行硅胶柱层析法分离.并对分离的产品用红外色谱仪进行表征.然后改变过氧化氢和氢溴酸的比例做平行试验,计算不同投料比下的各产品的产率.分别以水和四氯化碳做溶剂,并改变搅拌过程中的反应温度,用同样的方法进行实验,考察溶剂和温度对反应结果的影响.
2 结果与讨论
表2苯乙烯在不同条件下的H2O2/HBr体系中的多样性转化

说明:a代表的是苯乙烯、氢溴酸和过氧化氢的摩尔比.
2.1不同反应物比例下苯乙烯在H2O2/HBr体系中的反应
苯乙烯、双氧水、氢溴酸摩尔比例分别为1:1:1、1:1.5:1.5、1:1.5:1、1:1:1.5 的室温条件下进行反应,其产品的产率情况如表2(1-4)数据.
由表2可以看出,室温下,苯乙烯在氢溴酸和过氧化氢的水溶液体系中发生反应时,得到的产物主要是1-苯基-2-溴乙醇.如果增大氢溴酸的比例则会增大ω-溴代苯乙酮的产率,而增大双氧水的比例则会增加1-苯基-2-溴乙醇的产率.因此,通过增大双氧水用量,1-苯基-2-溴乙醇的产率可达61.96%(表2(4)).
2.2不同溶剂条件下苯乙烯在H2O2/HBr体系中的反应
为了比较不同溶剂条件下,苯乙烯在H2O2/HBr体系中的反应产品差异状况,实验中分别采用四氯化碳和水做溶剂,在同样的条件下进行实验,其结果如表2(1-2,7-8,11)数据.
通过比较表2中的数据可以看出:室温下,该反应在水作溶剂的条件下主要的反应产物是1-苯基-2-溴乙醇(表2(4)),而1,2-二溴-1-苯基乙烷的产率很低.在四氯化碳作溶剂的条件下,1,2-二溴-1-苯基乙烷的产率大大增加,而且采用四氯化碳做溶剂,可以明显降低其他副产物的生成(表2(11)).
2.3不同温度条件下苯乙烯在H2O2/HBr体系中的反应
分别在室温和加热回流的条件下,考察苯乙烯在H2O2/HBr体系中的反应,其结果如表2(1-2,5-6)数据.从该数据中可以看出:在加热回流的条件下,产物中不再有1,2-二溴-1-苯基乙烷的存在,而且1-苯基-2-溴乙醇和ω-溴代苯乙酮的产率也都普遍降低.这说明加热时,反应体系中的其他副产物开始增多.所以加热不利于1,2-二溴-1-苯基乙烷、1-苯基-2-溴乙醇和ω-溴代苯乙酮这三种化合物的产生.因此,本实验的反应条件确定为室温.
2.4苯乙烯在光照条件下的H2O2/HBr体系中的反应
通过比较表2(9-12)数据可以得出的结论是:在相同的比例下,体系受光照,可提高ω-溴代苯乙酮的生成比例.而反应物的投料比影响到1,2-二溴-1-苯基乙烷与ω-溴代苯乙酮的比例.
3 反应机理
过氧化氢首先把氢溴酸氧化成溴单质,Br2与苯乙烯中的双键形成一个溴鎓正离子.同时体系中的溴负离子会去进攻溴鎓离子上的碳,因而转变成了邻二溴代物,也就是生成了1,2-二溴-1-苯基乙烷.
若体系中有水, H2O中的氧原子也会进攻溴鎓离子上的碳,从而形成了邻溴代醇.对于苯乙烯这种不对称的烯烃,在形成了溴鎓离子这种环状中间体后,对于苯乙烯这种不对称的烯烃,在形成了溴鎓离子这种环状中间体后,连有苯环的碳受得苯环的给电子影响,容纳正电荷的能力比另一个碳强,因此H2O加到含氢较少的碳上,从而生成了1-苯基-2-溴乙醇.体系中生成了1-苯基-2-溴乙醇后,由于还有过氧化氢的存在,过氧化氢会把生成的1-苯基-2-溴乙醇中的羟基氧化成酮基,从而生成了ω-溴代苯乙酮.
4 结论
通过比较分析表2中的数据可以得到如下结论:
苯乙烯在H2O2/HBr体系中的多样性转化,能够影响各产物产率的关键因素主要有:溶剂、体系温度以及各反应物的投料比.光照情况对产物的影响并不明显,如表中编号为9、10、11、12中的数据.加热体系时,产物中不再有1,2-二溴-1-苯基乙烷的存在.如表2中编号为5和6中的数据.可能是在加热的条件下,1,2-二溴-1-苯基乙烷中的溴基团很容易被取代和氧化.
(1)若要得到较高产率的1,2-二溴-1-苯基乙烷,应该是室温下,使用四氯化碳作溶剂,苯乙烯、氢溴酸和过氧化氢的摩尔比是1:1.8:2.5,如表中编号11中的数据.这种条件下,生成物的种类也比较少,主要产物只有1,2-二溴-1-苯基乙烷和ω-溴代苯乙酮.1-苯基-2-溴乙醇的量很少.所以对于产物的分离也相对容易的多.
(2)若要得到较高产率的ω-溴代苯乙酮,应该是在室温下,使用四氯化碳作溶剂,并且在投料中应当着重增加过氧化氢的比例,尤其当苯乙烯、氢溴酸和过氧化氢的摩尔比是1:1.5:2时,ω-溴代苯乙酮的产率最高.如表2中编号10中的数据.
(3)若要得到较高产率的1-苯基-2-溴乙醇,应该在室温下使用水做溶剂,并且在氢溴酸适量的情况下,增大过氧化氢的比例.当苯乙烯、氢溴酸和过氧化氢的摩尔比是1:1:1.5时,1-苯基-2-溴乙醇产率最高.如表2中编号4中的数据.
利用苯乙烯在氢溴酸和过氧化氢的体系中来合成1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮和1-苯基-2-溴乙醇具有非常重要的现实意义.第一,从经济方面考虑,苯乙烯、氢溴酸和过氧化氢这些原料的价格都比较便宜.第二,从药品的毒性方面考虑,这些原料的毒性都不是太大,操作比较方便.第三,从实验条件方面考虑,这些反应都是在常温常压下进行,反应条件要求不苛刻,对仪器也没有特殊要求.第四,从得到的产物方面考虑,这三种化合物都是非常重要的有机合成中间体,因此在化学化工合成中有着广泛的应用前景.
利用苯乙烯、溴化氢和过氧化氢来合成这三种产物方便又经济,只要控制好反应物的投料比,选择好合适的溶剂,在比较温和的条件下就会分别得到较高产率的1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮和1-苯基-2-溴乙醇.
本论文通过对苯乙烯在H2O2/HBr体系中的多样性转化的探讨,找到了合成1,2-二溴-1-苯基乙烷、ω-溴代苯乙酮和1-苯基-2-溴乙醇的较优条件.
[1]Richard C. Larock. Comprehensive Organic Transformations [M]. 2nd ed. Wiley-VCH, New York, 1999, 789-792.
[2]Y.-F Zheng, J. Yu, G.-B Yan, X. Li, S. Luo. FeBr3-catalyzed dibromination of alkenes and alkynes [J]. Chin. Chem. Lett, 2011, 22:1195-1198.
[3] A. Butler, J.V. Walker, Marine haloperoxidases, Chem. Rev[J]. 1993, 93:1937-1944.
[4]G. W. Gribble. The diversity of naturally occurring organobromine compounds. Chem. Soc. Rev[J].1999, 28:335-337.
[5]S. Sudhir, B. Suresh, A. V. Ramaswamy. Photochemical α-bromination of ketones using N-bromosuccinimide: a simple, mild and efficient method. Tetrahedron Lett[J].2007, 48(8):1411-1415.
[6]W. A. Benjamin, H. O. House. Modern Synthetic Reactions[M].2nd ed, New York, 1972, 459-461.
[7]郭瑞霞,张宝华,史兰香,等. 新方法合成α-溴代苯乙酮类化合物[J]. 化学试剂,2010, 32(11): 1035-1036.
[8]D. Price, B. Iddon, B. J. Wakefield. In Bromine Compounds Chemistry and Applications[M]. Elsevier, 1988, 151-154.
[9]苏冰,鲍亚杰,李洪军,等.对甲氧基-α-溴代苯乙酮的合成[J].中国医药工业杂志,2001,32(8): 374-376.
[10]B. Das, V. Katta, K. Damodar, B. Das. Ammonium acetate catalyzed improved method for the regioselective conversion of olefins into halohydrins and haloethers at room temperature[J]. J. Mol. Catal. A: Chem, 2007, 269: 17-21.
[责任编辑:周峰岩]
The Different Reaction of Styrene in the Hydrogen Peroxide and Hydrobromic Acid System
YAN Peng,XIANG Cui,MAN Peng-cheng
(School of Chemical Engineering and Material Science , Zaozhuang University, Zaozhuang 277160,China)
Styrene in the hydrogen peroxide and hydrobromic acid system can produce a variety of compounds, and under different conditions, there will be a large difference in yield for various produces. The main products are 1,2-dibromo-1-phenylethane, ω- bromoacetophenone and 1-phenyl-2-bromoethanol. The main purpose is to study the various transformation for styrene in hydrogen peroxide and hydrobromic acid system in the article from designing different proportion of reactants, temperature, solution, illumination and so on.
styrene; hydrogen peroxide; hydrobromic acid
2016-09-07
枣庄学院博士科研启动基金(项目编号:307070806) .
闫鹏(1981-),男,山东临沂人,枣庄学院化学化工与材料科学学院讲师,理学博士,主要从事有机化学合成研究.
O621.3
A
1004-7077(2016)05-0135-04
