铜离子浓度对嗜酸性氧化亚铁硫杆菌生长特性和生长动力学的影响
2016-10-14叶茂友严苹方孙水裕韩大建庄圣炜黄绍松
叶茂友,严苹方,孙水裕, 2,韩大建,庄圣炜,郑 莉,黄绍松
铜离子浓度对嗜酸性氧化亚铁硫杆菌生长特性和生长动力学的影响
叶茂友1,严苹方1,孙水裕1, 2,韩大建1,庄圣炜1,郑 莉1,黄绍松1
(1. 广东工业大学环境科学与工程学院,广州 510006;2. 广东环境保护工程职业学院,佛山 528216)
通过研究Cu2+浓度对嗜酸性氧化亚铁硫杆菌()生长特性的影响,得到在不同Cu2+浓度下菌的生长曲线,探究不同Cu2+浓度对培养液中细菌浓度、pH、亚铁浓度和氧化还原电位的影响。结果表明:菌对Cu2+具有一定的耐受能力;当培养液中(Cu2+)≤0.5 g/L时,Cu2+对菌的生长活性影响较小;当(Cu2+)在1.0~2.0 g/L之间变化时,菌的生长活性开始受到Cu2+的影响,出现明显的延迟效应,Cu2+开始抑制细菌生长繁殖;当(Cu2+)≥3.5 g/L 时,菌生长完全受到抑制,几乎停止生长。随着培养液中Cu2+浓度的增加,菌生长活性受到的抑制作用也增大。依据Monod方程推导并建立了菌在不同Cu2+浓度下的生长动力学方程,各动力学曲线的相关性较好,表明动力学方程能较好地描述不同Cu2+浓度对氧化亚铁硫杆菌生长的影响。
嗜酸性氧化亚铁硫杆菌;铜离子;生长特性;生长动力学
随着社会的发展,矿物资源日渐贫乏,在富矿、易处理矿资源日渐减少、环保要求不断提高、现代工业和科技发展对金属的需求与日俱增的条件下,低品位矿的开发利用,越来越受到国内外的广泛重视[1−4]。利用传统的物理和化学方法来提取低品位的硫化矿中的金属是比较困难和昂贵的[5]。生物浸出方法具有操作简单、能耗低、环境友好等特点[6],逐渐成为研究的热点[7−9]。目前,生物浸出技术主要应用于低品位的铜矿的开采[10−12]。
生物浸出是通过微生物从矿石上提取有用金属的选矿方法,利用微生物在生命活动中自身的氧化和还原特性,使资源中的有用成分氧化或还原,以水溶液中离子态或沉淀的形式与原物质分离。在生物浸出过程中,矿石中金属被细菌氧化浸出,溶解进入溶液,一定量的金属离子对于细菌生长是必需的,但是当溶液中的金属浓度超过细菌生长耐受范围时,过高的渗透压以及金属离子与细菌的作用等因素会抑制细菌的生长,甚至导致细菌的死亡。大量研究表明过量的金属离子对浸矿细菌—氧化亚铁硫杆菌(,)一般都具有一定的毒性,溶液中的重金属离子会抑制细菌的生长[13−14],从而抑制生物浸出。金属离子和其他影响因素对氧化亚铁硫杆菌的生长动力学的影响已有报道[15−17],但从动力学方面考察Cu2+浓度对嗜酸性氧化亚铁硫杆菌生长动力学的影响却鲜见报道。
本文作者通过研究不同Cu2+浓度培养条件下的菌生长过程,考察Cu2+对细菌生长活性的影响;利用存在非竞争性抑制的Monod模型,获得不同Cu2+浓度培养条件下的菌生长动力学方程,为生物浸出含铜硫化矿的应用提供一定的理论依据和指导作用。
1 实验
1.1 实验材料和仪器
实验菌种:实验所用的嗜酸性氧化亚铁硫杆菌(,)菌株来源于广东省某矿山的酸性矿坑废水,采用9K培养基进行分离,利用9K固体培养基进行纯化,实验室保存,用于试验。经检测菌株与ATCC23270同源性为99%。
实验仪器:北京瑞利UV−2100 型紫外分光光度计;上海一恒−THZ−98C型恒温振荡器;岛津(Shimadzu)AUY120型电子分析天平;梅特勒−托利多(Mettler Toledo)DELTA320型酸度(pH)计及雷磁PHS−25型氧化还原电位计;奥林巴斯(Olympus)CX41型相差显微镜。
实验药品:硫酸(H2SO4),硫酸铵[(NH4)2SO4],氯化钾(KCl),磷酸氢二钾(K2HPO4),硫酸镁(MgSO4·7H2O),硝酸钙[Ca(NO3)2],硫酸亚铁(FeSO4·7H2O),硫酸铜(CuSO4·5H2O),所有的药品都为分析纯,购买于广州化学试剂厂。实验用水为二次蒸馏水。
9K培养基[18−19]:3.0 g (NH4)2SO4、0.1 g KCl、0.5 g K2HPO4、0.5 g MgSO4·7H2O、0.01 g Ca(NO3)2溶于去离子水 700 mL中,pH 用 1:1 H2SO4调为 2.0,在 121 ℃灭菌处理2 0 min;取44.7 g FeSO4·7H2O溶于300 mL无菌水中,用1:1 H2SO4调节 pH=2.0,用0.22 μm滤膜的针管过滤器过滤除菌,然后与上述培养基混合。
1.2 分析方法
利用酸度(pH)计进行pH的测定;利用氧化还原电位计进行氧化还原电位(Oxidation-reduction potential,ORP)的测定;采用UV−2100型紫外可见分光光度计,通过邻菲啰啉分光光度法进行Fe2+浓度的测定[20−21]。Fe2+与邻菲啰啉发生络合反应,产生橙红色的络合物,在510nm处测量吸光度,计算Fe2+浓度。细菌活体数采用血球计数法进行细菌浓度的测定[22]。
1.3 实验方案
在250 mL锥形瓶中装入100 mL 9K培养液中,加入适量Cu2+,将培养后的菌(菌种浓度达1×108mL−1)接入锥形瓶中,置于30℃、160 r/min的恒温振荡器内培养。定时测定培养液中的pH、ORP、细菌浓度、Fe2+浓度。定期期补加蒸馏水弥补损耗的水分。同时设置不加Cu2+的空白实验。具体实验方案如表1所示。
1.4 生长动力学模型
综合氧化亚铁硫杆菌的生长动力学模型,选择Monod方程[15, 23−24]作为菌的生长动力学模型,该方程表达形式如下:
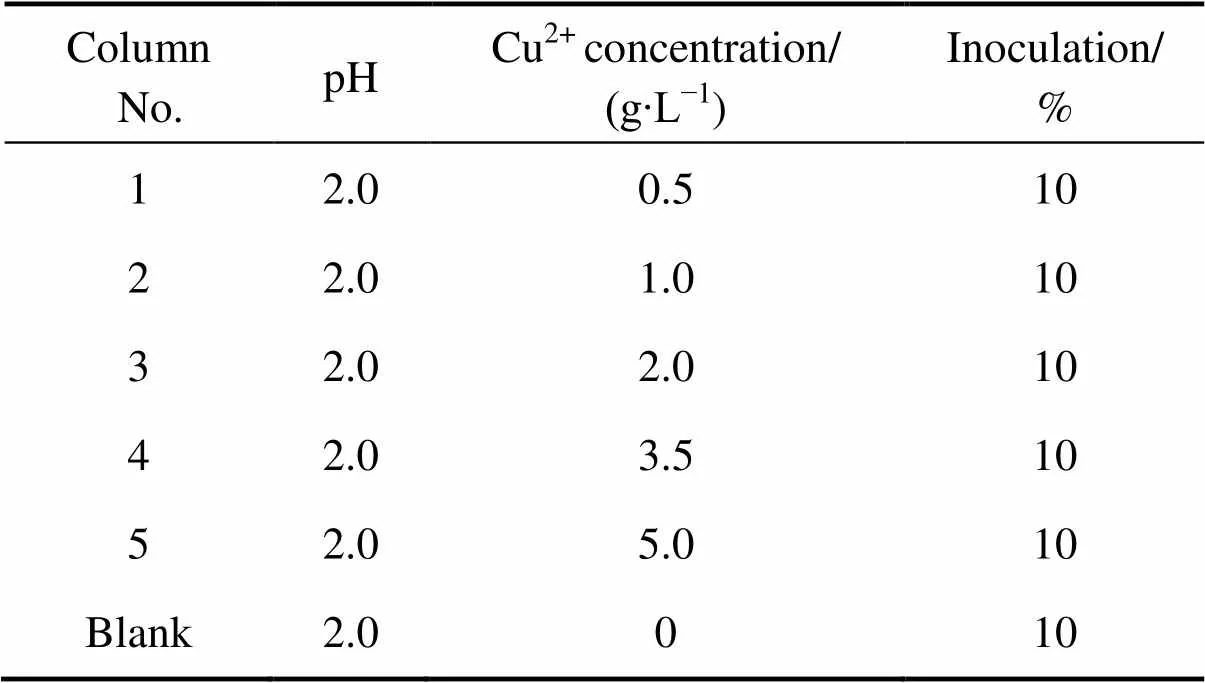
表1 氧化亚铁硫杆菌培养的实验条件
故式(1)可以写成
2 结果与讨论
2.1 Cu2+浓度对氧化亚铁硫杆菌生长活性的影响
通过改变培养基中Cu2+浓度,研究Cu2+浓度对菌生长过程的影响,实验过程中细菌浓度及Fe2+浓度((Fe2+))随时间的变化如图 1和2 所示。
研究结果表明,当培养基中Cu2+浓度增加会抑制菌的生长,浓度越大,抑制作用越明显;当培养液中Cu2+浓度上升时,开始产生延迟效应,抑制细菌生长。当培养液中不存在Cu2+时,菌在12 h后开始进入对数生长期,48 h后开始进入稳定期,Fe2+的氧化18 h后开始进入快速氧化阶段,到54 h时Fe2+基本氧化完全;当(Cu2+)≤0.5g/L时,Cu2+对细菌生长活性影响很小,Cu2+没有对细菌的生长繁殖造成不良影响,菌出现约3 h的延迟效应,培养液中Fe2+的氧化也相应地出现了一些延迟效应;当(Cu2+)=1.0 g/L时,菌生长受到抑制已经比较明显,停滞期明显增加,培养30 h后细菌才开始进入对数生长期,Fe2+的氧化也持续地明显延迟;当(Cu2+)=2.0g/L时,停滞期延长至54 h,菌对 Fe2+氧化活性显著降低,细菌经过60 h后,才进入Fe2+快速氧化阶段,当(Cu2+)≥ 3.5g/L时,菌的生长繁殖受到了极大抑制,细菌的生长繁殖基本处于停止状态,部分菌体死亡,培养液中Fe2+的氧化率很低,Cu2+对细菌生长活性影响很大,影响细菌的生长繁殖。Cu2+是细菌蛋白和酶的组成成分,是必需的微量元素,一般以辅基的形式参与细胞内的代谢[25],少量Cu2+对细菌的生长不会造成影响。但是随着培养液中Cu2+浓度的不断上升,菌的停滞适应期不断增长,微生物体内ATP酶的活性不断降 低[26],Cu2+能够与细胞蛋白质结合,Cu2+进入细胞后与酶上的—SH基结合而使其活性不断降低或失去活性,或与代谢中间产物结合而使代谢受阻,或取代细胞结构上的主要元素,使正常的代谢物变为无效的化合物,细菌的生长变得越来越缓慢,从而抑制细菌的生长,甚至导致细菌死亡[27]。同时随着 Cu2+质量浓度的上升,培养液中的渗透压也同时增大,进而影响细菌正常的生理功能Cu2+浓度越大,对菌生长的阻碍越大。当细菌生长环境中存在较高浓度Cu2+时,细菌会经过一定的改变和调整代谢途径以适应新环境。但是这种适应性一般是有限度的、暂时的,也可能是永久性的。

图1 不同 Cu2+浓度下细菌浓度的变化曲线

图2 不同 Cu2+浓度下ρ(Fe2+)随时间的变化曲线
2.2 Cu2+浓度对培养ORP和pH的影响
在不同Cu2+浓度范围内,考察培养液的pH和ORP的变化情况,菌培养液的pH值和ORP随培养时间的变化如图3和4所示。
由图3可知,在不同 Cu2+浓度下,随着培养时间的延长,pH值呈现先升高后降低的趋势。培养液中不含Cu2+时,培养液中的pH值在30h时达到最大值(pH=2.55);当培养液中(Cu2+)=0.5g/L时,pH值在36 h达到最高值(pH=2.56),当培养液中(Cu2+)为1.0 g/L和2.0 g/L时,pH值分别在48和78 h达到最高值(pH=2.55和2.60);当培养液中(Cu2+)≥3.5 g/L时,pH最高值的出现时间更加延后。随着溶液中Cu2+浓度的增加,培养液pH达到最大值的时间出现了延迟。
菌生长过程中的主要化学反应如下[28−30]:
Fe2++H++1/4O2→Fe3++1/2H2O (4)
Fe3++H2O→FeOH2++H+(5)
FeOH2++H2O→Fe(OH)2++H+(6)
Fe3++H2O→1/2Fe2(OH)42++H+(7)
1/2Fe2(OH)42++2H2O→Fe(OH)3+2H+(8)
Fe(OH)3+4/3SO24−+Fe3++H2O+2/3NH4+→
2/3NH4Fe3(SO4)2(OH)6+H+(9)
3Fe3++2SO42−+6H2O→KFe3(SO4)2(OH)6+6H+(10)
在细菌培养过程中,培养液的 pH开始呈上升趋势,由于Fe2+氧化成Fe3+过程中会消耗H+(见式(4)),从而在培养开始阶段出现pH上升的现象;当培养一段时间后,细菌进入指数增长期后,Fe3+发生连续的水解反应,培养液中开始出现黄铵铁矾[NH4Fe3- (SO4)2(OH)6]或者黄钾铁矾[KFe3(SO4)2(OH)6]沉淀,释放出H+(见式(5)~(10)),使pH开始下降,在细菌生长进入稳定期后,pH下降到2.20左右。细菌生长活性越强,Fe2+氧化成Fe3+的速率越快,pH上升得越快,随后pH值下降也越快。Cu2+浓度越大,对菌生长的抑制越大,细菌生长活性受到抑制,pH的变化就会出现明显的延迟现象。
培养液中的ORP值变化规律如图4所示。由图4可知,随着培养时间的延长,ORP值呈现上升的趋势,菌将培养液中的 Fe2+氧化为Fe3+,Fe3+浓度增加,(Fe3+)/(Fe2+)比值增加,导致溶液氧化还原电位上升[15]。随着培养液中Cu2+浓度的升高,ORP值上升出现延滞现象,培养液中Cu2+浓度越低,ORP上升的越快。经过一段时间后,ORP值也开始趋于比较稳定,稳定在540~550 mV左右。当(Cu2+)≥3.5g/L,菌的生长受到很大抑制,ORP值上升的很缓慢,基本处于停滞状态。随着Cu2+浓度增加,Cu2+抑制了菌的生长,导致对Fe2+的氧化能力降低,培养液中(Fe3+)/(Fe2+)比值随Cu2+浓度的增加而降低。
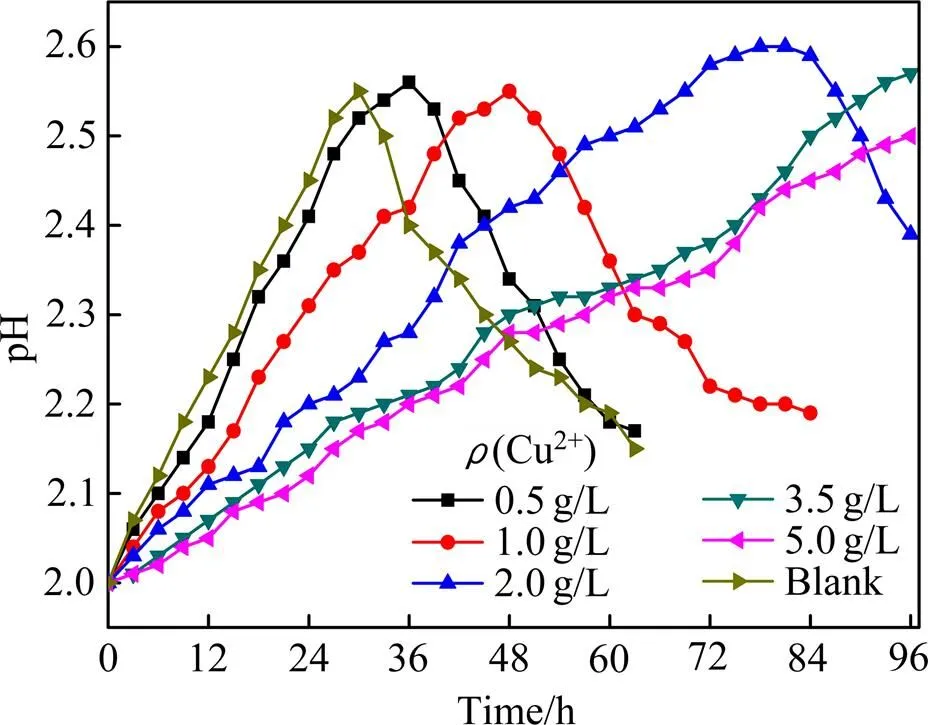
图3 不同 Cu2+浓度下pH随时间的变化曲线

图4 不同Cu2+浓度下ORP随时间的变化曲线
2.3 生长动力学参数的确定
参考相关的方法求解动力学方程,进行相关参数的计算,确定不同Cu2+浓度下细菌的最大比生长速率m、Monod饱和常数M、Cu2+抑制常数I。
细菌比生长速率利用两点法求解,其满足如下方程:
实验采用等间隔时间取点分析[15−16],综合上面的公式可以简化为
式中:为培养液中的细菌浓度(L−1),为培养时间(h)。
对于动力学模型,可以变形为
不同 Cu2+浓度下菌动力学参数的求解曲线如图 5 所示。对1/−1/(Fe2+)作图,曲线的截距为1/′m,的截距为−1/M,从而求出′m和M的值。可以从曲线求解得到的细菌生长的动力学参数′m和M。空白实验培养液中不含有Cu2+,因此,可认为空白实验的′m=m=0.2204 h−1。
图 5 中各动力学曲线的相关性较好,2都大于0.978,证明所得动力学参数与实验结果比较的吻合。由表2可知,M值基本不变,抑制剂对酶催化反应速率的非竞争性抑制中M值是保持恒定的,非竞争性抑制中抑制剂的浓度只影响m的值,而不影响M值,实验结果与非竞争性抑制结论相符。I和m均发生不同程度的变化,这一结果与实验选择的培养液中Cu2+浓度条件有关。表2中I的数值大小表示菌对Cu2+的亲和力的大小,随着培养液中Cu2+浓度的增加,菌对Cu2+的亲和力也相应增大,导致培养液中Cu2+的非竞争性抑制作用也相应增加,I值减小,I值的下降表明其抑制程度增加[15, 23]。随着培养液中Cu2+浓度的增加,Cu2+抑制作用随之增加。Cu2+通常能与酶的控制部位中的—SH作用,改变酶的空间结构,引起非竞争性抑制。抑制剂Cu2+浓度越大,形成不能转变为产物的EI(酶—抑制剂复合物)或IES(底物−酶−抑制剂三元复合物)越多,m降低的程度越显著。由于m降低,酶的反应速率也相应减小。抑制剂Cu2+的结合可导致酶活性中心的构型发生改变,削弱了底物(Fe2+)和酶活性中心的结合,即减小了最大反应速率m。非竞争性抑制作用的强弱取决于抑制剂的绝对浓度,因而不能用增大底物浓度的办法来消除非竞争性抑制作用[23]。
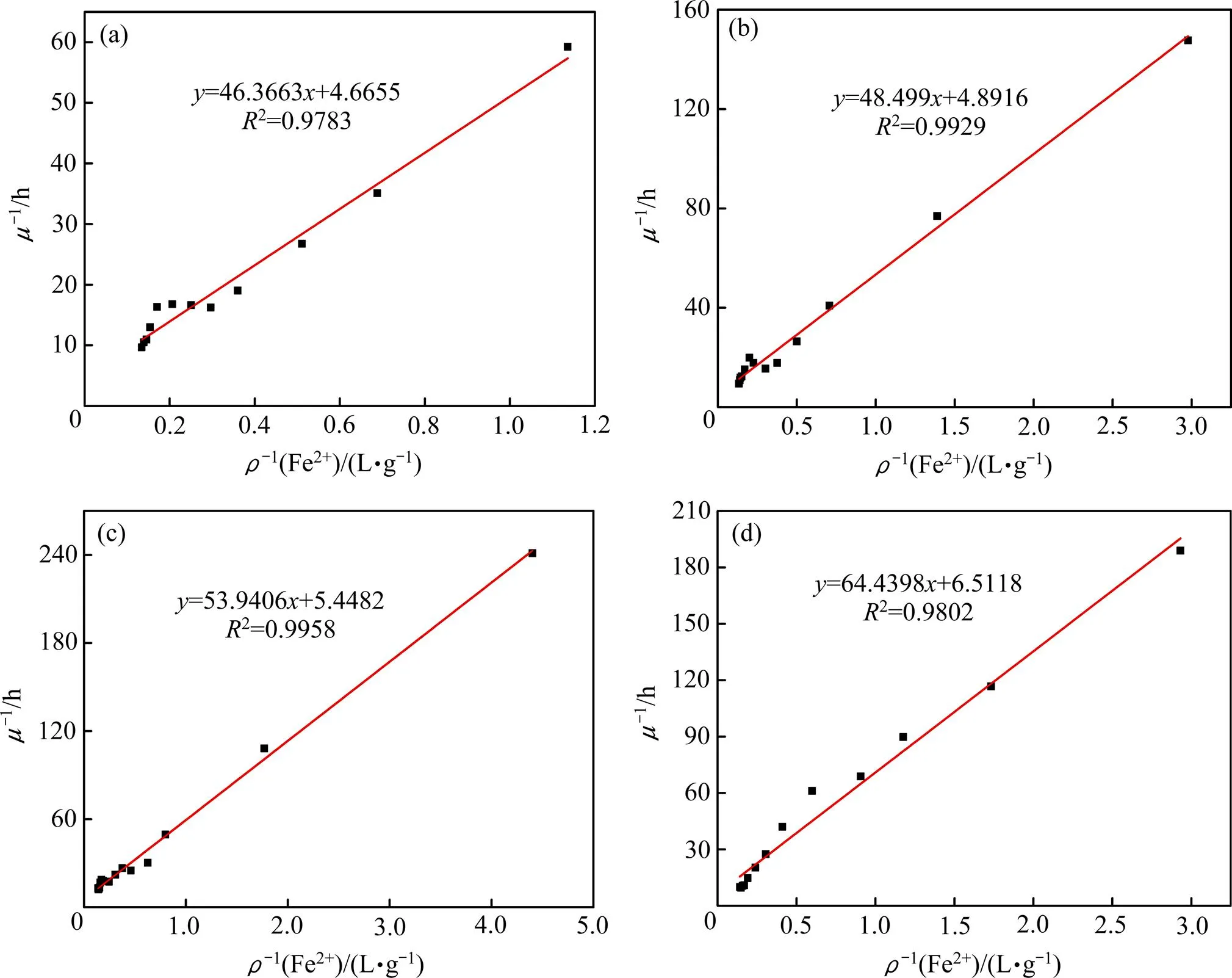
图5 不同Cu2+浓度下A. f菌的动力学曲线

表2 A.f菌生长动力学参数值
3 结论
1) 不同 Cu2+浓度下嗜酸性氧化亚铁硫杆菌的细菌浓度和(Fe2+)随时间的变化结果表明:菌对Cu2+具有一定的耐受能力,随着培养液中的Cu2+浓度的增加,菌生长繁殖的受到的阻碍越大,Cu2+浓度越大,菌受到的抑制作用越明显。Cu2+进入细胞后与酶上的—SH基结合,造成微生物体内ATP酶的活性不断降低,细菌的生长变得越来越缓慢,从而抑制细菌的生长,甚至导致细菌死亡。随着Cu2+质量浓度的上升,培养液中的渗透压也同时增大,进而影响细菌正常的生理功能。
2) 不同Cu2+浓度下嗜酸性氧化亚铁硫杆菌的pH和 ORP随时间的变化结果表明:pH值呈现先升高后降低的趋势,Fe2+氧化成Fe3+过程中消耗H+使pH上升,然后Fe3+发生水解反应,并释放出H+使pH开始下降;ORP呈现逐步上升,最后达到平稳,Fe2+氧化为Fe3+,培养液中(Fe3+)/(Fe2+)比值增加,导致ORP上升。随着Cu2+浓度的增加,细菌的生长繁殖受到抑制,pH和ORP的变化出现了明显的延迟现象。
3) 考察了不同Cu2+浓度下,嗜酸性氧化亚铁硫杆菌的细菌浓度和(Fe2+)随时间的变化,利用基于存在非竞争性抑制的Monod方程,建立了菌在不同Cu2+浓度下的生长动力学方程模型,得到4个Cu2+浓度下菌生长的动力学参数值。结果表明:随着 Cu2+浓度的增加,非竞争性抑制作用增加,削弱了底物(Fe2+)与酶活性中心的结合,I和m逐渐减小,表明在一定Cu2+浓度下(低于2.0 g/L时),菌才能正常生长。
REFERENCES:
[1] LI Shu-zhen, ZHONG Hui, HU Yue-hua, ZHAO Jian-cun, HE Zhi-guo, GU Guo-hua. Bioleaching of a low-grade nickel–copper sulfide by mixture of four thermophiles[J]. Bioresource Technology, 2014, 153: 300−306.
[2] 刘欣伟, 胡文韬, 李浩然, 冯雅丽. 高镁型低品位硫化镍矿浸出工艺及机理[J]. 中国有色金属学报, 2014, 24(6): 1599−1606. LIU Xin-wei, HU Wen-tao, LI Hao-ran, FENG Ya-li. Leaching process and mechanism of high magnesium low-grade nickel sulfide ore[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(6): 1599−1606.
[3] 谢红艳, 王吉坤, 路 辉, 嵇晓沧, 杨世诚. 加压浸出低品位锰矿的工艺[J]. 中国有色金属学报, 2013, 23(6): 1701−1711. XIE Hong-yan, WANG Ji-kun, LU Hui, JI Xiao-cang, YANG Shi-cheng. Technique of pressure leaching low grade manganese ore[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(6): 1701−1711.
[4] LI Chang-xin, ZHONG Hong, WANG Shuai, XUE Jian-rong, WU Fang-fang, ZHANG Zhen-yu. Manganese extraction by reduction-acid leaching from low-grade manganese oxide ores using CaS as reductant[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(4): 1677−1684.
[5] ZHU Jian-yu, LI Qian, JIAO Wei-feng, JIANG Hao, SAND Wolfgang , XIA Jin-lan, LIU Xue-duan, QIN Wen-qing, QIU Guan-zhou, HU Yue-hua, CHAI Li-yuan. Adhesion forces between cells oforand chalcopyrite[J]. Colloids and Surfaces B, 2012, 94: 95−100.
[6] CHEN Shen-yi, LIN Jih-gaw. Enhancement of metal bioleaching from contaminated sediment using silver ion[J]. Journal of Hazardous Materials, 2009, 161: 893−899.
[7] MOGHADDAM M Y, SHAFAEI S Z, NOAPARAST M, ARDEJANI F D, ABDOLLAHI H, RANJBAR M, SCHAFFIE M, MANAFI Z. Empirical model for bio-extraction of copper from low grade ore using response surface methodology[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(12): 4126−4143.
[8] 郝晓东, 曾伟民, 彭堂见, 胡 琪, 梁伊丽, 尹华群, 邱冠周, 刘学端. 高通量测序技术分析不同温度下赞比亚低品位铜矿生物浸出过程中的微生物多样性[J]. 中国有色金属学报, 2015, 25(9): 2558−2564. HAO Xiao-dong, ZENG Wei-min, PENG Tang-jian, HU Qi, LIANG Yi-li, YIN Hua-qun, QIU Guan-zhou, LIU Xue-duan. Analysis of microbial diversity during bioleaching of low grade copper ore from Zambia using high-throughput sequencing technology at different temperatures[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(9): 2558−2564.
[9] 顾帼华, 陈明莲, 苏丽君, 李建华, 胡岳华, 邱冠周. 氧化亚铁硫杆菌对黄铜矿表面性质及其浸出的影响[J]. 中南大学学报(自然科学版), 2010, 41(3): 807−812. GU Guo-hua, CHEN Ming-lian, SU Li-jun, LI Jian-hua, HU Yue-hua, QIU Guan-zhou. Effects ofon surface properties of chalcopyrite and bioleaching[J]. Journal of Central South University (Science and Technology), 2010, 41(3): 807−812.
[10] 王进龙, 王 军. 国内某露天剥离低品位铜矿石的生物柱浸研究[J]. 矿产保护与利用, 2015, 6: 27−30. WANG Jin-long, WANG Jun. Experimental research on column bioleaching of a low grade copper ore of an open pit in China[J]. Conservation and Utilization of Mineral Resources, 2015, 6: 27−30.
[11] PRADHAN N, NATHSARMA K C, RAO K S, SUKLA L B, MISHRA B K. Heap bioleaching of chalcopyrite: A review[J]. Minerals Engineering, 2008, 21: 355−365.
[12] 喻连香, 周 丹, 石丽娟, 王玉光, 曾伟民, 邱冠周. 国内某低品位难选铜矿的生物浸出研究[J]. 现代生物医学进展, 2014, 14(10): 1861−1864. YU Lian-xiang, ZHOU Dan, SHI Li-juan, WANG Yu-guang, ZENG Wei-min, QIU Guan-zhou. Bioleaching of some low grade refractory copper ore[J]. Progress in Modern Biomedicine, 2014, 14(10): 1861−1864.
[13] 谢鑫源, 孙培德, 楼菊青, 郭茂新, 马王钢. 模拟电镀污泥重金属浸出液对氧化亚铁硫杆菌活性的影响[J]. 环境科学, 2013, 34(1): 209−216. XIE Xin-yuan, SUN Pei-de, LOU Ju-qing, GUO Mao-xin, MA Wang-gang.Effect of simulated heavy metal leaching solution of electroplating sludge on the bioactivity of[J]. Environmental Science, 2013, 34(1): 209−216.
[14] 赵雪淞, 石倩倩, 李彩霞, 张孝松. 镍离子对氧化亚铁微螺菌和喜温嗜酸硫杆菌活性的影响[J]. 硅酸盐通报, 2016, 35(1): 306−309. ZHAO Xue-song, SHI Qian-qian, LI Cai-xia, ZHANG Xiao-song. Effect of nickel ions on activity ofand[J]. Bulletin of the Chinese Ceramic Society, 2016, 35(1): 306−309.
[15] 刘欣伟, 冯雅丽, 李浩然, 蔡震雷, 杨志超. 镁离子浓度对氧化亚铁硫杆菌生长动力学的影响[J]. 中国有色金属学报, 2012, 22(8): 2353−2359. LIU Xin-wei, FENG Ya-li, LI Hao-ran, CAI Zhen-lei, YANG Zhi-chao. Effect of magnesium ion concentration on growth kinetics of[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(8): 2353−2359.
[16] 汪智姝, 陈 晓, 李万全, 徐绍霞, 张永奎. 高铁浓度下氧化亚铁硫杆菌的生长动力学[J]. 化工进展, 2007, 26(10): 1475−1478. WANG Zhi-shu, CHEN Xiao, LI Wan-quan, XU Shao-xia, ZHANG Yong-kui. Growth kinetics ofat high iron concentration[J]. Chemical Industry and Engineering Progress, 2007, 26(10): 1475−1478.
[17] CABRERA G, GOMEZ J M, CANTERO D. Kinetic study of ferrous sulphate oxidation offerrooxidans in the presence of heavy metal ions[J]. Enzyme and Microbial Technology, 2005, 36: 301−306.
[18] 马 骏, 汪菊香, 武 彪, 温建康, 尚 鹤, 武名麟. 晶体结构对黄铜矿、黄铁矿生物浸出差异性影响[J].中国有色金属学报, 2015, 25(10): 2898−2904. MA Jun, WANG Ju-xiang, WU Biao, WEN Jian-kang, SHANG He, WU Ming-lin. Effects of crystal structure on differences of chalcopyrite and pyrite bioleaching[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(10): 2898−2904.
[19] 聂红燕, 朱能武, 杨婷婷, 张嘉妮. 嗜酸性细菌对废旧线路板浸出的吸附行为及动力学[J]. 环境科学学报, 2015, 35(5): 1471−1476. NIE Hong-yan, ZHU Neng-wu, YANG Ting-ting, ZHANG Jia-ni.Adsorption behavior and kinetics of adcidophilic bacteria on the leaching of waste printed circuit boards[J]. Acta Scientiae Circumstantiae, 2015, 35(5): 1471−1476.
[20] NGUYEN V K, LEE M H, PARK H J, LEE J U. Bioleaching of arsenic and heavy metals from mine tailings by pure and mixed cultures of.[J]. Journal of Industrial and Engineering Chemistry, 2015, 21: 451−458.
[21] 国家环境保护总局, 《水和废水监测分析方法》编委会. 水和废水监测分析方法[M]. 4版.北京: 中国环境科学出版社, 2002: 368−370. State Environmental Protection Administration, Editorial Committee of Analysis in Water and Wastewater. Analysis in water and wastewater[M]. 4th ed. Beijing: China Environmental Science Press, 2002: 368−370.
[22] 郑 莉, 黄绍松. 环境微生物学实验[M]. 广州: 华南理工大学出版社, 2012: 47−49. ZHENG Li, HUANG Shao-song. Environmental microbiology experiment[M]. Guangzhou: South China University of Technology Press, 2012: 47−49.
[23] 李再资, 黄肖容, 谢逢春. 生物化学工程基础[M]. 3版.北京: 化学工业出版社, 2011: 110−111. LI Zai-zi, HUANG Xiao-rong, XIE Feng-chun. Biochemical engineering fundamentals[M]. 3rd ed. Beijing: Chemical Industry Press, 2011: 110−111.
[24] 戚以政, 夏 杰, 王炳武. 生物反应工程[M]. 北京: 化学工业出版社, 2009: 19−21. QI Yi-zheng, XIA Jie, WANG Bing-wu. Biological response engineering[M]. Beijing: Chemical Industry Press, 2009: 19−21.
[25] 何云晓, 严万里, 陈晓明, 楚士晋. Cu2+、Fe3+对微生物生长及去除溶液中Cr(Ⅵ) 的影响研究[J].安全和环境学报, 2013, 13(8): 37−41. HE Yun-xiao, YAN Wan-li, CHEN Xiao-ming, CHU Shi-jin. Influence of Cu2+, Fe3+on the growth of microbes and removal of Cr(Ⅵ) in the solution[J]. Journal of Safety and Environment, 2013, 13(8): 37−41.
[26] 邓 蓉, 张小云, 张梦雪, 廖美霞, 曾子宁. 嗜酸氧化亚铁硫杆菌培养及其影响因素[J]. 湘潭大学自然科学学报, 2014, 36(4): 67−71. DENG Rong, ZHANG Xiao-yun, ZHANG Meng-xue, LIAO Mei-xia, ZENG Zi-ning. The cultivation ofand the investigation of influencing factors[J]. Natural Science Journal of Xiangtan University, 2014, 36(4): 67−71.
[27] 李洪枚, 柯家骏. Cu2+对氧化亚铁硫杆菌()生长活性的影响[J]. 黄金, 2000, 21(27): 27−29. LI Hong-mei, KE Jia-jun. Effect of Cu2+on the growth and activity of[J]. Gold, 2000, 21(27): 27−29.
[28] 邱冠周, 柳建设, 王淀佐, 徐 竞. 氧化亚铁硫杆菌生长过程铁的行为[J]. 中南工业大学学报, 1998, 29(3): 226−228. QIU Guan-zhou, LIU Jian-she, WANG Dian-zuo, XU Jing. Iron behavior in growth of[J]. Journal of Central South University of Technology, 1998, 29(3): 226−228.
[29] 郑 宇, 邸进申, 刘艳华, 李英杰, 胡 滨. 氧化亚铁硫杆菌培养过程中沉淀的研究[J]. 生物技术, 2005, 15(2): 66−69. ZHENG Yu, DI Jin-shen, LIU Yan-hua, LI Ying-jie, HU Bin. Study of precipitation produced during culture of[J]. Biotechnology, 2005, 15(2): 66−69.
[30] OJUMU T V, PETERSEN J. The kinetics of ferrous ion oxidation byin continuous culture: The effect of pH[J]. Hydrometallurgy, 2011, 106: 5−11.
(编辑 龙怀中)
Effect of copper ion concentration on growth activity and kinetics of
YE Mao-you1, YAN Ping-fang1, SUN Shui-yu1, 2, HAN Da-jian1, ZHUANG Sheng-wei1, ZHENG Li1, HUANG Shao-song1
(1. School of Environmental Science and Engineering, Guangdong University of Technology, Guangzhou 510006, China; 2. Guangdong Polytechnic of Environmental Protection Engineering, Foshan 528216, China)
The effect of initial copper ion concentration on the growth activity ofwas investigated, and the bacterial growth curves, bacteria concentration, pH, ferrous concentration and oxidation-reduction potential in the culture solution were obtained at different Cu2+concentrations. The results show that to some extentis tolerant to copper ion. When cultured in 9K medium containing(Cu2+)≤0.5 g/L, little effect on the growth and activity ofis brought to copper ion. When(Cu2+) is 1.0−2.0 g/L, the growth and activity ofare obviously influenced by copper ion and appear delayed effects, and then copper iron begins to inhibit the bacterial growth. When the concentration of copper ion is over 3.5 g/L, the inhibiting effect on activity ofis completely inhibited, bacteria almost stops growing. With the increase of Cu2+concentration in the culture medium, the inhibiting effect on growth activity ofincreases.Based on the model of Monod function, the growth kinetics equation ofat different copper iron concentration is built up. The correlation of kinetic curve is better, which shows that the kinetics equation can well describe the growth ofat different initial copper iron concentrations.
; copper ion; growth activity; growth kinetics
Projects(2015A030308008, 2015A030310143) supported by the Natural Science Foundation of Guangdong Province, China; Project(2016A040403068) supported by the Science and Technology Planning Project of Guangdong Province, China; Project(2016AG100482) supported by the Science and Technology Innovation Project of Foshan, China
2015-11-10; Accepted date:2016-04-18
SUN Shui-yu; Tel: +86-20-39322037; E-mail: sysun@gdut.edu.cn
1004-0609(2016)-10-2238-08
Q935
A
广东省自然科学基金资助项目(2015A030308008,2015A030310143);广东省科技计划资助项目(2016A040403068);佛山市科技创新项目资助(2016AG100482)
2015-11-10;
2016-04-18
孙水裕,教授,博士;电话:020-39322037;E-mail: sysun@gdut.edu.cn
