乙二醇为还原剂制备铁掺杂二氧化锰及其电容特性研究
2016-10-13陈俊明马莹莹王桂玲过家好汪徐春
陈俊明,岳 刚,马莹莹,王桂玲,姚 悦,过家好,汪徐春
(安徽科技学院化学与材料工程学院,凤阳 233100)
乙二醇为还原剂制备铁掺杂二氧化锰及其电容特性研究
陈俊明,岳刚,马莹莹,王桂玲,姚悦,过家好,汪徐春
(安徽科技学院化学与材料工程学院,凤阳233100)
通过简单的液相沉淀法制备出棉絮状二氧化锰纳米颗粒,采用掺杂铁离子的方式对二氧化锰进行改性。热重曲线显示,掺杂Fe之后增加了产物中结合水的含量。由SEM可知,加入铁离子之后并没有改变二氧化锰的表面形貌,XRD与面扫结果表明铁离子以均一的方式掺杂到了二氧化锰中。循环伏安与恒电流充放电测试了材料的电化学性能,结果显示当掺杂量为2%时材料具有最好的电化学性能,担载量为3 mg·cm-2的情况下,放电比容量高达347.0 F·g-1,循环1000圈后容量的保持率为81.4%。
二氧化锰; 液相沉淀; 铁掺杂; 超级电容器
1 引 言
因超级电容器具有功率密度高,循环寿命长,可逆性好等诸多优点,近来受到了广泛的关注[1,2]。按照能量储存机制,超级电容器分为双电层电容器和赝电容器两种类型。双电层电容器因为其存储方式仅仅是双电层存储,而赝电容器存储方式是双电层与表面法拉第反应两种类型,所以赝电容器与双电层电容器相比具有更高的能量密度,因而具有更优异的电化学性能[3]。对于赝电容器材料来说,二氧化锰因其具有高的理论比容量,价格低廉,环境友好,来源丰富等诸多优点,成为最具有发展前途的赝电容材料[4]。但是由于二氧化锰的刚性结构以及低的电子导电性,使得二氧化锰实际比容量远远低于理论值。为了克服这些缺点,研究者们进行了大量的研究工作来引进导电材料提高导电性,像引入导电聚合物[5],碳材料[6],等。但是引进的导电材料很难进入二氧化锰的结构内部,所以说导电性的提高仅仅在界面处。为了提高二氧化锰的电化学利用率,掺杂金属离子是一个非常有效的方法。掺杂金属离子可以改变二氧化锰的电子结构从而从根本上提高二氧化锰的导电性能[7,8]。在本实验中,我们以高锰酸钾为氧化剂,乙二醇为还原剂,通过简单的液相沉淀法[9,10]制备了棉絮状二氧化锰纳米颗粒,并通过铁掺杂的方式提高了二氧化锰的电化学性能。差热结果显示铁的掺杂影响了产物中结合水的含量,从而最终影响了材料的电化学性能。
2 实 验
2.1纳米二氧化锰材料的制备
纳米二氧化锰采用液相沉淀法制备。首先,将0.01 mol KMnO4加入到200 mL的去离子水中,并在常温下磁力搅拌使其完全溶解。接着,在高锰酸钾溶液中加入不同摩尔比率的FeSO4(与KMnO4相比分别为0%, 1.0%,1.5%, 2.0%, 3.0%, 4.0%),为方便起见,分别将样品记为Mn-Fe-0.0,Mn-Fe-1.0,Mn-Fe-1.5,Mn-Fe-2.0,Mn-Fe-3.0,Mn-Fe-4.0。最后再加入0.04 mol的乙二醇溶液,磁力搅拌120 min。然后将生成的浑浊溶液在室温下老化12 h,最后将沉淀过滤,在80 ℃的鼓风干燥箱中烘干,将干燥后的样品研磨,备用。
2.2电极制备和电化学性能测试
将活性物质(二氧化锰)、乙炔黑、PTFE(60%)按质量比80∶15∶5混合,加入小烧杯中,再加入少量无水乙醇,超声震荡直至混合均匀,再在80 ℃的水浴中微沸破乳,直至成粘稠状。将糊状物涂抹在1 cm×1 cm的泡沫镍极片上,80 ℃的烘箱中烘干12 h。用粉末压片机在2 MPa的压力下将极片压成2 mm的薄片,最后再将称取活性物质的质量,将极片浸泡在6 mol·L-1的KOH溶液中12 h。对电极的制备工艺与研究电极的制备工艺类似,步骤如下,将活性炭、乙炔黑、PTFE按质量比80∶15∶5混合,最后将糊状物涂覆在2.5 cm×2.5 cm的泡沫镍上。本课题采用模拟电池来测试锰氧化物的电化学活性,以活性碳电极为对电极,Hg/HgO电极为参比电极电极,6 mol·L-1的KOH溶液为电解液,进行电化学测试。循环伏安及交流阻抗测试所用仪器为CHI660E,电化学容量测试采用新威测试系统。
3 结果与讨论
图1是掺杂铁前后产物的热量变化曲线,通过图我们可以看到,掺杂前后的样品在460 ℃附近都有一个放热峰,这是由于氧的吸附所导致的[11]。但是两者又有不同,掺杂铁以后在200 ℃附近有一个尖锐的放热峰,这是由于晶格内结合水的失去所造成的,但是掺杂之前并没有明显的放热峰,这说明了掺杂铁之后产品的结合水增多了,而结合水的引入能够加快离子在电极材料内部的迁移[12],从而提高电容器的电化学性能。

图1 Mn-Fe-0.0与Mn-Fe-2.0的DTA图像 Fig.1 DTA image of Mn-Fe-0.0 and Mn-Fe-2.0
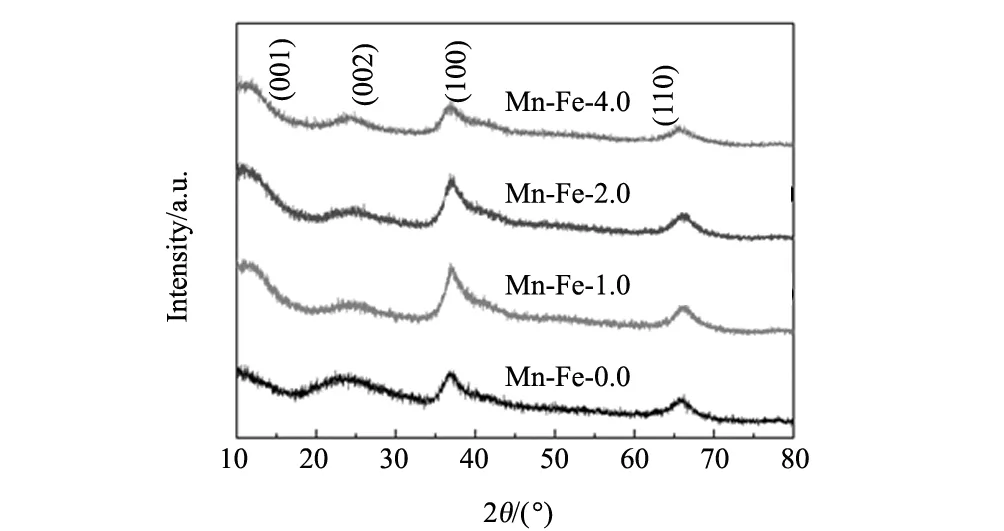
图2 不同铁掺杂量下样品的XRD图谱 Fig.2 XRD patterns of different iron doped
不同铁掺杂量下的XRD测试图谱如图2所示。由图2可知,在2θ为11.7°、22.4°、37.1°、65.7°分别对应着δ-MnO2(JCPDS 18-0802)的(001),(002),(100),(110)晶面。所有的样品均没有铁及其化合物的衍射峰出现,这可能是由于铁掺杂进入δ-MnO2内部,并没有单独成相,并且所有的衍射峰比较宽,说明合成材料结晶性比较差。这种弱晶结构与颗粒的大小有着直接的关系,因为固体表面通常不是理想的晶面,而是有台阶、裂隙、位错等,并且低温下生成的锰氧化物存在着大量的结合水,这也就使得材料的晶体结构特征不明显。
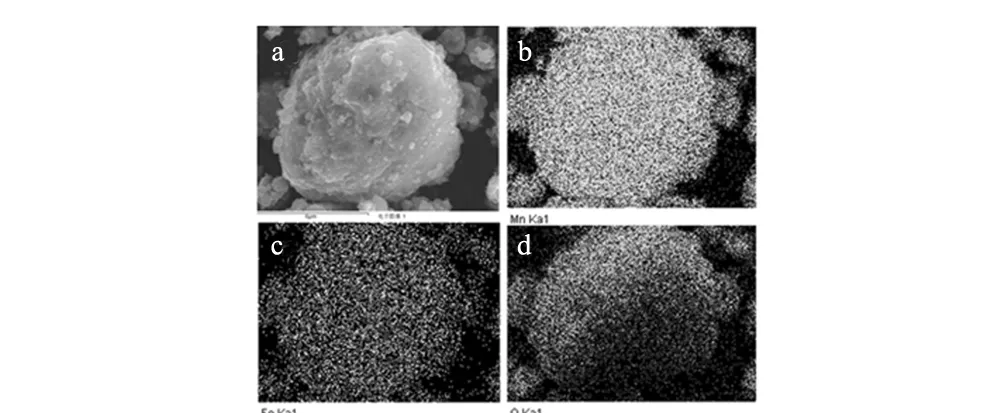
图3 Mn-Fe-2.0的面分布图像Fig.3 Plane distribution image of Mn-Fe-2.0
图3是Mn-Fe-2.0的面分布图谱,由图可以看到生成的样品中确实有铁元素存在,并且以均一的形式存在于生成物中,结合XRD图谱我们不难得出铁元素以均一的形式掺杂到二氧化锰结构中,形成了均一产物。
图4a, 4b分别为Mn-Fe-0.0与Mn-Fe-2.0的SEM图谱,由图我们可以看到掺杂铁之后样品的形貌并没有太大的变化,均是由纳米颗粒构成,由图4b我们可知,掺杂铁后纳米颗粒的大小约为50 nm。为了更进一步的观察产品的结构,我们采用了TEM测试,通过不同倍数下的TEM图像(图5)我们可以看到纳米二氧化锰并不是实心的颗粒,而是棉絮状结构,这种棉絮状的结构使得材料表面有更多的孔道,使得电解液的渗透更加容易,从而能够增加活性物质的利用率,材料的电化学性能也会相应的提高。

图4 Mn-Fe-0.0与Mn-Fe-2.0的SEM图像Fig.4 SEM images of Mn-Fe-0.0 and Mn-Fe-2.0

图5 Mn-Fe-2.0的TEM图像Fig.5 TEM images of Mn-Fe-2.0
图6是在5 mV·s-1的扫描速度下不同铁掺杂量的循环伏安曲线,其中扫描范围为0~0.55 V,活性物质的质量约为3 mg。从图可以看出,在0.42~0.46 V范围内有一个小的氧化峰,在0.3~0.36 V内有一个小的还原峰,这对应着这种物质是钾取代水钠锰矿[13,14],所有的曲线均没有其他的氧化还原峰,矩形特征良好,尤其是铁掺杂量为2%时,循环伏安曲线具有最大的i-V响应值,这说明当掺杂量为2%时,有最大的比容量。经过计算在5 mV·s-1的扫描速度下Mn-Fe-2.0的放电比容量为458.1 F·g-1,这与材料内部大量结合水的存在是分不开的。
图7是不同铁掺杂量下样品放电100圈后的放电比容量比较图,通过图我们知道当铁的掺杂量为2%时,产品具有最高的放电比容量。图8是电流密度为1 A·g-1的情况下,Mn-Fe-0.0与Mn-Fe-2.0的循环稳定性曲线。在电化学循环的前几圈,Mn-Fe-2.0的放电比容量由347.0降低到了314.6 F·g-1。这是由于二氧化锰的隧道结构由水分子以及K+等阳离子支撑隧道结构,当进行电化学循环的过程中,可能由于隧道结构中的离子的脱出导致了部分结构的坍塌,最终导致了比容量的衰减。继续循环至1000圈,比容量仍能维持在282.4 F·g-1。并且产品的库仑效率一直保持在100%左右,说明了活性物质具有较高的可逆性。
阻抗谱是一种已被广泛应用而且越来越重要的分析超级电容器电化学特征的一项电化学技术。图9是Mn-Fe-0.0,Mn-Fe-2.0和Mn-Fe-4.0的复平面阻抗图,即能斯特图。通过图9插图可以看到在高频区的半圆部分,所有样品的溶液电阻Ru大致不变,大约为0.46 Ω。掺杂Fe后高频区的半圆直径变小,说明掺杂Fe后材料与电解液之间的电荷转移电阻变小。在低频区的直线部分我们可以看到,Mn-Fe-2.0具有更大的斜率,更高的斜率对应着更快的离子反应时间。Mn-Fe-2.0的斜率最大,这说明其具有更好的电容特性以及更小的离子扩散阻力。
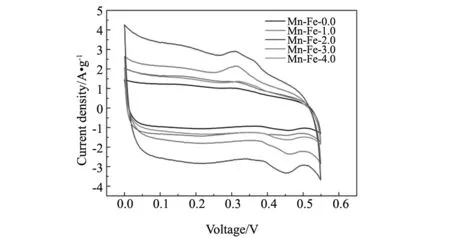
图6 不同铁掺杂量下样品的CV曲线(扫描速率为5 mV·s-1) Fig.6 CV curves of different iron doped
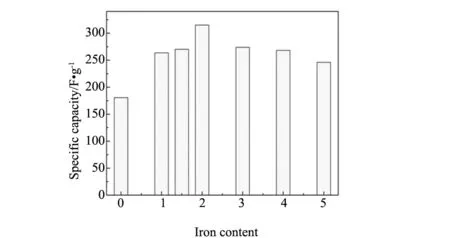
图7 不同铁掺杂量下产品的放电比容量比较图 Fig.7 Discharge specific capacity comparison chart of different iron doped
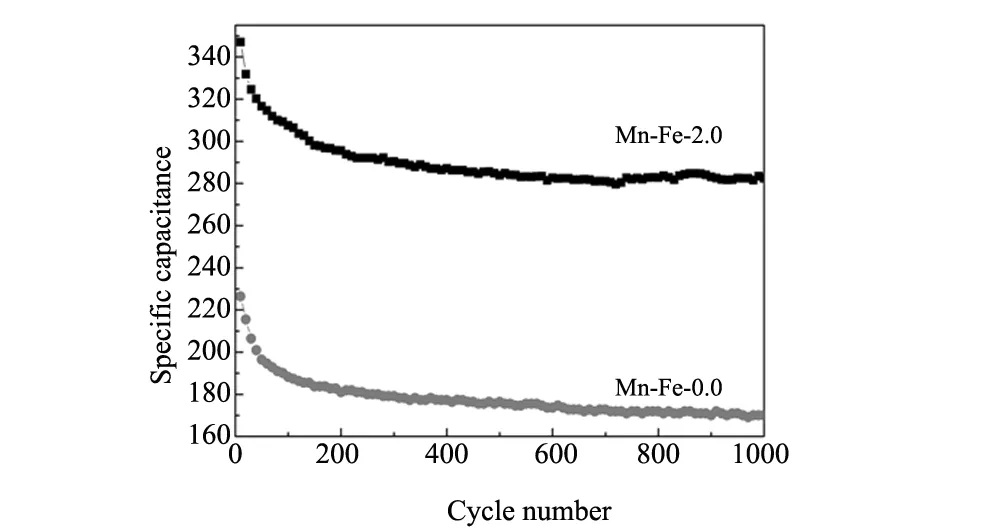
图8 不同铁掺杂量下循环稳定性的比较图Fig.8 Comparison of cycle stability under different iron doped
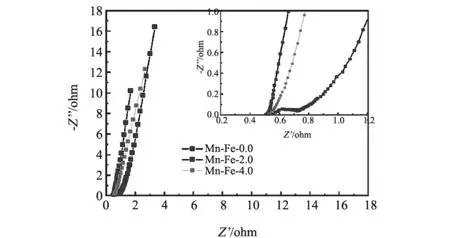
图9 不同铁掺杂量下材料的EIS图谱Fig.9 EIS image of different iron doped
4 结 论
本文采用简单的液相沉淀法制备出棉絮状铁掺杂的二氧化锰纳米颗粒,通过XRD、SEM、TEM等方法表征了其组成、结构和形态。差热结果表明铁的掺杂增加了产品中结合水的含量。恒电流和循环伏安测试表明,当铁的掺杂量为2%时,产品具有最高的放电比容量,当扫描速度为5 mV s-1时,Mn-Fe-2.0的放电比容量为458.1 F·g-1。在电流密度为1 A·g-1的情况下放电,初始比容量为347.0 F·g-1,经过1000圈的循环,比容量仍能维持在282.4 F·g-1,容量的保持率为81.4%,说明铁掺杂后产物比较适合作为超级电容器材料。
[1] Zhou M L,Chai H,Jia D Z,et al.The glucose-assisted synthesis of a graphene nanosheet-NiO composite for high-performance supercapacitors[J].NewJournalofChemistry,2014,38(6):2320-2326.
[2] Zhang Y Q,Xia X H,Tu J P,et al.Self-assembled synthesis of hierarchically porous NiO film and its application for electrochemical capacitors[J].JournalofPowerSources,2011,199(1):413-417.
[3] Simon p,Gogotsi Y,Dunn B.Where do batteries end and supercapacitor begin[J].Science,2014,343:1210-1211.
[4] Jonathon D,Stefanie A S,Zhe G,et al.Self-limiting electrodeposition of hierarchical MnO2and M(OH)2/MnO2nanofibril/nanowires:Mechanism and supercapacitor properties[J].ACSNano,2013,7(2):1200-1214.
[5] 殷金玲,李一栋.导电聚合物复合材料作为超级电容器电极材料[J].化学工程师,2011,(07):42-44,47.
[6] 田艳红,付旭涛,吴伯荣.超级电容器用多孔碳材料的研究进展[J].电源技术,2002,(06):466-469,479.
[7] Dong R,Ye Q,Kuang L,et al.Enhanced supercapacitor performance of Mn3O4nanocrystals by doping transition-metal ions[J].ACSAppl.Mater.Interfaces,2013,5 (19),9508-9516.
[8] 秦继伟.铁掺杂纳米二氧化锰的制备及其电化学性能[D].大连:大连理工大学硕士学位论文,2012.
[9] 韩静香,佘利娟,翟立新,等.化学沉淀法制备纳米二氧化硅[J].硅酸盐通报,2010,29(3):681-685.
[10] 张孟,朱协彬,陈海清,等.液相沉淀法制备的棒状α-MnO2研究[J].河南工程学院学报(自然科学版),2014,(01):44-48.
[11] Ragupathy P,Park D H,Campet G,et al.Remarkable capacity retention of nanostructured manganese oxide upon cycling as an electrode material for supercapacitor[J].JournalofPhysicsChemistryC,2009,113:6303-6309.
[12] Zheng J P,Cygan P J,Row T R.Hydrous ruthenium oxide as an electrode material for electrochemical capacitors[J].JournalElectrochemistrySociety,1995,142:2699-2703.
[13] Kanoh H,Tang W,Makita Y,et al.Electrochemical intercalation of alkali-metal ions into birnessite-type manganese oxide in aqueous solution[J].Langmuir,1997,13:6845-6849.
[14] Athouёl L,Moser F.Variation of the MnO2birnessite structure upon charge/discharge in an electrochemical supercapacitor electrode in aqueous Na2SO4electrolyte[J].JournalofPhysicsChemistryC,2008,112:7270-7277.
Enhanced Electrochemical Properties of Fe-doped Manganese Oxides Synthesized Using Glocol as Reductant
CHENJun-ming,YUEGang,MAYing-ying,WANGGui-ling,YAOYue,GUOJia-hao,WANGXu-chun
(College of Chemical and Materials Engineering,University of Science and Technology of Anhui,Fengyang 233100,China)
A simple liquid-phase process for the fabrication of iron doped manganese oxides nanoparticles was developed by using potassium permanganate as the source of manganese, glycol as reducing agent and iron ion as dopant. Differential thermal analyzer shows that the bound water content increasing with the addition of iron. XRD and Mapping suggest that iron ion has been doped into manganese oxides. the electrochemical properties of the prepared materials are studied using cyclic voltammetry (CV) and galvanostatic charge-discharge test in aqueous electrolyte. The product of Mn-Fe-2.0 shows a very high specific capacity of 347.0 F g-1 and retain 81.4% after 1000 cycles.
manganese oxides;liquid-phase method;iron doped;supercapacitor
安徽省人才基金(gxfxZD2016176);安徽省自然科学重点基金(KJ2013A079);材料科学与工程重点学科(AKZDXK2015A01);安徽高校自然科学研究项目(KJ2016A171);安徽科技学院大学生创新创业训练计划项目(16XCX35)资助;安徽科技学院自然科学研究项目(ZRC2016486)
陈俊明(1977-),硕士,讲师.主要研究方向为纳米材料和电化学方面的研究.
汪徐春,博士,教授.
O0646
A
1001-1625(2016)06-1873-04
