介孔Cr(OH)3的制备及其对钒(Ⅴ)离子的吸附性能
2016-10-13李华琳雒敏婷张红玲石义朗张炳烛蔡再华徐红彬张懿
李华琳,雒敏婷,张红玲,石义朗,张炳烛,蔡再华,徐红彬,张懿
介孔Cr(OH)3的制备及其对钒(Ⅴ)离子的吸附性能
李华琳1,2,3,雒敏婷2,3,张红玲2,3,石义朗4,张炳烛1,蔡再华4,徐红彬2,3,张懿2,3
(1河北科技大学化学与制药工程学院,河北石家庄 050018;2中国科学院过程工程研究所湿法冶金清洁生产技术国家工程实验室,北京 100190;3中国科学院绿色过程与工程重点实验室,北京 100190;4湖北振华化学股份有限公司,湖北黄石 435001)
以CrCl3·6H2O作为铬源,通过添加强碱制备出大比表面积(312.70 m2·g-1)、高孔隙率(0.48 cm3·g-1)的介孔Cr(OH)3,并研究了其对溶液中钒(V)离子的吸附性能,考察了溶液pH、吸附剂用量、吸附温度、吸附时间等条件对吸附效果的影响。结果表明,当溶液pH在2.0~9.0、钒离子浓度为100~500 mg·L-1时,采用该吸附剂均可实现溶液中钒离子的高效去除。在最优实验条件下,钒去除率接近100%,钒离子浓度可由500 mg·L-1降至0.81 mg·L-1。吸附热力学的研究结果表明,Cr(OH)3对钒离子的吸附过程遵循Langmuir等温吸附;吸附过程符合拟二级反应动力学方程,反应级数为拟二级。
Cr(OH)3;介孔;粉体;吸附;废水;除钒
引 言
铬铁矿大都伴生一定量的钒,因而,在以铬铁矿为原料生产铬盐产品时,所得到的铬盐溶液中常会混有钒杂质,该钒杂质会严重影响铬盐产品的性能,需要进行除钒处理。以无钙焙烧为例,所得铬酸钠中性液中钒浓度(以V5+计,下同)高达几百甚至上千毫克/升。为满足后续铬盐产品的生产要求,需要将其中的钒降低至小于45 mg·L-1甚至更低[1]。另一方面,钒作为一种重要的合金元素,广泛用于钢铁、化工、陶瓷、航空、火箭、原子反应堆中,并且在生物制药和钒电池等领域也有新的应用进展[2-3]。随着钒及其化合物应用领域和市场需求的不断扩大,钒工业迅速发展,由此产生的含钒废水数量和种类也越来越多,其中钒离子浓度一般在40~200 mg·L-1[4-5],大部分为酸性;高浓度含钒碱性废水也有报道[6-7]。含钒废水不仅破坏生态环境,对人体也有极大的危害[8],必须处理达标后才可排放。因此,含钒溶液中钒的去除具有重要意义。
去除溶液中钒的方法大致可分为3类:生物法、化学法和物理法[8-9]。生物法成本低且无二次污染,是一种较为理想的方法,但是目前仍处于实验室研究阶段,实际应用难度较大;化学法处理含钒废水,由于其处理产物难于分离,很难进行钒的回收和循环利用,势必造成资源的浪费;物理法主要是离子交换法和吸附法[3,9],离子交换法因其成本较高使其应用受到了制约,吸附法是目前应用较多的一种方法[10-11],由于其操作方便,并且可实现钒离子的回收再利用而被广泛认可[12-16]。然而,目前所报道的吸附剂大都只能处理较低浓度的含钒溶液,且存在对含钒溶液pH范围要求苛刻、处理后钒浓度达不到钒工业污染物国家排放标准[17]、寿命短等问题。例如,Naeem等[13]研究了以二氧化钛和铁为基础的金属氧化物吸附钒,可有效处理浓度为50 mg·L-1的钒溶液;司士辉等[14]研究了硫酸亚铁改性沸石对钒的吸附,当钒溶液初始浓度为50 mg·L-1时,去除率为92%;用树脂作为吸附材料吸附溶液中钒的研究也有报道[3,15-16],该法对所处理的含钒溶液的pH要求严格,仅可在溶液pH约2.0时取得较好的吸附效果。
为实现较高浓度含钒溶液中钒的高效去除,本文选择氢氧化物Cr(OH)3作为吸附剂,通过调控制备条件得到在酸、碱条件下稳定、比表面积大的介孔Cr(OH)3,并研究了其对钒离子的吸附性能,考察了pH、吸附剂用量、温度、时间等因素对静态吸附钒的影响,研究了吸附钒的热力学与动力学过程。
1 实验部分
1.1 仪器与试剂
主要仪器:ML104/02电子分析天平(梅特勒-托利多仪器(上海)有限公司)、实验室pH计FE20(梅特勒-托利多仪器(上海)有限公司)、DF-101S智能集热式恒温磁力搅拌器、冷冻干燥机(北京博医康实验仪器有限公司)、HZ-9612高温振荡培养箱(太仓市科教器材厂)。
主要试剂:六水合氯化铬、氢氧化钠、盐酸、偏钒酸钠等均为分析纯。
1.2 Cr(OH)3的制备
采用CrCl3·6H2O作为铬源,通过添加强碱制备Cr(OH)3。配制0.25 mol·L-1的CrCl3·6H2O溶液与0.75 mol·L-1的NaOH溶液,在搅拌条件下向CrCl3·6H2O溶液中逐滴加入NaOH溶液,加热至100℃,控制终点pH为7.0,陈化3.5 h,过滤、洗脱可溶性盐,将滤饼置于-60℃的冷冻干燥机中干燥后,得到Cr(OH)3粉体。
1.3 钒溶液的配制
称取一定量的NaVO3·2H2O配制成钒溶液,调至所需的浓度及酸度备用。
1.4 实验方法
取一定体积的钒溶液,调至所需的pH,置于50 ml的吸附瓶中,加入Cr(OH)3,放入180 r·min-1的高温振荡培养箱中振荡一段时间,过滤,分析。去除率和吸附量的计算式如下
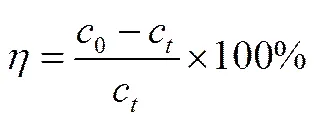

1.5 分析方法
吸附剂的物相分析采用X射线衍射(XRD)仪(荷兰Empyrean);形貌分析采用热场发射扫描电子显微镜(SEM)(日本JSM-7610F);比表面及孔径分析采用物理化学吸附仪(美国NOVA3200e);钒离子的浓度分析采用Optima 5300DV电感耦合等离子体原子发射光谱仪(美国Pekin-Elmer)。
2 结果与讨论
2.1 吸附剂表征
制备所得样品的红外光谱如图1所示。在400~800 cm-1处对应的吸收峰为CrO的晶格振动;在950 cm-1处的峰位对应着CrOH的弯曲振动;在1650、1510、1335 cm-1处的峰位对应Cr(OH)3的峰位[18];在2420 cm-1处的峰位属于非游离水分子的弯曲振动;在3500 cm-1处出现了解离化学水产生的羟基伸缩振动吸收峰。由此可说明该产品为Cr(OH)3。
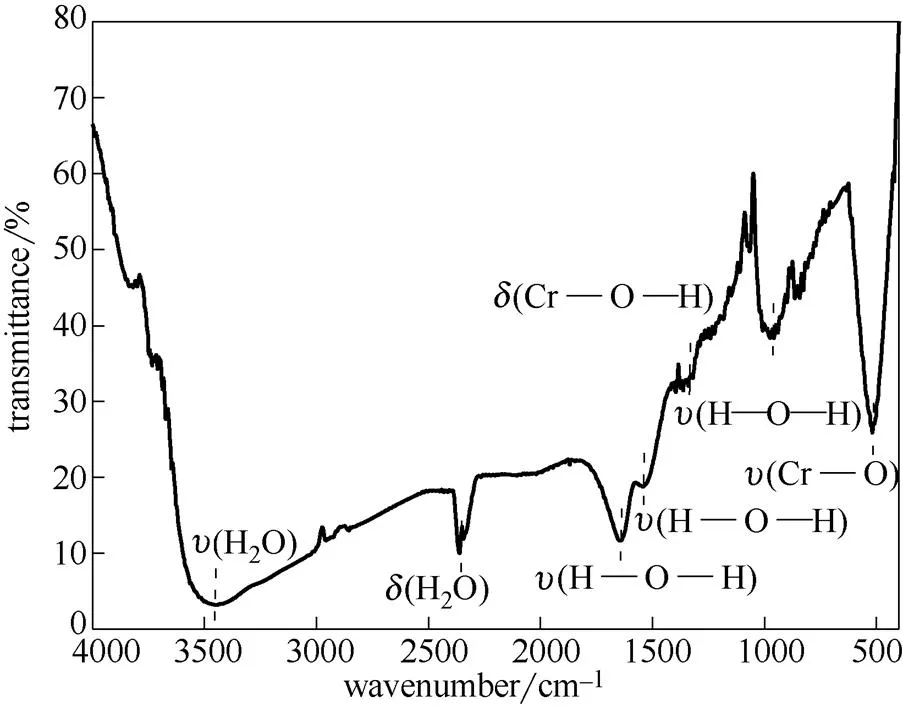
图1 样品的红外光谱
图2(a)、(b)分别为制备的Cr(OH)3粉体的XRD图谱与SEM照片。如图2(a)所示,图中并未观察到明显的衍射峰,说明此法制备出的Cr(OH)3为无定形状态。图2(b)所示Cr(OH)3的SEM图中,颗粒间表现出疏松状态,并未出现明显的团聚现象,可能正是这种疏松的形态使之成为了良好的吸附剂。
为了确定Cr(OH)3的比表面积与孔径大小,对其N2吸附/脱附曲线进行了检测。图3(a)、(b)分别展示了Cr(OH)3对N2的吸附脱附曲线与孔径分布。经过测试,该Cr(OH)3的比表面积为312.70 m2·g-1,孔体积为0.48 cm3·g-1。如图3(a)所示,该等温线出现了明显的滞后环,表明该样品在N2的吸附/脱附过程中产生了毛细凝聚现象,说明该样品中应含有介孔与微孔。图3(b)中孔径分布曲线表现出的峰主要分布于7~20 nm之间,表明该Cr(OH)3的孔结构属于典型的介孔结构。

图2 Cr(OH)3的XRD谱图(a)与SEM图(b)
2.2 溶液pH对吸附效果的影响
称取0.2 g的Cr(OH)3,分别取13份不同浓度的钒溶液各20 ml,调节溶液的pH1.0~13.0,温度25℃,在该实验条件下进行静态吸附24.0 h,钒溶液的pH对吸附效果的影响见图4。
由图4可知,pH对Cr(OH)3吸附钒的影响明显:当溶液pH1.0时,去除率较低,起始浓度为500 mg·L-1时去除率仅为58.3%;在pH≥10.0时,随pH的增大去除率急剧降低;当pH为2.0~9.0时,不同起始浓度钒溶液中钒的去除率均在95%以上。该pH及浓度范围优于目前所报道的大多数研究结果[1-3,15-16]。钒溶液中钒离子的存在状态与钒溶液的浓度和pH有关,根据已有文献报道,溶液pH为2.0~9.0时,钒离子的存在状态为、、、[15-16]。发生吸附的原因可能是由于Cr(OH)3本身的正电荷与钒负离子产生了静电吸引,而随着pH的升高,OH-与钒负离子产生了电荷竞争,从而导致钒去除率下降。为方便起见,后续实验均在中性pH7.0条件下进行,以500 mg·L-1的钒溶液为起始溶液。
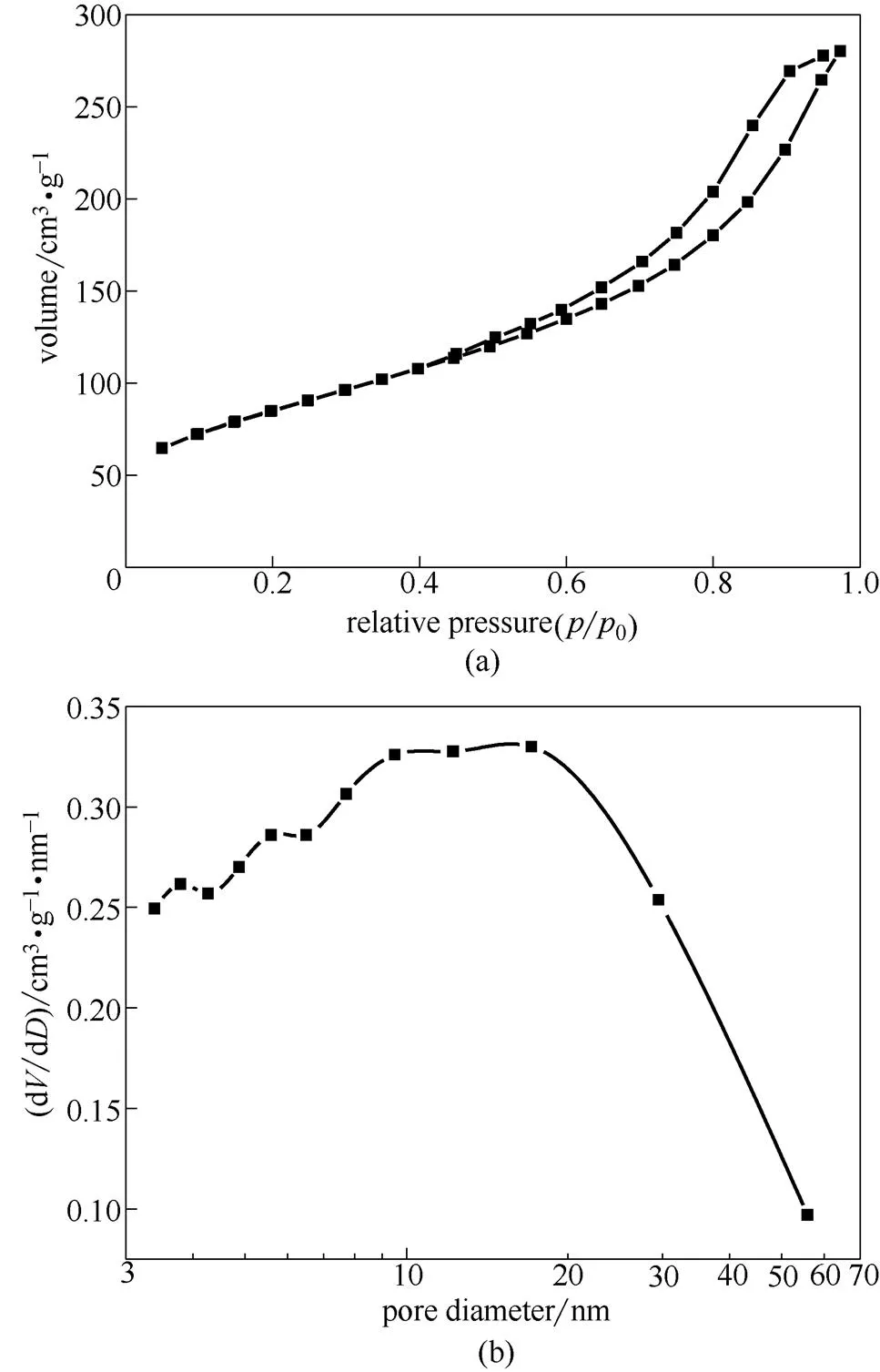
图3 Cr(OH)3的N2吸附/脱附等温线(a)与孔径大小分布(b)

图4 pH对钒吸附效果的影响
2.3 吸附剂用量对吸附效果的影响
根据溶液中钒离子的质量,选取一系列摩尔比例的吸附剂作为参考投加量,即:,在溶液pH为7.0,温度为25℃的条件下进行静态吸附24 h,Cr(OH)3对钒的去除率随其摩尔比的变化如图5所示。

图5 吸附剂用量对钒吸附效果的影响
由图5 可知,Cr(OH)3对钒的去除率随其摩尔比的增大而增大,当摩尔比大于14.85时,去除率几乎接近100%。表明随着吸附剂用量的增大,所提供的吸附位点逐渐增多,此时去除效果逐渐明显,当吸附位点数量达到饱和时,继续增加吸附位点,去除率基本保持不变。为了使Cr(OH)3能够提供较充分的吸附位点进而保证钒离子较高的去除率,最终确定吸附剂的用量投料摩尔比为:。
2.4 温度对吸附效果的影响
在溶液 pH为7.0,吸附剂用量摩尔比为14.85,吸附时间为24.0 h的条件下,考察Cr(OH)3对钒的吸附量随温度的变化趋势,结果见图6。

图6 温度对钒吸附效果的影响
由图6可知,当温度由25℃升到30℃时,Cr(OH)3对钒的吸附量稍有增大,这与Li等[12]的研究结果一致。当温度高于30℃时,吸附量稍有增大但变化不明显,说明该吸附反应属于吸热反应,此时吸附量均维持在32.60 mg·g-1左右,钒离子去除率均已接近100%。说明升高温度有助于吸附的进行,可能是因为温度升高,使Cr(OH)3颗粒孔隙变大,增加了Cr(OH)3表面活性位点的数量;也可能是因为温度升高,加快了分子运动速率,加快了传质速率。当达到一定温度时,Cr(OH)3表面活性位点已达到饱和,或者分子运动速率已基本达到极大值点,此时吸附量增加趋势减弱。
2.5 吸附动力学研究
吸附动力学的研究主要是用来描述吸附速率的快慢,通过动力学模型对数据进行拟合,进而推断其吸附机理。分别取0.3 g Cr(OH)3于一系列吸附瓶中,加入钒溶液各20 ml,溶液 pH为7.0,在温度为25℃的条件下进行静态吸附实验,吸附量随时间的变化见图7。
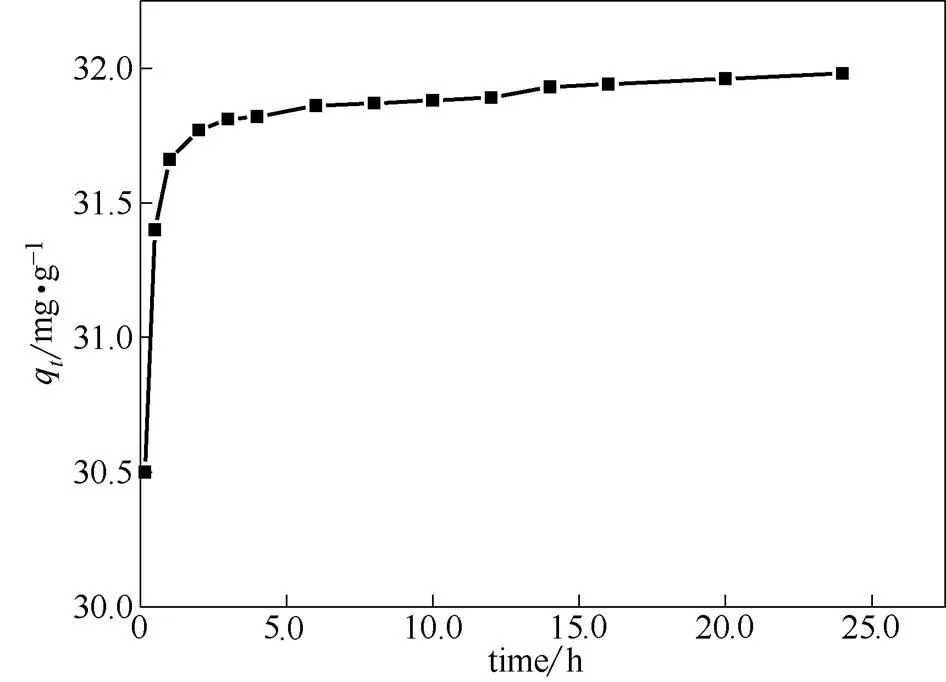
图7 吸附时间对钒吸附效果的影响
由图7可知,该吸附过程可分为3个阶段:0~2.0 h以内为快速吸附阶段,此时溶液中的钒离子浓度较高,Cr(OH)3表面活性位点较多,钒离子与吸附位点快速结合,导致吸附量快速增大;2.0~14.0 h为慢速吸附阶段,此时溶液中钒离子浓度降低,Cr(OH)3表面活性位点减少,吸附推动力减弱,所以吸附量随时间延长增大较慢;14.0~24.0 h为吸附平衡阶段,随时间的增加,吸附量变化不明显,表明当吸附时间达到14.0 h后,Cr(OH)3对钒的吸附基本达到饱和,此时,溶液的钒浓度已降低至0.81 mg·L-1,已低于钒工业污染物国家排放标准所规定的1.0 mg·L-1[17]。该结果明显优于李凌璞等[19-20]所采用的改性沸石与氯化铵去除钒离子的研究结果。
将以上数据分别进行拟一级动力学方程和拟二级动力学方程拟合处理,结果见图8,具体拟合数值见表1。

图 8 不同的动力学模型对Cr(OH)3吸附钒的拟合

表1 拟一级动力学方程和拟二级动力学方程的速率常数及qe的计算值
拟一级动力学方程

式中,e为平衡吸附量,mg·g-1;q为时刻的吸附量,mg·g-1;1为拟一级反应速率常数。
拟二级动力学方程
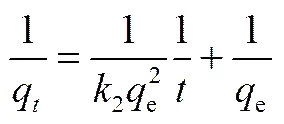
由图8和表1可以看出,Cr(OH)3对钒的吸附符合拟二级动力学方程,与高峰等[21]的研究结果一致,表明Cr(OH)3对钒的吸附主要是以化学吸附过程为主,反应级数为拟二级,由此方程计算出的理论吸附量为31.92 mg·g-1。

表2 Cr(OH)3吸附钒的Langmuir和Freundlich等温吸附模型常数及相关性
2.6 吸附热力学研究
为进一步研究Cr(OH)3对钒(Ⅴ)的吸附特性,对其热力学性能进行了研究。取5份0.3 g Cr(OH)3于吸附瓶中,分别加入浓度为100、200、300、400、500 mg·L-1的钒溶液各20 ml,溶液pH为7.0,在温度为25℃的条件下进行静态吸附,根据测定的平衡浓度e计算出相应的吸附量e。
将数据分别进行Langmuir单分子层等温吸附方程与Freundlich多分子层等温吸附方程拟合处理[22],结果见表2。
Langmuir吸附等温式

Freundlich吸附等温式
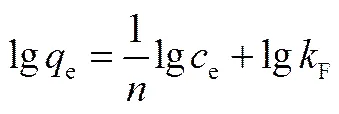
由表2可知,Langmuir等温吸附方程能够较好地描述Cr(OH)3对钒的吸附过程,说明该吸附过程以单分子层吸附为主,由该方程计算出的最大理论吸附量为29.51 mg·g-1;一般认为,在Freundlich等温吸附方程中,易于吸附,时难以吸附[12,23],由表2数据可知,处于0.30~0.40之间,表明Cr(OH)3对钒离子的吸附容易进行。
2.7 水中共存离子的影响
在实际水处理过程中,水体中会有多种杂质干扰,为此,采用模拟液进一步验证Cr(OH)3对钒(Ⅴ)吸附的高效性。目前国内采用钠化焙烧—水浸—酸性铵盐沉钒工艺所产生的含钒废水的主要成分见表3[4]。
参照以上数据,配制出具有相同组分的含钒废水模拟液,其中V5+500 mg·L-1,Cr6+50 mg·L-1,SiO2250 mg·L-1,Fe 3 mg·L-1,Ca 100 mg·L-1,Na2SO450000 mg·L-1,(NH4)2SO420000 mg·L-1,在2.2~2.5节确定的最佳实验条件下进行吸附实验。在3次实验结果中,吸附后溶液中钒离子的剩余浓度分别为:0.60、0.95、0.85mg·L-1;钒离子去除率分别为99.88%、99.81%、99.83%。结果表明,废水中的多种杂质并未对Cr(OH)3的除钒效率造成较大影响。

表3 含钒废水主要成分
3 结 论
(1)以CrCl3·6H2O作为铬源,添加强碱的方法制备得到了介孔Cr(OH)3,该Cr(OH)3具有较大的比表面积,孔径分布属于介孔结构,在较宽的pH范围(2.0~9.0)内对起始浓度为100~500 mg·L-1的含钒溶液中的钒离子均具有较好的吸附作用。
(2)以介孔Cr(OH)3为吸附剂吸附500 mg·L-1含钒溶液中钒离子的适宜条件为:吸附剂的用量与溶液中的钒离子的摩尔比为14.85(:),吸附时间为14.0 h,吸附温度为30℃。经该条件处理后的溶液钒浓度达到国家规定的排放标准。
(3)介孔Cr(OH)3对钒的吸附过程遵循Langmuir等温吸附方程,说明该吸附过程以单分子层吸附为主。动力学的研究结果表明,该吸附过程符合拟二级动力学方程,由该方程计算出的平衡吸附量为31.92 mg·g-1。
[1] 杨德军, 王少娜, 陈晓芳, 等. 铬盐无钙焙烧工艺铬酸钠中性液铁盐除钒 [J]. 中国有色金属学报, 2014, 24 (1): 279-285. YANG D J, WANG S N, CHEN X F,. Removing vanadium from sodium chromate neutral liquid by non-calcium roasting technology with chromium salt [J]. The Chinese Journal of Nonferrous Metals, 2014, 24 (1): 279-285.
[2] 罗南, 刘波, 李国良, 等. 活性氢氧化铁处理含钒(Ⅴ)废水的研究 [J]. 四川环境, 1989, 8 (1): 39-48. LUO N, LIU B, LI G L,. Study on disposal of wastewater vanadium (Ⅴ) containing by active iron hydroxide [J]. Sichuan Environment, 1989, 8 (1): 39-48.
[3] 万洪强, 宁顺明. 离子交换树脂吸附钒的动力学研究 [J]. 矿冶工程, 2010, 30 (4): 73-76. WAN H Q, NING S M. Kinetics study on adsorption of vanadium by ion-exchange resin [J]. Mining and Metallurgical Engineering, 2010, 30 (4): 73-76.
[4] 张清明, 艾南山, 徐帅, 等. 含钒废水的处理现状及发展趋势 [J].科技情报开发与经济, 2007, 17 (2): 142-143. ZHANG Q M, AI N S, XU S,. The present situation and developing trends of the treatment of vanadium containing wastewater [J]. Sci-Tech Information Development and Economy, 2007, 17 (2): 142-143.
[5] 赵坤. 离子交换树脂对钒(Ⅴ)离子的吸附行为及其应用[D]. 长沙: 中南大学, 2009. ZHAO K. Application and adsorption behavior of vanadium ions by ion-exchange resin [D]. Changsha: Central South University, 2009.
[6] 曾小明, 李凌璞, 舒晖, 等. 化学法处理高浓度含钒碱性工业废水 [J]. 工业水处理, 2009, 29 (7): 51-53. ZENG X M, LI L P, SHU H,. Chemical treatment of highly concentrated vanadium-containing industrial wastewater [J]. Industrial Water Treatment, 2009, 29 (7): 51-53.
[7] 李先荣, 陈宁, 董明甫, 等. 铬酸钠碱性液除钒工艺研究 [J]. 能源化工, 2015, 36 (1): 59-63. LI X R, CHEN N, DONG M F,. Research on removal process of vanadium impurity in sodium chromate alkaline solution [J]. Energy Chemical Industry, 2015, 36 (1): 59-63.
[8] 郑川立, 张红玲, 张炳烛, 等. 工业含钒废水处理工艺的研究进展 [J]. 化工环保, 2015, 35 (3): 247-252. ZHENG C L, ZHANG H L, ZHANG B Z,. Research progresses in treatment process of vanadium containing industrial wastewater [J]. Environmental Protection of Chemistry Industry, 2015, 35 (3): 247-252.
[9] 关洪亮, 操艳兰, 顾逸雅, 等. 硫酸亚铁沉淀法处理含钒废水 [J]. 武汉工程大学学报, 2012, 34 (12): 25-31. GUAN H L, CAO Y L, GU Y Y,. Precipitating treatment of vanadium contained wastewater by using ferrous sulfate [J]. J. Wuhan Inst. Tech., 2012, 34 (12): 25-31.
[10] BHATNAGAR A, MINOCHA A K, PUDASAINEE D,. Vanadium removal from water by waste metal sludge and cement immobilization [J]. Chemical Engineering Journal, 2008, 144: 197-204.
[11] NAMASIVAYAM C, SANGEETHA D. Removal and recovery of vanadium (Ⅴ) by adsorption onto ZnCl2activated carbon: kinetics and isotherms [J]. Adsorption, 2006, 12: 103-117.
[12] LI P, ZHENG S L, QING P H,. The vanadate adsorption on a mesoporous boehmite and its cleaner production application of chromate [J]. Green Chemistry, 2014, 16 (9): 4214-4222.
[13] NAEEM A, WESTERHOFF P, MUSTAFA S. Vanadium removal by metal (hydr)oxide adsorbents [J]. Water Research, 2007, 41: 1596-1602.
[14] 司士辉, 李凌璞, 王树国. 硫酸亚铁改性沸石对废水中钒(Ⅴ)的吸附研究 [J]. 黄石理工学院学报, 2009, 25 (3): 7-10. SI S H, LI L P, WANG S G. Study on adsorption of V(Ⅴ) from wastewater using zeolite modified by ferrous sulphate [J]. Journal of Huangshi Institute of Technology, 2009, 25 (3): 7-10.
[15] 冯其明, 孙健程, 张国范, 等. D201树脂吸附钒(Ⅴ)的过程 [J]. 有色金属, 2010, 62 (1): 73-75. FENG Q M, SUN J C, ZHANG G F,. Adsorption process of vanadium (Ⅴ) with D201 resin [J]. Nonferrous Metals, 2010, 62 (1): 73-75.
[16] 曾小明, 赵坤, 司士辉, 等. 312树脂吸附钒的行为研究 [J]. 稀有金属, 2009, 33 (3): 446-449.ZENG X M, ZHAO K, SI S H,. Adsorption of vanadium with 312 resin [J]. Chinese Journal of Rare Metals, 2009, 33 (3): 446-449.
[17] 中华人民共和国环境保护部, 国家质量监督检验检疫总局.钒工业污染物排放标准: GB 26452—2011 [S].北京: 中国环境科学出版社, 2011. Ministry of Environmental Protection of the People’s Republic of China, General Administration of Quality Supervision, Inspection and Quarantine of the People’s Republic of China. Discharge standard of pollutants for vanadium industry: GB 26452—2011 [S]. Beijing: Environmental Science Press of China, 2011.
[18] GIACOMELLI C E, AVENA M J, CAMARA O R,. Some physicochemical properties of the chromium (Ⅲ) hydrous oxide-aqueous solution interface [J]. Journal of Colloid and Interface Science, 1995, 169 (1): 149-160.
[19] 李凌璞. 含钒工业废水中钒的分离回收方法研究 [D]. 长沙: 中南大学, 2009. LI L P. Study on separation and recycling method of vanadium from industrial wastewater [D]. Changsha: Central South University, 2009.
[20] 关洪亮, 王杏林, 张璐, 等. 氯化铵处理含钒废水的研究 [J]. 环境科学与技术, 2014, 37 (5): 122-125. GUAN H L, WANG X L, ZHANG L,. Precipitating treatment of vanadium contained wastewater by using ammonia chloride [J]. Environmental Science and Technology, 2014, 37 (5): 122-125.
[21] 高峰, 颜文斌, 石美莲, 等. D201树脂吸附钒的静态性能及动力学研究 [J]. 应用化工, 2010, 39 (6): 806-811. GAO F, YAN W B, SHI M L,. Study on static adsorption properties and kinetics of vanadium for D201 resin [J]. Applied Chemical Industry, 2010, 39 (6): 806-811.
[22] 周学永, 周鑫. 由Langmuir方程计算标准平衡常数[J]. 大学化学, 2013, 28 (6): 50-53. ZHOU X Y, ZHOU X. Calculated standard constant by Langmuir equation [J]. University Chemistry, 2013, 28 (6): 50-53.
[23] 李小燕, 花明, 刘义保, 等. 改性玉米芯吸附溶液中U(Ⅵ) 的动力学和热力学 [J]. 化工学报, 2012, 63 (12): 4068-4074. LI X Y, HUA M, LIU Y B,. Kinetics and thermodynamics of U(Ⅵ) adsorption from aqueous solution by modified corncob [J]. CIESC Journal, 2012, 63 (12): 4068-4074.
Synthesis of mesoporous Cr(OH)3 and its adsorption of vanadium(Ⅴ) ion from V containing solution
LI Hualin1,2,3, LUO Minting2,3, ZHANG Hongling2,3, SHI Yilang4, ZHANG Bingzhu1, CAI Zaihua4, XU Hongbin2,3, ZHANG Yi2,3
(1School of Chemistry and Pharmaceutical Engineering, Hebei University of Science and Technology, Shijiazhuang 050018, Hebei, China; 2National Engineering Laboratory for Hydrometallurgical Cleaner Production Technology, Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China; 3Key Laboratory of Green Process and Engineering, Chinese Academy of Sciences, Beijing 100190, China; 4Hubei Zhenhua Chemical Co. Ltd., Huangshi 435001, Hubei, China)
Previous study have examined many materials to remove the vanadium ions from aqueous solution, but it is difficult to meet the national discharge standard. In this paper, a mesoporous chromium hydroxide (Cr(OH)3), which has a high specific surface area (312.70 m2·g-1) and a large pore volume (0.48 cm3·g-1), was synthesized by adding NaOH solution into CrCl3·6H2O solution drop by drop. The mesoporousCr(OH)3powders were used as adsorbents to remove vanadium ions from aqueous solution, which showed high efficiency in vanadium removing at pH from 2.0~9.0 and concentration of V5+ranging from 100 to 500mg·L-1. Under the optimal conditions, the adsorption rate of vanadium approached to 100% and the concentration of V5+decreased from 500 to 0.81 mg·L-1. The adsorption process belonged to the Langmuir isothermal adsorption and the coefficient was higher than 0.99. Dynamic analysis showed that the pseudo-second-order model could describe the adsorption process very well.
chromium hydroxide;mesoporous; powders; adsorption; waste water; vanadium removal
date: 2016-06-13.
Prof.ZHANG Bingzhu, 751895430@qq.com; ZHANG Hongling, hlzhang@ipe.ac.cn
10.11949/j.issn.0438-1157.20160808
TP 273
A
0438—1157(2016)12—5283—08
国家重点基础研究发展计划项目(2013CB632600);国家自然科学基金项目(21406233,21376251)。
supported by the National Basic Research Program of China (2013CB632600) and the National Natural Science Foundation of China (21406233, 21376251).
2016-06-13收到初稿,2016-08-29收到修改稿。
联系人:张炳烛,张红玲。第一作者:李华琳(1989—),男,硕士研究生。
