磺胺对甲氧嘧啶和二甲氧苄啶在肉鸡体内的残留消除
2016-09-21曾振灵周雨卉王嘉鹏韩可可
徐 维,曾振灵,权 丹,周雨卉,王 佩,王嘉鹏,韩可可,陈 红
(华南农业大学兽医学院国家兽药残留基准实验室,广东广州 510642)
磺胺对甲氧嘧啶和二甲氧苄啶在肉鸡体内的残留消除
徐维,曾振灵,权丹,周雨卉,王佩,王嘉鹏,韩可可,陈红*
(华南农业大学兽医学院国家兽药残留基准实验室,广东广州 510642)
采用高效液相色谱-串联质谱法研究磺胺对甲氧嘧啶(SMD)和二甲氧苄啶(DVD)预混剂在白羽肉鸡体内各组织中的残留消除规律。对48只健康白羽肉鸡连续饲喂添加1 000 mg/kg磺胺对甲氧嘧啶和二甲氧苄啶预混剂(含SMD 200 mg,DVD 40 mg)的全价饲料10 d,在停药后4 h,1、3、6、9、12、15 d分别宰杀6只鸡,采集各组织进行药物残留测定。通过空白样品添加回收试验,所有基质中SMD和DVD的定量限分别为10 μg/kg和5 μg/kg,SMD和DVD分别在50、100、200 μg/kg和25、50、100 μg/kg 3个添加水平下的平均回收率为71.7%~102.3%,相对标准偏差为1.0%~11.9%。结果表明,磺胺对甲氧嘧啶和二甲氧苄啶预混剂在肾脏中残留量最高,肝脏其次;肌肉和皮脂中的残留量显著低于肝脏和肾脏,停药9 d时,残留量低于药物残留限量。综合各组织中总残留量和最高残留限量规定,建议磺胺对甲氧嘧啶和二甲氧苄啶预混剂在鸡的休药期为7 d。
磺胺对甲氧嘧啶二甲氧苄啶预混剂;高效液相色谱-串联质谱;白羽肉鸡;残留;消除
磺胺类药物常用于畜禽疾病的治疗和预防,其中磺胺对甲氧嘧啶(sulfametoxydiazine,SMD) 用于控制畜禽细菌性疾病和鸡球虫病[1],但它有一定的毒性,对人类的健康具有潜在的危害性,因此该化合物在肉类等食品中残留问题受到关注[2-4]。敌菌净(diaveridine,DVD)属于二氨基嘧啶类药物,为动物专用抗菌增效剂,主要与磺胺类药物等抗菌药物组成复方制剂,使抗菌谱扩大、抗菌活性增强,从抑菌作用变为杀菌作用,在兽医临床上应用十分广泛[5]。DVD以1∶5比例与SMD合用制成预混剂,主要用于防治畜禽胃肠道细菌性感染及球虫病。目前,该预混剂在白羽肉鸡可食组织内药物残留消除规律研究尚未见报道。为了保证白羽肉鸡的食用安全,维护消费者利益,通过研究磺胺对甲氧嘧啶和二甲氧苄啶预混剂在白羽肉鸡组织内的残留消除规律,对指导临床合理用药提供参考依据。
1 材料与方法
1.1材料
1.1.1仪器液相质谱仪,Agilent6430型串联三重四级杆质谱,美国Agilent公司产品;配备Agilent1200液相色谱仪、可调微量移液器,法国Gilson公司产品;超纯水器,美国Milli2Q公司产品;台式高速离心机、Centrifuge5804,Eppendorf公司产品;FJ-200漩涡混悬器,上海沪西分析仪器厂产品。
1.1.2药品与主要试剂乙腈、甲醇、甲酸均为色谱纯,Merck公司产品;正己烷(分析纯),国产;磺胺对甲氧嘧啶和二甲氧苄啶预混剂(规格:100 g:含磺胺对甲氧嘧啶20 g与二甲氧苄啶4 g),河北地邦动物保健科技有限公司产品;磺胺对甲氧嘧啶标准品(含量99.0%),购于Dr.Ehrenstorfer GmbH;磺胺对甲氧嘧啶贮备液(1 mg/mL):准确称取10.10 mg磺胺对甲氧嘧啶对照品于10 mL棕色容量瓶中,用乙腈溶解并定容,配成浓度为1 mg/mL的标准储备液,于-20℃条件下贮存,根据需要再用乙腈稀释成适当浓度的标准工作液;二甲氧苄啶(含量100%),购于中国药品生物制品检定所;二甲氧苄啶贮备液(1 mg/mL):准确称取10.00 mg二甲氧苄啶对照品于10 mL棕色容量瓶中,少量0.1 mol/L盐酸溶解后用乙腈定容,配成浓度为1 mg/mL的标准储备液,于-20℃条件下贮存,根据需要再用乙腈稀释成适当浓度的标准工作液。
1.1.3试验用动物与分组供试鸡为白羽肉鸡,购自华南农业大学增城正大肉鸡发展中心,35日龄,体重在2.0 kg~2.5 kg之间,公母各半,笼养,自由饮水,采食饲料不含抗菌药物。供试鸡50只,试验前临床观察1周,健康者进入动物试验,编号并随机分为8组,其中1组为空白对照组。
1.2方法
1.2.1给药与采样按最高剂量给药:连续饲喂添加1 000 mg/kg磺胺对甲氧嘧啶和二甲氧苄啶预混剂(即每kg饲料添加SMD 200 mg和DVD 40 mg)的全价饲料10 d,然后改喂不含药物的饲料。空白组饲喂不含该预混剂的全价饲料。停药后的4 h(零休药期)、1 d、3 d、6 d、9 d、12 d、15 d,分别宰杀1组鸡,每只鸡分别取皮脂、肌肉、肝脏和肾脏等组织。样品采集后,将组织匀浆,置-20℃冷冻保存备用。
1.2.2样品处理将试验鸡肝脏、皮脂、肾脏和肌肉用剪刀剪碎,于15 000 r/min下匀浆3 min,准确称取1.0 g样品(鸡肉、皮脂、肝、肾)于50 mL离心管中,加入5 mL乙腈,涡旋1 min,超声10 min,于水平振荡器300 mot/min振荡20 min,8 000 r/min离心10 min,将乙腈层转移至15 mL离心管中。再用4 mL乙腈重复提取残渣一次,合并提取液,用乙腈定容至10 mL。准确移取1 mL提取液加1 mL乙腈饱和正己烷除脂两次后,于35℃水浴中氮吹浓缩至干后,用1 mL的1 mL/L甲酸水与乙腈(95∶5)混合溶液溶解残渣,涡旋混匀,15 000 r/min离心10 min,样品过0.22 μm滤膜后移入棕色进样瓶中,供HPLC-MS/MS分析。
1.2.3检测条件
1.2.3.1液相条件色谱柱:C18柱(150 mm×2 mm,5 μm,Phenomenex);流速:0.25 mL/min;进样体积:5 μL;流动相:溶液A:1 mL/L甲酸水;溶液B:乙腈。采用梯度洗脱程序:0 min~1 min,95.0% A;1 min~5 min,95.0% A~5.0% A;5 min~6 min,95.0% A;6 min~8 min,5.0 A~95.0% A;8 min~16 min,95.0% A。
1.2.3.2质谱条件离子源:电喷雾离子源(ESI);扫描模式:正离子扫描(Positive);检测方式:多反应监测(MRM);干燥气:N2;干燥气温度:350℃;正模式毛细管电压:3 500 V。1.2.4标准曲线采用空白基质匹配标准溶液法制得各个组织相应的标准曲线:准确称取1.00 g空白组织于50 mL离心管中,按照1.2.2所示方法处理样品,用各组织的空白提取液分别稀释SMD、DVD的储备液,分别使SMD的线性范围为1 ng/mL~200 ng/mL、DVD的线性范围为0.5 ng/mL~100 ng/mL,并按1.2.3液质条件进行测定。将测得的SMD和DVD的色谱峰面积(y)与相对应的药物浓度(x)作直线回归,求得标准曲线方程和相关系数。1.2.5定量限(LOQ)和检测限(LOD)准确称取空白组织1.0 g,依次加入100 μL SMD和DVD不同质量浓度的混合标准工作液,涡旋混匀,使得样品中SMD和DVD的浓度分别为2、3、4、5、10 μg/kg,每个浓度做5个平行,按照1.2.2方法处理样品,按1.2.3液质条件进行分析检测。以信噪比(S/N)≥3确定方法检测限,以(S/N)≥10确定方法定量限。
1.2.6回收率及变异系数空白组织制成匀浆后,将一定量的SMD和DVD的混合标准工作液加入到1.00 g 组织中,制得1/2MRL、MRL、2MRL 3个添加水平样品,涡旋混匀,静置30 min,按组织样品提取净化方法处理并进行HPLC-MS/MS测定。1 d内每个浓度设置5个平行样品,计算回收率和日内变异系数。
1.2.7各组织中磺胺对甲氧嘧啶与二甲氧苄啶的浓度测定各时间点所采鸡组织按 “1.2.2” 方法处理,进行HPLC-MS/MS 分析处理,求得磺胺对甲氧嘧啶和二甲氧苄啶的峰面积,按各组织标准曲线方程求得磺胺对甲氧嘧啶和二甲氧苄啶浓度,进而得到各时间点鸡各组织中磺胺对甲氧嘧啶和二甲氧苄啶的残留含量。
2 结果
2.1色谱行为
在此色谱条件下,目标组分得到了很好的分离,峰形尖锐、对称,药物峰附近未发现干扰峰,检测结果定性准确性高。DVD及SMD的保留时间分别在7.6 min及8.2 min左右。所得鸡空白组织、空白组织添加、实测样品色谱图见图1~图12。
2.2标准曲线
SMD在1 ng/mL~200 ng/mL浓度范围内色谱峰面积与浓度呈线性相关,其线性方程为:y=116.6x+134.2,R2=0.999 6。DVD在0.5 ng/mL~100 ng/mL浓度范围内色谱峰面积与浓度呈线性相关,其线性方程为:y=868.7x+1234.1,R2=0.998 6,若分析样品时,浓度超出此范围,则稀释样品即可。
2.3定量限和检测限
根据5个空白添加样品的基线噪音值求其平均值,按信噪比(S/N)≥3为检测限,(S/N)≥10为定量限,求得各组织中磺胺对甲氧嘧啶和二甲氧苄啶的LOD为2 μg/kg,LOQ分别为10 μg/kg和5 μg/kg。
2.4回收率及变异系数
样品的低、中、高3个浓度的添加回收率和精密度见表1和表2。从表1和表2中可知,SMD在50、100、200 μg/kg添加范围内,平均回收率在肌肉为85.6%~98.0%,皮脂为98.7%~102.3%,肝脏为86.3%~98.0%,肾脏为74.2%~96.5%,变异系数范围在2.0~11.9 (n=5) 之间。DVD在25、50、100 μg/kg添加范围内,平均回收率在肌肉为86.4%~91.9%,皮脂为79.5%~94.7%,肝脏为93.6%~96.1%,肾脏为71.7%~91.3%,变异系数范围在1.0~10.2 (n=5) 之间。可见,药物回收率都比较高,变异系数符合要求,该方法能够满足检测组织中磺胺对甲氧嘧啶和二甲氧苄啶残留的条件,快速、方便,稳定可靠。
2.5停药后鸡各组织中磺胺对甲氧嘧啶与二甲氧苄啶的残留测定
鸡各组织中磺胺对甲氧嘧啶及二甲氧苄啶的的平均残留量见表3。从表3可以看出停药后4 h磺胺对甲氧嘧啶在肌肉、皮脂、肝脏、肾脏的残留量分别为157、147、344、564μg/kg,停药1 d磺胺对甲氧嘧啶在肌肉的残留量已低于检测限,而在皮脂、肝脏和肾脏的残留量则分别降至为39、48、51 μg/kg,到停药后第6天,3种组织中磺胺对甲氧嘧啶的残留量均已低于检测限,表明磺胺对甲氧嘧啶残留量以肾脏最高,肝脏其次,肌肉最低。停药后4 h二甲氧苄啶在肌肉、皮脂、肝脏和肾脏的残留量分别为188、124、700、1451 μg/kg,停药1 d二甲氧苄啶在肌肉、皮脂、肝脏和肾脏的残留量则分别降至为23、37、67、366 μg/kg,停药后第3天在肌肉及肝脏的残留量均低于检测限,在皮脂及肾脏的残留量则分别为8 μg/kg、23 μg/kg,到停药后第9天,在皮脂及肾脏中均未检出二甲氧苄啶,结果表明,二甲氧苄啶在肾脏和肝脏的残留量明显高于肌肉和皮脂。
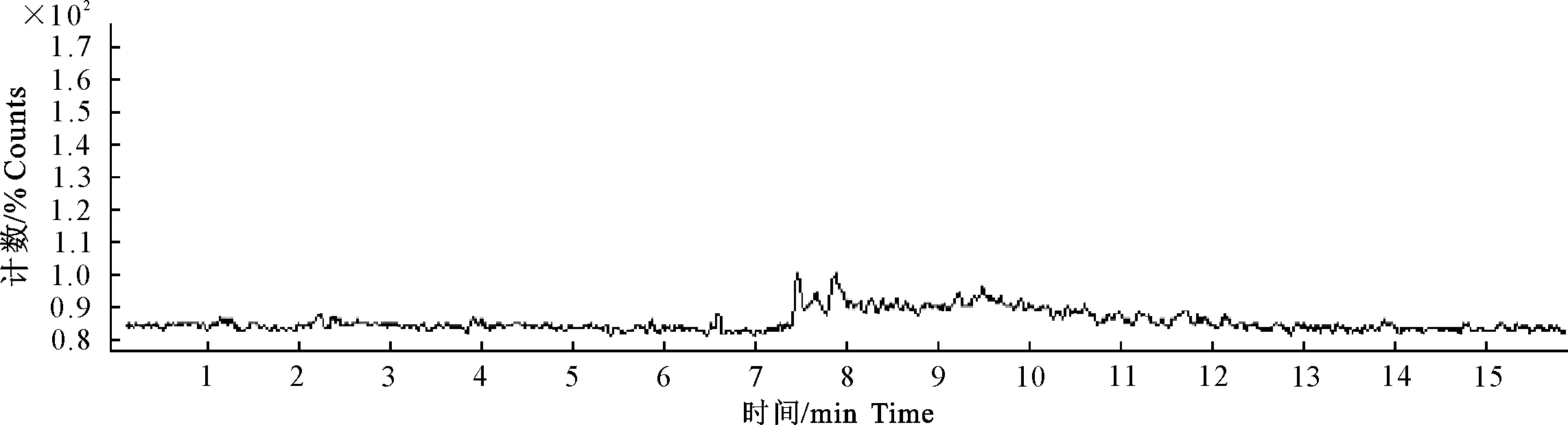
图1 空白肌肉色谱图
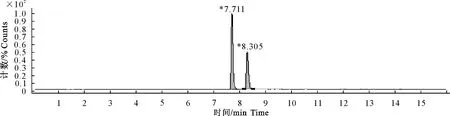
图2 空白肌肉添加DVD ( 100 μg/kg ) 和SMD ( 200 μg/kg )色谱图
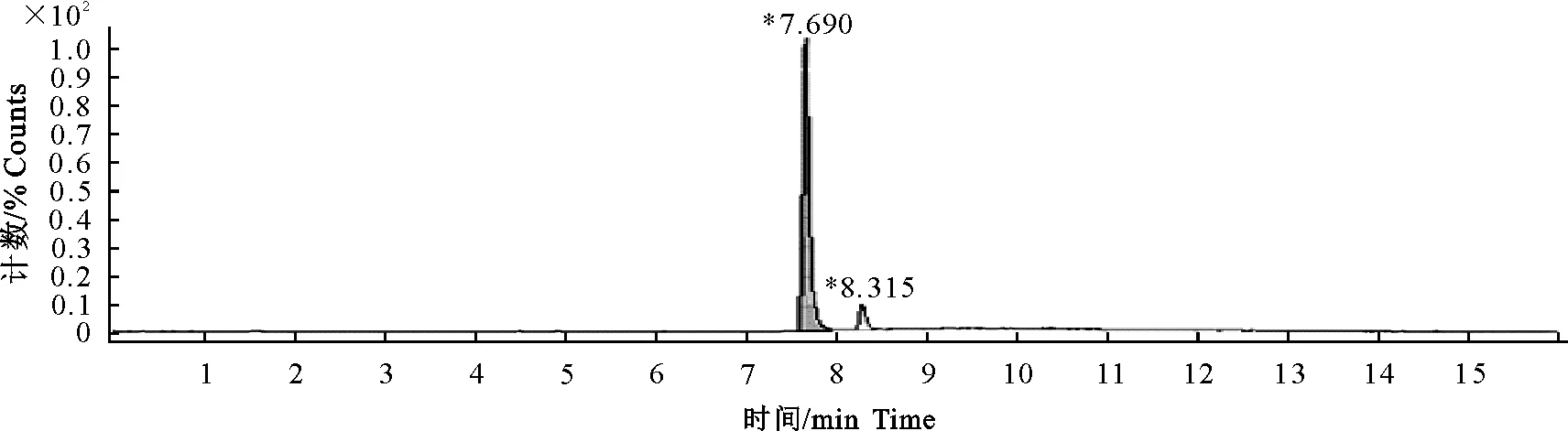
图3 停药后4 h时肌肉样品色谱图

图4 空白皮脂色谱图
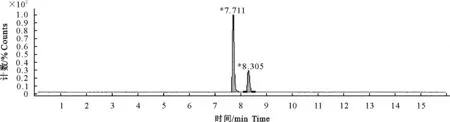
图5 空白皮脂添加DVD (100 μg/kg ) 和SMD(200 μg/kg)色谱图
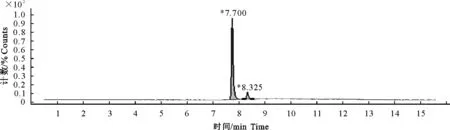
图6 停药后4 h时皮脂样品色谱图
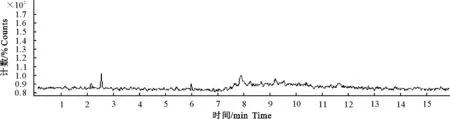
图7 空白肝脏色谱图
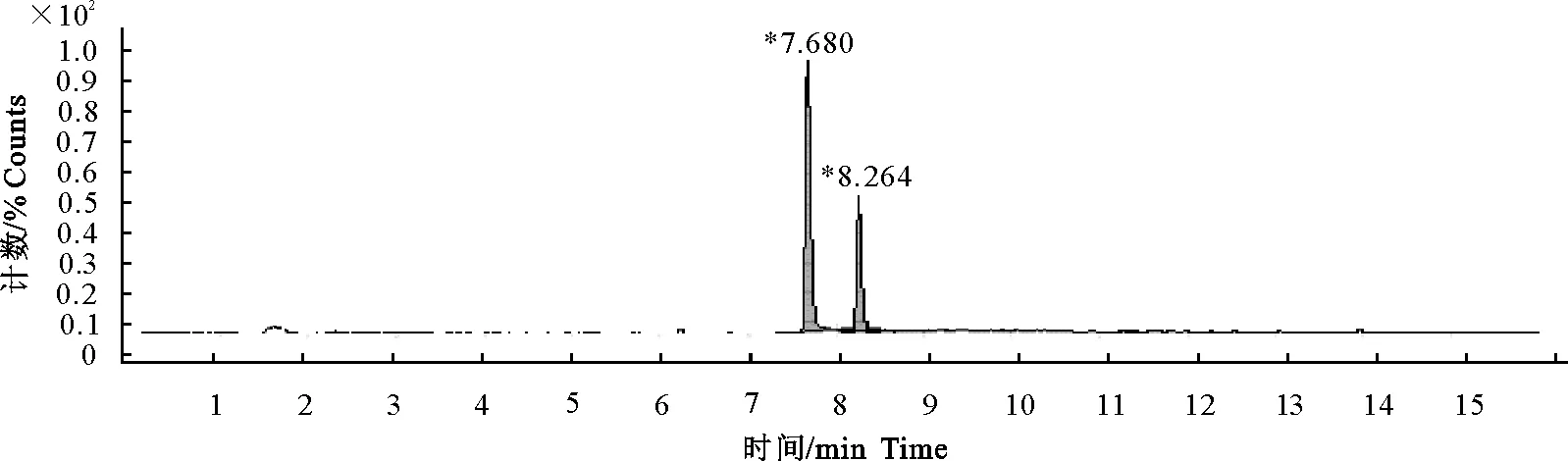
图8 空白肝脏添加DVD ( 100 μg/kg ) 和SMD(200 μg/kg)色谱图
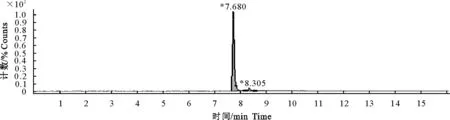
图9 停药后4 h时肝脏样品色谱图
图10 空白肾脏色谱图
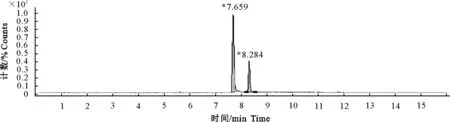
图11 空白肾脏添加DVD (100 μg/kg ) 和SMD(200 μg/kg)色谱图
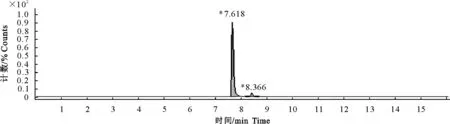
图12 停药后4 h时肾脏样品色谱图
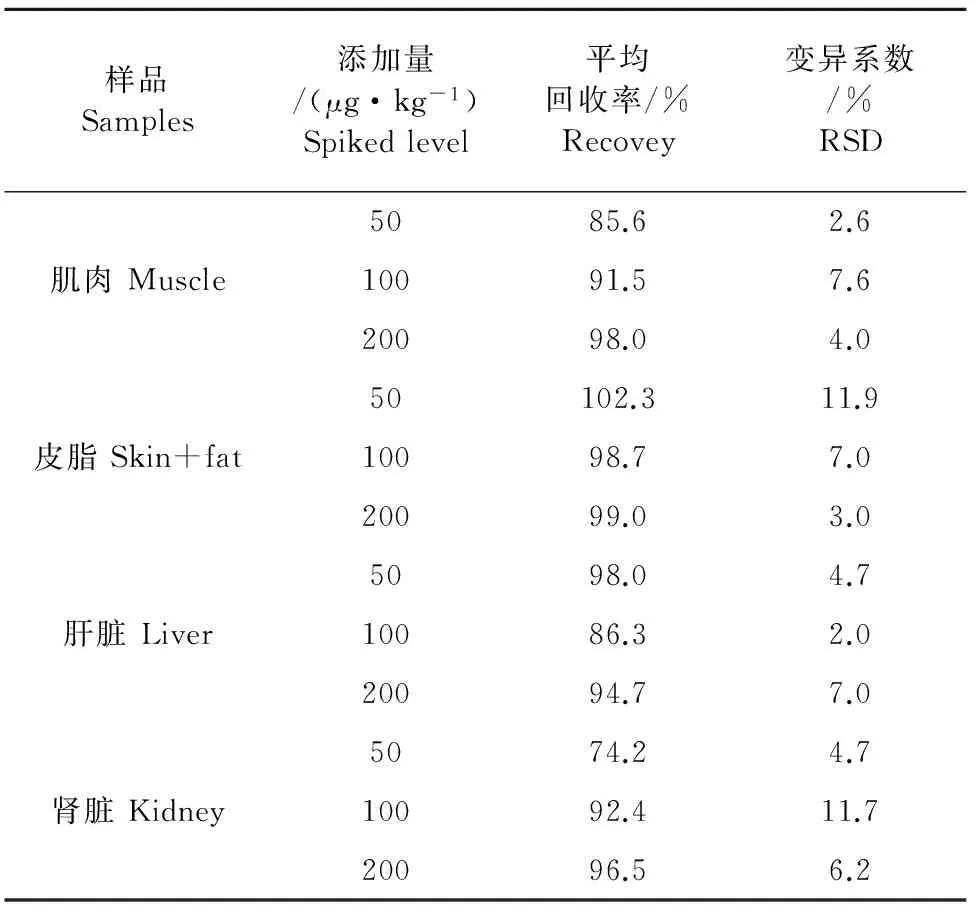
样品Samples添加量/(μg·kg-1)Spikedlevel平均回收率/%Recovey变异系数/%RSD5085.62.6肌肉Muscle10091.57.620098.04.050102.311.9皮脂Skin+fat10098.77.020099.03.05098.04.7肝脏Liver10086.32.020094.77.05074.24.7肾脏Kidney10092.411.720096.56.2
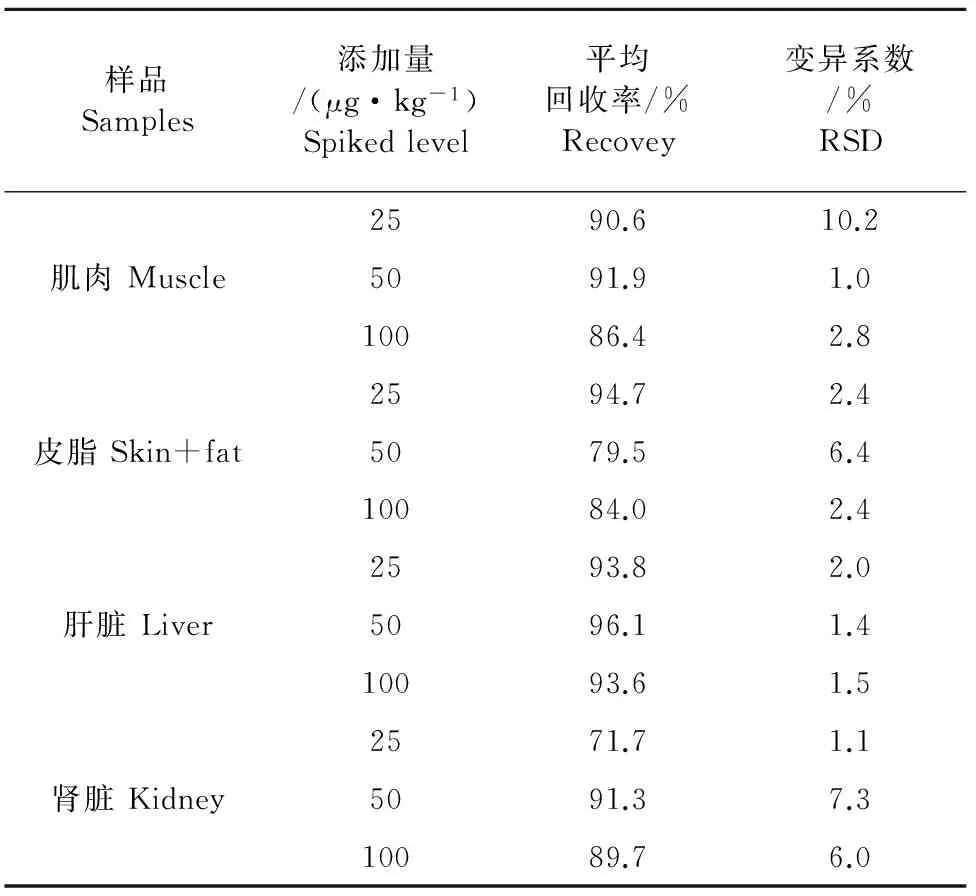
表2 二甲氧苄啶的添加回收率和精密度(n=5)
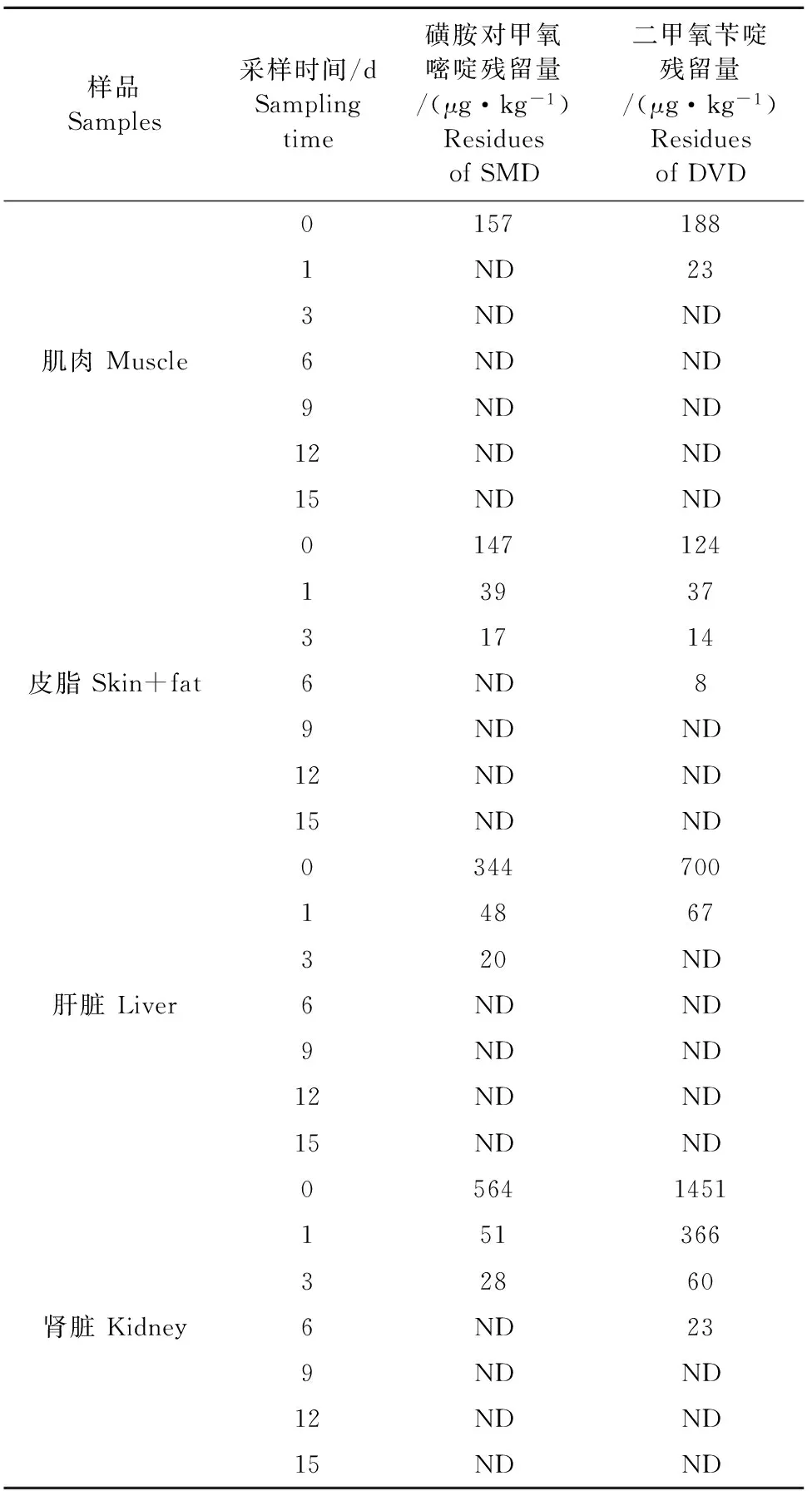
表3 不同采样时间鸡组织中磺胺对甲氧嘧啶和二甲氧苄啶平均残留量(n=6)
注: 表中所有数值均以平均值表示;ND:表示未检出。
Note:All the data in the table are average values; ND:Not Detectable.
3 讨论
3.1磺胺对甲氧嘧啶和二甲氧苄啶在鸡组织的残留检测
鉴于磺胺类药物可能导致的毒性,目前中国、欧盟、美国、日本等均将磺胺类药物列为动物饲养过程中限制使用的药物,欧盟规定牛奶和肉类食品磺胺类药物总量 ≤ 100 μg/kg[6-7],我国农业部公告235号文《动物性食品中兽药的最高残留限量》中规定磺胺类药物在鸡所有组织中的MRL均为0.1 mg/kg,而日本规定食品中不得检出SAs[8]。我国已批准二甲氧苄啶(DVD)的生产与使用,涉及的制剂主要是与磺胺类药物联合用于家禽球虫病的防治[9]。美国、欧盟及日本等国亦均有DVD与磺胺类药物合用的注册制剂产品,但美国、欧盟及日本等国均无明确的使用规定和安全标准,食品残留专家委员会(JECFA)和欧洲药品局(EMEA)等国际组织迄今未对DVD进行过任何评价[10]。二甲氧苄啶目前尚未制定残留限量,我们按照欧洲规定的甲氧苄啶(TMP)在组织中的最大残留浓度小于50 μg/kg为参考[11]。
3.2磺胺对甲氧嘧啶和二甲氧苄啶在鸡组织中的残留规律
磺胺对甲氧嘧啶和二甲氧苄啶预混剂防治畜禽胃肠道细菌性感染,球虫病临床推荐用法与用量为:混饲:每1 000 kg饲料1 000 g(以预混剂计)连续饲喂不超过10 d[12]。在残留消除研究中,试验按最大推荐剂量(每1 000 kg饲料1 000 g预混剂)连续给药10 d。试验结果表明:磺胺对甲氧嘧啶和二甲氧苄啶在肾脏中残留量最高,在停药4 h时,磺胺对甲氧嘧啶的平均残留量为564 μg/kg,二甲氧苄啶的平均残留量为1 451 μg/kg,在停药9 d时,肾脏中均未检测出药物;肝脏其次,在停药3 d时,肝脏中未检测出二甲氧苄啶,停药6 d时,磺胺对甲氧嘧啶残留量也降至定量限以下;肌肉和皮脂中的残留量显著低于肾脏和肝脏,停药3 d时,肌肉中均未检测出药物,停药9 d时,皮脂中的残留量均低于定量限。
本研究中磺胺对甲氧嘧啶在鸡各组织中的残留消除规律与刘明生等[13]报道的在艾维茵肉鸡各组织中残留消除的趋势是一致的,不同的是,文献中报道磺胺对甲氧嘧啶在鸡肝脏中的残留量最高,肾脏其次,停药10 d后,组织中的残留量均低于检测限,笔者认为存在这种差异可能跟鸡的品种有关。郝增坤[14]通过磺胺氯吡嗪钠、二甲氧苄啶溶液在鸡体内的残留消除试验表明,二甲氧苄啶浓度在停药4 h时各组织以肾脏中二甲氧苄啶浓度最高,达到1.57 μg/g,其他组织残留依次为皮脂和肝脏,肌肉中残留量最低,为0.31 μg/g。本研究中,二甲氧苄啶在鸡肾脏和肝脏中的浓度明显高于其他组织,与上述文献结果类似。
3.3磺胺对甲氧嘧啶、二甲氧苄啶预混剂休药期的确定
停药后磺胺对甲氧嘧啶在鸡体内各组织中的残留消除速率由快到慢依次为肌肉、皮脂、肝脏、肾脏;二甲氧苄啶的消除速率由快到慢依次为肝脏、肌肉、皮脂、肾脏。磺胺对甲氧嘧啶、二甲氧苄啶预混剂在肾脏中消除最慢且残留浓度高于其他组织,说明磺胺对甲氧嘧啶、二甲氧苄啶预混剂在鸡体内的分布是不均匀的,主要经肾脏消除,提示肾脏为磺胺对甲氧嘧啶、二甲氧苄啶预混剂在鸡体内残留的靶组织。
按照磺胺类药的最高残留限量和休药期计算的相关规定,实测数据经WT1.4[15]休药期计算软件计算结果表明,磺胺对甲氧嘧啶、二甲氧苄啶预混剂按最大剂量给鸡混饲给药后,磺胺对甲氧嘧啶在皮脂、肝脏和肾脏的休药期分别约为1.86、3.33、3.98 d。我国尚未制定二甲氧苄啶的最高残留限量(MRL),参照国际食品法典委员会(CAC) 和欧盟等大多数国家规定的动物性食品中TMP的最高残留限量(MRL)为50 μg/kg,二甲氧苄啶在皮脂、和肾脏的休药期分别约为4.11 d和6.70 d。依据靶动物鸡体内的消除规律研究数据,结合WT1.4软件计算的休药期结果,建议磺胺对甲氧嘧啶、二甲氧苄啶预混剂按推荐剂量给鸡混饲给药,连用10 d时,在鸡的休药期为7 d。
[1]梁小菊,罗显阳.磺胺对甲氧嘧啶在鸡蛋中残留的高效液相色谱法的研究[J].北京农业,2013(24):130-131.
[2]彭英,何欢,孙成,等.新型固相微萃取-高效液相色谱测定牛奶中4 种磺胺类药物残留[J].分析化学研究报告,2013,41(4):529-533.
[3]张睿,张晓燕,陈磊,等.液相色谱-串联质谱法同时测定蜂胶中的磺胺及林可胺类药物残留[J].分析试验室,2014,33(12):1420-1424.
[4]吴波,罗厚强,段龙川,等.磺胺间甲氧嘧啶在黄羽肉鸡组织中残留消解规律[J].浙江农业科学,2015,56(2):267-269.
[5]陈丽,杨长志,刘永,等.高效液相色谱法测定动物源性食品中敌菌净残留量[J].化学工程师,2008(12):50-53.
[6]张煌涛,李雪红,占秀梅,等.兽肉中磺胺类药物残留检测研究进展[J].草食家畜,2006(4):14-16.
[7]鲁晓翠,侯玉泽,邓瑞广,等.磺胺类药物在动物性食品中的残留与检测[J].动物医学进展,2007,28(2):70-74.
[8]李俊锁,邱月明,王超.兽药残留分析[M].上海:上海科学技术出版社,2002.
[9]赵振升,王建华.TMP和DVD对两种磺胺药抗球虫增效作用试验[J].动物医学进展,2007(3):40-43.
[10]孙晨明.磺胺氯吡嗪钠—二甲氧苄啶混悬液在鸡的抗球虫药效及药动学研究[D].江苏扬州:扬州大学,2012.
[11]苑瑞瑞.鸡组织中二甲氧苄啶和甲氧苄啶残留量的HPLC检测方法研究[D].江苏扬州:扬州大学,2012.
[12]中国兽药典委员会.兽药使用指南-化学药品卷[M].北京:中国农业出版社,2010.
[13]刘明生,甘辉群,谭菊,等.磺胺对甲氧嘧啶在肉鸡组织中的残留研究[J].饲料工业,2006(16):49-51.
[14]郝增坤.磺胺氯吡嗪钠—二甲氧苄啶溶液在鸡的残留消除研究[D].江苏扬州:扬州大学,2012.
[15]栗柱,宗海兵.休药期计算软件WT1.4的使用[J].饲料广角,2003(18):40-41.
Study on Residue Depletions of Sulfametoxydiazine and Diaveridine in Chickens
XU Wei,ZENG Zhen-ling,QUAN Dan,ZHOU Yu-hui,WANG Pei,WANG Jia-peng,HAN Ke-ke,CHEN Hong
(National Reference Laboratory of Veterinary Residues,College of Veterinary Medicine,South ChinaAgriculturalUniversity,Guangzhou,Guangdong,510642,China)
To develop high performance liquid chromatographic tandem mass spectrometry method of sulfametoxydiazine (SMD) and diaveridine (DVD) premix residue in chicken tissues,and to explore elimination rule on its residues in the chicken tissues. Forty-eight healthy white feather broiler chickens which were feeded with added level of SMD and DVD premix (1 000 mg/kg) for 10 d. Six chickens were slaughtered at 4 h,1,3,6,9,12,15 d after the last feeding,respectively.Tissues including kidney,liver,muscle and fat of each chicken were collected,and SMD and DVD of tissues were determined by high performance liquid chromatographic tandem mass spectrometry.The quantitative limits of the method for SMD and DVD were 10 μg/kg and 5 μg/kg respectively for all matrices,and the recoveries were in the range of 71.7%-102.3% with RSDs of 1.0%-11.9% while blank samples were spiked with SMD and DVD at 50,100,200 μg/kg and 25,50,100 μg/kg respectively. Results showed that the residues of SMD and DVD in kidney was the highest,and lower in liver.The residues of SMD and DVD in muscle and fat were much lower than that in liver and kidney,and was declined below the LOQ at 9 day. According to the residues in all tissues and the rule of Maximum Residue Limit, the withdrawal periods for all chicken tissues were 7 day.
sulfametoxydiazine and diaveridine premix; HPLC-MS/MS; white feather broiler chicken; residue; depletion
2015-05-07
农业部兽药行业标准制定和修订项目[农财发(2013)46号-32]
徐维(1990-),女,江西宜春人,硕士,主要从事基础兽医药理与毒理学研究。*通讯作者
S859.796
A
1007-5038(2016)08-0049-08
