废旧磷酸钒锂电池材料回收及再利用研究
2016-09-08戴长松纪大龙哈尔滨工业大学化工学院黑龙江哈尔滨150001
刘 正, 戴长松, 纪大龙, 贾 铮, 赵 力(哈尔滨工业大学化工学院,黑龙江哈尔滨150001)
废旧磷酸钒锂电池材料回收及再利用研究
刘 正,戴长松,纪大龙,贾铮,赵力
(哈尔滨工业大学化工学院,黑龙江哈尔滨150001)
针对磷酸钒锂电池材料溶解-沉淀回收困难的问题,采用NaOH溶液浸泡磷酸钒锂电极,溶解集流体铝箔,分析过滤产物中锂、钒、磷和碳的摩尔比,依据分析结果添加LiOH·H2O、V2O5、NH4H2PO4和蔗糖,使过滤产物和添加物的混合物中,锂、钒、磷和碳的摩尔比为3.15∶2∶3∶3,对混合物进行不添加酸和添加盐酸处理,在氩气气氛中于300℃下预烧结4 h,冷却和研磨后,再于氩气气氛中800℃下煅烧12 h,得到磷酸钒锂正极材料。与不经酸处理获得磷酸钒锂相比,X射线衍射(XRD)测试结果表明,经过酸处理工艺获得的磷酸钒锂结晶更好,其衍射峰与单斜结构磷酸钒锂谱图一致;扫描电子显微镜(SEM)测试结果表明,经过酸处理工艺获得的正极材料结晶粒径更小,粒径分布较均匀;能谱分析结果表明,产物中没有残存的氯;电化学测试结果表明,经过酸处理工艺获得的磷酸钒锂首次放电比容量为93.8 mAh/g,50次循环后的容量保持率为98.4%。
废旧电池;磷酸钒锂;回收;再利用
在通讯和数码产品等领域,锂离子电池以其优异性能获得越来越广泛的应用,其产量不断增大。未来,随着锂离子电池在交通等领域的成功应用,其产量将呈现爆炸性增长,而锂离子电池的使用寿命仅为2~5年。锂离子电池结束其使用寿命后,如不加处理直接丢弃到自然界中,不仅给环境造成潜在的巨大危害,也使得相应的资源如钴、镍、锰、铁和锂等使用量大幅增加。
目前磷酸铁锂锂离子电池被认为是电动车理想的动力源,但磷酸铁锂电池存在比能量低、大电流放电和低温放电性能差的缺点。与LiFePO4相比,Li3V2(PO4)3电池具有比容量高、比能量高、大电流放电好特别是低温放电性能好的优点。目前,关于Li3V2(PO4)3材料合成、改性以及电化学性能等方面的研究不断深入[1-2],但Li3V2(PO4)3电池回收方面的研究却未见报道。本文就废旧Li3V2(PO4)3锂离子电池的回收处理方法进行研究,以期实现Li3V2(PO4)3活性物质的循环利用。
1 实验
1.1废旧Li3V2(PO4)3电池材料回收
将废旧Li3V2(PO4)3电池拆解,分选出正极以后,加入到一定浓度的NaOH溶液中,溶解除去集流体铝箔,再过滤得到滤渣。将干燥后的滤渣放入管式炉中,400℃烧结1 h,目的是除去粘结剂PVDF以及导电剂乙炔黑,然后采用电感耦合等离子体光谱分析法 (ICP)分析Li、V、P和C元素比例,并按照Li∶V∶P∶C比例为3.15∶2∶3∶3补充一定量的LiOH· H2O、V2O5、NH4H2PO4和蔗糖。之后分两种方法再合成Li3V2-(PO4)3:一种方法是将混合物至于球磨机中,加入乙醇作为分散剂球磨7 h,真空干燥后在氩气气氛中于300℃下预处理4 h,研磨所得中间体,之后在氩气中800℃下继续烧结12 h,得到Li3V2(PO4)3样品(LVP-1);另一种方法是将补充锂源和钒源的烧结产物倒入6 mol/L的盐酸中处理,在80℃下搅拌直至水分蒸干,再将样品真空干燥后,于氩气气氛中300℃预处理4 h,研磨所得中间体,之后再在氩气中800℃下继续烧结12 h,得到Li3V2(PO4)3样品(LVP-2)。
1.2电极制备及电池组装
制备电极:将正极活性物质、粘结剂PVDF和导电剂乙炔黑按质量比为8∶1∶1混合,加入溶剂NMP后置于磁力搅拌器上,搅拌均匀后涂于铝箔上,真空120℃干燥12 h。最后制成14 mm的正极小圆片。
组装电池:以制备的正极电极片为研究电极,金属锂为对电极,l mol/L LiPF6/(EC+EMC+DEC)(体积比1∶1∶1)为电解液,Celgard 2400为隔膜,在充满惰性保护气Ar的手套箱中,组装成CR2025型扣式电池。再用封口机将电池密封,之后静置几小时再进行测试。
2 结果与讨论
2.1废旧Li3V2(PO4)3电极活性物质的回收
目前废旧锂离子电池回收利用的研究主要集中在正极活性材料回收上。而作为回收工艺一个重要步骤就是实现废旧Li3V2(PO4)3电池的活性物质与集流体分离,而后是活性材料的再制备。
2.1.1Li3V2(PO4)3活性物质与铝箔的分离
Li3V2(PO4)3电池的组成包括:正极、负极、电解液、隔膜及电池壳等。其中正极主要包括:Li3V2(PO4)3活性物质、导电剂乙炔黑、粘结剂PVDF和集流体铝箔。
实验中废旧电池拆解后,得到正极。拆选得到的正极先用NaOH溶液浸泡,溶解集流体铝箔,使铝以NaAlO2的形式进入溶液,而其他物质不溶于碱,残留在碱液的浸渣中,过滤实现集流体铝箔与Li3V2(PO4)3活性物质的初步分离,而碱浸液经过加酸调pH值,得到Al(OH)3。
不同浓度的NaOH溶液对铝箔溶解的反应时间存在较大的影响。图1为NaOH浓度与铝箔完全溶解所需时间曲线。由图1可见,随着NaOH浓度的增大,铝箔完全溶解所需时间逐渐变小,但当NaOH浓度达到2~4 mol/L时,反应速度增加变缓;同时,当NaOH浓度达4 mol/L时反应过于剧烈,因此选择3 mol/L的NaOH溶液进行下一步的实验。
2.1.2Li3V2(PO4)3活性物质与粘结剂、乙炔黑的分离
通过碱液溶解将集流体铝箔与Li3V2(PO4)3活性物质、乙炔黑和PVDF等物质分离过滤之后,得到的碱浸渣中包含有Li3V2(PO4)3活性物质、乙炔黑和PVDF。本实验采用烧结的方法除去乙炔黑和PVDF,以得到纯的Li3V2(PO4)3活性物质。图2为碱浸渣的热重-微分热重(TG-DTA)测试图,测试在空气中进行,升温区间为室温~800℃,升温速度为10℃/min。
由图2可知,样品质量的损失主要发生在300~450℃之间,是由于过滤产物中乙炔黑、PVDF和Li3V2(PO4)3中包覆的碳层氧化生产CO2等气体引起的。因此,本实验中采用400℃作为除去乙炔黑和PVDF的烧结温度。烧结之后的样品进行了碳含量的测试,其中碳含量为0.06%(质量分数),说明经过烧结过程基本上除去了过滤产物中的乙炔黑、PVDF和Li3V2-(PO4)3中包覆的碳。
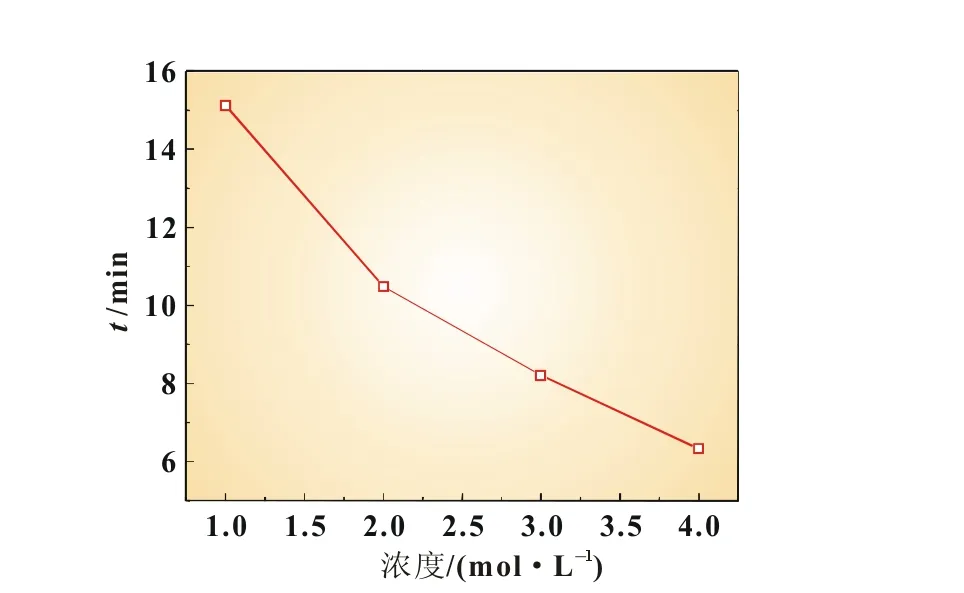
图1 NaOH浓度对溶解反应时间的影响(室温)
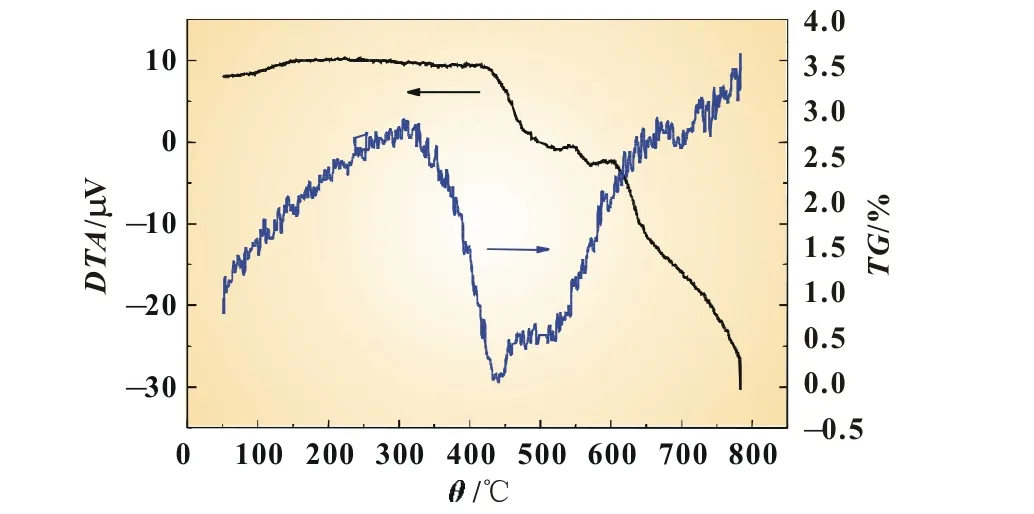
图2 碱浸渣的TG-DTA图
2.2废旧Li3V2(PO4)3电池的再利用
2.2.1废旧Li3V2(PO4)3电池再合成
在空气中400℃下烧结1 h除去了过滤产物中的乙炔黑、PVDF和Li3V2(PO4)3中包覆的碳之后,得到了含有Li、V、P等元素的混合物,其X射线衍射(XRD)谱如图3所示。从图3中可知,烧结之后的Li3V2(PO4)3结构已经被破坏,烧结产物由多种物质组成,Li主要以Li3P、LiPO3形成存在,V主要以V2O3形式存在。
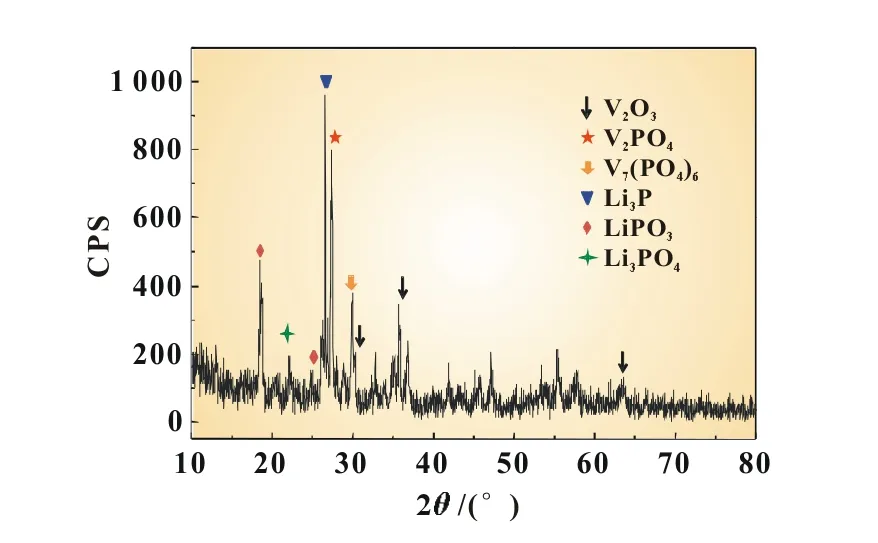
图3 烧结产物的XRD谱图
采用ICP测试,给出烧结产物中Li、V、P物质的量之比为2.6∶2∶3.3,其中P是过量的,向其中补充一定量的LiOH· H2O、V2O5和蔗糖使Li、V、P和C的物质量比为3.15∶2∶3∶3。
重新合成Li3V2(PO4)3时,采用两种不同方法。一种是将补充入锂源、钒源和蔗糖的混合物放入球磨机中,加入乙醇作为分散剂球磨7 h,取出干燥后在氩气中300℃预处理4 h,研磨所得中间体,之后在氩气中800℃下继续烧结12 h,得到Li3V2-(PO4)3样品(LVP-1);另一种是将补充入锂源、钒源和蔗糖的混合物溶于6 mol/L的盐酸中,在80℃下搅拌直至水分蒸干,然后再加去离子水直至蒸干,反复多次后,将样品送入真空干燥箱于120℃下干燥8 h,之后在氩气中300℃预处理4 h,研磨得到中间体,之后在氩气中800℃下继续烧结12 h,得到Li3V2-(PO4)3样品(LVP-2)。
2.2.2再合成Li3V2(PO4)3的物理表征
为了研究不同方法再合成的Li3V2(PO4)3样品晶相结构、晶相纯度和结晶状况,对再合成样品进行了XRD分析。
图4为不同方法再合成Li3V2(PO4)3样品的XRD谱图。由图4可知,不添加酸工艺合成Li3V2(PO4)3样品(LVP-1)的XRD谱图中存在明显的杂峰和“馒头峰”,而且衍射峰的强度也较弱,说明不添加酸条件下再合成的Li3V2(PO4)3的结晶度较差;而添加盐酸合成的Li3V2(PO4)3样品(LVP-2)的XRD谱图中衍射峰的位置和强度与文献[1]所给出的单斜结构Li3V2(PO4)3的标准XRD谱图一致,而且谱图中没有明显的杂峰存在,主要晶面的衍射峰明显而且尖锐,这说明增加溶酸的液相过程,有利于前述溶铝过滤物与添加物的混合均匀,有利于结晶良好的Li3V2(PO4)3/C材料生成。
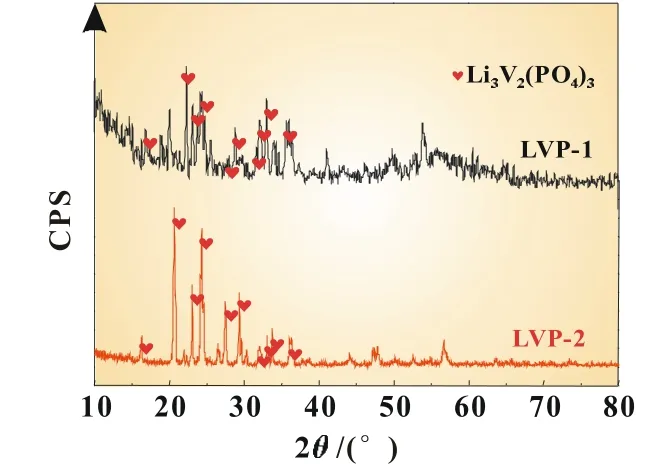
图4 再合成Li3V2(PO4)3样品的XRD谱图

图5 再合成Li3V2(PO4)3样品的SEM图
图5为不同方法再合成Li3V2(PO4)3样品的扫描电子显微镜(SEM)谱图。从图5可知,LVP-1样品的颗粒粒径较大,团聚现象较严重;LVP-2样品颗粒拥有较小的粒径。较小的粒径有利于锂离子的嵌入和脱出以及电子的传导,从而材料的电化学性能提升奠定基础。
为了检测将混合物加入到盐酸中是否会影响再制备的产物中Cl元素的含量,对两种样品进行了能量散射光谱(EDS)分析,结果见图6。从图6可见,两种方法再制备Li3V2(PO4)3样品几乎都不含Cl,换句话说,添加盐酸工艺在合成的磷酸钒锂样品中没有残存的Cl-。

图6 再合成Li3V2(PO4)3样品的EDS谱图
2.2.3再合成Li3V2(PO4)3电化学测试
为了考察不同方法再合成的Li3V2(PO4)3材料的电化学性能,将再合成的Li3V2(PO4)3材料组装成CR2025扣式电池,并对实验电池进行了1C下的充放电测试,充电截止电压4.3 V,放电截止电压3.0 V。
图7为1 C下再合成的Li3V2(PO4)3材料充放电曲线。由图7可知,LVP-1样品在充电过程中只有一个电压平台,放电过程中存在两个电压平台,与单斜结构的Li3V2(PO4)3充放电平台不一致[3-4];LVP-2的充放电曲线中明显存在三对充放电平台,同时放电比容量为93 mAh/g,明显高于LVP-1的放电比容量。
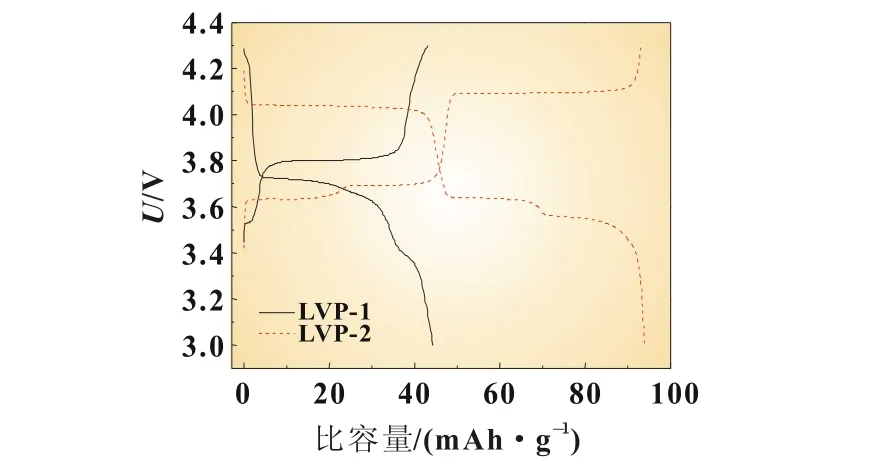
图7 再合成Li3V2(PO4)3样品在1C下的充放电曲线

图8 再合成Li3V2(PO4)3样品在1C下的循环性能
图8为再合成的Li3V2(PO4)3材料在1 C下的循环性能测试。由循环曲线可知,LVP-1的放电比容量较低,只有45 mAh/g;而LVP-2的首次放电比容量为93.8 mAh/g,50次循环后容量保持率达到了98.4%,说明LVP-2的循环性能要明显优于LVP-1。
为了进一步考察两种不同方法再合成的Li3V2(PO4)3材料的电极反应可逆性,对两种样品进行了循环伏安测试。图9为Li3V2(PO4)3样品在3.0~4.3 V电压范围内的循环伏安曲线,扫描速率为0.1 mV/s。由图9可知,LVP-1样品的氧化峰和还原峰位置与单斜结构Li3V2(PO4)3的氧化和还原峰的位置相差较大,表明其存在杂相;而LVP-2样品的氧化和还原峰的位置与单斜结构Li3V2(PO4)3的氧化峰和还原峰的位置吻合较好,LVP-2的氧化峰与相应的还原峰峰值电势差较小,说明其可逆性更好。
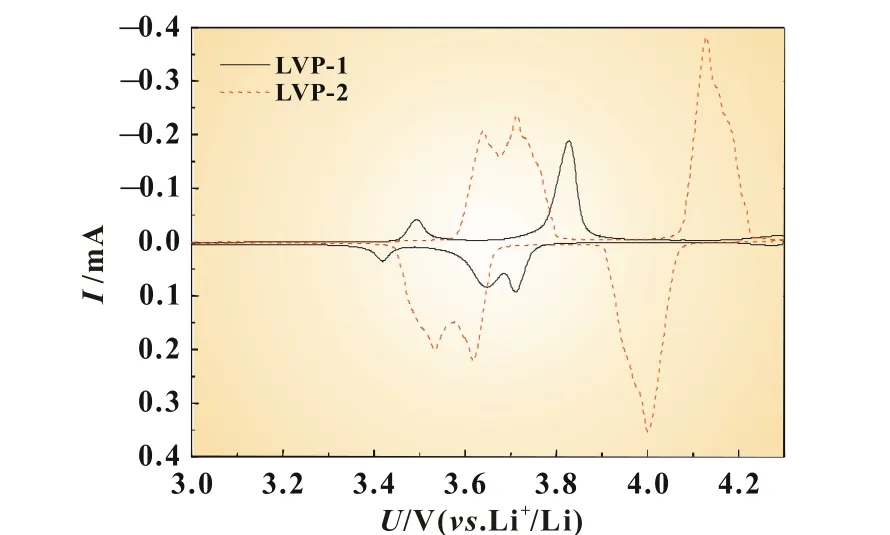
图9 再合成Li3V2(PO4)3样品的循环伏安曲线
3 结论
(1)采用碱液溶解集流体铝箔,过滤得到回收的正极材料,当NaOH溶液的浓度为3 mol/L时,铝箔的溶解速度最快。
(2)不添加酸,采用球磨混合(LVP-1)以及添加盐酸溶解(LVP-2)两种方法制得前驱体,并合成Li3V2(PO4)3材料。与不添加盐酸工艺制备的LVP-1样品相比,添加盐酸工艺合成的LVP-2样品结晶度高,所含杂相较少,颗粒更加均匀,Cl-离子没有残存,在1C下首次放电比容量达到了93.8 mAh/g,50次循环之后容量保持率达到了98.4%。尽管再合成Li3V2(PO4)3材料的比容量还比较低,但可以为Li3V2(PO4)3电池回收奠定基础。
[1]ZHANG L,XIANG H F,LI Z,et al.Porous Li3V2(PO4)3/C cathode with extremely high-rate capacity prepared by a sol-gel-combustion method for fast charging and discharging[J].Journal of Power Sources,2012,203:121-125.
[2]CHO A R,SON J N,ARAVINDAN V,et al.Carbon supported,Al doped-Li3V2(PO4)3as a high rate cathode material for lithium-ion batteries[J].Journal of Materials Chemistry,2012,22(14):6556-6560.
[3]YIN S C,GRONDEY H,STROBEL P,et al.Charge ordering in lithium vanadium phosphates:electrode materials for lithium-ion batteries[J].Journal of the American Chemical Society,2002,125 (2):326-327.
[4]CHEN Z Y,DAI C S,WU G,et al.High performance Li3V2(PO4)3/C composite cathode material for lithium ion batteries studied in pilot scale test[J].Electrochemical Acta,2010,55(28):8595-8599.
Spent lithium vanadium phosphate battery material recycling and reusing
LIU Zheng,DAI Chang-song,JI Da-long,JIA Zheng,ZHAO Li
(School of Chemical Engineering and Technology,Harbin Institute of Technology,Harbin Heilongjiang 150001,China)
Lithium vanadium phosphate electrodes were immersed in NaOH solution to dissolve aluminum foil current collector to solve recycling difficult issues of lithium vanadium phosphate battery material.The molar ratio of lithium, vanadium,phosphorus,carbon in residue was adjusted to 3.15∶2∶3∶3 using LiOH·H2O,V2O5,NH4H2PO4,sucrose respectively.Then the mixture in HCl compared with untreated was immersed.The mixture was presintered at 300℃for 4 h and sintered at 800℃for 12 h in argon-hydrogen mixtrue atmosphere after grinding.X-ray diffraction pattern shows that the diffraction spectrums of cathode material immersed in HCl is coincided with lithium vanadium phosphate standard spectrums.SEM images show that the cathode material immersed in HCl has smaller and uniform distribution particale size.The lithium vanadium phosphate shows a high initial discharge specific capacity of 93.8 mAh/g,the reversible specific capacities of lithium vanadium phosphate is more than 98.4%of initial capacity at the fiftieth cycle.
spent battery;lithium vanadium phosphate;recycling;reusing
TM 912
A
1002-087 X(2016)01-0035-04
2015-06-14
国家环保公益性行业科研专项(201009028);国家自然科学基金(51274075);广东省教育部产学研结合项目(2012B091100-315)
刘正(1986—),男,江苏省人,硕士,主要研究方向为锂离子电池回收。
戴长松,教授,E-mail:changsd@hit.edu.cn
