新型高效毛细管电泳手性整体柱拆分普罗帕酮
2016-09-05柯雅莉沈静茹郭小倩章冰娜
柯雅莉,沈静茹,郭小倩,章冰娜
(中南民族大学 化学与材料科学学院分析化学国家民委重点实验室,湖北 武汉 430074)
科研与开发
新型高效毛细管电泳手性整体柱拆分普罗帕酮
柯雅莉,沈静茹*,郭小倩,章冰娜
(中南民族大学 化学与材料科学学院分析化学国家民委重点实验室,湖北 武汉 430074)
以双-(6-氧-间硝基苯磺酰基)-β-环糊精作为手性选择剂,利用原位聚合反应制得双-(6-氧-间硝基苯磺酰基)-β-环糊精手性高效毛细管电泳(HPCE)整体柱,采用HPCE法考察该柱对手性药物普罗帕酮(Propafenone)的手性拆分能力,并对其拆分条件进行优化。结果表明:在最佳条件下,普罗帕酮两对映体分离度RS达到52.82,建立了一种有效的普罗帕酮两对映体分离分析新方法。
双-(6-氧-间硝基苯磺酰基)-β-环糊精;手性HPCE整体柱;普罗帕酮;手性拆分
高效毛细管电泳(HPCE)中环糊精类手性固定相以其高效、经济、自动化程度高和环保等优点在手性拆分中的应用很广[1-3],其中整体柱因其制备方法简单、通透性好、活性位点利用率高等优点,越来越受到关注[4-5]。普罗帕酮是广谱高效的钠通道阻滞类抗心律失常药,临床上以消旋体形式给药。在阻断β受体方面,S-型异构体活性是R-型的100倍,两对映体均有钠通道阻断作用,都存在药理活性[6-7]。在人体的药代动力学上却表现出立体选择性的差异[8],故探究其对映体拆分,获得单一对映体分离分析方法对于临床具有意义。从文献报道情况来看,对普罗帕酮进行手性拆分的方法主要包括化学拆分法、色谱拆分法及萃取拆分法[9],本文以新型手性选择剂双-(6-氧-间硝基苯磺酰基)-β-环糊精(简称β-CD-N2),制备成新型HPCE手性整体柱,拆分普罗帕酮外消旋体,建立了普罗帕酮对映异构体分离分析的新方法。
1 实验部分
1.1 仪器与试剂
高效毛细管电泳仪(CL1020,负电源,北京华阳利民仪器有限公司),融硅石英毛细管柱(75μm I.D.,40cm,河北永年光纤厂)。普罗帕酮标准品(中国药品生物制品检定所),超纯水(美国Moleculer超纯水机),β-CD-N2自行合成,其他试剂均为分析纯(略)。
1.2 电泳条件
β-CD-N2整体柱为固定相,Tris-H3PO4缓冲液为流动相,溶液均经0.22μm的微孔滤膜过滤。电泳整体柱每运行一次前,分别用水及相应条件下的Tris-H3PO4缓冲液冲洗30min,采用压力进样方式。
2 结果与讨论
2.1 缓冲液pH值的变化对分离情况的影响
选择β-CD-N2衍生物HPCE整体柱,波长254nm,分离电压-25kV,普罗帕酮外消旋体浓度1.054×10-8mol/L,压力进样时间30s,环境温度25℃,Tris-H3PO4缓冲液浓度为40mmol/L拆分条件下,改变缓冲液pH值,分离结果如表1所示。
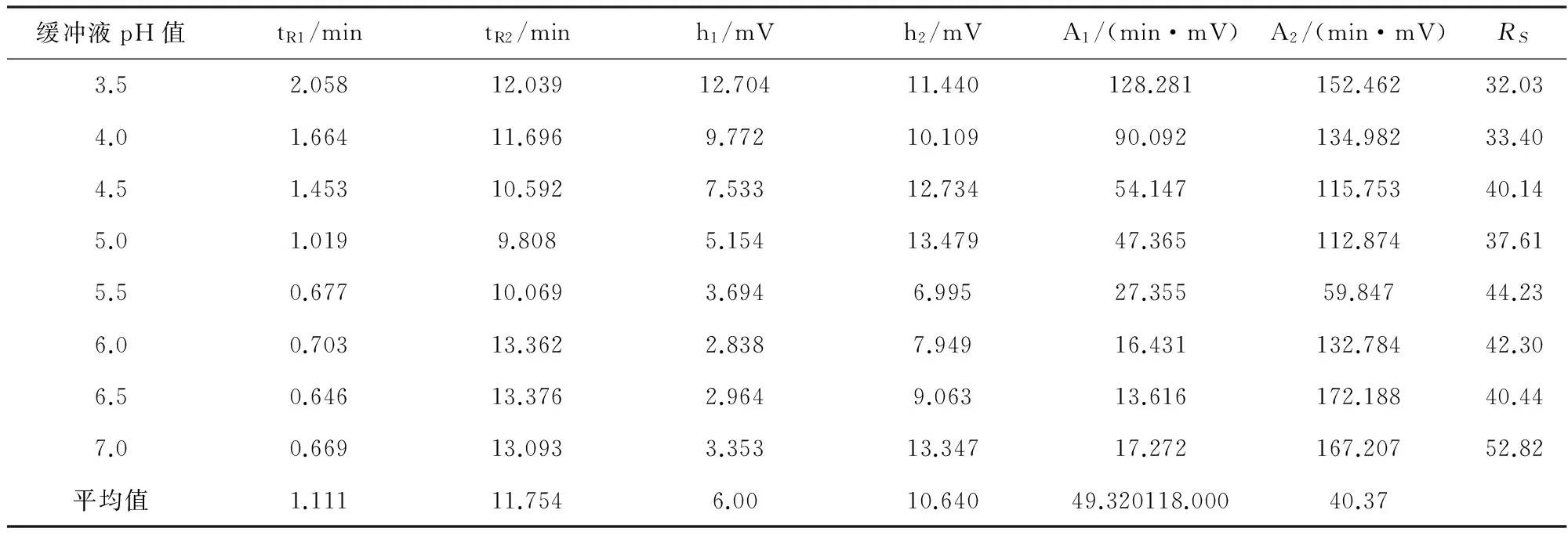
表1 缓冲液pH值的变化对分离情况的影响
在酸性至中性较宽的pH值范围(3.5~7.0),普罗帕酮外消旋体中两对映体分离度均大于32。但随着pH值的升高,流动相的洗脱强度变弱。前峰的变化更明显,综合考虑pH值4.0时对映异构体前后峰对称性、洗脱强度及基线均较理想。故选择缓冲液pH值4.0为最佳pH值。
2.2 缓冲液浓度的变化对分离情况的影响
选择2.1拆分条件,仅改变缓冲液浓度30mmol/L~70mmol/L,分离部分结果如图1所示。
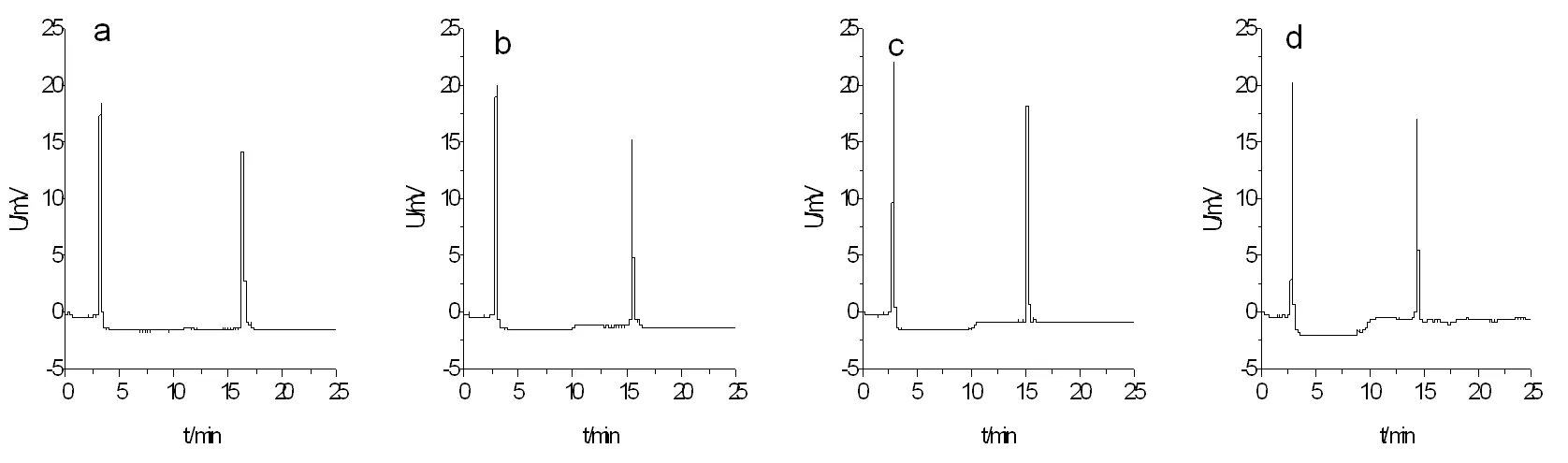
a. 30mmol/L ;b. 40mmol/L;c. 50mmol/L;d. 70mmol/L
图1 缓冲液浓度对普罗帕酮分离的影响
从图1结果可知,普罗帕酮对映异构体在此缓冲液体系适用浓度范围较宽,均能获得分离,浓度为40mmol/L时分离度达44.22,且峰型对称,基线平缓,故选定缓冲液最佳浓度为40mmol/L。
2.3 工作电压的变化对分离情况的影响
选择2.1拆分条件下,改变分离电压,分别考察-5kV、-10V、-15kV、-25kV和-28kV时普罗帕酮的拆分情况,分离部分结果如图2所示。

a.-10 kV;b. -15kV;c. -25kV;d. -28kV
图2 工作电压对普罗帕酮分离的影响
随着分离电压的升高,对映异构体的分析时间明显缩短,后峰的拖尾情况明显改善。但接近极限值-28kV对对映体峰形的干扰较大,故选择工作电压-25kV为最佳的分离电压。
2.4 方法评价
2.4.1 普罗帕酮对映体拆分的线性范围和精密度
最佳分离条件下(β-CD-N2衍生物HPCE整体柱,波长254nm,分离电压-25kV,普罗帕酮外消旋体浓度1.054×10-8mol/L,压力进样时间30s,环境温度25℃,Tris-H3PO4缓冲液浓度为40mmol/L,pH值4.0),考察线性范围,结果显示外消旋体浓度在2.280×10-9mol/L~1.054×10-8mol/L范围内与两对映体峰高、峰面积呈线性相关性。同样条件下,普罗帕酮浓度1.054×10-8mol/L,重复进样6次,考察精密度。结果显示,前峰,后峰保留时间RSD分别为3.79%,3.65%;峰高RSD分别为4.21%,6.31%;峰面积RSD分别为6.31%,1.73%。
2.4.3 对比实验
最佳条件下,在β-CD-N2衍生物HPCE整体柱和HPCE空柱中分别用等量的普罗帕酮外消旋体标准品作对照,结果如图3所示,可以看出普罗帕酮对映异构体在空柱中无分离迹象,而手性整体柱对其拆分作用理想。

a. β-CD-N2手性整体住;b.空柱
图3 普罗帕酮对映异构体在不同毛细管柱中的分离
3 结语
用双-(6-氧-间硝基苯磺酰基)-β-环糊精手性HPCE整体柱拆分手性药物普罗帕酮,采用单一变量法,分别考察缓冲液pH值、浓度和工作电压等条件对分离的影响,与空柱对比有显著的拆分效果,建立了手性药物普罗帕酮拆分的HPCE新方法。结果表明,具有环状疏水空腔的β-环糊精经衍生化后,苯环产生的π-π共轭作用,硝基、磺酰基与对映异构体的协同作用,增强了β-CD-N2衍生物与普罗帕酮两对映异构体的手性选择性差异,使得普罗帕酮对映异构体在适宜的条件下获得拆分。在pH值4.0,浓度为40mmol/L的Tris-磷酸缓冲液中,压力进样30s,工作电压-25kV,检测波长254nm的条件下,普罗帕酮对映体在β-CD-N2手性HPCE整体柱上分离度Rs达到52.82,明显优于文献9中结果(在毛细管区带电泳中,用单-3-氧-苯氨基甲酰基-β-CD为手性添加剂,分离普罗帕酮,分离度3.32)。实验结果经反复验证,重现性佳,普罗帕酮消旋体浓度在2.280×10-9mol/L~1.054×10-8mol/L范围内两对映体峰高和峰面积等响应信号与浓度有线性相关性。
[1] Escuder-Gilaber L, Martín-Biosca Y, Medina-Hernández M J. Cyclodextrins in capillary electrophoresis: Recent developments andnew trends[J].Journal of Chromatography A,2014,1357:2-23.
[2] Li L, Xia L, Quan L, et al. A comprehensive study of the enantioseparation of chiral drugs by cyclodextrin using capillary electrophoresis combined with theoretical approaches[J]. Talanta, 2015, 142:28-34.
[3] Szabó Z I, Tóth G, Völgyi G, et al. Chiral separation of asenapine enantiomers by capillary electrophoresis and characterization of cyclodextrin complexes by NMR spectroscopy,mass spectrometry and molecular modeling[J].Journal of Pharmaceutical & Biomedical Analysis, 2016,117:389-404.
[4] Tian Y, Zhong C, Fu E, et al. Novel β-cyclodextrin derivative functionalized polymethacrylate-based monolithic columns for enantioselective separation of ibuprofen and naproxen enantiomers in capillary electrochromatography[J].Journal of Chromatography A, 2009, 1216(6):1000-1007.
[5] Min L, Tarawally M, Xi L, et al. Application of cyclodextrin-modified gold nanoparticles in enantioselective monolith capillary electrochromatography[J]. Talanta, 2013, 109(9):1-6.
[6] Funck-Brentano C, Kroemer H K, Lee J T, et al. Propafenone[J].New England Journal of Medicine,1990,322: 516-525.
[7] Bryson H M, Palmer K J, Langtry H D, et al. Propafenone. A reappraisal of its pharmacology, pharmacokinetics and therapeutic use in cardiac arrhythmias[J].Drugs, 1993, 45(1):85-130.
[8] 钟大放,王亚芹,王爱民.普罗帕酮的对映体选择性药代动力学研究[J].中国临床药理学杂志,1997,2:82-87.
[9] Li G, Lin X, Zhu C, et al. New derivative of β-cyclodextrin as chiral selectors for the capillary electrophoretic separation of chiral drugs[J].Analytica Chimica Acta, 2000, 421(1):27-34.
(本文文献格式:柯雅莉,沈静茹,郭小倩,等.新型高效毛细管电泳手性整体柱拆分普罗帕酮[J].山东化工,2016,45(04):1-3.)
The Novel Chiral Monolithic HPCE Column for Propafenone Enantiomers Resolution
Ke yali,Shen Jingru*,Guo Xiaoqian,Zhang Bingna
(key laboratory of Analytical Chemistry of the State Ethnic Affair Commission,College of Chemistry and Materials Science,South-Central University for Nationalities,Wuhan 430074,China)
Using bis-(6-oxygen-m-nitro benzene sulfonyl)-β-cyclodextrins as chiral selector, a chiral HPCE monolithic column was prepared in Situ polymerization reaction. The chiral separation performance of column for Propafenone enantiomer was investigated, the separation conditions were optimized. Under optimal conditions, the resolutionRSreached 52.82. An effective separation method of Propafenone enantiomer was established.
bis-(6-oxygen-m-nitro benzene sulfonyl)-β-cyclodextrins; chiral HPCE monolithic column; propafenone; chiral separation
2016-01-09
中央高校基金资助项目(CZW14053)
柯雅莉(1990—),女,福建晋江人,硕士研究生,手性药物分离分析;通讯作者:沈静茹。
O657.7
A
1008-021X(2016)04-0001-03
