琥乙红霉素与二甲酚橙荷移反应及其测定*
2016-09-03王晓玲
王晓玲,张 萍,王 欢
(咸阳师范学院化学与化工学院,陕西 咸阳 712000)
琥乙红霉素与二甲酚橙荷移反应及其测定*
王晓玲,张萍,王欢
(咸阳师范学院化学与化工学院,陕西咸阳712000)
研究了在无水乙醇-盐水介质中,琥乙红霉素与二甲酚橙能发生电荷转移反应,生成电荷转移型络合物,据此建立了琥乙红霉素荷移光度分析的新方法。实验最大吸收波长为580 nm,表观摩尔吸光系数为9.82×103L·mol-1·cm-1线性回归方程为y=1.245x-0.0598,相关系数r=0.9997,琥乙红霉素的量在200~600 μg/10 mL范围内服从比尔定律。方法灵敏度较高、选择性和重现性好,用于琥乙红霉素片及琥乙红霉素胶囊中琥乙红霉素含量的测定,其相对标准偏差为0.23%~0.75%,加标回收率为99.0%~101%。
分光光度法;琥乙红霉素;荷移反应;二甲酚橙
电荷转移反应是由电子相对丰富的分子-电子给予体和电子相对缺乏的分子-电子接受体之间通过电荷转移而形成新的络合分子的过程,若反应过程吸收的是可见光的能量,则该物质就会是因电荷转移而显色。琥乙红霉素分子中叔氨基上的氮原子有孤对电子,可作为电子给予体; 二甲酚橙是一平面缺电子体系,其中心碳原子和两个氮原子上都带有正电荷,显正电性,可作为电子接受体,二者在无水乙醇-盐水介质中,能发生电荷转移反应而显色,据此建立了电荷转移光度法测定琥乙红霉素的新方法,目前测定琥乙红霉素的方法主要有色谱法[1-2]、药典学[3]、流动注射化学发光法[4-5]、差示旋光法[6]、分光光度法[7-10]等。而利用二甲酚橙和琥乙红霉素的荷移反应测定琥乙红霉素的方法未见报道。该方法利用氯化钠作为增敏剂和增温剂,灵敏度较高,体系稳定,成功测定了药剂中琥乙红霉素的含量。
1 实 验
1.1主要仪器及试剂
722S可见分光光度计(上海佑科仪器仪表有限公司)UPK-11-40型优普超纯水机(上海优普实验有限公司);PHS-2C型精密酸度计。
1 mg/mL琥乙红霉素标准液:在分析天平上准确称取琥乙红霉素的标准样品0.1000 g于小烧杯中,加少量无水乙醇使之完全溶解,用无水乙醇定溶到100 mL;2.63×10-3mol/L 二甲酚橙溶液:准确称量二甲酚橙0.5000 g在烧杯中,用水溶解溶解后定容至250 mL。
1.2实验方法
在两只25 mL比色管中,分别加入二甲酚橙溶液0.3 mL,向其中一支加入0.2 mL琥乙红霉素标准溶液,另一支不加,再分别加入饱和食盐水2.5 mL、无水乙醇0.2 mL,加水定容至10 mL,摇匀。以试剂空白为参比,用1 cm比色皿在分光光度计上,测定580 nm处吸光度值 A。
2 结果与讨论
2.1吸收曲线
根据实验方法配制空白和试剂溶液,在400~650 nm波长范围内测定吸光度A0和A,作出吸收曲线图。如图1所示,曲线1为二甲酚橙的吸收曲线,其最大波长在440 nm,曲线2为琥乙红霉与二甲酚橙反应生成荷移络合物的曲线图,其最大吸收波长为580 nm,荷移络合物的最大吸收波长比试剂空白的最大吸收波长红移了140 nm。选择580 nm为实验波长。
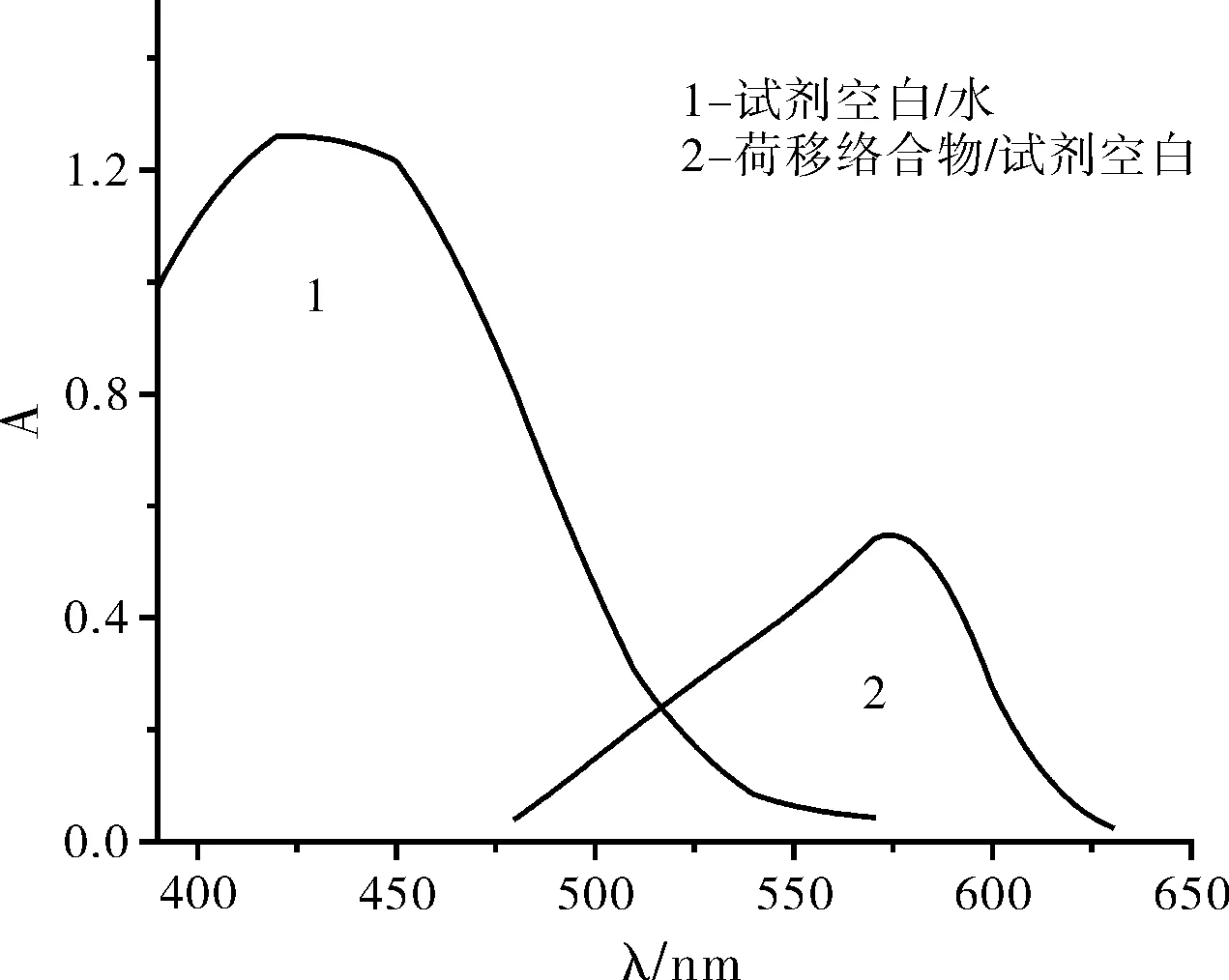
图1 吸收曲线图
2.2反应条件探索
2.2.1介质的选择及用量
按实验方法,试验了HCl、H2SO4、H3PO4、KCl-HCl、邻苯-HCl、KH2PO4-NaOH(pH=7.2)、H3BO3-KCl-NaOH(pH=8.53)、硼砂-NaOH(pH=11.04)、KCl-NaOH(pH=13.0)无水乙醇等溶液对反应体系的影响。实验显示在无水乙醇介质中显色反应效果较好。实验选用无水乙醇为介质。
2.2.2无水乙醇的用量
试验设4个处理,采取随机区组排列,3次重复,小区面积为1m×50m=50m2,播种量为15 g/m2。4个处理播种期:T1:4月 10 日,T2:5月 10 日,T3:6 月9日,T4:8月9日。选用120 cm宽的黑地膜,对试验地进行一致处理,微起垄,垄高10 cm,垄面100 cm,垄间距20 cm。地膜覆好后,2 m一个土腰带(宽10 cm),在膜面上用点播器打穴眼,穴眼深0.5 cm,穴距9 cm,行距3 cm,打眼器直径为9 cm,播种行数为8行,全部铺设喷灌在干旱时及时补水,种植密度40 穴 /m2。
实验显示,无水乙醇的用量在0.1~0.3 mL 范围内A趋于稳定,此后吸光度A虽然在慢慢增大,但反应体系不够稳定,综合考虑以0.2 mL为无水乙醇的最佳用量
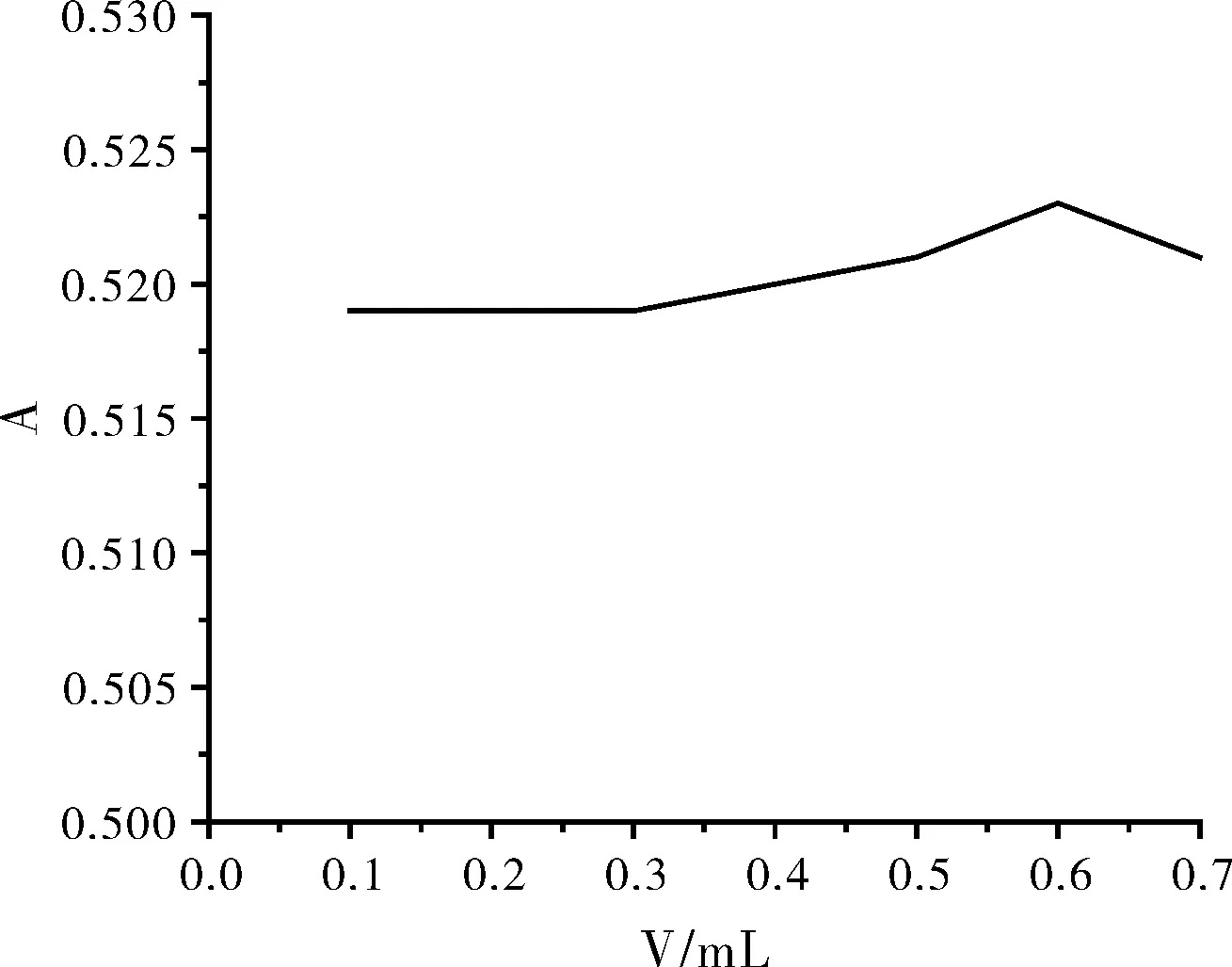
图2 无水乙醇用量
2.2.3二甲酚橙的用量
随着二甲酚橙用量的增加,吸光度在A在慢慢增大,当二甲酚橙的量为0.3 mL时A值达到最大且稳定,此后随着其用量的增大A值漫漫减小,以0.3 mL作为二甲酚橙的最佳用量。
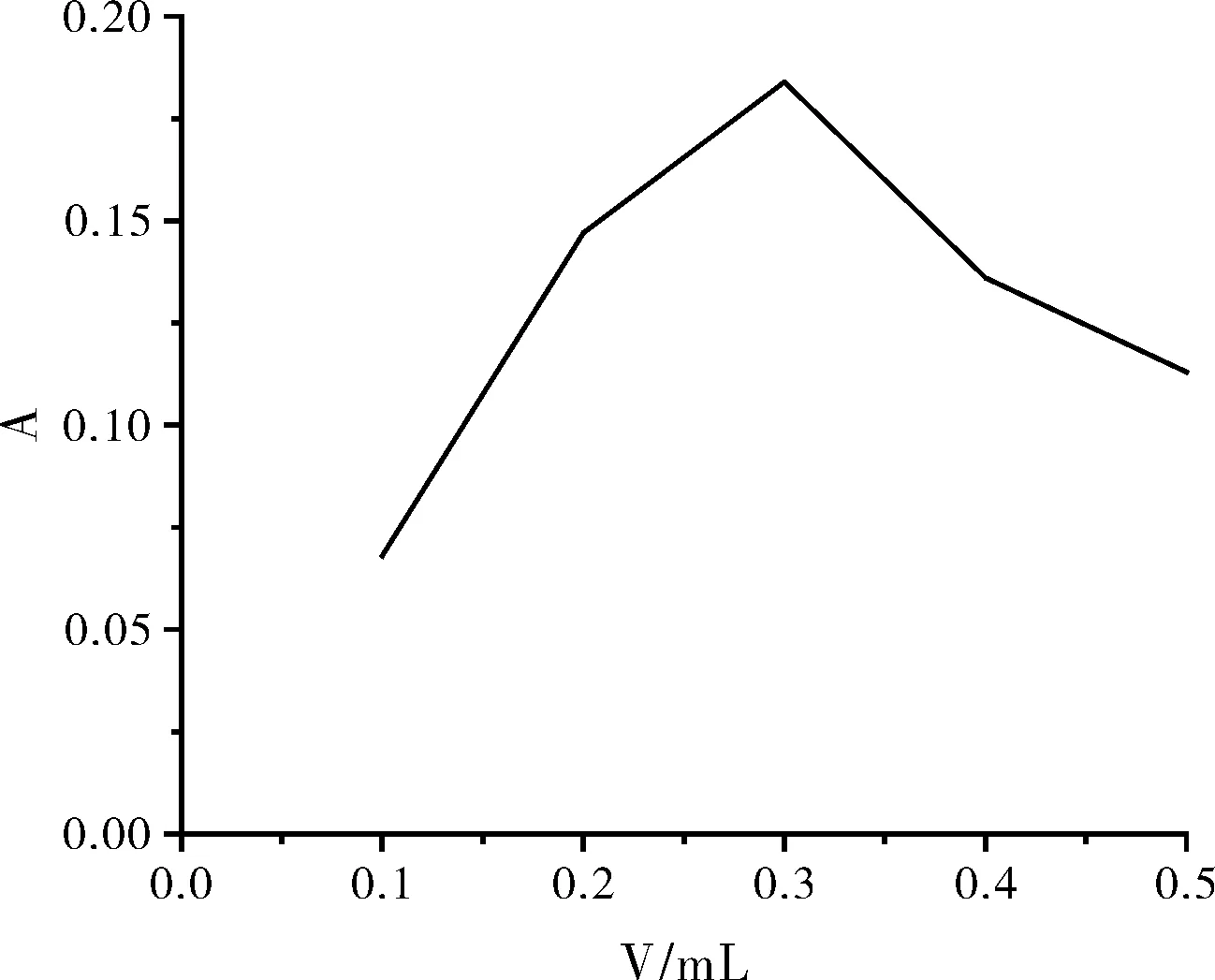
图3 二甲酚橙的用量
2.2.4离子强度的影响
按照实验方法,试验了可溶性的硝酸盐、硫酸盐、盐酸盐等,发现加入饱和氯化钠后,反应体系的稳定性和灵敏度都有明显提高,当饱和氯化钠用量在1.5 mL~3.0 mL时,ΔA大且稳定。实验选用饱和氯化钠的最佳用量为2.5 mL。
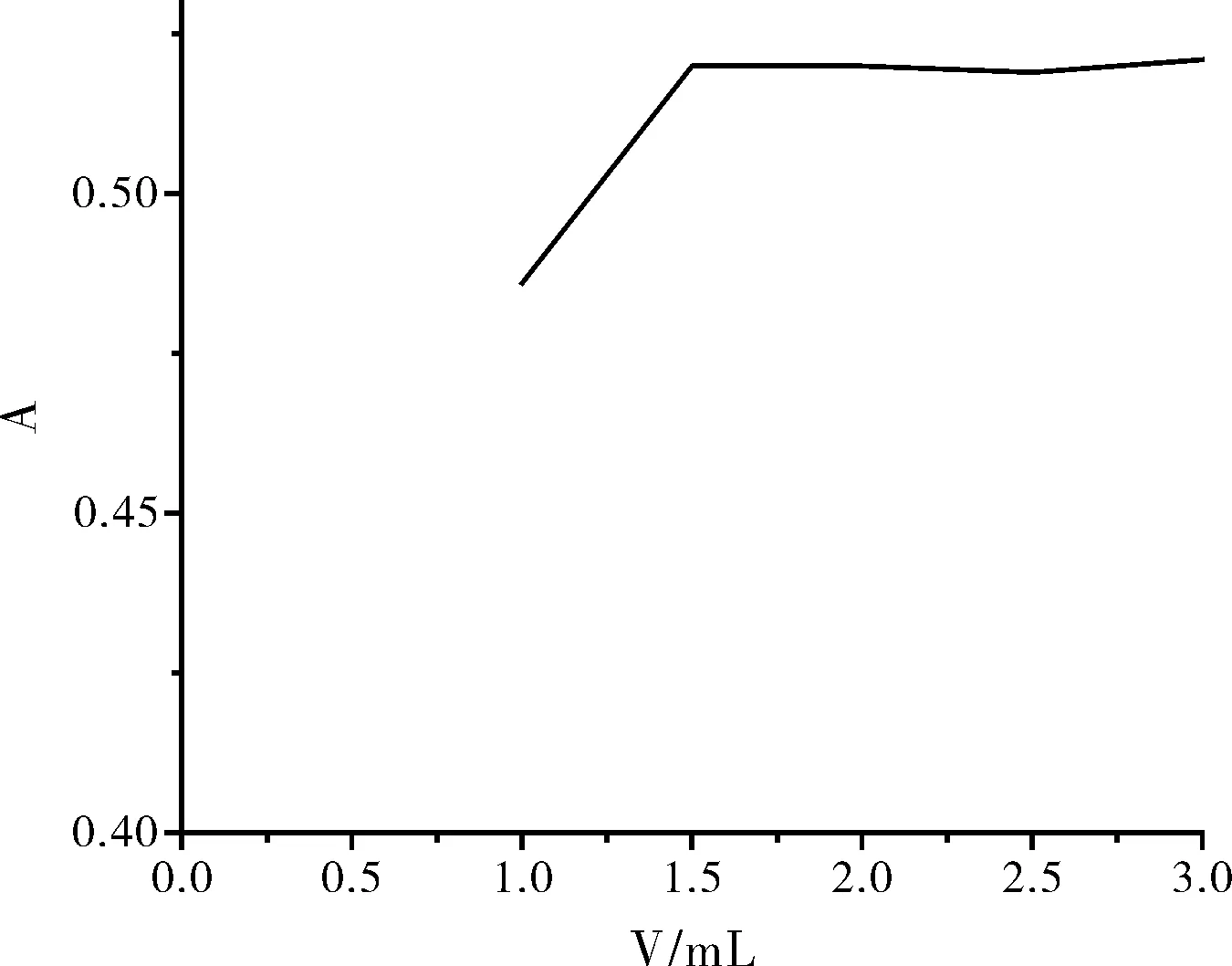
图4 饱和氯化钠用量

琥乙红霉素V/mL不加饱和盐水A加饱和盐水AΔA灵敏度0.30.2510.3180.067提高26.8%
2.2.5反应温度和时间影响
在常温下,显色反应迅速发生,在不同的反应时间下,测定A值的变化。结果发现A值基本没有变化。故此反应在常温下进行,与反应时间无关。
2.2.6反应顺序的影响
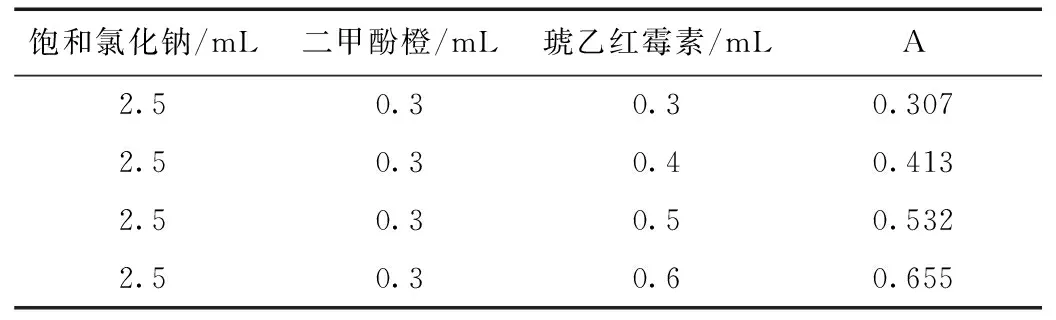
表2 反应顺序1

表3 反应顺序2
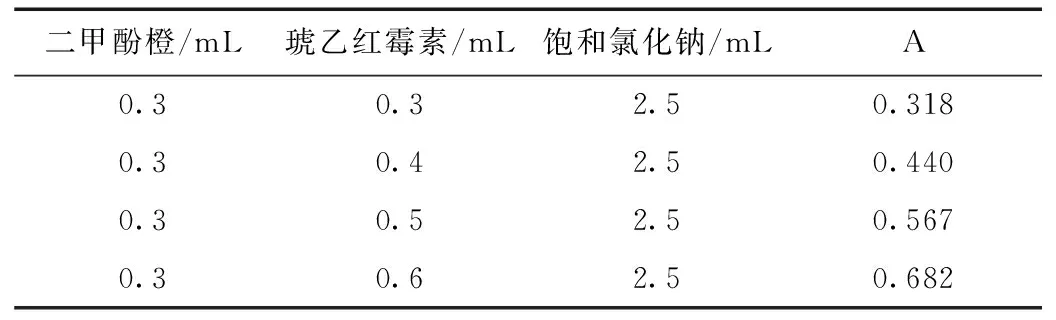
表4 反应顺序3
2.2.7工作曲线
配制琥乙红霉素的系列标准溶液,在最大吸收波长580 nm处,测定其不同的吸光度A值,以标准溶液的量为横坐标,吸光度值为纵坐标,绘制工作曲线,其线性回归方程为y=1.245x-0.0598,相关系数r=0.9997,表观摩尔吸光系数为9.82×103L·mol-1·cm-1,琥乙红霉素的量在200~600 μg/10 mL范围内与A呈良好的线性关系。
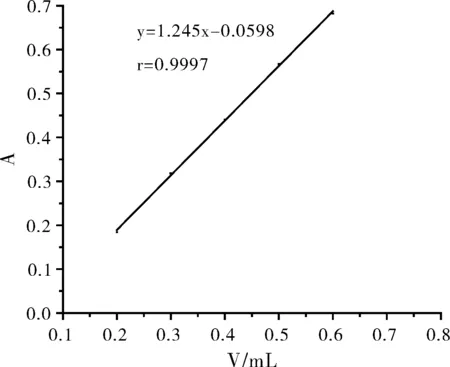
图5 工作曲线图
2.2.8干扰离子
对0.3 mg/10 mL琥乙红霉素进行测定,当相对误差≤±5%时,考察了常见离子和药物赋形剂的干扰情况。实验表明,200倍的淀粉;60倍的精氨酸;40倍的葡萄糖均不干扰测定。
2.3琥乙红霉素与二甲酚橙反应机理探讨
按试验方法,应用等摩尔连续变化法和斜率比法测得琥乙红霉素与二甲酚橙络合比为1:1。琥乙红霉素分子中叔氨基上的氮原子有孤对电子,可作为电子给予体; 二甲酚橙是一平面缺电子体系,其中心碳原子和两个氮原子上都带有正电荷,显正电性,可作为电子接受体,二者反应可以生成1:1的电荷转移络合物。荷移反应可表示如下:
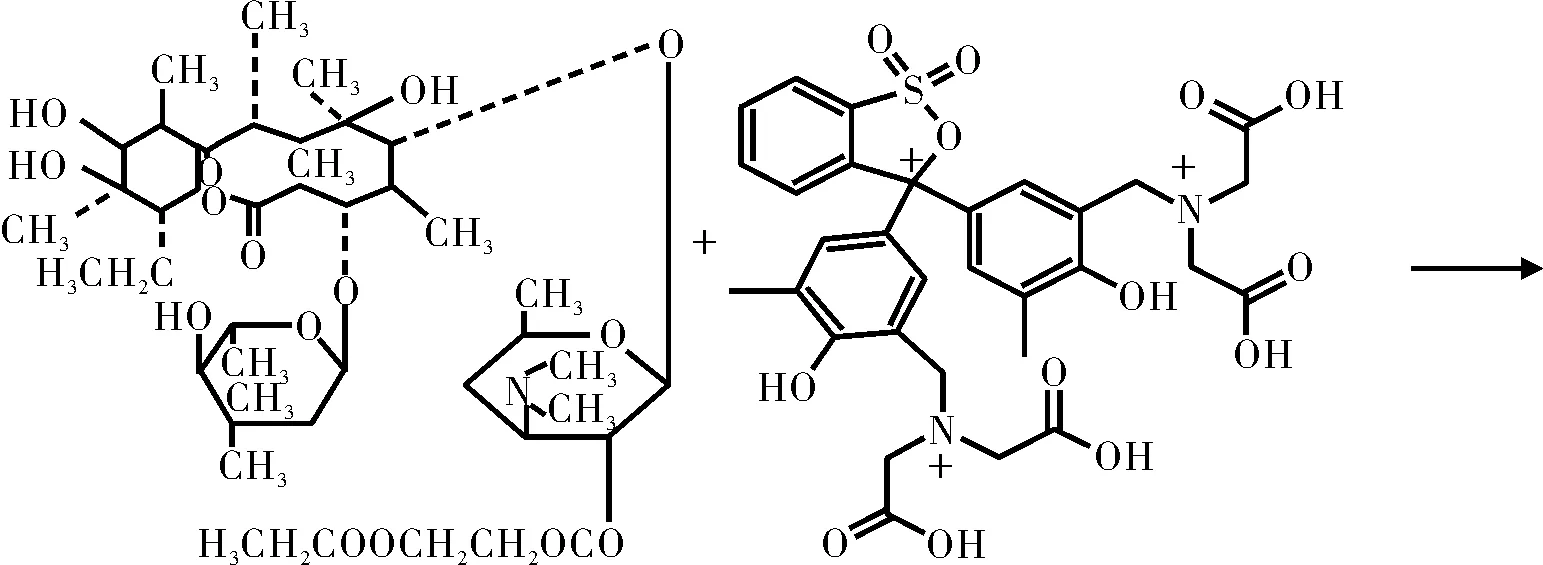

3 样品分析
3.1琥乙红霉素片
取琥乙红霉素片四片于50 mL的小烧杯中,加无水乙醇搅拌溶解、过滤,用无水乙醇定容到250 mL的容量瓶中。测定时每次取0.2 mL。
3.2琥乙红霉素胶囊
取琥乙红霉素胶囊一粒,将内容物倒入小烧杯,加适量乙醇溶解、过滤、滤液用无水乙醇定容至50 mL容量瓶中,,再取该液10 mL稀释到25 mL作为样品测定液。测定时取0.2 mL。
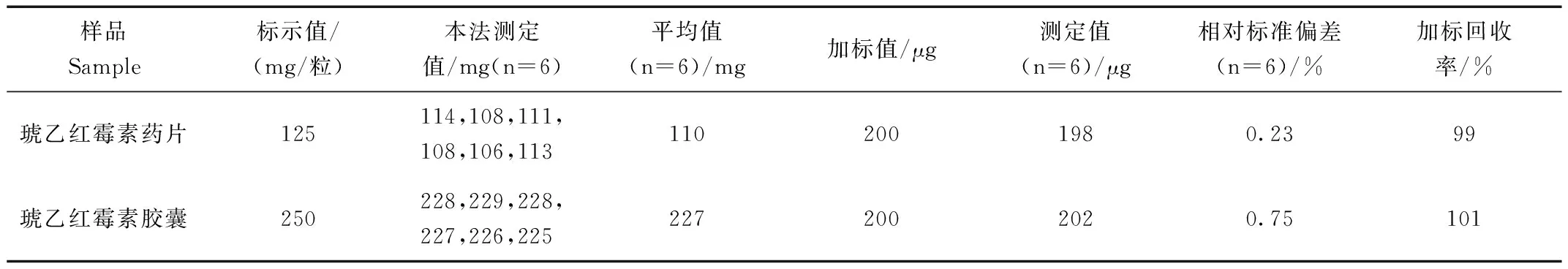
表5 样品测定结果
4 结 论
研究了在无水乙醇—盐水介质中,琥乙红霉素与二甲酚橙能发生电荷转移反应,生成电荷转移型络合物,据此建立了琥乙红霉素荷移光度分析的新方法。方法灵敏度较高、选择性和重现性好,用于琥乙红霉素片及琥乙红霉素胶囊中琥乙红霉素含量的测定,其相对标准偏差为0.23%~0.75%,加标回收率为99.0%~101%。
[1]关日晴. 高效液相色谱法测定琥乙红霉素[J].中国药品标准,2002, 3(3): 161-162.
[2]黄榕珍, 修虹, 陈水专. 高效液相色谱法测定琥乙红霉素胶囊的含量[J]. 海峡药学, 2000, 12(4): 26-27.
[3]国家药典委员会. 中华人民共和国药典.二部[M]. 北京: 化学工业出版社, 2000: 801.
[4]王建国, 汪敬武. 流动注射化学发光测定琥乙红霉素[J]. 南昌大学学报, 2007, 31(4): 370-373.
[5]张社增, 马红艳. 流动注射电化学发光分析法测定琥乙红霉素[J]. 理化检验(化学分册), 2007,.43(5): 345-347.
[6]胡德放, 黄泽兰, 殷美兰. 差示旋光法测定琥乙红霉素的含量[J]. 安徽医药, 2005, 9(10): 750-751.
[7]李华侃, 荣玉梅, 徐大庆. 红霉素琥珀酸乙酯与茜素磺酸钠的荷移反应研究[J]. 光谱实验室, 2005, 22(1): 76-79.
[8]王晓玲, 李东, 李玉兰. 紫外分光光度法测定琥乙红霉素胶囊中琥乙红霉的含量[J]. 中国药业, 2003, 12(12): 42-43.
[9]李华侃,肖井坤.琥乙红霉素与紫色素的荷移反应及其测定[J] 理化检验(化学分册), 2006, 42(9): 735-755.
[10]孙曙光.茜素红的荷转移反应测定琥乙红霉素[J] 数理医药学杂志2005, 18(1): 56-57.
Determination of Erythromycin Ethylsuccinate Based on Charge Transfer Reaction between Erythromycin Ethylsuccinate and Xylenol Orange*
WANGXiao-ling,ZHANGPing,WANGHuan
(School of Vhemistry & Vhemical Engineering, Xianyang Normal University, Shaanxi Xianyang 712000, China)
A novel spectrophotometric method for the determination of erythromycin ethylsuccinate was established based on the charge transfer reaction between ethylsuccinate and xylenolorange in ethanol-salt water. The apparent molar absorptivity of the color compleex was 9.82×103L·mol-1·cm-1at 580 nm. The linear regression equation was y=1.245x-0.0598. Beers law was obeyed in the range of 200~600 μg/10 mL of erythromycin ethylsuccinate correlation coefficient was 0.9997. The method has high sensitivity, good selectivity and reproducibility for the determination of erythromycin ethylsuccinate in erythromycin ethylsuccinate tablets with RSD of 0.23%~0.75%, and recoveries between 99.0%~101%.
spectrophotometry; erythromycin ethylsuccinate; charge-transfer reaction; xylenol orange
陕西省科技厅科研项目(2012JQ2014)。
王晓玲(1964-),女,高级工程师,大学本科,主要研究方向为光度分析和催化动力学分析。
O657.32
A
1001-9677(2016)07-0125-04
