上尿路尿路上皮癌中RASSF1A基因启动子区域的甲基化状态及其临床意义
2016-09-01熊耕砚李学松周利群
刘 瑾,熊耕砚,唐 琦,方 冬,李学松,周利群
(北京大学第一医院泌尿外科, 北京 100034)
·论著·
上尿路尿路上皮癌中RASSF1A基因启动子区域的甲基化状态及其临床意义
刘瑾,熊耕砚,唐琦,方冬,李学松△,周利群△
(北京大学第一医院泌尿外科, 北京100034)
目的:通过检测上尿路尿路上皮癌(upper tract urothelial carcinoma,UTUC)组织中RAS相关结构域家族蛋白1异构体A(RAS-association domain family protein 1 isoform A,RASSF1A)基因启动子区域的甲基化状态,探讨RASSF1A基因异常甲基化与患者临床病理特征以及术后复发的关系。方法: 采用回顾性分析方法,共入选687例在北京大学第一医院泌尿外科接受手术的UTUC患者,通过甲基化特异性聚合酶链反应的方法对RASSF1A基因启动子区域的甲基化状态进行检测。结果: UTUC组织中RASSF1A基因的甲基化率为26.6%(183/687),RASSF1A基因异常甲基化与患者年龄、性别、肿瘤多发、术前输尿管镜检查、根治性手术、肿瘤直径及合并原位癌均无相关性(P>0.05),但分别与患者吸烟史(P=0.044)、患侧肾积水(P<0.001)、肿瘤位置(P<0.001)、肿瘤形态(P=0.013)、肿瘤分期(P=0.001)、肿瘤分级(P=0.007)以及淋巴结转移(P=0.001)相关,而且后四项均为提示肿瘤恶性程度高和预后不良的病理特征。RASSF1A基因的异常甲基化状态是患者术后膀胱复发(P<0.001,HR=0.471)和对侧上尿路复发(P=0.030,HR=0.269)的独立危险因素。RASSF1A基因启动子高甲基化组的UTUC患者术后的膀胱无复发生存时间和对侧无复发生存时间均比低甲基化组长,其无复发生存时间较长和累积无复发生存率较高,此外,肿瘤多发(P=0.002,HR=1.538)和术前输尿管镜检(P=0.001,HR=1.725)分别是UTUC患者术后膀胱复发的独立危险因素。结论:RASSF1A基因启动子区域的甲基化状态是与UTUC肿瘤恶性程度显著相关的表观遗传学生物标记物和尿路复发的预后因素。
癌,移行细胞;RASSF1A基因;甲基化;生物标志物;预后因素
上尿路尿路上皮癌(upper urinary tract urothelial carcinoma,UTUC)起源于尿路上皮,位于肾盏、肾盂或输尿管等被覆移行上皮的UTUC,仅占所有尿路上皮癌的5%~10%[1-2]。根治性肾输尿管全长结合膀胱袖状切除术(radical nephroureterectomy with bladder cuff excision)是目前公认的手术治疗UTUC的金标准[3],UTUC术后容易复发,膀胱复发率为20%~47%,对侧上尿路复发率为2%~6%[1, 4-5]。膀胱复发患者大多需膀胱肿瘤电切术,对侧复发患者需再次行肾输尿管全长切除术、保留肾单位手术或姑息性输尿管镜切除术等。高复发率导致患者手术次数增加、并发症发生率增高、治疗费用增加等。广泛的全泌尿系尿路上皮癌患者,最终可能需要行根治性膀胱切除术或双侧肾输尿管切除术,降低了患者生存率并且严重影响患者生活质量。
由基因失活引起的抑癌基因功能缺失是肿瘤发生和复发的重要原因之一,可由基因缺失、基因突变或基因启动子区域高甲基化引起。近年来越来越多的研究证实表观修饰导致的基因沉默参与了尿路上皮癌的发生、发展并发挥重要作用[6-8]。RAS蛋白参与重要的细胞信号通路,调节细胞增殖、分化、凋亡等重要过程,RAS信号通路异常变化可参与肿瘤的发生发展。RAS相关结构域蛋白是RAS信号通路中重要的负效应调节子,属于RAS相关结构域蛋白家族(RAS-association domain family,RASSF),迄今共发现10种RASSF蛋白,其中9种在恶性肿瘤中表达降低或缺失。RASSF蛋白1异构体A(RAS-association domain family protein 1 isoform A, RASSF1A)属于RASSF,其基因位于人类3p21,该蛋白通过三磷酸鸟苷依赖途径与RAS蛋白结合,调节RAS的凋亡效应[9-11]。RASSF1A是研究者普遍认定的肿瘤抑制因子,多项研究证实RASSF1A基因启动子的异常高甲基化与膀胱尿路上皮癌(bladder urothelial carcinoma, BUC)的肿瘤分期、分级或复发相关[12-14]。
目前,关于RASSF1A启动子甲基化状态与UTUC患者术后复发及肿瘤特异性生存的系统性研究较少见,而且标本量少、随访时间短、诊疗标准不统一、患者入组标准不严格。由于BUC与UTUC均起源于移行尿路上皮,所以推测基因组学及表观遗传学特点有相似之处[15]。在本课题组前期的研究中,已经针对RASSF1A基因的部分表观遗传学特点进行阐述[16-17],本研究在前期研究的基础上,分析UTUC患者肿瘤标本的RASSF1A启动子甲基化状态,结合患者临床转归及生存时间等数据,探讨其与UTUC患者预后的相关性。
1 资料与方法
1.1研究对象
选择1999年至2011年就诊于北京大学第一医院泌尿外科接受手术治疗,病理诊断为UTUC且随访资料完整的患者病历资料及其肿瘤组织蜡块标本。本研究开始前经过北京大学第一医院伦理委员会审查批准,所有患者均书面知情同意。
手术方式:孤立肾或慢性肾病Ⅳ~Ⅴ期且患侧肾功能良好的UTUC患者行输尿管镜肿瘤切除术或部分输尿管切除吻合术,其余患者行肾输尿管全长切除术;对术前影像学检查显示可疑淋巴结转移或术中触及增大淋巴结的患者行局部淋巴结清扫术。排除其中有膀胱尿路上皮癌病史、或合并膀胱尿路上皮癌、或双侧UTUC的患者,最终有687位UTUC患者纳入本研究。
在术后两年内,患者每3个月定期复诊1次,若无特殊发现,两年之后复诊改为每年1次,复诊内容包括体格检查、血常规、尿常规、血生化、胸部X线、腹部超声(或CT 、MRI)、膀胱镜、尿细胞学检查(或尿荧光原位杂交)等。
1.2甲基化特异性聚合酶链反应
提取DNA:切取8片厚度为5 μm的肿瘤组织蜡块标本切片,使用DNA提取试剂盒(QIAamp DNA FFPE Tissue Kit, Qiagen, Germany)并按照其操作说明提取组织DNA,并测量DNA浓度。
亚硫酸氢盐转化:取1.5 μg DNA使用亚硫酸氢盐转化试剂盒(EpiTect Fast Bisulfite Conversion Kits, Qiagen, Germany) 进行亚硫酸氢盐转化及纯化。
甲基化特异性聚合酶链反应(methylation-specific polymerase chain reaction,MSP):扩增RASSF1A基因启动子序列-204~-36 bp(相对于RASSF1A基因的转录位点),该区域存在16个CG位点[18-19],本研究检测了位点1、2、3、14、15、16(图1)。使用亚硫酸氢盐转化DNA和MSP试剂盒(EpiTect MSP Kit, Qiagen, Germany)进行RASSF1A基因启动子甲基化状态的检测,RASSF1A基因启动子高甲基化上游引物为5′-GGGTTTTGCGAGAGCGCG-3′,下游引物为5′-GCTAACAAACGCGAACCG-3′,退火温度为64℃,扩增片段为169 bp;RASSF1A基因启动子低甲基化上游引物为5′-GGTTTTGTGAGAGTGTGTTTAG-3′,下游引物为5′-CACTAACAAACACAAACCAAAC-3′,退火温度为59 ℃,扩增片段为169 bp。甲基化人类基因组DNA(EpiTect Control DNA and Control DNA Set, Qiagen, Germany)作为阳性对照,无核酸酶水(nuclease-free water, Qiagen, Germany)作为阴性对照,将PCR管置于PCR仪中,95 ℃ 10 min,94 ℃变性15 s,退火30 s,72 ℃扩展30 s;重复前一步骤,至38个循环,72 ℃扩展10 min。
电泳及显像:制作3%(质量分数)琼脂糖凝胶,显像剂为0.6%(质量分数)溴化乙锭溶液,置于电泳槽中的电泳液中;PCR产物及DNA ladder各取10 μL加到凝胶上样孔中,电压120 V,直流电泳15 min;将凝胶置于凝胶成像分析系统Gel Doc 1000中紫外线显像。
由于癌旁正常组织中RASSF1A基因启动子的甲基化率极低,本实验未配对检测癌旁正常组织[12-14]。
1.3统计学分析
使用SPSS 21.0软件进行统计处理,分析患者的临床随访数据和标本甲基化数据,明确RASSF1A基因启动子区域甲基化与UTUC患者临床病理特征的相关性,以及对肿瘤特异性生存(cancer-specific survival,CSS)、术后膀胱无复发生存(bladder recurrence-free survival,BRFS)和术后对侧无复发生存(contralateral recurrence-free survival,CRFS)进行生存分析,明确预后因素。数据分析方法:Pearson’s卡方检验用来分析分类变量; Mann-WhitneyU检验和Kruskal-WallisH检验用来分析连续变量;Log-rank检验和Cox 回归分析分别用来进行单变量和多变量的生存分析;CSS、BRFS和CRFS的生存分析分别以肿瘤特异性死亡及手术后出现膀胱复发或对侧上尿路复发为终点时间,P<0.05认为差异有统计学意义。
2 结果
共有687位病理诊断为UTUC的患者纳入本研究,年龄20~90岁(表1),中位年龄为68岁,随访3~144个月,中位随访时间为48个月,中位生存时间为115个月(95%CI: 99~131个月), 5年累积生存率为69.6%(±2.0%)。随访期间有225位患者(32.8%)死于UTUC,有228位患者(33.2%)术后膀胱复发,有36位患者(5.2%)术后对侧复发(表2)。
2.1RASSF1A基因启动子区域高甲基化与提示预后不良的临床病理特征显著相关
通过单因素Logistic回归方法,分析UTUC患者的临床病理特征与RASSF1A基因启动子甲基化状态的关联性,共有183例患者(26.6%)的DNA样本中可检测到RASSF1A基因启动子高甲基化,异常的甲基化状态分别与患者的吸烟史(P=0.044)、同侧肾积水(P<0.001)、肿瘤位置(P<0.001)、浸润型生长形态 (非乳头状,P=0.013)、高肿瘤分期(pT3/4,P=0.001)、高肿瘤分级 (G3,P=0.007)以及有淋巴结转移 (pN+,P=0.001)相关,而后4项均为提示患者预后不良的病理特征(表1)。
2.2RASSF1A基因启动子的甲基化状态与UTUC患者的肿瘤特异性生存分析
因UTUC死亡组患者和因其他疾病死亡组患者的RASSF1A基因启动子高甲基化的比率分别为25.5%(118/462 例)和28.9%(65/225 例),两组间差异无统计学意义(P=0.352,表2)。通过单变量及多变量生存分析,老年、男性、肿瘤多发、并发肾积水、术前未进行输尿管镜检、肿瘤直径大、肿瘤高分期及有淋巴结转移均是肿瘤特异性生存的不良预后因素(表3和4)。RASSF1A基因启动子高甲基化组与低甲基化组的患者之间,肿瘤特异性生存时间和累积生存率差异均无统计学意义(P=0.093,图2A)。
2.3RASSF1A基因启动子的甲基化状态与UTUC患者术后的膀胱无复发生存分析
膀胱无复发组患者和膀胱复发组患者的RASSF1A基因启动子高甲基化的比率分别为33.1% (152/459例)和13.6%(31/228例), 前者高于后者 (P<0.001,表2)。通过单变量及多变量生存分析发现, UTUC患者术后膀胱复发的独立危险因素是RASSF1A基因启动子低甲基化(P<0.001,HR=2.123)、肿瘤多发(P=0.002,HR=1.538)、术前输尿管镜检(P=0.001,HR=1.725)以及无淋巴结转移(P=0.021,HR=3.228,表3和4)。相比RASSF1A基因启动子低甲基化组,高甲基化组的UTUC患者术后的膀胱无复发生存时间较长,累积生存率较高(P<0.001,图2B)。

表1 RASSF1A基因启动子的甲基化状态与UTUC患者临床病理特征
n=687,*Statistically significant:P<0.05. ☆Age is a continuous variable and is presented as median and range. # In the univariate analysis, tumor stage was stratified into low tumor stage (T1 or T2) and high tumor stage (T3 or T4),and tumor grade was stratified into low tumor grade (G1 or G2) and high tumor grade (G3).

表2 UTUC死亡或复发的患者中RASSF1A基因启动子甲基化状态的分布
*Statistically significant:P<0.05 . # Presented as the number of patients.
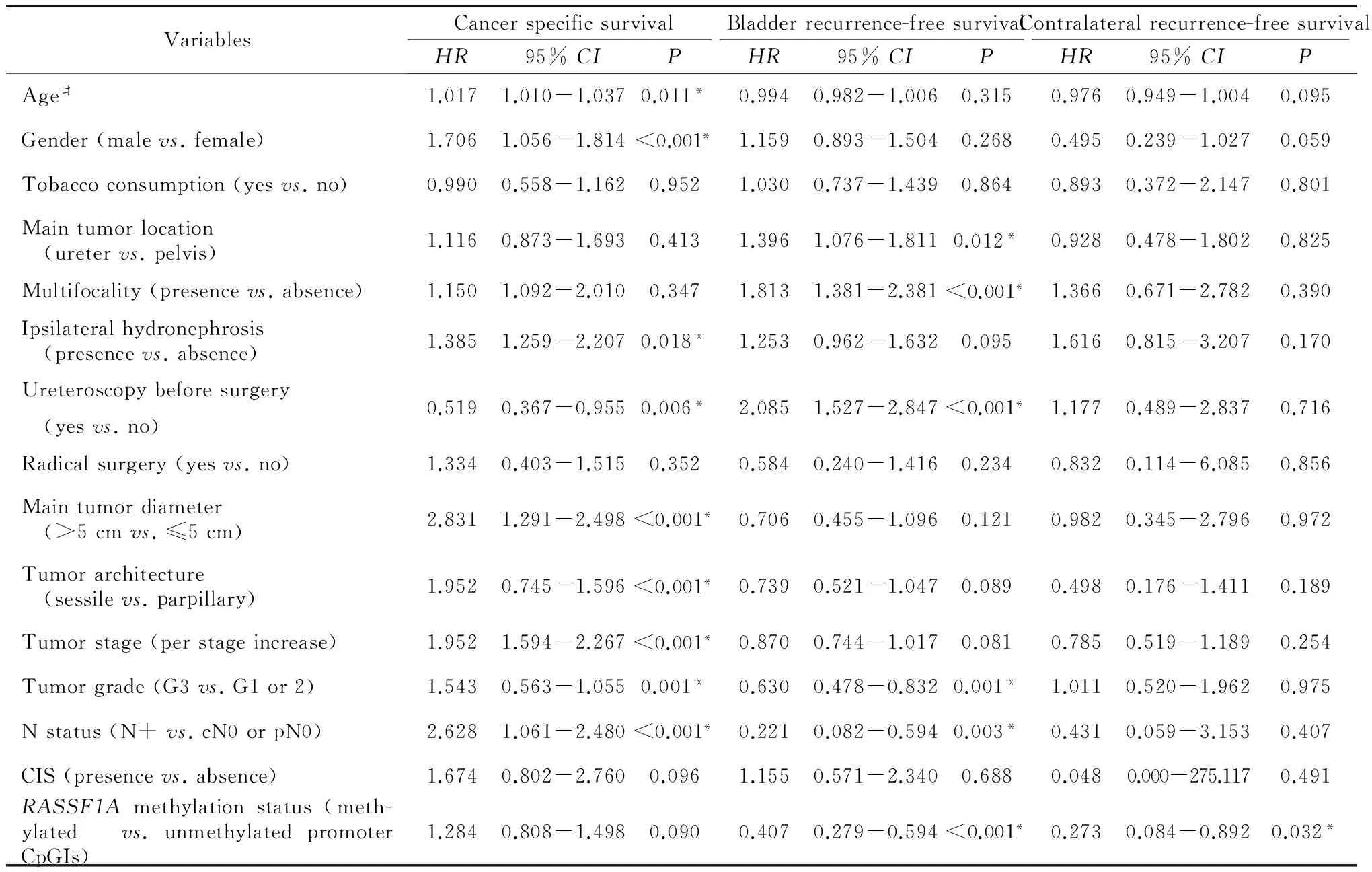
表3 UTUC患者生存和复发预后因素的单因素分析
HR, hazard ratio. # Age is a continuous variable and it is presented as median and range. *Statistically significant:P<0.05.

表4 UTUC患者生存和复发预后因素的多因素分析
HR, hazard ratio. # Age is a continuous variable and is presented as median and range. *Statistically significant:P<0.05.
2.4RASSF1A基因启动子的甲基化状态与UTUC患者术后的对侧上尿路无复发生存分析
对侧无复发组患者和对侧复发组患者的RASSF1A基因启动子高甲基化的比率分别为 27.6%(180/651例)和8.3% (3/36例), 前者明显高于后者 (P=0.011,表2)。通过单变量及多变量生存分析发现, UTUC患者术后对侧复发的独立危险因素是RASSF1A基因启动子低甲基化(P=0.032,HR=3.663,表3和4)。相比RASSF1A基因启动子低甲基化组,高甲基化组的UTUC患者术后的对侧无复发生存时间较长,累积生存率较高(P=0.021,图2C)。
The primers designed for MSP were aimed at the 1, 2, 3 and 14, 15, 16 CG sites which are shown in red, and the rest CG sites are shown in blue. The 16 CG sites (1-16) are shown in bold.
图1甲基化特异性聚合酶链反应检测的RASSF1A基因启动子序列
Figure 1The nucleotide sequences of RASSF1A gene promoter amplified by MSP
3 讨论
RASSF1A是研究者普遍认定的肿瘤抑制因子,属于RAS相关结构域蛋白家族,其基因位于人类3p21,与鼠蛋白Nore1的基因序列同源。RASSF1A蛋白含有C端的RAS相关结构域、N端二酰基甘油结合/蛋白激酶C保守结构域以及ATM磷酸化位点,该蛋白通过三磷酸鸟苷依赖途径与RAS蛋白结合,调节RAS的凋亡效应[10-11]。最初在肺癌和乳腺癌的肿瘤组织中发现了RASSF1A基因启动子的高甲基化[18],之后,许多研究发现表观修饰导致的RASSF1A基因表达降低在肿瘤发展中的作用(如神经胶质瘤、前列腺癌、鼻咽癌等), 并在体内外细胞实验中发现再表达RASSF1A基因可抑制肿瘤细胞的生长[20-22]。最近研究表明,RASSF1A基因启动子的甲基化状态可作为肿瘤诊断或预后的生物标记物[23-24]。本实验进一步证实了RASSF1A基因启动子的甲基化作为潜在的UTUC肿瘤早期诊断和肿瘤进展预测因子的可行性。
3.1临床病理特征
本实验共有183例患者(26.6%)的DNA样本中可检测到RASSF1A基因启动子高甲基化,统计分析结果显示,RASSF1A高甲基化与4项提示肿瘤恶性度高、患者预后不良的病理特征显著相关,分别为浸润型生长、高肿瘤分期(pT3/4)、高肿瘤分级 (G3)以及淋巴结转移 (pN+)。有学者也发现RASSF1A高甲基化与肌层浸润、高肿瘤分期或分级、肿瘤进展等提示患者预后不良的病理特征相关[12-14],与本实验的研究结果一致。基因启动子高甲基化导致抑癌基因RASSF1A表达降低,可能是其与肿瘤恶性度高、患者预后不良的病理特征显著相关的原因。
3.2肿瘤特异性生存分析
本实验发现在肿瘤恶性程度高的UTUC患者中,肿瘤标本的RASSF1A高甲基化比例更高,与之前的研究一致[14, 25],但RASSF1A基因启动子高甲基化组与低甲基化组的患者之间,肿瘤特异性生存时间和累积生存率差异无统计学意义(P=0.093),这可能是因为患者的肿瘤特异性生存还与其年龄、性别、肿瘤多发、肿瘤直径、患侧肾积水等多因素相关(表4)。
3.3膀胱无复发生存分析与对侧上尿路无复发生存分析
本实验入组UTUC患者中,在随访期间出现术后膀胱复发或对侧上尿路复发的患者比率分别为33.2%和5.2%,与其他报道一致[1]。RASSF1A基因启动子低甲基化是UTUC患者术后膀胱复发和对侧复发的独立预后因素。尽管RASSF1A基因启动子高甲基化与不良预后的病理特征相关,但通过BRFS和CRFS生存分析,与RASSF1A低甲基化组患者相比,高甲基化组患者的无复发生存时间较长,累积无复发生存率较高(表2,图2B、2C)。在一项关于非肌层浸润型膀胱癌(non-muscle invasive bladder cancer,NMIBC)的甲基化状态的回顾性研究中[26],发现无复发NMIBC组患者的甲基化比率明显高于复发组NMIBC组患者,与本实验的研究结果一致。此外,单因素和多因素生存分析显示术前膀胱镜检、肿瘤多发以及无淋巴结转移是UTUC患者术后膀胱复发的独立危险因素。
本研究以上结果的可能原因分析如下:第一,有淋巴结转移的患者可能在癌症复发前已经死亡,所以患者术前无淋巴结转移,实质上并不是膀胱复发的真正的独立危险因素;第二,有报道在肿瘤分期和临床转归方面[27],膀胱复发高危组和低危组的患者间并没有显著差异,提示肌层浸润与膀胱复发的机制可能并不相同,所以,尽管RASSF1A高甲基化的UTUC患者的肿瘤恶性程度高,是局部浸润和远处转移的高危患者,但并不意味着这部分患者是膀胱复发的高危人群;第三,本实验发现RASSF1A基因启动子低甲基化组患者的肿瘤恶性程度相对较低,一项关于巴尔干地区性肾病(Balkan endemic nephropathy,BEN)流行地区50年的回顾性研究中发现[28],BEN并发UTUC患者的肿瘤分期和分级普遍较低,近年来的研究证实BEN和BEN患者中的UTUC均与马兜铃酸(aristolochic acid,AA)暴露有关[29-30],由于马兜铃酸在人体内形成稳定的马兜铃内酰胺-DNA加合物,使整个泌尿系统的尿路上皮持续暴露于致癌因素,所以马兜铃酸相关性UTUC(aristolochic acid-associatedUTUC, AA-UTUC)患者更易发生尿路复发[31]。本试验发现,与RASSF1A高甲基化组的UTUC患者相比,低甲基化组的患者肿瘤恶性度较低但尿路复发比例较高,由此可见RASSF1A低甲基化组的UTUCs和AA-UTUCs都具有肿瘤恶性程度相对较低、尿路复发率相对较高的特点。由于含AA中药制剂曾在中国人群中应用广泛而且AA加合物在人体内稳定,其致癌作用可在停药多年后持续存在,我们推测AA-UTUC与非马兜铃酸相关性UTUC(non-aristolochic acid-associated UTUC,NAA-UTUC)间不同的基因组学和表观遗传学机制可能是中国UTUC患者人群具有独特特性的原因之一。目前实验尚存在不足,进一步我们将进行RASSF1A基因启动子序列的亚硫酸氢盐测序及RASSF1A基因功能实验,明确单个CG位点的甲基化状态、高频率甲基化位点以及基因功能改变的影响,深入探寻其与UTUC及AA-UTUC的关系。
A, estimated survival curves of cancer-specific survival (P = 0.089); B, estimated survival curves of bladder recurrence-free survival (P<0.001); C, estimated survival curves of contralateral recurrence-free survival (P= 0.021).
图2肿瘤组织中不同的RASSF1A基因启动子甲基化状态的UTUC患者术后Kaplan-Meier生存曲线
Figure 2Estimated survival curves of UTUC patients survival and recurrence stratified by methylation status of RASSF1A gene promoter CpGIs using univariable analysis by Kaplan-Meier test
3.4RASSF1A基因启动子甲基化可作为肿瘤标记物和药物作用靶点
在肿瘤进展过程中,肿瘤组织中的抑癌基因启动子高甲基化是可遗传、可持续存在、可检测到的,而在其他正常组织中肿瘤抑制基因启动子的异常甲基化几乎检测不到,因此,这种表观修饰可能成为较为可靠的、高特异性的肿瘤标记物。基于本实验结果,RASSF1A甲基化可以作为UTUC监测治疗的诊断与预后的生物标记物。由于肿瘤DNA可被释放到外周血或体液、尿液中,通过监测患者血液或尿液中的游离DNA中的RASSF1A甲基化状态,用以疾病诊断与预后评估,可减少入侵式检查方法如活组织检查的使用,此外,RASSF1A甲基化可作为新的抑癌药物作用靶点。启动子区异常甲基化导致的肿瘤抑制基因表达沉默是肿瘤发生发展的重要原因之一,因此应用DNA甲基转移酶抑制剂降低甲基化水平、重新激活沉默基因是潜在的肿瘤治疗作用靶点。
综上所述,表观修饰导致的RASSF1A表达沉默与UTUC患者的高肿瘤分期、高肿瘤分级、淋巴结转移及浸润型生长等肿瘤高恶性度的特征密切相关。RASSF1A基因启动子的甲基化状态是UTUC患者术后膀胱或对侧上尿路复发的独立危险因素,与RASSF1A基因启动子低甲基化组相比,高甲基化组的UTUC患者术后的膀胱无复发生存或对侧无复发生存的生存时间较长,累积生存率较高,因此RASSF1A基因启动子区域的甲基化状态可能是评估UTUC肿瘤侵袭性及预测患者复发有效的表观遗传学生物标记物。
[1]Roupret M, Babjuk M, Comperat E, et al. European association of urology guidelines on upper urinary tract urothelial cell carcinoma: 2015 update[J]. Eur Urol, 2015, 68(5): 868-879.
[2]Siegel R, Ma J, Zou Z, et al. Cancer statistics, 2014[J]. CA Cancer J Clin, 2014, 64(1): 9-29.
[3]Margulis V, Shariat SF, Matin SF, et al. Outcomes of radical nephroureterectomy: a series from the upper tract urothelial carcinoma collaboration[J]. Cancer, 2009, 115(6): 1224-1233.
[4]Xylinas E, Rink M, Margulis V, et al. Multifocal carcinoma in situ of the upper tract is associated with high risk of bladder cancer recurrence[J]. Eur Urol, 2012, 61(5): 1069-1070.
[5]Li WM, Shen JT, Li CC, et al. Oncologic outcomes following three different approaches to the distal ureter and bladder cuff in nephroureterectomy for primary upper urinary tract urothelial carcinoma[J]. Eur Urol, 2010, 57(6): 963-969.
[6]Besaratinia A, Cockburn M, Tommasi S. Alterations of DNA methylome in human bladder cancer[J]. Epigenetics, 2013, 8(10): 1013-1022.
[7]Costa VL, Henrique R, Danielsen SA, et al. Three epigenetic biomarkers, GDF15, TMEFF2, and VIM, accurately predict bladder cancer from DNA-based analyses of urine samples[J]. Clin Cancer Res, 2010, 16(23): 5842-5851.
[8]Monteiro-Reis S, Leca L, Almeida M, et al. Accurate detection of upper tract urothelial carcinoma in tissue and urine by means of quantitative GDF15, TMEFF2 and VIM promoter methylation[J]. Eur J Cancer, 2014, 50(1): 226-233.
[9]Hesson LB, Cooper WN, Latif F. The role of RASSF1A methylation in cancer[J]. Dis Markers, 2007, 23(1/2): 73-87.
[10]Agathanggelou A, Bieche I, Ahmed-Choudhury J, et al. Identification of novel gene expression targets for the Ras association domain family 1 (RASSF1A) tumor suppressor gene in non-small cell lung cancer and neuroblastoma[J]. Cancer Res, 2003, 63(17): 5344-5351.
[11]Allen NP, Donninger H, Vos MD, et al. RASSF6 is a novel member of the RASSF family of tumor suppressors[J]. Oncogene, 2007, 26(42): 6203-6211.
[12]Bilgrami SM, Qureshi SA, Pervez S, et al. Promoter hypermethy-lation of tumor suppressor genes correlates with tumor grade and invasiveness in patients with urothelial bladder cancer[J]. Springerplus, 2014, 3: 178.
[13]Kim J S, Chae Y, Ha Y S, et al. Ras association domain family 1A: a promising prognostic marker in recurrent nonmuscle invasive bladder cancer[J]. Clin Genitourin Cancer, 2012, 10(2): 114-120.
[14]Catto JW, Azzouzi AR, Rehman I, et al. Promoter hypermethylation is associated with tumor location, stage, and subsequent progression in transitional cell carcinoma[J]. J Clin Oncol, 2005, 23(13): 2903-2910.
[15]Zhang Z, Furge KA, Yang XJ, et al. Comparative gene expression profiling analysis of urothelial carcinoma of the renal pelvis and bladder[J]. BMC Med Genomics, 2010, 3: 58.
[16]Xiong G, Liu J, Tang Q, et al. Prognostic and predictive value of epigenetic biomarkers and clinical factors in upper tract urothelial carcinoma[J]. Epigenomics, 2015, 7(5): 733-744.
[17]Zhang L, Xiong G, Fang D, et al. Contralateral upper tract urothelial carcinoma after nephroureterectomy: the predictive role of DNA methylation[J]. J Exp Clin Cancer Res, 2015, 34: 5.
[18]Dammann R, Li C, Yoon JH, et al. Epigenetic inactivation of a Ras association domain family protein from the lung tumour suppressor locus 3p21.3[J]. Nat Genet, 2000, 25(3): 315-319.
[19]Lee MG, Kim HY, Byun DS, et al. Frequent epigenetic inactivation of RASSF1A in human bladder carcinoma[J]. Cancer Res, 2001, 61(18): 6688-6692.
[20]Hesson L, Bieche I, Krex D, et al. Frequent epigenetic inactivation of RASSF1A and BLU genes located within the critical 3p21.3 region in gliomas[J]. Oncogene, 2004, 23(13): 2408-2419.
[21]Kuzmin I, Gillespie JW, Protopopov A, et al. The RASSF1A tumor suppressor gene is inactivated in prostate tumors and suppresses growth of prostate carcinoma cells[J]. Cancer Res, 2002, 62(12): 3498-3502.
[22]Chow LS, Lo KW, Kwong J, et al. RASSF1A is a target tumor suppressor from 3p21.3 in nasopharyngeal carcinoma[J]. Int J Cancer, 2004, 109(6): 839-847.
[23]Spitzwieser M, Holzweber E, Pfeiler G, et al. Applicability of HIN-1, MGMT and RASSF1A promoter methylation as biomarkers for detecting field cancerization in breast cancer[J]. Breast Can-cer Res, 2015, 17(1): 125.
[24]Nawaz I, Moumad K, Martorelli D, et al. Detection of nasopharyngeal carcinoma in Morocco (North Africa) using a multiplex methylation-specific PCR biomarker assay[J]. Clin Epigenetics, 2015, 7(1): 89.
[25]Maruyama R, Toyooka S, Toyooka KO, et al. Aberrant promoter methylation profile of bladder cancer and its relationship to clinicopathological features[J]. Cancer Res, 2001, 61(24): 8659-8663.
[26]Casadio V, Molinari C, Calistri D, et al. DNA Methylation profiles as predictors of recurrence in non muscle invasive bladder cancer: an MS-MLPA approach[J]. J Exp Clin Cancer Res, 2013, 32: 94.
[27]Hisataki T, Miyao N, Masumori N, et al. Risk factors for the development of bladder cancer after upper tract urothelial cancer[J]. Urology, 2000, 55(5): 663-667.
[28]Cukuranovic R, Ignjatovic I, Visnjic M, et al. Characteristics of upper urothelial carcinoma in an area of Balkan endemic nephropathy in south Serbia. A fifty-year retrospective study[J]. Tumori, 2010, 96(5): 674-679.
[29]Grollman AP, Shibutani S, Moriya M, et al. Aristolochic acid and the etiology of endemic (Balkan) nephropathy[J]. Proc Natl Acad Sci USA, 2007, 104(29): 12129-12134.
[30]Nortier JL, Martinez MC, Schmeiser HH, et al. Urothelial carcinoma associated with the use of a Chinese herb (Aristolochia fangchi)[J]. N Engl J Med, 2000, 342(23): 1686-1692.
[31]Chen CH, Dickman KG, Moriya M, et al. Aristolochic acid-associated urothelial cancer in Taiwan[J]. Proc Natl Acad Sci USA 2012, 109(21): 8241-8246.
(2016-04-10收稿)
(本文编辑:王蕾)
Methylation status ofRASSF1Agene promoter in upper tract urothelial carcinoma and its clinical significance
LIU Jin, XIONG Geng-yan, TANG Qi, FANG Dong, LI Xue-song△, ZHOU Li-qun△
(Department of Urology, Peking University First Hospital, Beijing 100034, China)
Objective: To investigate the methylation status of theRASSF1Agene promoter in upper tract urothelial carcinoma (UTUC) tissues and its correlation with clinicopathologic characteristics and postoperative recurrence of primary UTUC.Methods: In a retrospective design, a total of 687 patients who underwent surgeries for primary UTUC in the urology department of Peking University First Hospital were enrolled. The methylation status of theRASSF1Agene promoter was analyzed using methylation-sensitive polymerase chain reaction on tumor specimens. Results: Aberrant methylation for theRASSF1Agene promoter was detected in 183 (26.6%) DNA samples in total. Aberrant methylation of theRASSF1Agene was strongly associated with tobacco consumption (P=0.044), ipsilateral hydronephrosis (P<0.001 ), tumor location (P<0.001 ), tumor stage (P=0.001), tumor grade (P=0.007), lymph node metastasis (P=0.001) and growth pattern (P=0.013). The methylatedRASSF1Agene promoter was an independent risk factor for bladder recurrence (P< 0.001,HR=0.471) and contrala-teral recurrence (P=0.030,HR=0.269) of UTUC after surgery. HypermethylatedRASSF1Awas predictive for improved bladder recurrence-free survival (BRFS) (P<0.001) and contralateral recurrence-free survival (CRFS) (P=0.021) in the UTUC patients. Compared with the patients with unmethylatedRASSF1A, the patients containing tumors with hypermethylatedRASSF1Ahad tendency toward longer recurrence-free survival time [(114.4±3.9) monthsvs. (84.0±3.2) months for BRFS, (138.1±1.8) monthsvs. (132.9±1.9) months for CRFS] and higher estimated cumulative recurrence-free survive rates ( five-year survival rate for example, 79.8%±3.4%vs. 57.4%±2.6% for BRFS, 98.9%±0.8%vs. 93.0%±1.4% for CRFS). Additionally, tumor multifocality (P=0.002,HR=1.538), and ureteroscopy before surgery (P=0.001,HR=1.725) were independent risk factors for bladder recurrence in postoperative UTUC patients.Conclusion: The methylation status of theRASSF1Agene promoter appears to be a promising epigenomic biomarker for assessing the aggressiveness of UTUC and a predictor predicting the urinary tract recurrence after surgery.
Carcinoma, transitional cell;RASSF1Agene; Methylation; Biomarker; Predictors
北京自然科学基金(7152146)和北京市科学技术委员会“首都临床特色应用研究”(151100004015173)项目资助Supported by the Natural Science Foundation of Beijing (7152146) and the Clinical Features Research of Capital (151100004015173)
R737.1
A
1671-167X(2016)04-0571-08
10.3969/j.issn.1671-167X.2016.04.001
△Corresponding authors’ e-mail, pineneedle@sina.com, zhoulqmail@sina.com
网络出版时间:2016-7-413:17:44网络出版地址:http://www.cnki.net/kcms/detail/11.4691.R.20160704.1317.014.html
