TG-DTA方法用于橙色发烟剂配方设计研究
2016-08-26宋东明
郜 永,关 华,宋东明,杜 珺
TG-DTA方法用于橙色发烟剂配方设计研究
郜 永,关 华,宋东明,杜 珺
(南京理工大学爆炸科学与技术国家重点实验室,江苏 南京,210094)
TG/DTA热分析技术对染料和KClO3/可燃剂体系进行分析,快速筛选出适合发烟剂体系的染料和可燃剂,并进行配方设计和发烟效果测试。选择最合适反应体系的染料1#与乳糖和KClO3作为原材料进行配方设计,测试发烟剂体系发烟时间为18s,烟雾为橙色,燃烧后残渣疏松多孔,发烟剂体系OB=-41.7%。
发烟剂;TG/DTA;KClO3;乳糖;染料
橙色烟雾信号是船舶行驶必须装配的救援信号[1],在设计时面临原料选择、配比确定等众多问题,并且研发周期较长,而DTA/TG热分析技术具有准确快速地测定含能材料的物化反应过程的特点,可以为发烟剂原材料的性能进行研究选择,所以在设计橙色发烟剂时结合热分析方法可以快速选择原料配比,缩短研发周期。
目前,国内外对于发烟剂的研究主要集中在配方设计、发烟结构设计、理论计算等方面[2]。刘洪艳[3]论述了发烟剂及其形成机理;宋志民、赵家玉等[4]设计了对人体无害的环保型红、黄、蓝彩色发烟剂;唐萌、谈伟君等[5]使用正交试验表设计了烟雾剂的组分和配方;赵陕冬、马永忠等设计了一种新型的蓝色发烟剂[6];杨建辉、姚增铜等[7]介绍了国产的发烟手榴弹和发烟罐等发烟装置;高元科、仵和平等[8]通过设计发烟装置和装药结构延长发烟时间;张全可、赵传新等[9]设计研究了设计了一种输入能量小、输出能量大、点火能力强,且输出点火时间相对较短的新型点火装置。王金生、刘艳、余庆等[10]用热分析方法研究了赤磷发烟剂的相容性等问题。
本文将DTA/TG等热分析技术与发烟剂配方设计相结合,更有效率地设计一种适用于海上救援用的橙色发烟剂。
1 实验原料及仪器
氯酸钾:济宁佰一化工有限公司,分析纯,过筛80目;乳糖:惠兴生化试剂有限公司,过80目筛;蔗糖:惠兴生化试剂有限公司,过80目筛;玉米淀粉:上海赛翁福农业发展有限公司,过80目筛;超级生粉:上海赛翁福农业发展有限公司,过80目筛;木薯粉:上海赛翁福农业发展有限公司,过80目筛。
仪器设备:HCT-2微机差热仪,北京恒久热温仪器厂。
2 发烟剂原料选择
2.1 氧化剂选择
发烟剂中染料在高温下会分解影响成烟效果,所以要求氧化剂在低温下能够点火和反应。通常采用KClO3、KClO4和硝酸盐作为氧化剂,但是大量研究实验表明效果最好的为KClO3,其分解温度为370~400℃。在遇到可燃剂时由于可燃剂碎片的进入松弛KClO3的晶格,从而降低反应温度,提高反应性,所以本文选择KClO3作为氧化剂[11]。
2.2 染料的选择
图1是4种待选染料的热分析图。
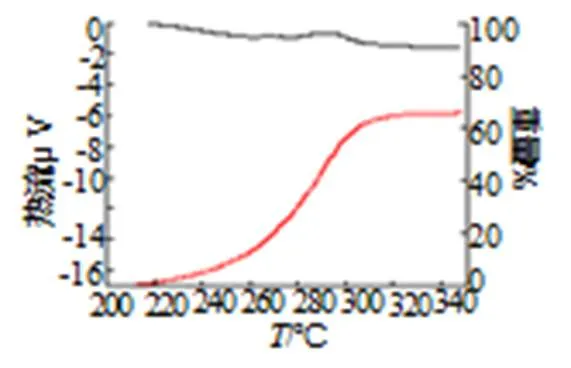
(b) 染料2

(c) 染料3
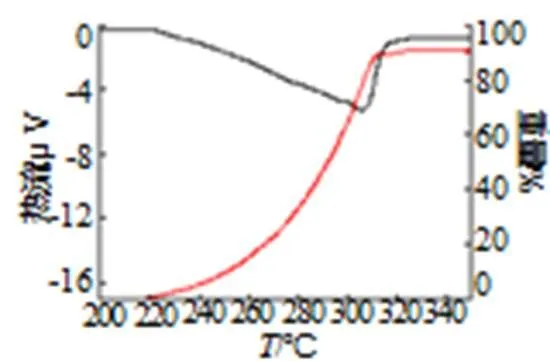
(d) 染料4
从图1中可以看到,染料的升华温度都在210~330℃之间,升华时伴随吸热过程。
表1为4种染料的热分析数据,结合表1可以看到,1号染料的失重率最高,达到100%完全升华,其次为3#和4#,约90%,最低的为2#,只有65.08%,从热分析后坩埚内部情况可以看到,1号升华干净,3#和4#均有残留,2#残留物更多,在底部结块;分析4种不同染料的单位焓变,1#最高,达到10.55J/g,3#和4#相差不大,分别为3.76J/g和3.31J/g,而2号几乎无吸热反应。有色发烟剂染料选择时要求染料尽量升华,升华速率尽可能快,以免在做成弹药时产生过多残渣,同时应避免染料氧化影响烟色,所以选择1#作为本次橙色发烟剂的染料。
表1 4种染料的热分析数据
Tab.1 Thermal analysis data of four dyes
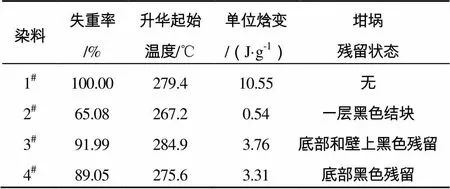
染料失重率/%升华起始温度/℃单位焓变/(J·g-1)坩埚残留状态 1#100.00279.410.55无 2#65.08267.20.54一层黑色结块 3#91.99284.93.76底部和壁上黑色残留 4#89.05275.63.31底部黑色残留
2.3 可燃剂的选择
有色发烟剂的可燃剂不能选择金属粉等与氧化剂反应过于迅速、燃烧热量过高的材料,以防止染料分解氧化,尽可能要求可燃剂燃烧产生大量气体带走升华染料,所以一般选择碳水化合物作为可燃剂[11]。本文用热分析方法研究乳糖、蔗糖和几种淀粉等常见的碳水化合物与KClO3的反应,并结合染料的热分析情况,从中选取适合橙色发烟剂的可燃剂。图2为5种不同碳水化合物可燃剂与氯酸钾反应的TG/DTA曲线,表2为热分析数据。
表2 5种可燃剂与KClO3反应体系的热分析数据
Tab.2 Thermal analysis data of different reaction between KClO3and combustible agent

KClO3+可燃剂失重百 分数/%单位焓变/(J·g-1)反应起始温度/℃峰温/℃反应时间/s KClO3+蔗糖68.968.58167.5171.11.4 KClO3+乳糖83.928.38195.9201.61.27 KClO3+玉米淀粉72.574.66242.4246.81.18 KClO3+超级生粉86.765.41245.4250.11.35 KClO3+木薯粉86.215.45244.1248.40.76
当KClO3与碳水化合物在负氧平衡条件下反应时,剩余的残渣应该只有KCl,所以失重率应该在42.5%。从图2中可以看到,这几种体系的失重率都高于理论值,这是因为生成物中产生的气体带走部分残渣所致。
从图2、表2中可以看到,蔗糖和氯酸钾的起始反应温度较低,在167.5℃就可以反应,乳糖和氯酸钾在195.9℃,而淀粉类都在240~250℃之间;从反应焓变来看,蔗糖为8.58J/g,乳糖为8.38J/g,玉粉淀粉由于其中添加剂的缘故反应焓变较低,只有4.66J/g,超级生粉和木薯粉在5.4J/g左右。在2.2节中选择染料1#作为染料,其升华温度在279.4℃,单位焓变为10.55J/g,对比KClO3+可燃剂体系发现,淀粉类放热量远低于单位染料1#升华吸热,且初始反应温度较高,又在染料升华区间,做成配方之后不易点火。对比几种体系的失重率发现,超级生粉和木薯粉与乳糖相近,都在83%以上,而玉米淀粉由于食用添加剂的原因只有72%,但是蔗糖较低,只有69%,所以如果使用蔗糖作为添加剂时可能带来残渣残留较多,影响发烟效果,而且蔗糖与氯酸钾反应温度太低,可能带来感度问题,所以综合考虑,选择乳糖作为可燃剂。

图2 5种可燃剂与KClO3反应的TG/DTA曲线
