A流动注射Ferene分光光度法测定海水中溶解态铁的方法优化
2016-08-23王洪亮刘保华丁忠军于凯本
王洪亮,刘保华,丁忠军,于凯本
(国家深海基地管理中心,山东 青岛 266061)
A流动注射Ferene分光光度法测定海水中溶解态铁的方法优化
王洪亮,刘保华,丁忠军,于凯本
(国家深海基地管理中心,山东 青岛 266061)
热液流体中溶解态铁是海水原位测量的重要参数之一。本研究采用Ferene分光光度法,搭建流动注射分析系统,优化进样条件、显色条件,实现了热液流体中溶解态铁的在线测定。结果表明,测定Fe(II)时,Ferene、缓冲液浓度分别为8×10-3、0.4 mol/L,Ferene、样品流速分别为0.8、0.6 mL/min,显色盘管长度为40 cm时,方法的灵敏度、检测限最佳;测定Fe(III)时,Ferene、缓冲液、抗坏血酸浓度分别为1×10-2、0.5、0.01 mol/L,Ferene/抗坏血酸、样品流速均为1.0 mL/min,还原、显色盘管长度均为40 cm时,方法的灵敏度、检测限最佳。最佳实验条件下,Fe(II)、Fe(III)在 0.2~10 μmol/L和0.5~16μmol/L范围内,工作曲线回归方程分别为A=0.0834 C+0.0564(μmol/L,n=8,R²=0.997)和A= 0.0478C+0.0423(μmol/L,n=8,R²=0.997)。Fe(II)、Fe(III)检测限分别为24、39 nmol/L,相对标准偏差分别为0.8%、1.2%(n=10),加标回收率为97.9%~103.0%。共存离子实验表明,流体中的Na+、Mn2+、Cu2+、Cu+不会对测量造成干扰。
溶解态铁;Ferene;流动注射分析;分光光度法;热液流体
doi:10.11759/hykx20150629002
Fe(II)、Fe(III)组成的溶解态铁,是海洋中重要的生物营养元素,是热液流体中的主要元素和海底热液活动及其演化的主要示踪剂之一[1-2],在喷口生物区浓度范围为0~10 μmol/L[3],影响并控制以化学能合成为基础的热液口生态系统[4]。高温、酸性的热液流体与低温、微碱性、富氧的海水混合时,Fe(II)易氧化为Fe(III),半衰期为1.6~1.8 h[5],同时Fe(II)易与水体中的S2-反应生成FeS并从水体中沉淀[4]。溶解态铁可与热液羽状流中的有机配体络合,通过长距离(>2 000 km)运输,增加大洋中铁的浓度,因此热液活动可能是溶解态铁的主要来源之一[6]。
基于传感器的原位测量技术可减小水样采集、样品转移、实验操作等过程中的污染,避免采样过程中因温度、压力等变化造成的测量浓度、化学形态变化[7],获取高密度、长时间序列数据[8],是研究深海热液活动及热液极端生态系统的有效技术手段。传感器原位测量深海热液中溶解态铁时多采用进样管装配过滤器(0.45 μm滤膜)方式[9]排除流体中颗粒物的影响,灵敏度和出限是影响原位测量的关键因素[9-10]。
测量溶解态Fe(III)时,一般将其还原为Fe(II)后进行测定[11]。Ferrozine分光光度法是原位测量Fe(II)最常见的方法之一[10-12],其摩尔吸光系数为27 900 L/(mol·cm)。基于Ferrozine分光光度法和流动注射分析,部分原位传感器已用于海水中溶解态铁的原位测量[2-3]。Ferene与Fe(II)形成[FeII(fer)3]4-,在最大吸收波长593 nm处的摩尔吸光系数为35 500 L/(mol·cm),因此理论上Ferene分光光度法测定溶解态铁应具有更好的灵敏度和检出限,但目前的研究和应用仍较少。
流动注射分析(Flow injection analysis,FIA)是一种成熟的分析方法,常用分光光度法、荧光光度法等联用,分析速度快,方法的检出限与进样条件、显色条件等有关[9-11,13]。本文基于流动注射分析-Ferene分光光度法,优化进样速度、显色条件等,增加方法的灵敏度,降低检出限,为热液流体原位溶解态铁化学传感器的研制奠定基础。
1 材料与方法
1.1 仪器与试剂
1.1.1 仪器
BS100-1A+DG-2B型蠕动泵(保定思诺流体科技有限公司);C65-3186I型六位选择阀(美国VICI Valco公司);PX-2型氘灯、QE65000型光谱仪、FIAZSMA-20-PE型流通池(光程长度2 cm,美国Ocean Optics公司)。氙灯-流通池-光谱仪由 QP600-1-UV-VIS型光纤(美国Ocean Optics公司)连接。反应盘管(直径为60 mm)由PTFE管(内径0.8 mm,外径1.6 mm)弯曲组成。流路通道由PTFE管、1057型三通(美国Beionfluid公司)连接。
1.1.2 试剂
Fe(II)标准溶液:(NH4)2Fe(SO4)2·12H2O用纯水配制成浓度为10 mmol/L的标准储备液,加入体积分数为1%的浓HCl。用时蒸馏水稀释,并利用1%(v/v)HCl调节pH 到2.0,同时加入Na2SO3到1 μmol/L防止Fe(II)的氧化。
Fe(III)标准溶液:NH4Fe(SO4)2·12H2O用纯水配制成浓度为10 mmol/L的标准储备液。加入体积分数为1%的浓HCl。用时蒸馏水稀释,并利用1%(v/v)HCl调节pH到2.0。
Ferene(呋喃三嗪二钠盐,美国Sigma公司,分析纯)用1︰1醋酸-醋酸钠缓冲液配制成。Ferene浓度及缓冲液浓度、抗坏血酸浓度见表1,使用时溶液pH值均调至2.0。所用试剂均为分析纯,实验用纯水经Millipore超纯水系统处理。
1.2 实验方法
测定溶解态Fe(II)时,由六位选择阀SV选择进入蒸馏水/样品/标准溶液,与显色试剂R在三通T中汇合,在显色混合盘管MCF中混合并发生显色反应,经流通池FC,由氙灯L、光谱仪SP测定后排出,如图1(a)所示。测定溶解态Fe(III)时,利用抗坏血酸A在还原混合盘管MCR中将Fe(III)还原为Fe(II)后进行测定,如图1(b)所示。
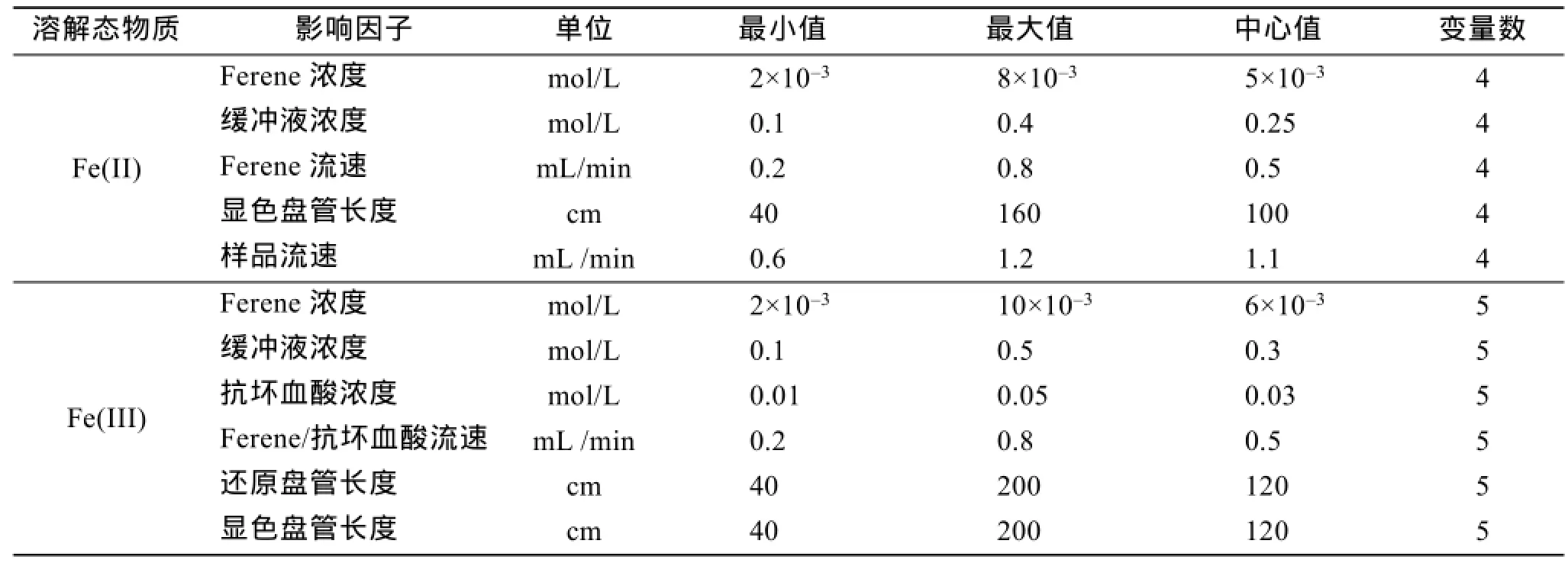
表1 实验设计中影响参数变化范围Tab.1 Description and levels of the influencing factors in the experimental design
选择[FeII(fer)3]4-的最大吸收波长593 nm为检测波长,无吸收的810 nm为校正波长,以消除纹影效应(Schlieren effect)和光强波动引起的测量误差[9,13]。双光路吸光度的计算公式如下:
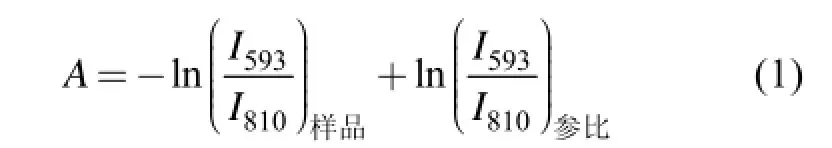
式中,A为吸光度,I593、I810分为593、810 nm时光的强度。
测量时,以蒸馏水作为参比,用蒸馏水与显色试剂的混合液所得的、相对于参比的吸光度作为基线,以基线的标准偏差(Bs)作为噪音,评价测量方法的检出限。标准溶液浓度分别为2、5、10 μmol/L时,用标准溶液与显色试剂显色后所得到的、相对于基线的吸光度与浓度的比值,分别记为S2、S5、S10,作为评价灵敏度的定量依据。计算公式分别为
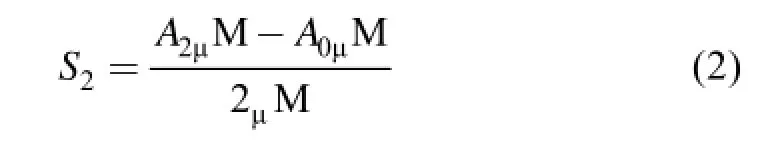
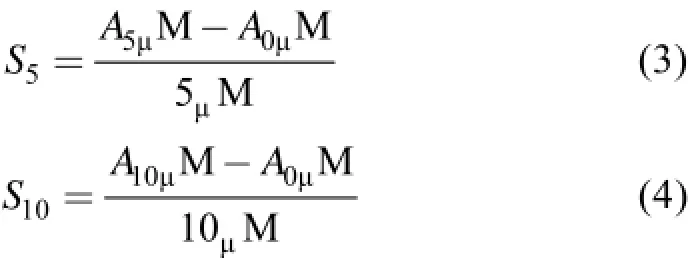

图1 FIA流路图Fig.1 Schematic diagram of FIA system(a)测定溶解态Fe(II);(b)测定溶解态Fe(III)(a)Determination of Fe(II);(b)Determination of Fe(III)SV.六位选择阀(6-Position selection valve);S.样品(Sample);St 1~4.标准溶液(Standard solution);R.显色试剂(Color-forming reagent);A.抗坏血酸(Ascorbic acid);T.三通(Tee);MCR.还原混合盘管(Reduction mixing coil);MCF.显色混合盘管(Color-forming mixing coil);P.蠕动泵(Peristaltic pump);L.氙灯(Xenon lamp);SP.光谱仪(Spectroscopy);FC.流通池(Flow cell);W.废液(Waste)
采用正交实验方法,优化流动注射分析-Ferene法的影响参数。Fe(II)实验中,主要影响参数为Ferene及缓冲液浓度、Ferene及样品流速、显色盘管长度[9-11]。Fe(III)实验中,考虑到现场使用环境和蠕动泵条件限制,我们固定样品流速为1.0 mL/min,并固定Ferene及抗坏血酸流速为同一流速,主要影响参数为Ferene、缓冲液及抗坏血酸浓度、Ferene及抗坏血酸流速、还原及显色混合盘管长度[10-11]。正交实验中实验参数的变化范围如表1所示。
2 结果与讨论
2.1 实验参数的优化
利用 SPSS软件(V16.0,SPSS Inc.,Chicago,USA),采用多元线性回归方法,分析影响参数对基线和吸光度的影响因子。Fe(II)、Fe(III)分析结果分见表2、表3。
实验结果表明,Fe(II)的Bs、S2、S5变化范围分别为8.4×10-4~3.3×10-4、4.0×10-5~8.8×10-2、1.6×10-3~8.0×10-2;Fe(III)的 Bs、S5、S10变化范围分别为7.1×10-4~3.9×10-3、5.3×10-3~8.6×10-2、6.7×10-3~8.6× 10-2。在本实验中,尽管络合剂Ferene是过量的,但络合剂浓度的增加,保证Fe(II)及Fe(III)还原后生成的Fe(II)处于充分络合状态,减少因解离造成的[FeII(fer)3]4-浓度下降[10,14]。因此Ferene浓度的增加,显著增大Bs、S2、S5、S10。醋酸缓冲液浓度的增加,同样增大Bs、S2、S5、S10。这可能是因为缓冲液增加了Ferene的稳定性[14],从而增加了Ferene的有效浓度。
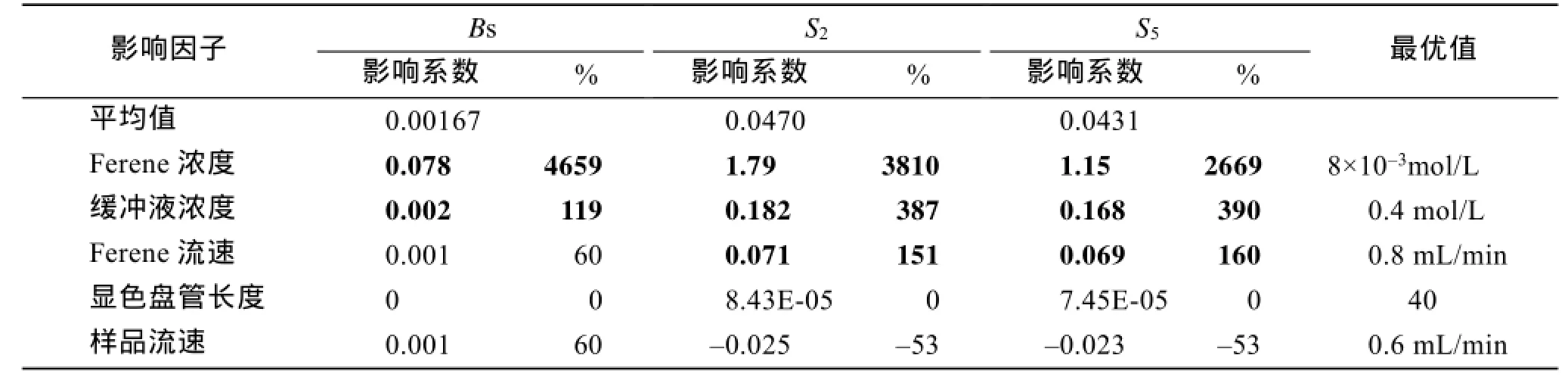
表2 Fe(II)实验参数的影响评估Tab.2 Estimated effects of each experimental factor of Fe(II)
抗坏血酸是Fe吸收促进剂,可与Fe(II)发生络合反应[15]。Fe(III)实验中,抗坏血酸浓度为0.01 mol/L时,可充分还原Fe(III)到Fe(II),因此过量抗坏血酸会抑制Ferene的络合,从而降低吸光度值和灵敏度。Fe(II)实验中,Ferene流速增加,而其他条件不变,相当于增加了反应混合物中Ferene的浓度,同时降低了Fe(II)的浓度。由于Ferene浓度的增加可以增大Bs、S2、S5,而Fe(II)浓度的减小可以降低Bs、S2、S5。二者的协同作用,导致Ferene流速的增加,对Bs、S2、S5的影响相对较小。同样,样品流速增加,而其他条件不变,相当于增加了反应混合物中Fe(II)的浓度,同时降低了Ferene的浓度。由于Ferene浓度的减小可以降低Bs、S2、S5,而Fe(II)浓度的增加可以增大Bs、S2、S5。二者的协同作用,同样导致样品流速的增加,对Bs、S2、S5的影响相对较小。Fe(III)实验中,Ferene/抗坏血酸流速的增加,同样是Ferene、抗坏血酸浓度的增加和Fe(II)浓度的减少之间的协调作用。由于抗坏血酸浓度的增加同样可降低S2、S5,因此该影响系数相对Fe(II)较低。还原盘管和显色盘管长度对Bs、S2、S5、S10影响不大,这表明40 cm长度可满足Ferene与Fe(II)、Fe(III)的充分还原、混合及络合反应。
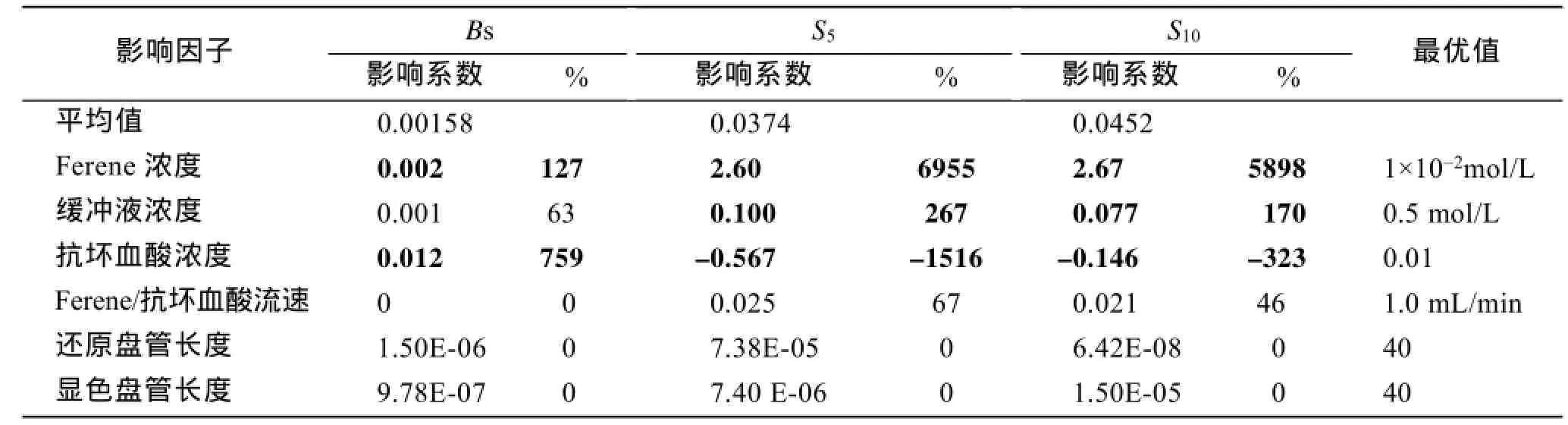
表3 Fe(III)实验参数的影响评估Tab.3 Estimated effects of each experimental factor of Fe(III)
结果表明,Ferene、缓冲液浓度分别为8×10-3、0.4 mol/L,Ferene、样品流速分别为0.8、0.6 mL/min,显色混合盘管长度为40 cm时,Fe(II)原位测量实验条件最佳;Ferene、缓冲液、抗坏血酸浓度分别为1×10-2、0.5、0.01 mol/L,Ferene/抗坏血酸、样品流速均为1.0 mL/min,还原、显色盘管长度均为40 cm时,Fe(III)原位测量实验条件最佳。
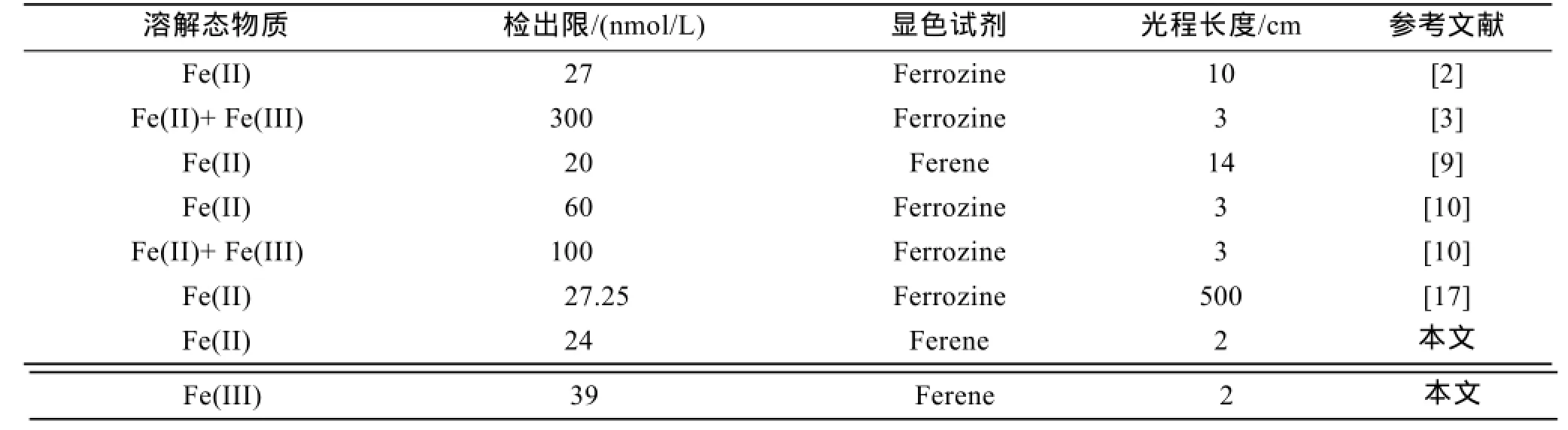
表4 溶解态铁检出限的比较Tab.4 Comparation of detection limits of dissolved iron
2.2 共存离子的影响
以±5%偏差为限,分别选取2 μmol/L Fe(II)、5 μmol/L Fe(III)标准溶液进行干扰实验。Fe(II)干扰实验中,考虑到Fe3+可以氧化水体中的SO32-,因此在同样的实验条件,在不添加SO32-的情况下进行Fe3+的干扰实验。结果显示,200倍的Fe3+对Fe(II)的测定无干扰。同时,2000倍的Na+;100倍的Mn2+;20倍的Cu2+、Cu+对Fe(II)、Fe(III)测定均无干扰。考虑实际热液流体中Fe/Cu的比值为30~170[16],因此共存离子不会影响现场测量。
2.3 方法的准确度
2.3.1 工作曲线、检出限与精密度
最佳实验条件下,Fe(II)、Fe(III)在0.2~10 μmol/L 和0.5~16 μmol/L范围内,工作曲线回归方程分为A= 0.0834 C+0.0564(μmol/L,n=8,R²=0.997)和 A= 0.0478 C+0.0423(μmol/L,n=8,R²=0.997)。对空白溶液平行测定5次,以3倍信噪比计算检出限,结果见表4。由于抗坏血酸的加入,降低了反应混合物中Fe(II)的浓度,因此Fe(III)工作曲线的斜率相对较低,而检出限相对较高。
由表4可知,本方法的检出限与文献2、9、17相当,而优于文献3、10。由于本文中的光程为2 cm,因此,在同样的光程长度下,使用优化后的实验条件,应可获得更低的检出限。
连续测定2 μmol/L Fe(II)、5 μmol/L Fe(III)标准溶液各10次,计算的相对标准偏差(RSD)分别为0.8%、1.2%。
2.3.2 加标回收实验
对样品进行加标回收实验,分别加入Fe(II)、Fe(III)标准溶液,进行4次平行测定,每个平行测定3次,计算所得平均回收率在97.9%~103.0%,结果见表5。
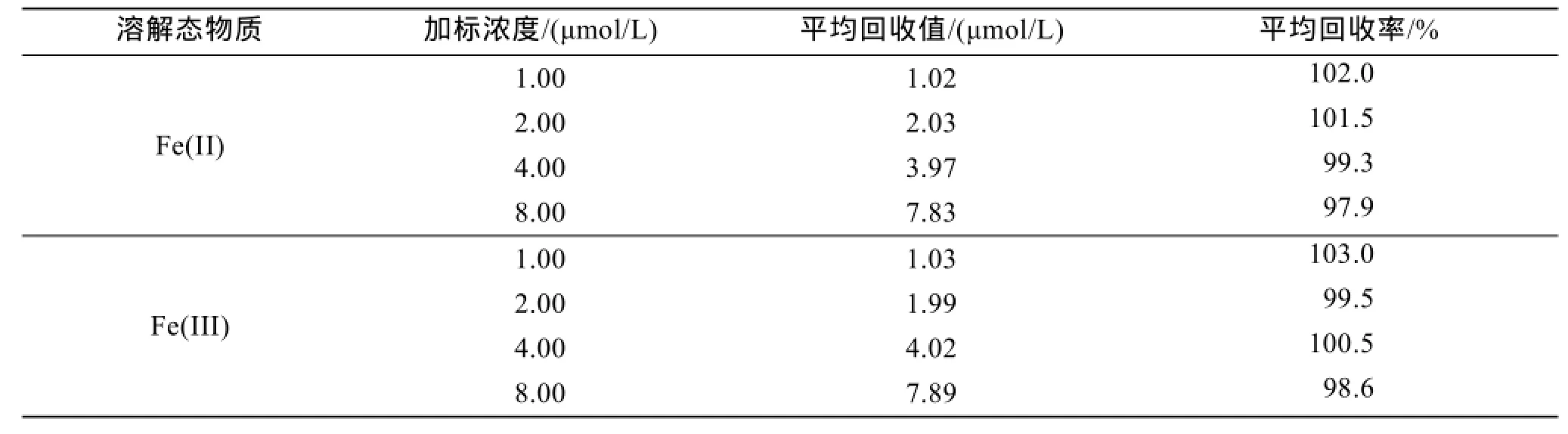
表5 加标回收实验Tab.5 Standard recovery test
3 结论
(1)通过各项实验条件探索,建立了流动注射分析法测定热液流体中溶解态Fe的方法,并确定了实验的最佳反应条件,即:测定Fe(II)时,Ferene、缓冲液浓度分为别8×10-3、0.4 mol/L,Ferene、样品流速分别为0.8、0.6 mL/min,显色盘管长度为40 cm;测定Fe(III)时,Ferene、缓冲液、抗坏血酸浓度分别为1×10-2、0.5、0.01 mol/L,Ferene/抗坏血酸、样品流速均为1.0 mL/min,还原、显色盘管长度均为40 cm。
(2)最佳实验条件下,Fe(II)、Fe(III)在0.2~10μmol/L 和0.5~16 μmol/L范围内,工作曲线回归方程分为A= 0.0834 C+0.0564(μmol/L,n=8,R²=0.997)和 A= 0.0478 C+0.0423(μmol/L,n=8,R²=0.997)。Fe(II)、Fe(III)检测限分别为24、39 nmol/L,相对标准偏差分别为0.8%、1.2%(n=10),加标回收率为97.9%~103.0%。
(3)共存离子实验表明,热液流体中的Na+、Mn2+、Cu2+、Cu+共存离子均不会对Fe(II)、Fe(III)的测量造成干扰。
[1] 包申旭,张一敏,周怀阳,等.现代海底热液化学组成特征及其控制因素[J].海洋科学,2010,34(4):95-99.
Bao Shenxu,Zhang Yimin,Zhou Huaiyang,et al.The chemical characteristics and their controlling factors of seafloor hydrothermal fluids[J].Marine Sciences,2010,34(4):95-99.
[2]MilaniA,Statham PJ,Mowlem M C,etal.Development and application of a microfluidic in-situ analyzer for dissolved Fe and Mn in natural waters[J].Talanta,2015,136:15-22.
[3] Vuillemin R,Le Roux D,Dorval P,et al.Chemini:A new in situ CHEmicalMINIaturizedanalyzer[J].Deep Sea Research Part I:Oceanographic Research Papers,2009,56(8):1391-1399.
[4] Luther G W,Rozan T F,Taillefert M,et al.Chemical speciation drives hydrothermal vent ecology[J].Nature,2001,410:813-816.
[5] Wang H,Yang Q,Ji F,et al.The geochemical characteristics and Fe(II) oxidation kinetics of hydrothermal plumes at the Southwest Indian Ridge[J].Marine Chemistry,2012,134:29-35.
[6] Wu J,Wells M L,Rember R.Dissolved iron anomaly in the deep tropical-subtropical Pacific:Evidence for long-range transport of hydrothermal iron[J].Geochimica et Cosmochimica Acta,2011,75:460-468.
[7] Prien R D.The future of chemical in situ sensors[J].Marine Chemistry,2007,107:422-432.
[8] 翟世奎,李怀明,于增慧,等.现代海底热液活动调查研究技术进展[J].地球科学进展,2007,22:769-776.
Zhai Shikui,Li Huaiming,Yu Zenghui,et al.Advances in the investigation technology of modern sea floor hydrothermal activities[J].Advances in Earth Science,2007,22:769-776.
[9] Meyer D,Prien R D,Dellwig O,et al.In situ determination of iron(II)in the anoxic zone of the central Baltic Sea using ferene as spectrophotometric reagent[J].Marine Chemistry,2012,130:21-27.
[10]Sarradin P M,Le Bris N,Le Gall C,et al.Fe analysis by the ferrozine method:adaptation to FIA towards in situ analysis in hydrothermal environment[J].Talanta,2005,66:1131-1138.
[11]Achterberg E P,Holland T W,Bowie A R,et al.Determination of iron in seawater[J]. Analytica Chimica Acta,2001,442:1-14.
[12]潘安阳,杨群慧,周怀阳,等.深海溶解态锰和铁的原位分析技术研究进展[J].地球科学进展,2013,28(4):420-428.
Pan Anyang,Yang Qunhui,Zhou Huaiyang,et al.Development of in situ analyzing technologies of dissolved manganese and iron in deep-sea seawater[J].Advances in Earth Science,2013,28(4):420-428.
[13]Worsfold P J,Clough R,Lohan M C,et al.Flow injection analysis as a tool for enhancing oceanographic nutrient measurements—A review[J]. Analytica Chimica Acta,2013,803:15-40.
[14]Artiss J D,Vinogradov S,Zak B.Spectrophotometric study of several sensitive reagents for serum iron[J].Clinical Biochemistry,1981,14(6):311-315.
[15]Zhu L,Glahn R P,Yeung C K,et al.Iron uptake by Caco-2 cells from NaFeEDTA and FeSO4:Effects of ascorbic acid,pH,and a Fe(II)chelating agent[J].Journalofagricultural and food chemistry,2006,54(20):7924-7928.
[16]Douville E,Charlou J L,Oelkers E H,et al.The rainbow vent fluids(36 14′N,MAR):the influence of ultramafic rocks and phase separation on trace metal content in Mid-Atlantic Ridge hydrothermal fluids[J].Chemical Geology,2002.184(1):37-48.
[17]Jin B,Chen Z,Zhu S.Development of an in situ analyzer for iron in deep sea environment[J].Advanced Materials Research,2013,694:1187-1191.
(本文编辑:康亦兼)
Ferene method flow injection analysis as optimized in situ analysis of dissolved iron in marine waters
WANG Hong-liang,LIU Bao-hua,DING Zhong-jun,YU Kai-ben
(National Deep Sea Center,Qingdao 266061,China)
Jun.29,2015
Dissolved iron;Ferene;Flow injection analysis;Spectrophotometry;Hydrothermal fluid
In this study,we adapted and optimized the ferrozine method flow injection analysis to perform an in situ analysis of dissolved iron.Optimal conditions were achieved for Fe(II)when the Ferene reagent(8×10-3mol/Lin a 0.4-mol/Lacetic/acetate buffer)was flowing at 0.8 mL/min,the sample flow rate was 0.6 mL,and the reaction coil length was 40 cm.Moreover,optimal conditions were obtained for Fe(III)when the Ferene reagent(1×10-2mol/L in a 0.5-mol/Lacetic/acetate buffer),the ascorbic acid reducing solution(0.01mol/L),and the sample were flowing at 1.0 mL/min,and the length of the reaction and reduction coils were 40 cm.Under these conditions,the calibration curves were A=0.0834 C+0.0564(μmol/L,n=8,R²=0.997)for Fe(II)and A=0.0478 C+0.0423 (μmol/L,n=8,R²=0.997)for Fe(III).The limits of detection and relative standard deviations were 24 nmol/L,0.8% (n=10)for Fe(II)and 39 nmol/L,1.2%(n=10)for Fe(III).The recovery was in the range 97.9%-103.0%.The results showed that,using this method,there was no significant interference for Na+,Cu2+,Mn2+,and Cu+.
P716+.5
A
1000-3096(2016)05-0082-06
2015-06-29;
2015-10-25
国家自然科学基金项目(41306103);国家重点基础研究973项目课题 (2015CB755901);海洋公益性行业专项经费资助项目(201405036)
[Foundation:National Natural Science Foundation of China,No.41306103;National Basic Research Program of China,No.2015CB755901;Marine Specific Welfare Project of China,No.201405036]
王洪亮(1979-),男,山东济宁人,博士,助理研究员,主要从事海洋原位传感器研究,电话:0532-88967091,E-mail:whl@ndsc.org.cn
