山木瓜枝中抑制黄嘌呤氧化酶活性的化学成分研究
2016-08-19唐跃勋祝伦伦谭红胜付文卫
唐跃勋 祝伦伦 张 洪 谭红胜 付文卫
(1 上海中医药大学中药学院,上海,201203; 2 中药创新药物研发上海高校工程研究中心,上海,201203)
山木瓜枝中抑制黄嘌呤氧化酶活性的化学成分研究
唐跃勋1,2祝伦伦1,2张洪1,2谭红胜1,2付文卫1,2
(1 上海中医药大学中药学院,上海,201203; 2 中药创新药物研发上海高校工程研究中心,上海,201203)
目的:研究山木瓜枝中抑制黄嘌呤氧化酶活性的化学成分。方法:通过活性导向分离,筛选山木瓜枝中具有抑制黄嘌呤氧化酶活性的粗提物及组分,采用多种色谱分离技术对活性部位进行系统分离,通过理化常数和光谱分析,结合相关文献确定所得化合物的结构;并对所得化合物进行黄嘌呤氧化酶抑制活性的研究。结果:从山木瓜枝的乙酸乙酯部位分离得到6个化合物,经鉴定分别为桑橙素(1)、4,6,3′,4′-tetrahydroxy-2-methoxybenzophenone(2)、2,4,6,3′-tetrahydroxybenzo-phenone(3)、3,6,7-trihydroxy-1-methoxyxanthone(4)、2S,3S-3,5,7,3′,5′-pentahydroxyavane(5)、丁香酸(6);实验研究证实化合物1对黄嘌呤氧化酶具有一定的抑制活性(IC50=28.9 μM)。结论:从活性部位鉴定的6个化合物均为首次从该植物中分离得到,其中化合物1是主要的活性成分。
山木瓜;化学成分;黄嘌呤氧化酶抑制活性;桑橙素
痛风是一种嘌呤代谢紊乱,尿酸产生过多或因尿酸排泄不良而导致血中尿酸升高,尿酸盐结晶沉积在关节滑膜、滑囊、软骨及其他组织,从而引起的反复发作性的炎性疾病。其临床特点为高尿酸血症。目前常用的治疗痛风和高尿酸血症的药物主要是黄嘌呤氧化酶(XOD)抑制剂。临床上最常用的黄嘌呤氧化酶抑制剂是别嘌呤醇[1]。然而由于严重的不良反应,该药的使用受到了限制[2],因此寻找新的、作用显著的、不良反应小的黄嘌呤氧化酶抑制剂显得极为重要且迫切。另外,黄嘌呤氧化酶会对某些疾病造成影响,包括缺血再灌注损伤、心肌梗死、高血压、动脉粥样硬化等[3]。所以寻找新的黄嘌呤氧化酶抑制剂不仅是抗痛风的需要,同时也会对治疗其他某些疾病产生积极的影响。
藤黄属植物共有450余种,其中我国分布22种。本课题组对多种藤黄属植物的提取物进行了较为系统的黄嘌呤氧化酶活性抑制筛选,结果显示山木瓜枝80%乙醇提取物的乙酸乙酯萃取部位具有较强的抑制黄嘌呤氧化酶活性。乙酸乙酯萃取部位经MCI柱色谱分离得到的30%,60%和90%乙醇洗脱部位(M1~M3)均显示了一定的黄嘌呤氧化酶抑制活性。课题组前期对60%乙醇洗脱部位(M2)进行了较为系统的化学成分研究,从中分离得到多个具有黄嘌呤氧化酶活性抑制活性的成分[4]。为进一步探索山木瓜枝条中具有抑制黄嘌呤氧化酶活性的成分,笔者对30%乙醇洗脱部位(M1)进行了系统的化学成分研究,从中分离得到6个化合物。通过理化性质、光谱分析,结合相关文献,这些化合物分别被鉴定为桑橙素(1)、4,6,3′,4′-tetrahydroxy-2-methoxybenzophenone(2)、2,4,6,3′-tetrahydroxy-benzophenone(3)、3,6,7-trihydroxy-1-methoxyxanthone(4)、2S,3S-3,5,7,3′,5′-pentahydroxyavane(5)和丁香酸(6),实验证实化合物1对黄嘌呤氧化酶具有一定的抑制活性(IC50=28.9 μM)。本次研究发现和鉴定的6个化合物均首次从该植物中分离得到。
1 材料与仪器
1.1药材山木瓜枝,于2010年8月采自云南省怒江市,经云南中医学院周元川教授鉴定为藤黄属植物山木瓜(G.esculentaY.H.Li.),标本存放于上海中医药大学中药创新药物研发上海高校工程研究中心(编号:No.20100801)。
1.2药品与试剂黄嘌呤氧化酶(批号:No.27093203,Oriental Yeast公司);别嘌呤(Tokyo Chemical Industry公司);黄嘌呤(批号:No.TGG4402,Wako Pure Chemical Industries公司);DMSO(Sigma-Aldrich公司);其他所有化学药品、盐酸、PBS等均购于国药集团。别嘌呤及受试化合物纯度高于98%。
1.3仪器与填料核磁共振波谱仪用Bruker AV-400型核磁共振波谱仪(TMS为内标);ESI-MS和HR-ESI-Q-TOF-MS分别用Agilent 6210 ESI-TOF和Agilent 6520 ESI-Q-TOF质谱仪;高效液相色谱仪采用Waters 2535高效液相色谱仪(色谱柱采用Xbridge C18column; 4.6 mm×250 mm,5 μm);薄层色谱硅胶板和柱色谱硅胶均为青岛海洋化工厂生产;凝胶Sephadex LH-20为GE Healthcare BioSciences AB;反相C18柱(50 μm,YMC)。
2 方法
2.1山木瓜枝不同极性提取物和M1组分的制备山木瓜枝不同极性提取物S1~S4由石油醚、乙酸乙酯和水等不同极性溶剂制备得到。制备方法如下[4]:干燥的山木瓜枝4 kg,粉碎后用石油醚提取得石油醚提取部位(S1),药渣继续用体积分数80%的乙醇回流提取,滤液减压浓缩至浸膏。浸膏加水悬浮后用乙酸乙酯萃取,得乙酸乙酯萃取部位(S2)和水萃取部位(S3),药渣继续用蒸馏水回流提取得水提部位(S4)。其中S2经MCI柱色谱,经30%乙醇洗脱,得到30%乙醇洗脱部位M1。
2.2山木瓜枝不同极性提取物及M1组分抑制黄嘌呤氧化酶活性试验[5]
2.2.1溶液的配制缓冲溶液配制:精密称取KH2PO40.478 0 g,K2HPO4·3H2O 3.473 0 g,加入纯净水约240 mL,定容至250 mL即得含75 mmol·L-1磷酸根离子,pH 7.4的磷酸盐缓冲液(PBS)。
底物的配制:精密称取黄嘌呤适量,加入PBS,定容,配成黄嘌呤浓度为150 μM的底物溶液,底物溶液新鲜配制,现配现用。
酶液配制:取黄嘌呤氧化酶适量,加入PBS,定容,配成0.1U的黄嘌呤氧化酶溶液。
供试药物的配制:精密称取适量供试品,用适量二甲基亚砜(DMSO)溶解,于-20 ℃避光保存。用时用PBS稀释至所需浓度。DMSO含量低于5%。
2.2.2山木瓜枝不同极性提取物S1~S4和M1组分抑制黄嘌呤氧化酶活性试验本试验采用别嘌呤作为阳性对照,将供试样品溶液、阳性对照溶液及空白溶液(空白为PBS)各50 μL、酶液30 μL、PBS 70 μL依次加入96孔板,37 ℃孵育15 min后,加入底物60 μL启动反应,在295 nm处,每隔15s读数1次,记录吸光度A,共计3 min。每组平行设置两个复孔。抑制率(%)可通过样品组及空白组A值的变化,用下列公式计算:抑制率(%)=(1-A样品/A空白)/100。取两个复孔的平均值即为样品的抑制率。
2.3提取和分离30%乙醇部位(M1,6 g)经硅胶柱色谱,用二氯甲烷-甲醇(v/v,30∶1→1∶1)梯度洗脱,得到F1~F4共4个组分。F1组分经Sephadex LH-20甲醇纯化,得到化合物2(8 mg);F2组分经Sephadex LH-20甲醇纯化,得到化合物3(15 mg);F3组分经Sephadex LH-20甲醇分离,TLC薄层制备(v/v,CH2Cl2:MeOH=10∶1)得到化合物1(17 mg),4(3 mg),5(6 mg);F4组分经HPLC制备(v/v,CH3CN∶H2O=42∶58)得到化合物6(7 mg)。
2.4化合物1~6对黄嘌呤氧化酶抑制活性的评价方法同2.2.2,测试分离所得的6个化合物体外抑制黄嘌呤氧化酶活性。
3 结果
3.1结构鉴定化合物1:黄色粉末,分子式C13H10O6。1H NMR(CD3OD,600MHz)δH:5.88(s,2H,H-3,H-5)、6.77(1H,d,J=8.3 Hz,H-5′)、7.15(1H,dd,J=8.3,2.0 Hz,H-6′)、7.21(1H,d,J=2.0 Hz,H-2′);13C NMR(CD3OD,150MHz)δC:95.9(C-3,C-5)、107.2(C-1)、115.5(C-5′)、117.6(C-2′)、124.1(C-6′)、133.8(C-1′)、145.8(C-3′)、151.2(C-4′)、161.9(C-2,C-6)、164.0(C-4)、199.1(C-7)。上述数据与文献[6]报道的桑橙素(Maclurin)数据基本一致,鉴定化合物1为桑橙素。
化合物2:黄色粉末,分子式C14H12O6。1H NMR(DMSO-d6,600MHz)δH:3.54(3H,s,2-OCH3)、5.95(1H,d,J=1.6 Hz,H-3)、5.99(1H,d,J=1.6 Hz,H-5)、6.75(1H,d,J=8.2 Hz,H-5′)、7.03(1H,dd,J=8.2,1.9 Hz,H-6′)、7.14(1H,d,J=1.9 Hz,H-2′);13C NMR(DMSO-d6,150MHz)δC:55.2(2-OCH3)、90.7(C-3)、95.4(C-5)、108.3(C-1)、156.2(C-6)、158.4(C-2)、159.4(C-4)、193.3(C-7)、130.4(C-1′)、116.2(C-2′)、144.8(C-3′)、150.4(C-4′)、115.0(C-5′)、122.1(C-6′)。上述数据与文献[7]报道的4,6,3′,4′-tetrahydroxy-2-methoxybenzophenone数据基本一致,鉴定化合物2为4,6,3′,4′-tetrahydroxy-2-methoxybenzophenone。
化合物3:黄色粉末,分子式C13H10O5。1H NMR(CD3OD,600MHz)δH:5.86(s,2H,H1-3,H1-5)、6.90(1H,dd,J=8.0,1.8 Hz,H-6′)、7.03-6.98(1H,m,H-2′)、7.06(1H,d,J=7.7 Hz,H-4′),7.20(1H,t,J=7.8 Hz,H-5′);13C NMR(CD3OD,150MHz)δC:95.9(C-3,C-5)、106.3(C-1)、116.1(C-5′)、119.3(C-2′)、129.9(C-6′)、144.3(C-1′)、158.2(C-3′)、120.7(C-4′)、163.7(C-2,C-6)、165.8(C-4)、200.7(C-7)。上述数据与文献[8]报道的2,4,6,3′-tetrahydroxybenzophenone数据基本一致,鉴定化合物3为2,4,6,3′-tetrahydroxybenzophenone。
化合物4:黄色粉末,分子式C14H10O6。1H NMR(CD3OD,600MHz)δH:3.80(3H,s,1-OCH3)、6.23(1H,s,H-2)、6.26(1H,s,H-4)、6.59(1H,s,H-5)、7.35(1H,s,H-8)。13C NMR(CD3OD,150MHz)δC:56.4(1-OCH3)、161.3(C-1)、96.6(C-2)、165.2(C-3)、96.8(C-4)、102.8(C-5)、157.0(C-6)、145.3(C-7)、109.2(C-8)、163.3(C-4a)、152.5(C-4b)、115.0(C-8a)、105.9(C-9a)、177.0(C-9)。上述数据与文献[9]报道的3,6,7-trihydroxy-1-methoxyxanthone数据基本一致,鉴定化合物4为3,6,7-trihydroxy-1-methoxyxanthone。
化合物5:黄色粉末,分子式C15H14O6。1H NMR(CD3OD,600MHz)δH:2.45(1H,m,H-4a)、2.67(1H,dd,J=16.3,4.4 Hz,H-4b)、4.00(1H,d,J=3.3 Hz,H-3)、4.73(1H,s,H-2)、5.72(1H,d,J=2.2 Hz,H-8)、5.90(1H,d,J=2.2 Hz,H-6)、6.65(1H,d,J=1.6 Hz,H-2′)、6.66(1H,s,H-6′)、6.89(1H,d,J=1.4 Hz,H-6′)。13C NMR(CD3OD,150MHz)δC:28.2(C-4)、64.9(C-3)、78.1(C-2)、155.8(C-5)、95.1(C-6)、156.6(C-7)、94.1(C-8)、156.3(C-9)、98.5(C-10)、130.6(C-1′)、114.8(C-2′)、144.5(C-3′)、118.0(C-4′)、144.5(C-5′)、114.9(C-6′)。上述数据与文献[10]报道的2S,3S-3,5,7,3′,5′-pentahydroxyavane数据基本一致,鉴定化合物5为2S,3S-3,5,7,3′,5′-pentahydroxyavane。
化合物6:白色粉末,分子式C9H10O5。1H NMR(CD3OD,600MHz)δH:7.33(2H,s,H1-2,H1-6)、3.88(6H,s,3-OCH3,5-OCH3);13C NMR(CD3OD,150MHz)δC:170.1(C-7)、147.3(C-3,5)、139.7(C-4)、123.1(C-1)、106.9(C-2,6)、55.4(C-3-OCH3,5-OCH3)。上述数据与文献[11]报道的丁香酸的波谱数据基本一致,鉴定化合物6为丁香酸(syringic acid)。
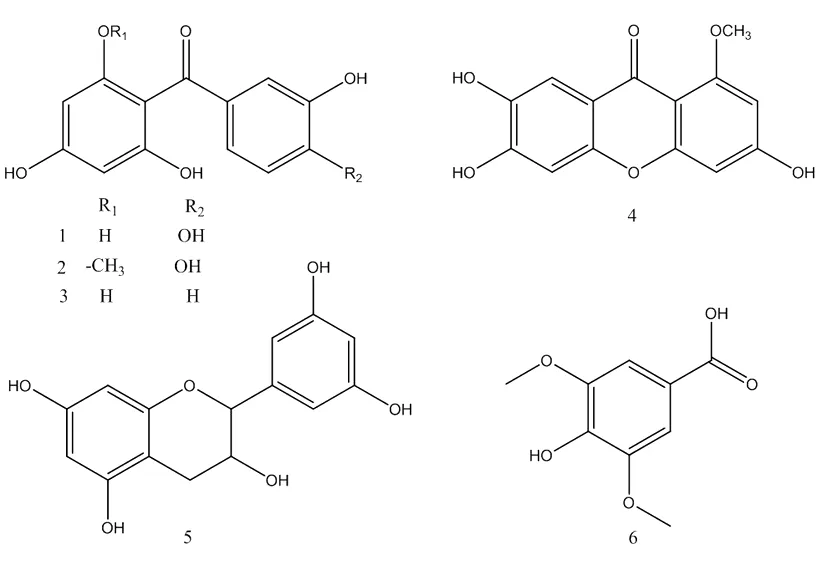
图1 化合物1-6的结构式
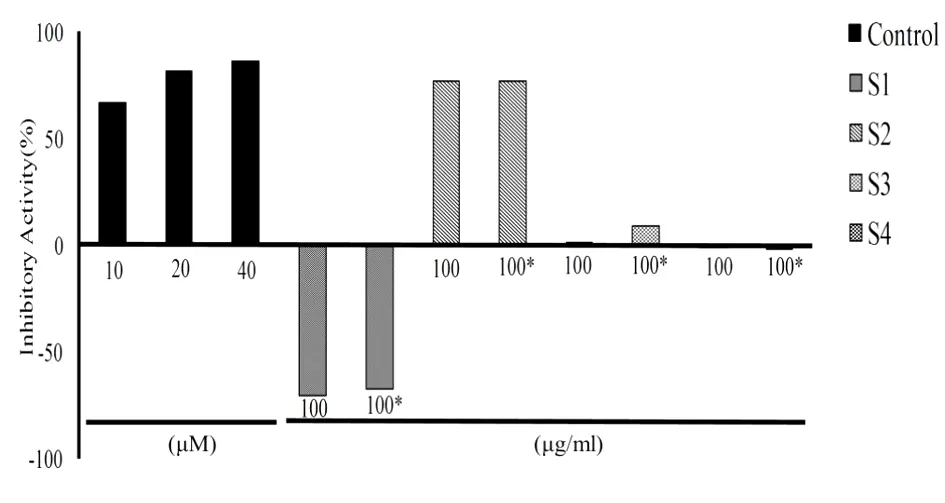
图2 提取物S1~S4抑制黄嘌呤氧化酶活性

表1 提取物S2、组分M1及桑橙素(1)抑制黄嘌呤氧化酶活性的IC50(n=3)
3.2山木瓜枝不同极性提取物S1~S4、组分M1以及分离所得化合物1~6抑制黄嘌呤氧化酶活性实验结果提取物S2、组分M1以及化合物1具有较强的抑制黄嘌呤氧化酶活性,其IC50如表1及图2所示。
4 讨论
本研究通过活性导向分离,从山木瓜枝中具有黄嘌呤氧化酶抑制活性的30%乙醇洗脱部位分离得到6个化合物。这些化合物均首次从该植物中分离得到,其中桑橙素(1)具有一定的黄嘌呤氧化酶抑制活性。化合物1、2、3具有相似的结构。化合物1和化合物2的区别在于化合物1的2位由酚羟基取代,而化合物2的2位由甲氧基取代,化合物1具有黄嘌呤氧化酶抑制活性,而化合物2无活性,推断化合物1的2位羟基与黄嘌呤氧化酶的抑制活性密切相关;化合物1和化合物3的区别在于化合物1比化合物3多了4′位酚羟基,化合物3没有抑制黄嘌呤氧化酶活性,推断化合物1的4′位酚羟基也可能与黄嘌呤氧化酶的抑制活性密切相关。
本研究首次报道桑橙素具有抑制黄嘌呤氧化酶活性。桑橙素最早于1975年从藤黄属植物山竹中分离得到。研究表明桑橙素具有抗布氏锥虫[12]、抗寄生原生动物[13]及抗氧化活性[6]。桑橙素是一类二苯甲酮类衍生物,V.Lakshmi Ranganatha等[14]合成的一类具有二苯甲酮结构片段的噻唑烷类化合物具有显著的抑制黄嘌呤氧化酶活性,提示二苯甲酮类化合物在抑制黄嘌呤氧化酶活性方面的潜在应用。
[1]Pacher P,Nivorozhkin A,Szabó C,et al.Therapeutic Effects of Xanthine Oxidase Inhibitors:Renaissance Half a Century after the Discovery of Allopurinol[J].Pharmacol Rev,2006,58:87-114.
[2]Okamoto K,Eger BT,Nishino T,et al.An Extremely Potent Inhibitor of Xanthine Oxidoreductase.Crystal Structure of the Enzyme-Inhibitor Complex and Mechanism of Inhibition[J].J Biol Chem,2003,278:1848-1855.
[3]Borges F,Fernandes E,Roleira F,et al.Progress Towards the Discovery of Xanthine Oxidase Inhibitors[J].Curr Med Chem,2002,9:195-217.
[4]Zhu LL,Fu WW,Xu HX,et al.Xanthine Oxidase Inhibitors from Garcinia esculenta Twigs[J].Planta Med,2014,80:1721-1726.
[5]Kong LD,Zhang Y,Pan X,et al.Inhibition of xanthine oxidase by liquiritigenin and isoliquiritigenin isolated fromSinofranchetiachinensis[J].Cell Mol Life Sci,2000,57:500-505.
[6]Holloway DM,Scheinmann,F.Extractives from Guttiferae.Phenolic Compounds from the Heartwood ofGarciniaMangostana[J].Phytochemistry,1975,14:2517-2518.
[7]Chiang YM,Kuo YH,Fukuyama Y,et al.Xanthones and Benzophenones from the Stems ofGarciniaMultiflora[J].J Nat Prod,2003,66:1070-1073.
[8]Atkinson JG,Gupta P,Lewis JR,et al.Phenolic Constituents ofGentianaLutea[J].Tetrahedron,1969,25:1507-1511.
[9]Silvere N,Fabien Z,Joseph DC,et al.Xanthones and Other Constituents ofAllanblackia Monticola(Guttiferae)[J].Nat Prod Res,2005,19:685-688.
[10] Zeng XB,Qiu Q,He XJ,et al.Antioxidant Flavanes fromLivistonaChinensis[J].Fitoterapia,2011,82:609-614.
[11]郑丽花,李小宝,宋鑫明,等.狭叶栀子茎化学成分研究[J].天然产物研究与开发,2012,24:1382-1384.
[12]Shapiro A,Nathan HC,Hutner SH,et al.In Vivo and in Vitro Activity by Diverse Chelators Against Trypanosoma Brucei Brucei[J].Journal of Protozoology,1982,29:85-90.
[13]Winter RW,Riscoe MK,Hinrichs DJ,et al.Bridged Diphenyl Compounds as Drugs Against Parasitic Protozoa[P].PCT Int,Appl.35 pp.1997,coden:PIXXD2.
[14]Lakshmi Ranganatha1V,Bushra Begum1A,Naveen1P,et al.Synthesis,Xanthine Oxidase Inhibition,and Antioxidant Screening of Benzophenone Tagged Thiazolidinone Analogs[J].Arch Pharm Chem Life Sci,2014,347:1-10.
[15]Liao CH,Ho CT,Lin JK,et al.Eects of Garcinol on Free Radical Generation and NO Production in Embryonic Rat Cortical Neurons and Astrocytes[J].Biochem Bioph Res Co,2005,329:1306-1314.
(2016-07-05收稿责任编辑:洪志强)
Xanthine Oxidase Inhibitors from The Twigs of Garcinia Esculenta
Tang Yuexun1,2,Zhu Lunlun1,2,Zhang Hong1,2,Tan Hongsheng1,2,Fu Wenwei1,2
(1SchoolofPharmacy,ShanghaiUniversityofTraditionalChineseMedicine,Shanghai201203,China; 2EngineeringResearchCenterofShanghaiCollegesforTCMNewDrugDiscovery,Shanghai201203,China)
Objective:To study the xanthine oxidase inhibitors from the twigs of Garcinia esculenta,and identify novel xanthine oxidase inhibitors.Methods:Bioassay-guided fractionation was used in the investigation of the extracts from the twigs of Garcinia esculenta,as well as means of column chromatography.The structures of the isolated compounds in the investigation were elucidated by comprehensive NMR and MS spectroscopic data analysis,as well as compared with previously publications.The effects of the isolated compounds on xanthine oxidase have been further investigated.Results:Six compounds were isolated from EtOAc fraction of the twigs of Garcinia esculenta,and their structures were identified to be maclurin(1),4,6,3′,4′-tetrahydroxy-2-methoxybenzophenone(2),2,4,6,3′-tetrahydroxybenzophenone(3),3,6,7-trihydroxy-1-methoxyxanthone(4),2S,3S-3,5,7,3′,5′-pentahydroxyavane(5),syringic acid(6).Compound 1 showed moderate inhibition on xanthine oxidase activity with an IC50value of approximately 28.9 μM.Conclusion:Compounds 1-6 were isolated from the plant,and the xanthine oxidase inhibitory effect of compound 1 was reported for the first time.
Garcinia esculenta; Chemical Constituents; Xanthine Oxidase Inhibition; Maclurin
国家自然科学基金项目(编号:81173485,81303188,81303266);上海自然基金青年基金(编号:13ZR1462000);2013年度上海晨光计划(编号:13CG46)
唐跃勋(1990.05—),男,硕士研究生,研究方向:中药活性成分研究,E-mail:tangyuexun90@126.com
付文卫(1970.09—),男,博士,副研究员,研究方向:中药活性成分研究,E-mail:fu_wenwei@163.com
R284
A doi:10.3969/j.issn.1673-7202.2016.07.003
