A型主动脉夹层术后急性肾损伤并行肾脏替代治疗患者的预后因素分析
2016-08-19黄浩汪薇柳林伟王宏飞
黄浩,汪薇,柳林伟,王宏飞
A型主动脉夹层术后急性肾损伤并行肾脏替代治疗患者的预后因素分析
黄浩1,汪薇1,柳林伟1,王宏飞2
目的 回顾性分析2007年6月~2015年3月在我院就诊的96例A型主动脉夹层术后急性肾损伤并行肾脏替代治疗患者的临床资料,进而探讨影响其预后的危险因素。方法 按照临床结局将纳入的患者分为生存组(56例)和死亡组(40例),比较两组患者术前、术中和术后资料,并行多元素Logistic回归分析评估影响该人群预后的独立危险因素。结果 通过比较两组患者的资料,发现死亡组术前心功能Ⅳ级、神经系统障碍、肝功能不全、术后低血压、消化道出血发生率和APACHEⅡ评分均较高,差异具有统计学意义(P<0.05)。多因素Logistic回归分析表明术前心功能Ⅳ级、术后肝功能不全、术后低血压和APACHEⅡ评分是患者死亡的独立危险因素(P<0.05)。结论 A型主动脉夹层术后急性肾损伤并行肾脏替代治疗患者的预后与术后肝功能不全、术后低血压、APACHEⅡ评分和术前心功能Ⅳ级有关,因此,应重视患者围手术期的危险因素并加以干预,以改善患者的预后情况。
主动脉夹层;急性肾损伤;肾脏替代治疗;危险因素
Stanford A 型主动脉夹层其剥离范围累及升主动脉,病情凶险,手术得在深低温停循环(DHCA)的条件下进行,手术时间长,过程复杂,且易发术后并发症[1]。急性肾损伤(AKI)是其中一种常见的术后并发症,有调查显示,其发病率为28%~54%,需要行肾脏替代治疗(RRT)的约占3%~11%[2]。RRT治疗是治疗AKI的一项积极有效的方法,但AKI患者行RRT治疗的预后并不理想[3]。本研究通过分析行Stanford A型主动脉夹层手术后并发AKI且行RRT的患者的预后情况,探讨影响其预后的危险因素,为早期介入和预防提供依据,从而改善患者的预后情况。
1 资料和方法
1.1临床资料 选取于2007年6月~2015年3月于湖北省天门市第一人民医院经CT及UCG检查确诊为Stanford A型主动脉夹层的654例,而术后并发AKI的患者有375例,其中接受RRT进行治疗的患者有96例。
1.2方法 根据患者的临床结局将96例A型主动脉夹层术后急性肾损伤并行RRT的患者分为生存组和死亡组。收集所有患者的临床资料,包括:年龄、性别、脑血管疾病史、糖尿病史、高血压史、心功能分级(NYHA)、心脏手术史、慢性肾功能不全史、术前基础血肌酐值、超声心动图左心室射血分数(LVEF)、估算的肾小球滤过率(eGFR)、心脏手术急性肾衰竭风险评分(Thakar score)、欧洲心血管手术危险因素评分(EuroScore);是否急诊手术,手术类型、主动脉阻断时间、体外循环时间、停循环时间,是否采用深低温停循环;术后行RRT治疗前急性生理记忆慢性健康状况评分Ⅱ(APACHE Ⅱ),术后并发症情况,如呼吸衰竭、及血压、肝功能不全、消化道出血、纵隔感染、神经系统功能障碍、败血症等,输红细胞和血浆量、术后24 h内引流量、术后是否再次开胸止血以及应用体外膜肺氧合(ECMO)情况。
2 结果
2.1A型主动脉夹层术后AKI并行RRT患者的临床资料 调查纳入的654例患者的临床资料,有588例进行了弓部手术,其余96例进行非弓部手术,最后发现375例(57.3%,375/654)患者术后发生AKI,而在这375例患者中,弓部手术有343例(61.5%,343/588),非弓部手术有32例(33.3%,32/96)。其中有96例(25.6%,96/375)AKI患者术后行RRT,平均年龄52岁,范围20~74岁,病程为6 h~3个月,其临床资料(表1)。

表1 96例A型主动脉夹层术后AKI并行RRT患者的临床资料
2.2比较两组患者的临床资料 96例行RRT患者中,死亡40例,占41.67%,其平均死亡时间为(11.53±6.32)d,死因有5种,多器官功能衰竭(MODS)者28例,脑血管意外者6例,肾功能衰竭者3例,恶性心律失常、纵隔感染以及消化道出血者各1例。其平均住院时间为(10.63± 5.78)d,平均机械通气时间为(98.76±35.94)小时,平均ICU停留(7.75±3.54)d,透析时间为(4.56±2.75)d。生存组56例,患者出院时,肾功能已恢复正常者39例,恢复尿量者15例,其在出院时已停止RRT,但血肌酐仍偏高,肾功能仍未完全恢复,2例患者在出院后仍继续行透析。生存组患者出院时均已停用呼吸机,平均住院时间为(38.64±17.93)d,平均机械通气时间为(242.36±102.13)h,肾功能恢复时间为(22.82±14.01)d,尿量恢复时间为(5.32± 4.37)d,平均ICU停留(16.74±7.92)d,透析时间为(7.63±7.01)d。
比较两组患者的临床资料(表2),发现其术中资料差异并无统计学意义(P>0.05),但死亡组术前心功能Ⅳ级、术后神经系统障碍、术后肝功能不全、术后低血压、术后消化道出血的发生率、APACHEⅡ评分高于生存组(P均<0.05)。
2.3多因素分析A型主动脉夹层术后AKI行RRT患者的死亡危险因素 将上述分析得到的具有统计学意义的结果及年龄、手术方式等因素列入多因素Logistic回归分析表(表3),经过多因素分析,发现术后肝功能不全、术后低血压、心功能Ⅳ级和APACHEⅡ评分是A型主动脉夹层术后AKI并行RRT患者死亡的独立危险因素(P均<0.05),差异具有统计学意义。而术后低血压、术后肝功能不全、术后消化道出血、术后神经系统功能障碍、年龄、手术方式等影响因素不具有统计学意义(P>0.05)。
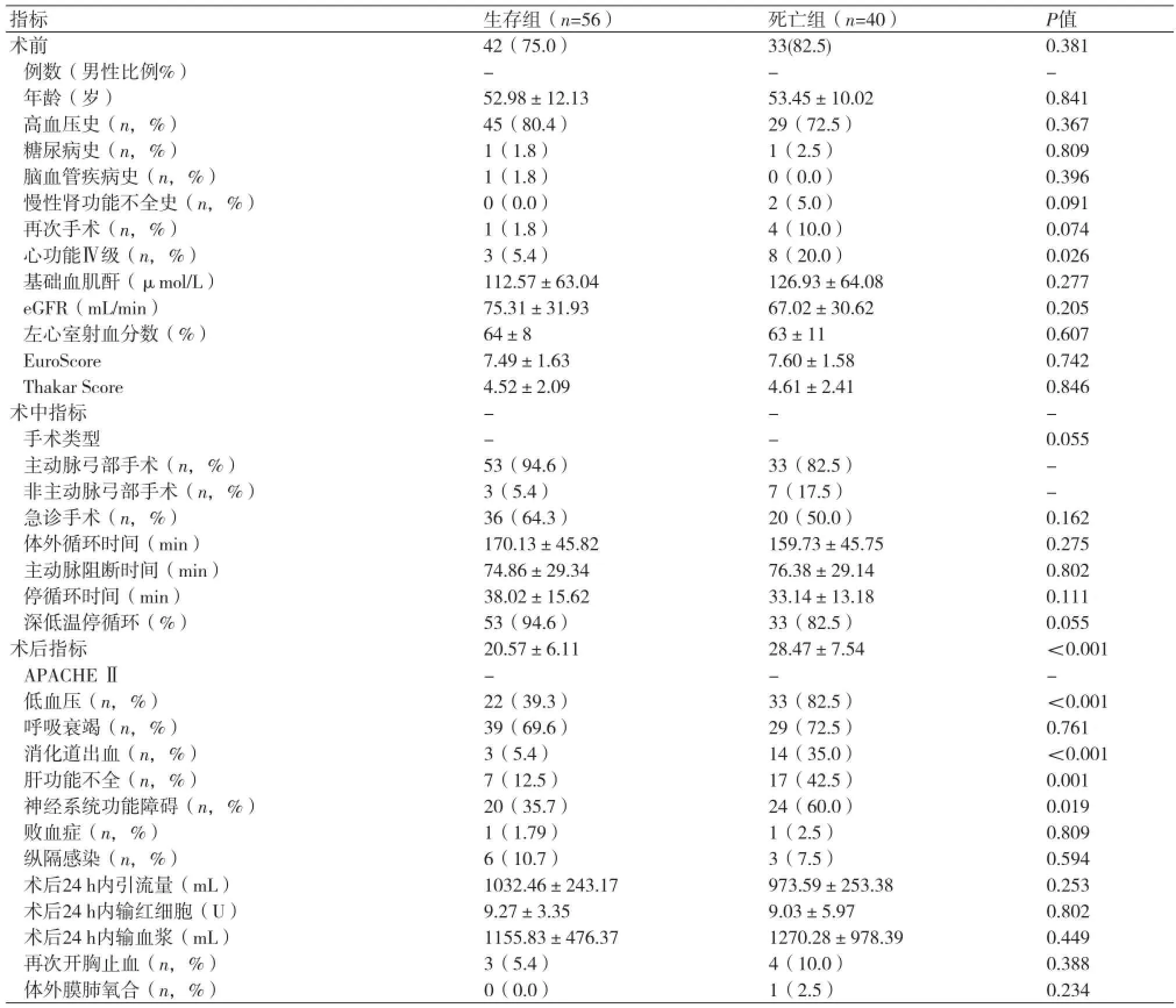
表2 比较两组患者的临床资料
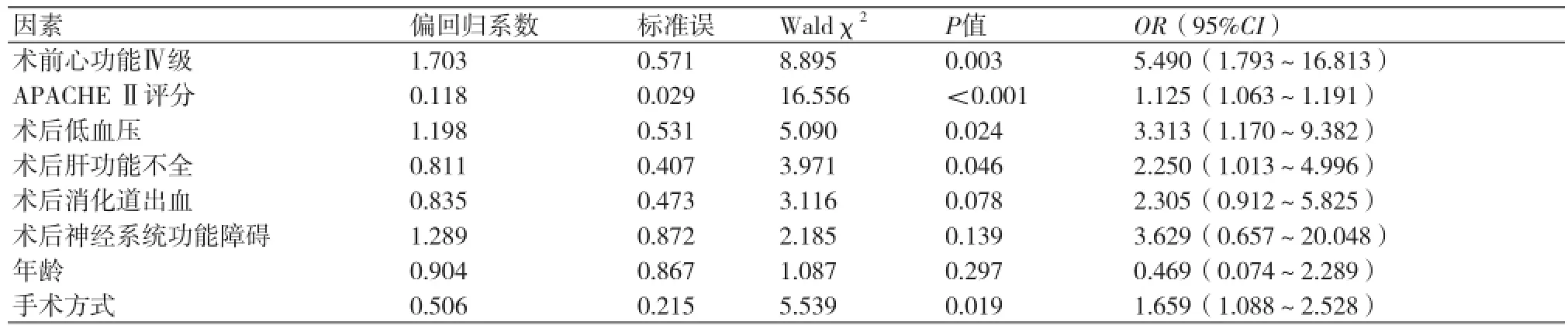
表3 多因素分析A型主动脉夹层术后AKI行RRT患者的死亡危险因素
3 讨论
AKI是Stanford A型主动脉夹层术后常见的并发症,也是造成患者死亡的独立危险因子,其病死率与肾功能RIFLE分级有关,级别越高,病死率越高,风险期(R)为9%,损伤期(I)为12%,衰竭期(F)为38%[4]。Stanford A型主动脉夹层术后并发AKI的病因有可能为:围手术期时患者血压过低导致肾脏灌注不足;体外循环时间过长,血红蛋白尿对肾脏造成影响;手术过程中肾脏缺血时间过长;术前患者长期高血压,夹层累及肾动脉,导致肾功能不全[5]。
有报道显示,心脏术后出现AKI的患者行RRT治疗,其死亡率高达35.0%~66.7%,且患者的住院时间长[6]。本研究中,患者死亡率为41.67%,与报道的结果相近。A型主动脉夹层术后AKI行RRT患者预后因素的报道比较少,本研究通过分析患者的临床资料,证实术前心功能Ⅳ级、术后肝功能不全、术后低血压和APACHEⅡ评分是患者术后死亡的独立危险因素。
大多数A型主动脉夹层患者术前无心脏疾病史,但若夹层发病后累及主动脉瓣,易引起主动脉瓣关闭不全,而主动脉瓣中度以上关闭不全易引发急性左心功能衰竭。若夹层发病累计冠状动脉,严重者易发生急性心肌梗死,或者心功能不全。此外,若夹层破入患者心包,易引发心包压塞,导致心功能衰竭。本研究中,心功能Ⅳ级的患者多为主动脉瓣关闭不全、心包压塞或者心肌梗死,其术前情况不佳,术后出现AKI即使行RRT,其预后仍未有太大改善[7-9]。
APACHEⅡ评分系统包括年龄、慢性健康状况(CPS)以及急性生理学(APS)等在内的12项指标,国际上多用于评价危重病患者的预后情况[10]。低分值(3~10分)的患者死亡率为3%,高分值(31~40分)的患者死亡率高达84.6%,因此APACHEⅡ评分与患者的死亡率密切相关[11]。本研究发现,死亡组患者APACHEⅡ评分远高于生存组,APACHEⅡ评分是A型主动脉夹层术后合并急性肾损伤并行肾脏替代治疗的预测因子。
本研究发现,术后低血压与患者的预后有关。造成主动脉夹层术后低血压的原因主要有:夹层累及冠状动脉引发心肌缺血,进而导致泵衰竭;术中、术后失血过多;术后心包压塞;低灌注引发乳酸性酸中毒或肠系膜缺血和多器官功能衰竭,以及急性脊髓或者脑缺血引发神经反射性低血压。主动脉夹层术后低血压患者,发生精神状态改变、神经系统障碍,以及肠系膜缺血、肢体缺血和心肌缺血等并发症的概率增加,其病死率也明显上升[12,13]。
有学者研究了1159例腹主动脉和降主动脉修复术后胃肠道并发症,结果发现肝功能不全的发病率为1.6%,而病死率为38%,说明肝功能不全与术后死亡率有密切相关性[14]。主动脉夹层术中,深低温、低流量、停循环,心肺转流时间较长,系统炎性反应和缺血再灌注,这些因素导致肝功能的损伤;此外,大量输血、广泛形成的微血栓和炎性反应,也都是导致患者肝功能损伤的原因。本研究发现,术后肝功能损伤也是患者的独立预测因子。若患者术后并发肝功能不全,往往预测者多器官功能衰竭的发生,其预后往往较差。
本研究中,死亡组患者其术后神经系统功能障碍和消化道出血的发病率都比生存组患者高,但多因素分析中并未证实其为患者预后的独立危险因素,推测原因可能是研究病例较少,需进一步研究中扩大样本,以寻求更科学的结果。
为改善A型主动脉夹层手术后AKI行RRT患者的预后情况,应对其危险因素加强监测。预防、处理患者术前急性左心功能衰竭,评估患者的APACHEⅡ评分,防止患者术后低血压、左心功能衰竭以及肝功能不全的发生,均可达到改善预后的效果。
[1] Tolwani A. Continuous renal-replacement therapy for acute kidney injury[J]. New England Journal of Medicine,2012,367(26):2505-14.
[2] 倪妮,王代红,王沂芹,等. 主动脉夹层术后急性肾损伤行肾脏替代治疗1例[J]. 第三军医大学学报,2014,36(12):1344.
[3] 杨晓梅,刘岚,庄亚敏,等. Stanford A型主动脉夹层术后急性肾损伤行肾脏替代治疗患者的预后[J]. 中华胸心血管外科杂志,2014,30(6):346-9.
[4] Di Eusanio M,Trimarchi S,Patel HJ,et al. Clinical presentation,management, and short-term outcome of patients with type A acute dissection complicated by mesenteric malperfusion: observations from the International Registry of Acute Aortic Dissection[J]. The Journal of thoracic and cardiovascular surgery,2013,145(2):385-90.
[5] 曾嵘,范瑞新,范小平,等. 急性A型主动脉夹层患者术后急性肾损伤的危险因素[J]. 中华胸心血管外科杂志,2014,30(1):30-2,37.
[6] James M,Bouchard J,Ho J,et al. Canadian Society of Nephrology commentary on the 2012 KDIGO clinical practice guideline for acute kidney injury[J]. American Journal of Kidney Diseases,2013,61(5): 673-85.
[7] Bragadottir G,Redfors B,Ricksten SE. Mannitol increases renal blood flow and maintains filtration fraction and oxygenation in postoperative acute kidney injury: a prospective interventional study[J]. Crit Care,2012,16(4):R159.
[8] 宋先荣,韩雪萍. Stanford A型主动脉夹层术后急性肾损伤的影响因素[J]. 中华胸心血管外科杂志,2012,28(10):603-4,613.
[9] Hao Z,Zhi-Wei W,Zhen Z,et al. Endovascular stent-graft placement or open surgery for the treatment of acute type B aortic dissection: a meta-analysis[J]. Annals of vascular surgery,2012,26(4):454-61.
[10] Chao CT,Lin YF,Tsai HB,et al. Acute kidney injury network staging in geriatric postoperative acute kidney injury patients: shortcomings and improvements[J]. Journal of the American College of Surgeons,2013,217(2):240-50.
[11] 张兆喻,董逸飞,孟毅,等. Stanford A型主动脉夹层术后并发急性肾损伤行连续性肾脏替代治疗时机的选择[J]. 临床军医杂志,2014,42(5):458-60.
[12] 王肇,高长青,肖苍松,等. 主动脉夹层术后早期急性肾损伤的危险因素分析[J]. 解放军医学院学报,2014,35(7):692-5.
[13] Roh GU,Lee JW,Nam B,et al. Incidence and risk factors of acute kidney injury after thoracic aortic surgery for acute dissection[J]. The Annals of thoracic surgery,2012,94(3):766-71.
[14] 霍春颖. Stanford A型主动脉夹层术后多器官功能障碍患者的护理[J]. 护理学杂志,2012,27(12):34-6.
本文编辑:阮燕萍
Prognosis factors in patients with acute kidney injury after type A aortic dissection surgery undergonerenal replacement therapy
HUANG Hao*, WANG Wei, LIU Lin-wei, WANG Hong-fei. *Department of nephrology,First People's Hospital of Tianmen City, Hubei Province, Tianmen 431700, China.
HUANG Hao, E-mail: huanghao988@yeah.net
Objective To analyze retrospectively the clinical materials of patients with acute kidney injury (AKI) after type A aortic dissection surgery undergone renal replacement therapy (RRT), and discuss the risk factors influencing prognosis. Methods The patients (n=96) were chosen from Jun. 2007 to Mar. 2015, and then divided,according to their clinical outcomes, into survival group (n=56) and death group (n=40). The clinical materials were compared between 2 groups before, during and after the operation. The independent risk factors influencing prognosis were reviewed by using multivariate Logistic regression analysis. Results The comparison in materials of 2 groups showed that incidence rates of NYHA functional class IV, neurological disorders and hepatic insufficiency before the operation, and hypotension, gastrointestinal bleeding, APACHE II scores after the operation were higher in death group (P<0.05). The results of multivariate Logistic regression analysis showed that NYHA functional class IV before the operation, and hepatic insufficiency, hypotension and APACHE II scores after the operation were independent risk factors of death (P<0.05). Conclusion The prognosis is related to hepatic insufficiency,hypotension and APACHE II scores after the operation and NYHA functional class IV before the operation in patients with AKI after type A aortic dissection surgery undergone RRT. The perioperative risk factors should be paid more attention to and given intervention for improving patient’s prognosis.
Aortic dissection; Acute kidney injury; Renal replacement therapy; Risk factors
1.3统计学方法 将调查得到的数据录入SPSS10.0软件,定量资料用(±s)表示,两组间均数的比较采用t检验。定性资料用百分比表示,组间比较采用χ2检验。用单因素分析方法探讨影响RRT患者预后的危险因子。筛选出单因素分析中具有统计学意义的因素,通过多因素Logistic回归分析,探究其独立危险因素。当P<0.05时认为差异有统计学意义。
R543.1
A
1674-4055(2016)01-0103-04
1431700 天门,湖北省天门市第一人民医院肾内科;1430030 武汉,华中科技大学同济医学院附属协和医院心血管外科
10.3969/j.issn.1674-4055.2016.01.30
黄浩,E-mail:huanghao988@yeah.net
根据2005年AKIN标准对AKI进行定义,即48h内血肌酐上升≥26.4 μmol/L,或者相较于基础值增加了≥50%;和(或)尿量<0.5 ml·kg-1·h-1达到6 h。当血肌酐<115μmol/L时认为肾功能恢复。当尿量>0.5 ml·kg-1·h-1时认为尿量恢复。对术前基础血肌酐进行定义:术前刚入院的血肌酐值。术后低血压定义为:收缩压<90 mmHg(1 mmHg=0.133 kPa)和(或)平均压<60 mmHg达1h。肝功能不全定义为:术后一周内总胆红素(TBIL)>50 mmol/L,谷丙转氨酶(GPT)>200 U/L,乳酸脱氢酶(LDH)>500 U/L。神经系统功能障碍定义为:昏迷、苏醒延迟、偏袒、抽搐、双下肢肌力障碍。行RRT治疗的指征有:少尿(尿量<0.3 ml·kg-1·h-1)达12 h以上;高钾血症(血钾≥5.5 μmol/L);血肌酐>354 μmol/L;体液过多,组织水肿。
