CMC-g-PAA/AM/ATP水凝胶对水体中Cd(II)的吸附性能及机理研究
2016-08-10邓红梅张紫君许楠广州大学环境科学与工程学院广州50006北京大学深圳研究生院环境与能源学院深圳58055通信作者Emailxunanszpkueducn
邓红梅 张紫君,2 许楠. 广州大学环境科学与工程学院广州 50006;2. 北京大学深圳研究生院环境与能源学院深圳 58055;† 通信作者E-mail:xunan@szpku.edu.cn
CMC-g-PAA/AM/ATP水凝胶对水体中Cd(II)的吸附性能及机理研究
邓红梅1张紫君1,2许楠2,†
1. 广州大学环境科学与工程学院广州 510006;2. 北京大学深圳研究生院环境与能源学院深圳 518055;† 通信作者E-mail:xunan@szpku.edu.cn
在凹凸棒黏土(ATP)的存在下以羧甲基纤维素(CMC)为主链过硫酸铵(APS)作为引发剂以 N,N-亚甲基双丙烯酰胺(MBA)作交联剂与丙烯酸(AA)和丙烯酰胺(AM)进行接枝共聚合成羧甲基纤维素-接枝-聚丙烯酸/丙烯酰胺/凹凸棒黏土(CMC-g-PAA/AM/ATP)复合水凝胶。采用该种材料吸附去除水体中的 Cd(Ⅱ),考察溶液初始 pH、金属离子浓度、反应时间、反应温度、吸附剂投加量等因素对吸附反应的影响并借助傅里叶转换红外光谱(FT-IR)和 X射线光电子能谱(XPS)探究吸附机理。结果表明初始 pH范围在 4.0~8.0内吸附效果佳吸附反应在 40 分钟内达到平衡整个吸附过程更符合准二级动力学模型吸附过程中放热。CMC-g-PAA/AM/ATP 可以快速、有效地去除水溶液中的 Cd(II)吸附机理包括静电作用、络合作用和离子交换作用。
CMC-g-PAA/AM/ATP;Cd(II);吸附;机理
北京大学学报(自然科学版) 第52卷 第3期 2016年5月
Acta Scientiarum Naturalium Universitatis PekinensisVol. 52No.3(May 2016)doi:10.13209/j.0479-8023.2016.066
现代社会经济飞速发展产生大量的生活污水、工业废水以及固体废弃物的渗滤液这些废水通常含有众多的重金属离子进入水体中难以降解,并具有生物积累性极易通过食物链富集威胁人类健康。镉(Cd)是生物毒性最强的重金属元素之一各种化学形态存在的 Cd 通过废水、废气及废渣进入环境或者生态系统后会发生迁移、转化和积累不仅造成严重的污染也威胁着饮用水安全。因此世界自然基金会的《环境中具有生殖和内分泌干扰作用的化学物质清单》将其与 PbHg一起列为仅有的 3种金属类内分泌干扰物美国环保总署和日本环境厅也分别将 Cd列为疑似内分泌干扰物[1]。目前常用的去除水体中 Cd(Ⅱ)的方法有化学沉淀法[2]、吸附法[3]、离子交换法[4]、生物法[5]等。化学沉淀法因沉淀难于处理而造成二次污染离子交换法因处理成本昂贵而使其推广受到限制吸附法因其工艺简单、成本低、去除效果好而颇受青睐。
水凝胶是一种经适度交联而具有三维网络结构的新型功能高分子材料含有大量的如羟基、羧基、磺酸基、酰胺基等多种活性基团它们可通过配位作用、离子交换作用等与重金属结合[6]。由于水凝胶合成成本低廉吸附性能好可循环利用,因此在水处理领域的研究愈来愈多[7-8]已经公认为是一种有发展潜力的从工业废水和自然水体中富集、分离和回收重金属的新材料。羧甲基纤维素(carboxymethyl celluloseCMC)是一种含有羧甲基取代基的天然纤维素衍生物其成本低廉、来源广泛无毒且抗盐性强[9]。CMC 分子量不大其黏度、强度和吸水性受到一定限制。然而CMC分子链上丰富的羧基和羟基使其易于进行接枝改性形成不溶于水的水凝胶性能得以改善和提高。并且,CMC接枝型水凝胶具有良好的生物降解性是一种环境友好型高分子材料[10]。凹凸棒黏土(attapulgiteATP)是一种天然富含镁铝的硅酸盐矿物其表面含有大量的—OH 和 Si—O 等活性基团,选用其做基体水凝胶的接枝材料既能改善其性能,又能降低成本[11]。近年来用化学引发、辐射引发等技术合成纤维素基水凝胶并将其用于超水材料及染料和重金属废水处理的研究较多但对于吸附去除重金属离子的机理研究报道却较少[12]。
本文在ATP的存在下以CMC为主链选用过硫酸铵(ammonim peroxodisulphateAPS)作为引发剂以 N,N′-亚甲基双丙烯酰胺(MBA)作交联剂,与丙烯酸(acrylic acidAA)和丙烯酰胺(acrylic amideAM)进行接枝共聚合成羧甲基纤维素-接枝-聚丙烯酸/丙烯酰胺/凹凸棒黏土(CMC-g-PAA/AM/ATP)复合水凝胶材料考察其对 Cd(II)的吸附性能及脱附再生行为并借助傅里叶转换红外光谱(FT-IR)以及X射线光电子能谱(XPS)对吸附机理进行探究。本文的结果对开发高性能水凝胶材料的合成方法研究吸附过程的化学本质和参与吸附作用的化学功能团具有重要的科学意义。
1 材料和方法
1.1 仪器与试剂
羧甲基纤维素(CMC):国药集团化学试剂公司,化学纯;丙烯酸(AA):C. P上海五联化学试剂厂,化学纯使用前经减压蒸馏;丙烯酰胺(AM):上海化学试剂公司分析纯;过硫酸铵(APS):上海化学试剂公司分析纯使用前使用蒸馏水重结晶;N,N-亚甲基双丙烯酰胺(MBA):上海化学试剂公司,化学纯直接使用;天然凹凸棒石(ATP):工业级,江苏盱眙奥特邦矿物有限公司经碾碎过320目。所用试剂 HClNaOHHNO3CH3COOH 和Cd(NO3)2均为分析纯购自中国广州化学试剂厂,实验室用水为超纯水。
实验仪器有 AA6800 原子吸收分光光度计(日本)、Phs-3C 赛多利斯酸度计、TDL-5-A 冷冻离心机、81-2 型恒温磁力搅拌器、BT125D 电子分析天平、ZHWY-100B 经典型多振幅轨道摇床、JSM-7001F 型扫描电子显微镜、Nicolet Nexus型红外光谱分析仪(KBr 压片)以及 Kratos ASIS-HS 型 X 射线电子能谱仪。
1.2 CMC-g-PAA/AM/ATP的制备
在装有搅拌棒、回流冷凝管、温度计和 N2管的250 mL四口烧瓶中加入0.72gCMC搅拌至完全溶解然后加入 7.2 g AA (中和度为 70%)和0.95 g AM同时加入0.0296g交联剂MBA搅拌使之完全溶解后再加入3.0 g ATP。通入N230分钟后开始升温到 40°C 时加入APS引发剂0.0956g在 80°C 维持3小时后产物用蒸馏水洗涤然后在 70°C 烘干后粉碎过 40~80 目筛,备用。
1.3 去除Cd(Ⅱ)的静态吸附实验
取一定初始质量浓度的 Cd(Ⅱ)溶液 20 mL 置于 50 mL 离心管内通过滴加稀 HCl和稀 NaOH调节 pH值加入一定量的 CMC-g-PAA/AM/ATP后放入恒温振荡器中调节反应温度转速 250 rpm。振荡结束后通过 0.45 μm 微孔滤膜过滤分离得上清液用火焰原子吸收光谱(FAAS)测定Cd(Ⅱ)浓度。根据实验设计在保持其他反应条件不变的情况下改变其中一个条件进行批实验。具体实验参数如表1所示。
脱附实验使用的脱附剂为 0.1 mol/L 的 HNO3和 CH3COOH 溶液。将吸附 Cd(Ⅱ)后的吸附剂烘干重新装入盛有20 mL酸液的离心管中室温下振荡脱附4小时结束后测定溶液中 Cd(Ⅱ)的浓度计算脱附量与脱附率。
1.4 数据分析
吸附达到平衡时CMC-g-PAA/AM/ATP 对Cd(Ⅱ)的吸附量 qe(mg/g)以及去除率(Ads%)的计算公式为
式中qe表示平衡时单位吸附剂吸附溶液中重金属的量(mg/g)C0表示初始溶液中重金属离子的浓度(mg/L)Ce表示平衡时溶液中重金属离子的浓度(mg/L)V 表示溶液体积(L);m表示吸附剂用量(g)。
脱附率(%)的计算公式为
脱附率=吸附容量/脱附容量×100。
所有检测的数据都重复3次所有处理均独立重复3次以平均值作为测定结果。
2 结果与讨论
2.1 溶液初始pH对吸附的影响
重金属溶液的初始 pH 是吸附过程中一个重要的影响因素考虑到 Cd(Ⅱ)的水解和沉淀作用在pH为 2~8的范围内进行研究。CMC-g-PAA/AM/ ATP 对不同 pH 值溶液中 Cd(II)的吸附结果如图 1所示。
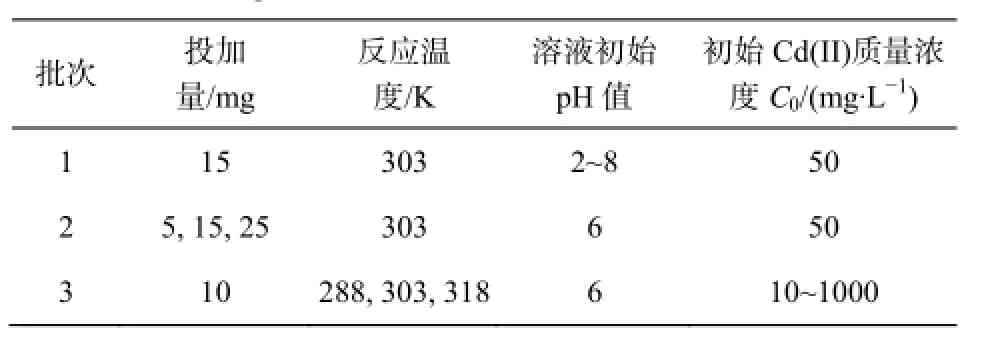
表1 CMC-g-PAA/AM/ATP吸附Cd(II)批实验参数Table1 Parameters of batch test for Cd(II) adsorption onto CMC-g-PAA/AM/ATP
从图1可以看出在pH为2时CMC-g-PAA/ AM/ATP 对 Cd(Ⅱ)的吸附量非常小;当 pH 值逐渐增加至4时吸附量随之迅速增大;当 pH 继续增大至8时CMC-g-PAA/AM/ATP对Cd(Ⅱ)吸附量的变化趋于平缓逐渐达到平衡状态。这可能是因为低pH值时吸附剂中的—NH2的质子化作用非常明显形成大量—NH3+与 Cd2+之间产生静电斥力减少了可吸附金属离子的结合位点。此外,大量的羧酸基团被质子化并且参与分子间的氢键形成这就意味着一些结合位点被氢原子占据导致CMC-g-PAA/AM/ATP 的吸附能力降低。随着pH值的逐渐增大—NH2的质子化作用减小更多的—NH2可能与金属离子发生络合作用使得吸附率逐渐增大[13]。此外较高的pH值条件下—COOH可电离产生—COO-与金属离子之间产生静电引力使得吸附量增加;并且—COOH 还可能直接与二价金属离子产生离子交换作用[14]。因此可以推断CMC-g-PAA/AM/ATP对Cd(II)的吸附机理可能包括静电作用、络合作用和离子交换作用具体过程如下:
—NH2的质子化作用:R—NH2+ H+↔ R—NH3+,
Cd2+与—NH2的络合作用:R—NH2+ Cd2+↔ R —NH2Cd2+;
—COOH的电离:R—COOH ↔ R—COO-+ H+;
Cd2+与—COO-的络合作用:R—COO-+ Cd2+↔R—COO-Cd2+;
—COOH与Cd2+的离子交换作用:R—COOH+
Cd2+↔ R—COO-Cd2++ H+。
2.2 吸附动力学
为探究这种复合水凝胶材料对Cd(Ⅱ)的吸附速率对其进行吸附动力学实验。图2显示3种不同吸附剂用量(515和25mg)下不同反应时间点吸附容量和吸附去除率的变化。从图2可以看出,吸附反应的前10分钟CMC-g-PAA/AM/ATP 对Cd(Ⅱ)的吸附容量急速增加反应速率非常快。当吸附剂用量较大时(1525 mg)吸附反应在20分钟内达到平衡吸附剂用量较小时(5 mg)吸附速率显得稍慢些但也在 40 分钟内达到平衡。从吸附容量的变化来看随着吸附剂用量的增加单位吸附剂上的Cd(Ⅱ)吸附容量逐渐降低这主要是由于吸附位点不饱和引起的。投加量为515和25mg时对应的最大吸附去除率分别为96.55%98.45%和98.47%。这是因为更多的吸附剂意味着更大的吸附表面以及更多的有效吸附位点而当吸附剂用量达到一定水平时吸附剂与吸附质之间达到平衡,吸附位点饱和去除率不再增加。
采用准一级和准二级吸附动力学模型对实验结果进行拟合方程如下:
准一级方程:ln(qe- qt) = ln(qe) - k1t ,
准二级方程:t/qt= 1/(k2qe2) + t/qeqt是 t 时间的吸附量(mg/g)qe是平衡吸附容量(mg/g)。
表 2 列出CMC-g-PAA/AM/ATP吸附 Cd(Ⅱ)动力学准一级和准二级模型参数。可以看出二者都可以很好地拟合吸附过程但准二级动力学的相关性更大比准一级模型更优越。此外准二级动力学模型计算得到的最大吸附容量值与实验测定值非常接近而准一级动力学的计算值与真实值差别很大因此准二级能够真实准确的拟合吸附容量随时间的变化趋势。化学键的形成是影响准二级动力学吸附作用的主要因素这种结果也说明吸附速率是被化学吸附所控制的不受物质传输步骤的控制。
2.3 等温吸附曲线
3种温度(288303和 318 K)下 CMC-g-PAA/ AM/ATP 对不同初始浓度 Cd(Ⅱ)的吸附等温线如图3所示。从图3可以看出在整个研究浓度范围内CMC-g-PAA/AM/ATP对 Cd(Ⅱ)的吸附都随着初始浓度的增大而增大甚至当 Cd(Ⅱ)初始浓度达到 1000 mg/L 时吸附才慢慢接近平衡。Cd(Ⅱ)的吸附容量随着反应温度的升高而降低说明吸附过程中放热温度过高会影响吸附反应的进行。为了更好地解释上述趋势采用 Langmuir 型和 Freundlich 型吸附等温线对实验结果进行拟合各参数的计算结果见表3。

表2 不同吸附剂用量下CMC-g-PAA/AM/ATP吸附Cd(Ⅱ)的动力学参数Table 2 Constants and correlation coefficients of the two kinetic models for Cd(Ⅱ)adsorption onto CMC-g-PAA/AM/ATP composites at different dosage
其中k1(min-1)和 k2(g/(mg · min))是吸附速率常数,
Langmuir方程属于理论推导公式:
式中qe是平衡吸附容量(mg/g);qm为理论单层最大吸附容量(mg/g);Ce为平衡时溶液中重金属离子的浓度(mg/L);kL为Langmuir吸附特征常数(L/g)是表征吸附剂与吸附质之间亲和力的一个参数其值越大吸附亲和力越大[15]。
Freundlich 模型一般应用在不均匀表面发生的多分子层吸附和非理想吸附中吸附剂表面的被吸附分子存在吸附热分布不均匀的相互反应属于纯经验公式:
式中kF表示吸附能力(mg/g)其值越大吸附能力越强;n是与吸附强度和吸附剂表面不均匀性有关的常数值越大吸附能力越大。
相关系数的计算结果表明CMC-g-PAA/AM/ ATP 吸附 Cd(Ⅱ)更符合 Langmuir 模型但两种模型的拟合结果相关性差别不大说明 CMC-g-PAA/ AM/ATP 吸附 Cd(II)更倾向于 Langmuir 单分子层吸附这可能是因为 CMC-g-PAA/AM/ATP 中的—COO-基团与 Cd2+之间的静电引力作用以及—NH2基团与 Cd2+之间的络合作用更强烈。kL的计算结果均在 0~1 之间说明 CMC-g-PAA/AM/ATP 对 Cd(Ⅱ)的吸附过程为优惠吸附[16]。
2.4 脱附再生实验
采用 CH3COOH 的吸附-脱附实验进行一遍,采用 HNO3的吸附-脱附实验重复进行三遍结果见图 4。CH3COOH 溶液的脱附效果远不及 HNO3,HNO3洗脱 CMC-g-PAA/AM/ATP 上的 Cd(Ⅱ)的一次脱附率为 94.6%;CH3COOH 洗脱 Cd(Ⅱ)的一次脱附率仅为 15.9%。这可能是因为HNO3的酸性强,产生大量的 H+可以将与羧基离子交换和氨基络合的金属离子脱附下来。从图4还可以看出采用HNO3对水凝胶材料进行再生实验对比第一次与第三次的吸附结果CMC-g-PAA/AM/ATP 对Cd(Ⅱ)的吸附容量从 67.3mg/g降低至 59.7mg/g降低11.3%。可以看出经过三次脱附再生实验的复合水凝胶材料对 Cd(Ⅱ)仍具有较好的吸附性能。然而经过再生后的水凝胶强度有一定程度的降低,开始分解为细小的颗粒因此不宜再进一步重复利用。

表3 不同温度下CMC-g-PAA/AM/ATP吸附Cd(II)的Langmuir和Freundlich模型参数Table3Langmuir and Freundlich isotherm constants and correlation coefficients for Cd(II) sorption onto CMC-g-PAA/AM/ATP at different temperatures
2.5 FT-IR表征
图5是CMC-g-PAA/AM/ATP吸附Cd(Ⅱ)的红外光谱图。可以看出吸附前在 3392 和 3200 cm-1附近有酰胺吸收峰以及 CMC 和 AM 的 N—H,—OH特征吸收峰在2947 cm-1处的吸收峰为亚甲基的伸缩振动峰在 1670 和 1560 cm-1处出现—CONH2中羰基特征吸收峰此特征峰是酰胺基和羧基相互作用的结果[17]在 1450 cm-1处出现
—COONa 的特征吸收峰1402 cm-1处为羟基(面内)吸收峰。由此可知AAAM 与 CMC 大分子链发生了聚合所用原料的特征吸收峰在产物的红外光谱上均有体现制得的产物接枝聚合效果良好。在1025 cm-1处出现的特征峰可归因为 ATP 中 Si—O —Si 键的存在。这说明 ATP的羟基并未完全发生共聚反应过量的部分以物理填充的方式存在复合材料中[18]。CMC-g-PAA/AM/ATP吸附 Cd(Ⅱ)之后的红外谱图发生以下变化:—NH2和—OH 振动引起的宽峰变宽强度变弱并向高频移动(3423cm-1);1670 cm-1处—COOH基团中的 C==O 振动强峰明显减弱;1560 cm-1处的 C==O 谱峰变弱。这些吸附 Cd(Ⅱ)后的红外谱图的变化表明—NH2,—OH 和—COOH 官能团都参与了吸附反应由此可以推断络合作用在 CMC-g-PAA/AM/ATP 吸附 Cd(Ⅱ)的过程中占重要部分。下面采用 XPS 分析复合材料的元素组成和形态进一步验证该反应机理。
2.6 XPS表征
XPS分析有助于判断特定元素的存在以及元素的价态图6是 CMC-g-PAA/AM/ATP 吸附 Cd(II)前后的全扫描 XPS 图以及 C 1s 和 O 1s 的 XPS 分峰谱图。从图 6(b1)中可以看出C 1s 峰被分为4 个结合能值不同的峰分别归属为 C==OC—N,C—O 和 C—C 键而 C==O 和 C—N 键又分别来自于羰基和氨基。图 6(c1)显示O 1s 峰被分为两个不同结合能值的峰分别归属为 C==OC—O 和 —OH 键。吸附 Cd(Ⅱ)后的全扫图可以看出吸附反应后 Cd 的特征峰为 405.5 eV说明 Cd 吸附在材料表面。由于 Cd含量较少同时与 N 的特征峰值接近二者能谱扫描可能存在重叠部分所以特征峰并不明显。N的电子结合能从吸附前的 399.4 eV升高至 399.8 eV。与 N 相关的基团的电子结合能中—NH2> —NH2M2+> —NH+这是因为 N 的外层电子偏移使得N价态升高进而引起N的电子结合能升高[19]。这说明 CMC-g-PAA/AM/ATP 中的 N 与 Cd 通过络合作用相结合N 与 Cd2+共用一对电子N 的电子云密度降低结合能值升高。CMC-g-PAA/AM/ATP 中 C==OC—NC—O 和 C —C 的结合能值从287.8285.8284.6和284.3eV分别变为288.0285.8284.9和284.0 eVC==O和C—O 的结合能值升高。这可能也是由于 O 原子和N 原子向 Cd2+提供电子对从而使得邻近的 C 原子周围电子密度降低说明羰基和氨基参与了吸附过程。CMC-g-PAA/AM/ATP吸附 Cd(Ⅱ)之后的 O 1s仍分为两个峰未见新的峰型说明 O 与 Cd2+之间不存在共用电子即不存在络合作用。然而吸附后,C==O峰与 C—O峰的峰面积比有所下降可能是离子交换作用引起的。
结合上述分析CMC-g-PAA/AM/ATP 吸附Cd(Ⅱ)的吸附机理包括静电作用—NH2(或
—NH+)、—OH 与 Cd2+之间的络合作用以及—COOH与Cd2+之间的离子交换作用。
3 结论
CMC-g-PAA/AM/ATP 能够高效快速地去除水体中的 Cd(Ⅱ)。溶液初始pH值对反应的影响较大,初始 pH 在 4.0~8.0 范围内吸附效果佳。吸附反应在 40 分钟内达到平衡整个吸附过程更符合准二级动力学模型。与 Freundlich 模型相比Langmuir模型能够更好地拟合吸附过程。吸附过程放热随着温度升高去除率降低。三次脱附再生实验结果显示CMC-g-PAA/AM/ATP 对 Cd(Ⅱ)始终保持较好的吸附性能。红外谱图的变化和 XPS 表征结果分析得出 CMC-g-PAA/AM/ATP 吸附 Cd(Ⅱ)的吸附机理包括静电作用—NH2或—NH+—OH与Cd2+之间的络合作用以及—COOH与Cd2+之间的离子交换作用。综合考虑其制备工艺、耐酸碱、优越的吸附和再生能力CMC-g-PAA/AM/ATP 是去除水体中Cd(Ⅱ)的理想材料。
图6 CMC-g-PAA/AM/ATP的XPS谱图
Fig.6 XPS images of CMC-g-PAA/AM/ATP
[1] 黄鑫高乃云张巧丽. 改性活性炭对镉的吸附研究. 同济大学学报200836(4):508-513
[2] 郭燕妮方增坤胡杰华等. 化学沉淀法处理含重金属废水的研究进展. 工业水处理201131(12):9-13
[3] Hardiljeet KBoparaiJosephMet al. Cadmium (Cd2+) removal by nano zerovalent iron:surface analysiseffects of solution chemistry and surface complexation modeling. Environmental Science and Pollution Research201320(9):6210-6221
[4] 李孟璐胡书红崔跃男. 离子交换法的发展趋势及应用. 广东化工201414(41):112
[5] 王璞闵小波柴立元. 含镉废水处理现状及其生物处理技术的进展. 工业安全与环保200632(8):14-20
[6] El-Hag A AShawky H AEl-Rehim H A Aet al. Synthesis and characterization of PVP/AAc copolymer hydrogel and its applications in the removal of heavy metals from aqueous solution. European Polymer Journal200339(12):2337-2344
[7] Alexandre T PLaurence A BLauro T Ket al. Efficiency of hydrogels based on natural polysaccharides in the removal of Cd2+ions from aqueous solutions. Chemical Engineering Journal2011,168(1):68-76
[8] Pekel NGüven O. Separation of heavy metal ions by complexation on poly (N-vinyl imidazole) hydrogels. Polymer Bulletin200451(4):307-314
[9] 徐浩龙. 羧甲基纤维素接枝丙烯酸复合材料的制备及对 Cr(VI)的吸附研究. 科学技术与工程201212 (14):3532-3536
[10] 曹向宇李垒陈灏. 羧甲基纤维素/Fe3O4复合纳米磁性材料的制备、表征及吸附性能的研究. 化学学报201068(15):1461-1466
[11] 张秀兰栗印环牛明改等. 沸石/羧甲基纤维素接枝丙烯酰胺复合型保水剂的制备. 信阳师范学院学报:自然科学版201225(4):534-538
[12] 曹春巨天珍陈兴鹏. CMC/P (AMPS-co-AA)水凝胶对 Pb(II)的吸附动力学及吸附机理研究. 环境化学201332 (10):1909-1916
[13] Liu YCao XHua Ret al. Selective adsorption of uranyl ion on ion-imprinted chitosan/PVA crosslinked hydrogel. Hydrometallurgy2010104(2):150-155
[14] Liu JMa YXu Tet al. Preparation of zwitterionic hybrid polymer and its application for the removal of heavy metal ions from water. Journal of Hazardous Material2010178:1021-1029
[15] Dong XMa L QLi Y. Characteristics and mechanisms of hexavalent chromium removal by biochar from sugar beet tailing. Journal of Hazardous Material2011190:909-915
[16] Wang QZhang J PWang A Q. Preparation and characterization of a novel pH-sensitive chitosan-gpoly (acrylic acid)/attapulgite/sodium alginate composite hydrogel bead for controlled release of diclofenac sodium. Carbohydrate Polymers200978(4):731-737
[17] 苏文强杨磊朱明华. 羧甲基纤维素与丙烯酸的接枝共聚. 东北林业大学学报200432(4):58-61
[18] 胡盛周红艳田大听等. 凹凸棒石/聚丙烯酸高吸水复合材料的制备与表征. 化工新型材料2012,40(7):134-137
[19] Li NBai R B. A novel amine-shielded surface crosslinking of chitosan hydrogel beads for enhanced metal adsorption performance. Industrial & Engineering Chemistry Research200544(17):6692-6670
Studies on Removal and Mechanisms of Cd(II) Ions from Aqueous Solution Using CMC-g-PAA/AM/ATP
DENG Hongmei1ZHANG Zijun1,2XU Nan2,†
1. School of Environmental Science and EngineeringGuangzhou UniversityGuangzhou 510006;2. School of Environment and EnergyPeking University Shenzhen Graduate SchoolShenzhen 518055;† Corresponding authorE-mail:xunan@szpku.edu.cn
In presence of the attapulgitethe absorbent carboxymethyl cellulose-g-poly(acrylic acid)/acrylamide /attapulgite (CMC-g-PAA/AM/ATP) was synthesized by solution grafting copolymerization of carboxymethyl celluloseacrylic acid and acrylic amide with ammonim peroxodisulphate as an initiator and MBA as crosslink agent. CMC-g-PAA/AM/ATP was applied in the Cd(II) adsorption from aqueous solution. The influences of pH,initial Cd(II) concentrationreaction timetemperature and dosage on the adsorption were investigated. The adsorption capacity reached a high level when pH was in the range of 4.0-8.0. The reaction reached equilibrium within 40 min and the adsorption kinetics was better described by pseudo-second order equation. The reaction was an exothermic process. The as-prepared and Cd-loaded CMC-g-PAA/AM/ATP were characterized by Fourier transform infrared spectroscopy (FT-IR) and X-ray photoelectron spectroscopy (XPS) to identify the structure of the adsorbentsand verify the removal mechanisms. CMC-g-PAA/AM/ATP proved to be a promising candidate for the fast removal of Cd(II) from aqueous solution. The Cd(II) removal mechanisms by CMC-g-PAA/AM/ATP include electrostatic interactionchelation and ion exchange.
CMC-g-PAA/ATP;Cd(II);adsorption;mechanisms
X522
国家自然科学基金(41170399)和广州市科技计划2015科学研究专项(20151010225)资助
2015-05-23;
2016-04-11;网络出版日期:2016-05-17
