基于血液微透析技术探究五味子甲素的体内代谢过程
2016-07-31诸明娜徐瑞鑫
诸明娜,徐瑞鑫
1.无锡市第二人民医院药剂科,江苏 无锡 214002;2.长春金赛药业有限责任公司,吉林 长春 130012
基于血液微透析技术探究五味子甲素的体内代谢过程
诸明娜1,徐瑞鑫2
1.无锡市第二人民医院药剂科,江苏 无锡 214002;2.长春金赛药业有限责任公司,吉林 长春 130012
目的建立高效液相色谱法测定大鼠血浆中五味子甲素的方法,探讨五味子甲素在大鼠血中的代谢过程。方法采用血液微透析技术,将探针由右侧颈静脉植入大鼠右心房膨大处,透析取样。透析液检测的色谱条件为:以甲醇-乙腈-水(40∶35∶25)为流动相,流速1.0mL/min,柱温30 ℃,UV检测波长254 nm。经体内测定探针的回收率校正后,绘制药时曲线,采用DAS2.0软件计算五味子甲素灌胃给药后在大鼠血液中的药动学参数。结果五味子甲素在2~500 μg/mL浓度范围内线性关系良好(r=0.999 5),日内精密度和日间精密度均 RSD<3%,五味子甲素的含药透析液室温放置 12 h内稳定性良好。药动学参数 ke为(0.364± 0.047)/h,t1/2为(1.637±0.302)h,Tmax为(0.612±0.194)h,Cmax为(165.92±28.830)μg/mL,AUC0-t为(240.793±25.540)μg·h/mL,AUC0-∞为(282.710±30.727)μg·h/mL。结论本方法操作便捷、液相保留时间短,能满足透析液中五味子甲素含量测定的需要,可用于五味子甲素在大鼠血液中代谢过程的研究。
血液微透析;五味子甲素;高效液相色谱法;药时曲线
微透析技术是近年来发展起来的一种新型的生物在体采样技术,在组织或者血管中植入具有半透膜的探针,小分子物质可以随着浓度梯度通过半透膜,而分子量较大的物质如蛋白等则不能自由通过半透膜。采用微量灌流泵使一定量的灌流液流经探针,即可在收集装置中定量检测所测物质的含量。微透析技术最早用于测定实验动物脑内神经递质的含量[1],目前,该技术已成为研究各种动物脑内神经递质变化所不可缺少的方法之一。由于微透析技术可从实验动物血液中连续动态取样,而且所采集的样本都是小分子物质,无需除去血清中蛋白的纯化过程,可以直接采用高效液相色谱法(HPLC)进行检测,大大提高了实验验操作的便利利性[2],因此此近年来其在药动学领域的应用越来越广泛[3-4]。
五味子是多年生木兰科科植物,具有收敛固涩、补肾宁心、益气生津的功效。现代药理学研究表明,五味子可作用于机体多个系统统,如中枢神经系统、心血管系统和免疫系统等[5],尤其是在保护肝损伤[6]和抗氧化[7]方面具有有非常显著的的疗效。五味子甲素是中药五味子中的木脂素类成分之一,具有诱导肝微粒体细胞色素P450酶活性进而增强肝的解毒功能、降低血清转氨酶、阻断多种毒性物质对肝细胞膜的损伤伤等作用用。中药的药药效物质基础研究是中药现代化的重点和核心内容,本研究采用微透析技术对对五味子中主要药效成分之一五味子甲素在大鼠体内的代谢过程进行研究,以期初步阐明五味味子甲素在血液中的代谢特点,为五味子制剂在临床的的更广泛应用提供依据。
1 仪器、试药药与动物
e2695高效效液相色谱仪仪(Waters公公司),2998UUV二极极管阵列检测测器,kromaasil C18色谱柱柱(250 mmm× 4.66 mm,5 μmm,大连依利利特分析仪器器有限公司)),CMMA402透析液液灌流泵(瑞瑞典CMA公公司),微透析析探针(shaft:5 cmm,cut off:15 kD,瑞典典MAB公司司)。
五味子甲素,成都科普普生物有限公公司,HPLC测定纯纯度>98%,批号1108557-201311。吐温-80,化化学纯,天津市东丽丽区天大化学学试剂厂;甲甲醇,HPLC级级,美国迪马试剂公公司;氯化钠钠,分析纯,天津市红岩岩化学试试剂厂;氯化化钾,分析纯纯,天津市东东丽区天大化化学试剂剂厂;硫酸镁镁,分析纯,天津市风船船化学试剂科科技有限公司;纯净净水,Milliporre water puriffication systems制备备;氯化钙,,分析纯,天天津市基准化化学试剂有限公司;磷酸二氢钾钾,分析纯,天津市风船化化学试剂科技有限公公司;碳酸氢氢钠,分析纯纯,齐齐哈尔市华侨化工厂。
清洁级雄性Wistar大鼠鼠6只,体质量(250±20)g,购自南京医科大学动物实验中心,许许可证号 SYXK(苏)2002-00013。实验前前在本实验室室条件下单笼饲养1周,以适应应环境,减少少应激对实验验结果的影响,温度20~22 ℃℃,相对湿度45%~65%%。
2 方法与结果
2.1 微透析取样方法的建建立
2.1.1 透析液的配制 采用Ringer's Solution作为透析液[8],包括00.4 mmol/L KH2PO4、3.0 mmol/L KCl、25.0 mmol/L NaHCO3、1.2mmol/L CaCl、1.2 mmol/L MggSO4、122.0mmol/L NaCl,另加入1%吐温-80,混悬后超声震荡20 min使其形成均一稳定的溶液。透析液均为每次使用前现配。
2.1.2 微透析探针的植入 10%乌拉坦溶液(10mL/kg))麻醉大大鼠,仰位固定于手术台上,剪开颈部皮毛,钝性剥离右侧颈静脉脉,远心端结扎,采用眼科剪刀在静脉血管管处开一小口口,将含有保护套管的微透析探针经由颈静脉植入大鼠右心房膨大处[9](上腔静脉与下腔静脉汇合位置,距离颈外静脉和颈内静脉汇合处约约3.3~3.5 cm),用非吸附性手术线固定,防止探针脱位。整个植入过程中用吐温-80润滑保护套管,以保证探针顺利植入。
2.2 五味子甲素测定方法
2.2.1 色谱条件 参考文献[10-12]中五味子甲素的的HPLCC检测方法,并结合本试验中透析液的特性,对检测条条件进行适当当优化。最终确定色谱条件如下:流动相为为甲醇-乙腈-水(40∶35∶25),流速1.0mL/min,柱温30 ℃,UV检测波长2554 nm。
2.2.2 对照品储备液的制备 精密称取五味子甲素对照品1.0 mg,溶解在2 mLL透析液中,配制成浓度为0.55 mg/mL的对对照品储备液。
2.2.3 专属性考察 分别进样五味子甲素对照品储备液、、空白透析液和大鼠给药后血液透析液各10 μL,按“2.2.1”项下色谱条件进行检测,考察该色谱条件的专属性。五味子甲素对照品、空白透析析液和大鼠给药后血液透析液的的高效液相色谱图见图1,五味子甲素的保保留时间约为为9.8 min,五味子甲素峰与周围杂质峰能够达到基线分分离,且峰形形良好,透析析液中其他成分对信信号峰无干扰扰。
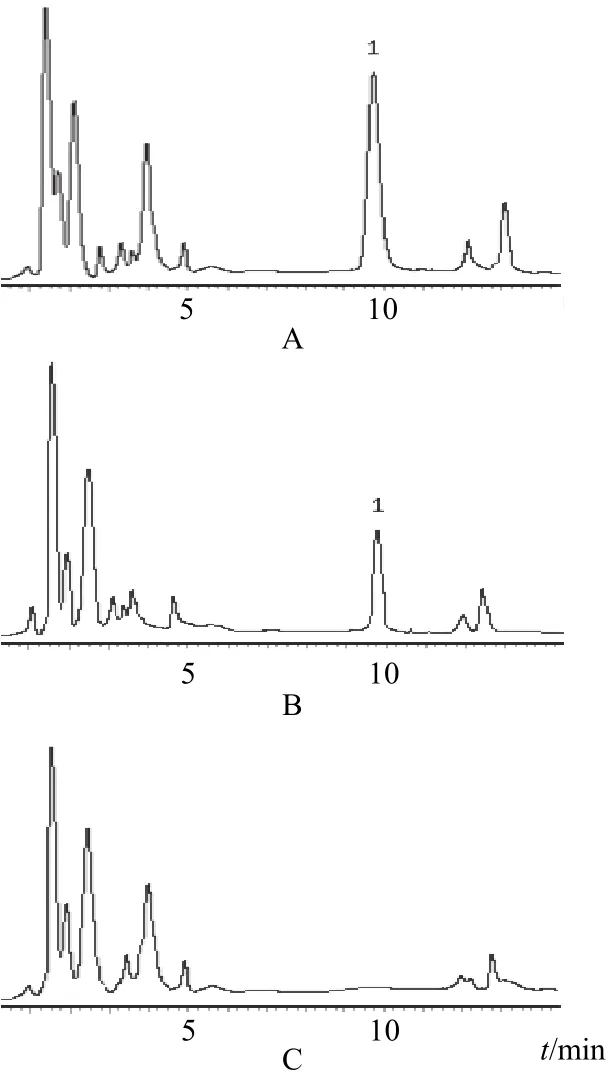
图1 透析液中五味子甲素高效液相色谱图
2.2.4 标准曲线的制备 取对照品储备液适量用空白透析液进行梯度稀释,得到系列浓浓度梯度的对对照品透析液,即500、200、100、20、2 μμg/mL。按“2.2.1”项下色谱条件进样分析,进样量为10 μL,以峰面积对五味子甲素浓度做线性回归,制备标准曲线,回归方程为Y=44781.0X+188 697.1,r=00.999 5,表明明五味子甲素在2~~500 μg/mLL浓度范围内线性关系良好。
2.2.5 日内精密度和日间精密度考察 取浓度分别为500、200、、20 μg/mL的的五味子甲素透析液,按“2.2.1”项下色谱条条件在同日内连续5次进样样分析,进样样量为10 μL,分别别测定3个浓度的日内精密度。将上上述3个浓度的五味子甲素透析液连续5d重复进样检测,进样量为10 μL,测定日间精密度。结果见表1。结果表明,无论论日内精密度还是日间精密度,500、、200、20 μg/mL五味子甲素峰面积RSDD值均在 0.558%~2.89%之间,,符合定量检测的要求。
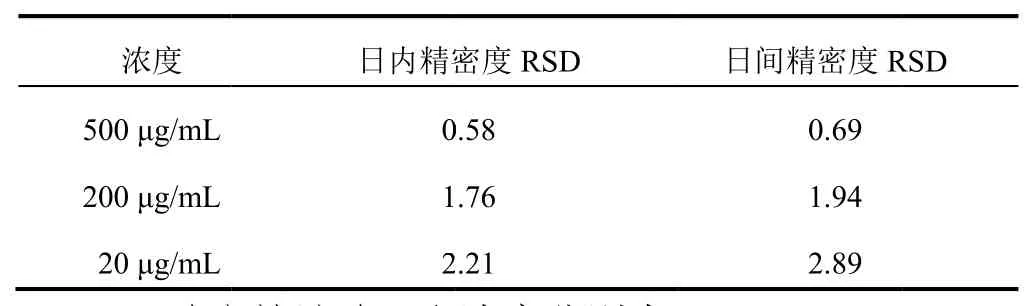
表1 日内精密度和和日间精密度考察结果(%)
2.2.6 稳定定性试验 取浓度分别为500、200、20μg/mL的五味子甲素透析液,室温放置,按按“2.2.1”项项下色谱条件分别别于2、4、6、8、12 h进样分析,进样量为10 μL,记录峰面积。结果表明5000、200、20 μμg/mL五味子甲素峰面积 RSDD值分别为0.62%、0.882%、1.34%,符合定量检测的的要求,表明五味子甲素透析液室温放置置12 h内稳定定性良好。
2.3 五味子甲素药动学学研究
2.3.1 样品采集与测定定 打开透析析液灌流泵(流速2 μL/min),用空白透析析液灌流1 h后后,灌胃给药五味子甲素20 mmg/kg,灌胃后后立即开启透透析液自动收集装置,样品采采集点分别为第5、15、225、35、45、55、65、75、85、、95、115、1135、155、1885、215、2455 min,共连续收集16个样品。。所得透析液样品按“2.2.1”项下色谱条件立即进样分析,进样量为10 μL,记录峰面积。
2.3.2 体内回收率测定定 收集样品后,用空白透析液继续灌流流2 h,然后换用已知浓度的五味子甲素透析液(浓度100 μg/mL)继续灌流,,平衡1 h后后,收集连续 3个个样品,收集间隔为 10min。收集样品按“2.2.1”项下下色谱条件立即进样分析,进样量为110 μL,记录峰面积,测定探针在在大鼠体内的的回收率(RR),计算公式R=(1-Cout/Cin)×100%[13]。个体血药浓度均经自身的体内回收率进行校正。个体实验结束后,处死大鼠,开胸检查探针半透膜植入的的位置,位置不正确的个体数据不纳入统计。
2.3.3 药动学参数的计算 运用 DAAS2.0药动学学软件 进行统计分析,采用统计矩的方法计算各药动学参数,并以血药浓度对时间做药时曲线,,结果见图2、表2。

图2 五味子甲素在在大鼠体内的药时时曲线
表2 五味子甲素在大鼠体内的药动学参数(±s)
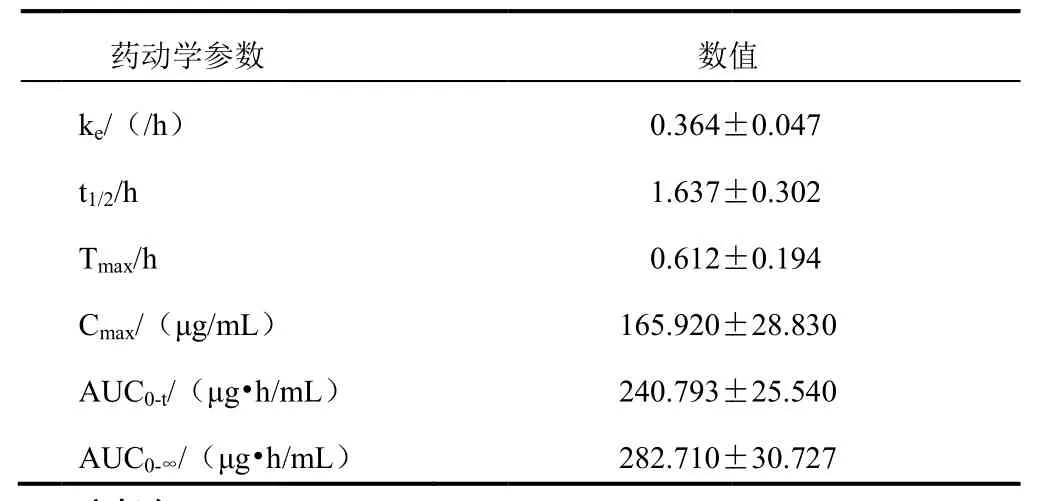
表2 五味子甲素在大鼠体内的药动学参数(±s)
药动学参数ke/(/h)t1/2/h Tmax/h Cmax/(μg/mL)AUC0-t/(μg·h/mAUC0-∞/(μg·h/mL)/mL)数值0.364± 1.637± 0.612± 165.920± 240.793± 282.710±值±0.047 ±0.302 ±0.194 ±28.830 ±25.540 ±30.727
3 讨论
血液微透析技术可在在同一实验动物的不同组织中植入探针,进而同时连续动态地监测药物在多个组织的代谢过程,既降低了实验误差,又减少了实验动物的样本数。与传统的采静脉血测定方方法相比,血液微透析的在体取样技术不减少动物体液液含量,而且透过透析膜的小分子物质可直接进行液相相检测,所测血药浓度更加准确。另外,采得的样本都是游离态药物,相对来说能更加准确反映有效成分的药物浓度[14]。。
有研究表明,雄性大鼠细胞色素P3A1、P3A22、P33A18在微粒体内的含量分分别为雌性大大鼠的5、100、200倍以上,另另外,雄性大大鼠细胞色素P450酶的含含量也也较雌性大鼠高10%~30%%[15],这也解解释了与五味味子甲素同为木脂脂素类成分的的五味子醇甲甲在雌性大鼠鼠体内代谢相对较慢的现象。为为最大程度上上减少实验动动物性别因素对结果的影响,本本研究全部采采用Wistar品系雄雄性大鼠。
探针的植入位置对实验结果的影响较大[16]。在本研究的预实验中,曾考察过过其他植入位位置,如大鼠的颈静脉,但此处空间狭小且血流速度较慢,探针植入后阻碍颈静脉血液回流,并且极易造成凝血,致使探针透析膜堵塞。最终选用大鼠上下腔静脉汇合处作为探针植入处,此处接近大鼠的右心房,空间较大,将探针植入此处,虽然阻碍了一小部分上腔静脉血液的回流,但下腔静脉会提供充足的血流供透析采样。经过反复预试验的摸索,最后确定采用体质量250g左右的大鼠、探针由颈静脉植入的深度在 3.3~3.5 cm之间较为合适。
常用的测定微透析探针回收率的方法主要有体外测定和体内测定2种[17-18]。由于体内测定的环境、温度、pH值和血流速度等都与探针实际透析时一致,测定结果更加准确、客观。因此,本研究采用体内减量法测定探针的回收率。
本研究考察的是大鼠灌胃给药五味子甲素后在体内的代谢过程,在预实验中没有考察五味子甲素在大鼠体内是否符合线性药动学的特征,在药动学参数的计算过程中采用房室模型拟合是不合理的,因此,本研究采用统计矩的方法计算相关的药动学参数,该方法主要通过药时曲线下面积分析药物在体内的代谢过程,不受限于数学模型,适用于任何隔室模型,是非隔室分析法之一[19]。
五味子甲素在大鼠体内的药时曲线表明,大鼠灌胃五味子甲素后血药浓度迅速升高,约35 min后血药浓度达到峰值(165 μg/mL左右),随后迅速下降。由药动学参数可以看出,五味子甲素在大鼠体内的半衰期和滞留时间均较短,属于快速代谢型药物,这与以往文献报道的结果相似[20]。
[1] DELGADO J M, DEFEUDIS F V, ROTH R H, et al. Dialyt rode for long termintracerebral per fusion in awake monkeys[J]. Arch Int Pharmacody Ther,1972,198(1):9-21.
[2] 张英丰,汪小根,吴阳,等.微透析技术进行药动学研究的发展趋势及局限性探讨[J].中国实验方剂学杂志,2011,17(15):270-273.
[3] 单连菊,丁涵滢,王锐,等.关节微透析技术在药动学及药效学的研究进展[J].中国新药杂志,2015,24(10):1124-1127.
[4] 何治芬,张岩,汤湛,等.HPLC测定大鼠微透析液和血浆中苦参碱的浓度[J].中国现代应用药学,2014,32(12):1514-1519.
[5] 齐雁辉,赵彩玉.五味子的现代药理作用研究进展[J].中国医药指南,2011,9(26):43-44.
[6] 高雁,李廷利.五味子有效成分的药理作用研究进展[J].中医药学报,2011,39(6):104-106.
[7] 赵云,单安山,郭晓秋.五味子乙醇提取物对肉仔鸡抗氧化功能和血液生化指标的影响[J].安徽农业科学,2012,40(9):5268-5270.
[8] Lisa A H Rottbøl l, Christian Friis. Microdialysis as a tool for drug quanti fication in the bronchioles of anaesthetized pigs[J]. Basic & Clinical Pharmacology & Toxicology,2014,114(3):226-232.
[9] 张英丰.微透析法进行青藤碱贴剂透皮特性及药物动力学的研究[D].广州:广州中医药大学,2006.
[10] 史敏,林超,秦华.HPLC测定养肝片中五味子醇甲、五味子甲素、五味子乙素含量[J].食品与药学,2014,16(6):433-435.
[11] 汪荣斌,王义祁,秦亚东,等.LC-UV法测定华中五味子中五味子酯甲、五味子甲素、五味子乙素含量[J].长春中医药大学学报,2014,30(2):213-215.
[12] 乔春凤,董仲生.高效液相色谱法测定抗风湿液中染料木苷、染料木素、去氢二异丁香酚、五味子甲素的含量[J].中南药学,2014,12(9):896-899.
[13] 左代英,吴英良,曹悦.微透析结合 HPLC-ECD测定头抱他啶在大鼠血中含量及其药动学研究[J].中国药学杂志,2005,40(12):931-933.
[14] 魏凤环.微透析采样技术在药动学研究中的应用及意义[J].中药材,2008,31(6):940-943.
[15] HEDLUND E, GUSTAFSSON J A, WARNER M. Cytochrome P450 in the brain:a review[J]. Cur r Drug Metab,2001,2(3):245-263.
[16] 鄢欢,曹玲娟,李焕德.提高微透析探针回收率方法的研究进展[J].中南药学,2014,12(2):140-144.
[17] 吴丽颖,吕红博,张运好,等.替硝唑、达克罗宁和氯己定微透析探针体外回收率及大鼠体内稳定性的研究[J].药物分析杂志,2014,34(11):1942-1947.
[18] 王秀云,方俊聪,杨光,等.基于LC-MS/MS技术的罗库溴铵微透析探针回收率测定的方法学研究[J].第二军医大学学报,2015,36(4):396-401.
[19] 梁文权,李高,刘建平.生物药剂学与药物动力学[M].3版.北京:人民卫生出版社,2000:272.
[20] 郭庆英,王振华,张长水,等.五柴颗粒中五味子甲素的小鼠血清药动学研究[J].时珍国医国药,2008,19(10):2487-2488.
Exp loration of Deoxyschizandrin Metabolic Processes in Vivo Based on Blood Microdialysis
ZHU Ming-na1, XU Rui-xin2
(1. Department of Pharmacy, Wuxi No.2 People's Hospital, Wuxi 214002, China;2. GeneScience Pharmaceuticals Co. Ltd., Changchun 130012, China)
ObjectiveTo establish an HPLC method for evaluating deoxyschizandrin in rat plasma; To explore deoxyschizandrin metabolic processes in blood.MethodsThe blood microdialysis probe was implanted into the right atrial enlargement through right jugular vein to detect the concentration of deoxyschizandrin in blood. Chromatographic conditions for detecting of dialysis fluid were as follows∶ mobile phase was methanol-acetonitrilewater (40∶35∶25); flow rate was 1mL/min; column temperature was 30 ℃; UV detection wavelength was 254 nm. The data obtained after being calculated by the recovery rate of the probe in vivo were dealt with DAS 2.0 software. Pharmacokinetic parameters were calculated, and the concentration-time related curves were plotted.ResultsThe deoxyschizandrin curve was linear (r=0.999 5) within the range of 2–500 μg/mL. The RSD of intra-day pecision and inter-day pecision were both <3%. The stability of the solution was good in 12 hours at room temperature. kewas(0.364±0.047)/h; t1/2was (1.637±0.302)h; Tmaxwas (0.612±0.194)h; Cmaxwas (165.92±28.830) μg/mL; AUC0-twas(240.793±25.540) μg·h/mL; AUC0-∞was (282.710±30.727) μg·h/mL.ConclusionThe method is convenient to perform, and the retention time of HPLC is short. This method is suitable for detecting the content of deoxyschizandrin in dialysis fluid, which can also be used to investigate the metabolic processes of deoxyschizandrin in the rat blood.
microdialysis; deoxyschizandrin; HPLC; concentration-time curve
10.3969/j.issn.1005-5304.2016.06.025
R284
A
1005-5304(2016)06-0099-04
2015-07-10)
(
2015-08-03;编辑:陈静)
徐瑞鑫,E-mai l:11092239@qq.com
