外翻肠囊法研究奥硝唑对映体在大鼠不同肠段的吸收特性
2016-07-27王嫦鹤刘雪峰耿庆光
王嫦鹤, 刘雪峰,王 莉, 耿庆光
(陕西省食品药品检验所,西安 710061)
·药物分析·
外翻肠囊法研究奥硝唑对映体在大鼠不同肠段的吸收特性
王嫦鹤, 刘雪峰,王莉, 耿庆光
(陕西省食品药品检验所,西安710061)
摘要:目的考察奥硝唑在大鼠各肠段的吸收特性及奥硝唑两手性对映体在大鼠不同肠段吸收的差异性。方法采用大鼠外翻肠囊法,以HPLC手性色谱柱法测定奥硝唑在不同肠段的吸收量以及S-奥硝唑及R-奥硝唑的同一肠段肠吸收量,并分别计算吸收速率常数(Ka)和表观渗透系数(Papp),同法考察了P-蛋白抑制剂(维拉帕米和环孢素A)对奥硝唑肠吸收特性的影响。结果奥硝唑在不同肠段吸收均呈线性,符合零级药物吸收速率,吸收趋势为空肠>回肠>结肠。在空肠段两对映体以近于1∶1的比例同时吸收,吸收速率不存在显著差异,随着供试液中奥硝唑质量浓度的上升,Ka呈线性增加(R2>0.99),Paap基本保持不变,P-蛋白抑制剂对奥硝唑的肠吸收没有显著性影响(P>0.05)。结论奥硝唑在不同肠段的吸收有差异,空肠部位是吸收的最佳部位(P<0.05),S-奥硝唑与R-奥硝唑在肠道中吸收速率不存在显著差异,吸收以被动扩散机制为主,奥硝唑不是P-糖蛋白的底物。
关键词:奥硝唑;肠外翻;对映体;P-糖蛋白
奥硝唑是硝基咪唑类药物,结构中有一个手性中心,故有一对手性对映体。目前临床上使用的大多是奥硝唑的消旋体,其抗厌氧菌的作用比甲硝唑更强[1]。研究报道[2],左旋奥硝唑[S-(-)-1-(3-氯-2-羟丙基)-2-甲基-5-硝基咪唑]是奥硝唑的L-型对映体,其药动学特性优于奥硝唑的消旋体,但毒性、中枢抑制作用均低于右旋体和消旋体。因此,左旋奥硝唑的研究和应用也越来越受到研究者的重视[3]。为深入探讨奥硝唑的肠吸收特性,本文采用大鼠肠外翻模型,研究了奥硝唑在不同肠段的吸收及奥硝唑S-奥硝唑和R-奥硝唑在肠道中的吸收情况,为阐明奥硝唑对映体的肠吸收动力学机制、指导临床用药和提高临床疗效提供实验依据。
1仪器与材料
1.1仪器岛津Nexera UHPLC LC-30A高效液相色谱仪(含New LC-30AD泵系统、SIL-30AC自动进样器、CTO-20AC柱温箱、SPD-20A紫外检测器、CBM-20A控制器、Empower色谱数据理系统);Chiralcel OB-H手性色谱柱(250 mm×4.6 mm,5 μm,日本Daicel Chemical IND公司);Allegra 64R低温高速离心机(美国 Beckman Coulter 公司);JXDC-20型氮吹仪(上海净信科技有限公司);Direct-Q3型超纯水机(默克化工技术(上海)有限公司);DK-98-IIA恒温水浴锅(天津泰斯特仪器有限公司);AB135-S型电子分析天平(瑞士梅特勒-托利多仪器有限公司); XH-C型涡旋振荡器(南京东迈科技仪器有限公司);混合气体(95%O2,5%CO2)。
1.2试药奥硝唑消旋体对照品(中国食品药品检定研究院,批号:100608-201102);左旋奥硝唑对照品(S-奥硝唑,中国食品药品检定研究院,批号:100874-200501);右旋奥硝唑对照品(R-奥硝唑,光学质量分数>99. 5%)由南京圣和药业有限公司提供;盐酸维拉帕米(verapamile,Ver,中国食品药品检定研究院,批号:100223-200102);环孢素A(cycloporine,CsA,中国食品药品检定研究院,批号:30495-200202);甲醇、正己烷和异丙醇均为德国 Merck公司色谱纯试剂。
1.3实验动物雄性SD大鼠,体质量250±20 g,西安交通大学医学实验动物中心提供(SCXK(陕)2012-003)。
2实验方法
2.1色谱条件色谱柱:Daicel Chiralcel OB-H手性柱(250 mm×4.6 mm,5 μm);流动相:正己烷-异丙醇-甲醇(95∶1∶4);进样体积:5 μL;柱温:30 ℃;流速:0.5 mL·min-1;检测波长:318 nm。
2.2溶液的配制台氏液(Tyrode液):称取氯化钠8.0 g,氯化钾0.2 g,碳酸氢钠1.0 g,磷酸二氢钠0.05 g,氯化镁0.1 g,加蒸馏水溶解;称取氯化钙0.2 g,加蒸馏水溶解;称取葡萄糖1.0 g,加蒸馏水溶解;混匀,用蒸馏水定容至1 L即得。
混合对照品储备溶液:分别精密称取S-奥硝唑和R-奥硝唑对照品适量,用流动相配制成质量浓度均为100 μg·mL-1的溶液作为混合对照品储备溶液。
奥硝唑供试液:精密称取奥硝唑对照品适量,加台氏液超声溶解并定容,分别制备成质量浓度约为5,10,25,50和100 mg·L-1的等系列溶液作为奥硝唑供试液。
含Ver的奥硝唑供试液:精密称取奥硝唑对照品适量,加适量台氏液超声溶解,向其中分别加入Ver适量,用台氏液定容,制备成含100 μg·mL-1的Ver及5,25和50 μg·mL-1奥硝唑的供试液。
含CsA的奥硝唑供试液:精密称取奥硝唑对照品适量,加适量台氏液超声溶解,向其中分别加入CsA适量,用台氏液定容,制备成含100 μg·mL-1的CsA及5,25 和50 μg·mL-1奥硝唑的供试液。
2.3大鼠翻转肠囊实验大鼠随机分组,每组5只,实验前禁食12 h,自由饮水。采用文献报道[4]的翻转肠囊法实验。在给药后 30,45,60,90,120和180 min从肠囊内取样1 mL,同时补充相同体积的空白台氏液。样品置于5 mL带盖离心试管中,加入乙酸乙酯200 μL,漩涡振荡3 min,以13 000 r·min-1离心5 min;分取上层有机层,用乙酸乙酯重复萃取2次,合并有机层,氮吹仪吹干除去乙酸乙酯;加流动相200 μL溶解,以0.45 μm微孔滤膜过滤,取续滤液5 μL进样分析,测定样品中S-奥硝唑及R-奥硝唑含量。实验结束后将肠管纵向剖开,自然摊于滤纸上,测量长度和宽度,记录肠段吸收面积A。
2.4线性实验取混合对照品储备液,用流动相逐级稀释,配制成质量浓度分别为0.5~150 μg·mL-1的系列溶液作为线性溶液。分别精密量取该系列溶液5 μL,按照2.1项下的色谱条件进样分析。以对照品溶液质量浓度X为横坐标、峰面积Y为纵坐标,绘制标准曲线,进行线性回归。R-奥硝唑回归方程:Y=34 716X-6.4×105(r=0.999 5),线性范围:0.5~150 μg·mL-1;S-奥硝唑回归方程:Y=34 598X-6.4×105(r=0.999 2),线性范围:0.5~150 μg·mL-1。
2.5数据处理
2.5.1药物累积吸收量按照下式计算。
Q为药物各时间的累积吸收量,Cn为n时间点的实际检测质量浓度,Vs为取样体积,Ci为样品质量浓度。

3结果
3.1高效液相测定方法Chiralcel OB-H手性柱可用于分离含有酰胺基、芳香基团、羰基、硝基、磺酰基、氰基和羟基类化合物。流动相中甲醇和异丙醇的变化对分离度影响较大,且异丙醇的比例过小会出现溶液分层现象。台氏液对奥硝唑的测定无干扰,专属性较好,见图1。

图1奥硝唑手性分离HPLC图
A.奥硝唑对照品; B.肠吸收液样品; C.台氏液空白; 1.R-奥硝唑; 2.S-奥硝唑
Fig.1 HPLC chromatograms of ornidazole analyzed by chiral chromatographic column
A.reference substance of ornidazole;B.sample of intestinal absorption; C.blank sample; 1.R-ornidazole; 2.S-ornidazole
3.2奥硝唑在不同肠段的吸收情况取同一大鼠的不同肠段置于2.2项下25 μg·mL-1的奥硝唑供试液中进行实验,结果表明,奥硝唑在空肠、回肠和结肠均有不同程度的吸收,并且在同一肠段累计吸收量随时间延长呈线性增加,两对映体在180 min内均未呈现饱和。回归分析结果表明,两对映体在不同肠段的吸收与时间呈线性关系,相关系数(R2) 均大于 0.9,符合零级药物吸收速率。
奥硝唑在空肠段的Ka和Papp分别为0.039±0.012 μg·cm-2·min-1和0.001 3±0.000 4 cm·min-1,均高于回肠段0.020±0.008 μg·cm-2·min-1和0.000 75±0.000 16 cm·min-1(P<0.05)以及结肠段0.009 8±0.002 6 μg·cm-2·min-1和0.000 39±0.000 09 cm·min-1(P<0.05)。结果表明,奥硝唑在不同肠段吸收趋势为:空肠>回肠>结肠。3.3S-奥硝唑和R-奥硝唑在肠道中的吸收差异取大鼠的空肠部位置于2.2项下不同质量浓度的奥硝唑供试液中进行实验,结果表明,S-奥硝唑或R-奥硝唑在空肠中的累积吸收量(Q)随时间延长均呈线性增加。随着时间的增长,S-奥硝唑与R-奥硝唑在肠道中吸收速率不存在显著差异,而是以接近于1∶1的比例同时吸收;随着供试液中奥硝唑质量浓度的上升,Ka呈线性增加(R2>0.99),Paap基本保持不变,表明奥硝唑的吸收以被动扩散机制为主。结果见表1。
3.4P-gp抑制剂对奥硝唑肠吸收的影响取大鼠的空肠部位置于2.2项下含Ver和CsA的奥硝唑供试液中进行实验,结果表明,相对于空白组,含Ver的奥硝唑供试液在空肠中的Ka和Papp分别为0.059±0.016 μg·cm-2·min-1和0.001 8±0.000 9 cm·min-1,稍高于空白组的0.049±0.012μg·cm-2·min-1和0.001 3±0.000 4 cm·min-1,但差异无统计学意义(P>0.05)。含CsA的奥硝唑供试液在空肠中的Ka和Papp分别为0.048±0.015 μg·cm-2·min-1和0.000 9±0.000 6 cm·min-1,与空白组比较,差异无统计学意义(P>0.05)。表1空肠中S-奥硝唑与R-奥硝唑的吸收特性比较
Tab.1 Comparison of the absorption characteristics of S-ornidazole and R-ornidazole at jejunum
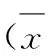
±s,n=3)
4讨论
文献报道[5-6],由于离体肠囊体外时间过长可能会失去生理活性,导致肠囊的通透性发生变化,因此目前离体组织实验多在60~90 min内。研究结果表明,奥硝唑在空肠、回肠和结肠均有吸收,各个肠段Papp均大于1×10-4cm·min-1,空肠是奥硝唑肠吸收的最佳部位。随着供试液中奥硝唑质量浓度增加,药物吸收速率常数Ka呈线性增加(R2>0.94),其表观渗透系数Paap不变,表明奥硝唑的吸收以被动扩散吸收机制为主。
大鼠翻转肠囊吸收实验结果显示,S-奥硝唑与R-奥硝唑在肠道中的吸收速率基本一致,不存在显著性差异。有研究报道[7],S-奥硝唑和R-奥硝唑在大鼠体内的药代动力学特性存在一定的差异,奥硝唑口服给药后,S-奥硝唑和R-奥硝唑的t1/2分别为2.49和3.42 h,AUC分别为168.21和207.19 μg·min·mL-1,这些差异可能与S-奥硝唑与R-奥硝唑在大鼠体内的代谢速度不同有关。
本实验中,空肠段是奥硝唑吸收的最佳部位,选取空肠进一步探究了P-蛋白抑制剂对奥硝唑吸收的影响。从数据结果可知,P-蛋白抑制剂对奥硝唑的吸收没有明显影响,结果说明奥硝唑不是P-糖蛋白的底物。参考文献:
[1]田怀平, 马小亚, 王美纳.奥硝唑在兔体内的药动学和生物利用度研究[J].西北药学杂志,2005,20(3):104-106.
[2]孙继红,王志强,顾兴丽,等.左旋和右旋奥硝唑对小鼠中枢神经系统毒副作用的比较研究[J].中国药科大学学报,2008,39(4):343-347.
[3]陈忆冰,李健和,黎银波,等.左旋奥硝唑氯化钠注射液细菌内毒素检查[J].西北药学杂志,2006,22(3):141-142.
[4]董宇,张英丰,杨庆,等.戊己丸提取物不同配伍的肠外翻吸收研究[J].中国药理学通报,2010,26(10):1377-1382.
[5]郭竹君,崔志清,段宏泉.缚管翻转肠囊法研究委陵菜黄酮在大鼠小肠内的吸收行为[J].天津医科大学学报,2009,15(3):348-350.
[6]何卉,陈西敬,王广基.药物转运体在反式白藜芦醇肠道吸收中的作用[J].中国药科大学学报,2008,39(4):324-328.
[7]陈燕,石涛,柳晓泉,等.左旋和右旋奥硝唑在大鼠体内的药代动力学[J].中国药科大学学报,2006,37(1):41-44.
基金项目:陕西省社会科学基金项目(编号:13G020)
作者简介:王嫦鹤,女,博士,副主任药师
*通信作者:耿庆光,女,副主任药师
doi:10.3969/j.issn.1004-2407.2016.04.013
中图分类号:R945
文献标志码:A
文章编号:1004-2407(2016)04-0371-04
(收稿日期:2015-09-22)
Study on the absorption characteristics of ornidazole enantiomers at different intestine segments by isolated in vitro-everted intestine model
WANG Changhe, LIU Xuefeng, WANG Li, GENG Qingguang*
(Shaanxi Institute for Food and Drug Control, Xi′an 710061, China)
Abstract:Objective To study the absorption characteristics of ornidazole and the absorption difference of ornidazole enantiomers at different intestine segments by isolated in vitro-everted sac intestine model, and to investigate the effect of P-inhibitors to ornidazole intestinal absorption.Methods Rat in vitro-everted intestine sac was used to determine the characteristics of ornidazole.The concentration of ornidazole and its enantiomers at different intestine segments were determined by HPLC equipped with chiral chromatographic column.Then the constant of absorption rate(Ka) and the apparent permeability coefficient(Papp) were calculated.Same method was applied in investigating the impact of the P-glycoprotein inhibitors(verapamil and cyclosporin A) on the absorption of ornidazole in intestinal segments.Results The absorption of ornidazole in different intestinal segments showed a linear absorption and complied with the zero order kinetics.The descending order of ornidazole absorption was jejunum, ileum and colon.There was no significant difference among the absorption rate of the two enantiomers.Ka increased linearly(R2>0.99) and Paapremained unchanged with the rise of concentration for ornidazole in solution at jejunum.P-protein inhibitors had no significant effect on the intestinal absorption(P>0.05).Conclusion The absorption of ornidazole in different intestinal segments was different and the Ka and Paapat jejunum were significantly higher than that at the other segments of intestine (P<0.05).There was no significant difference between S-ornidazole and R-ornidazole in the intestinal absorption rate and met the passive transport mechanism.Ornidazole would not be the substrate of P-protein inhibitor.
Key words:ornidazole; intestinal eversion; enantiomer; P-protein inhibitor
