某三甲医院859例药品不良反应回顾性分析
2016-07-15张群卫吴新安
张群卫,金 镭,吴新安,刘 梅
(中国人民解放军第一〇五医院药剂科,安徽 合肥 230031)
某三甲医院859例药品不良反应回顾性分析
张群卫,金镭,吴新安,刘梅
(中国人民解放军第一〇五医院药剂科,安徽 合肥 230031)
摘要:目的回顾性分析某三甲医院859例药品不良反应,了解不良反应发生特点及相关因素,为临床安全合理用药提供依据。方法对该院2013年7月至2015年6月期间的859例药品不良反应(adverse drug reactions,ADR)报告进行回顾性分析,按药品不良反应报告类型、来源、患者性别、年龄、给药途径、药品种类、累及的器官或系统及临床表现等进行统计和分析。结果859例ADR报告中,男性发生ADR的概率为女性的1.2倍;61~70岁的老年患者发生ADR的比例最高(23.40%);肿瘤用药引起的ADR最多(39.23%);静脉滴注为引发ADR为主要的给药途径 (72.76%);ADR累及器官或系统以消化系统损害最多(33.48%)。结论临床用药应加强不良反应监测,尤其针对老年患者加强用药监护,规范肿瘤用药,尽可能选择口服给药途径,减少或避免不良反应发生。
关键词:药物副反应报告系统;药物毒性;回顾性研究
药品不良反应(adverse drug reactions,ADR)是指合格药品在正常用法、用量下出现的与用药目的无关的或意外的有害反应[1]。ADR监测体系是监测临床用药安全、及时发现药品安全隐患的重要手段之一[2]。截止到2014年,我国已有24万余个医疗机构、药品生产经营企业注册为药品不良反应监测网络用户,并通过该网络报送药品不良反应报告,其中医疗机构仍是报告的主要来源[3]。笔者对中国人民解放军第一〇五医院2013年7月至2015年6月之间的859例ADR报告采用回顾性分析,为临床安全用药提供参考。
1资料与方法
利用医院ADR监测系统,检索2013年7月至2015年6月期间上报的有效ADR报告,利用Excel对ADR报告数据进行处理和分析。采用回顾性分析,对859例ADR报告分别按患者年龄、性别、药品种类、给药途径、累及系统或器官与主要临床表现等进行统计和分析。药品分类方法参照2010年版《中国国家处方集(化学药品与生物制品卷)》[4],中成药单独分为一类。ADR累及器官或系统及临床表现采用《WHO药品不良反应术语集》定义[5]。根据国家食品药品监督管理局ADR监测中心的评价标准,对ADR进行程度分级,分为新的一般的,新的严重的,严重的及一般的。
2结果
2.1ADR报告类型及来源859例ADR报告中,新的严重的1例(0.12%),新的一般的40例(4.66%),严重的8例(0.93%),一般的811例(94.30%)。859例ADR报告中,临床医生报告628例(73.11%),护士报告131例(15.25%),药师报告100例(11.64%)。
2.2ADR患者的性别与年龄分布859例ADR报告中,男性患者467例(54.37%),女性患者392例(45.63%),男性发生ADR是女性的1.2倍。发生ADR最高的年龄段是在60岁以上至70岁及以下的患者,有201例(23.40%)。ADR患者年龄、性别分布情况见表1。
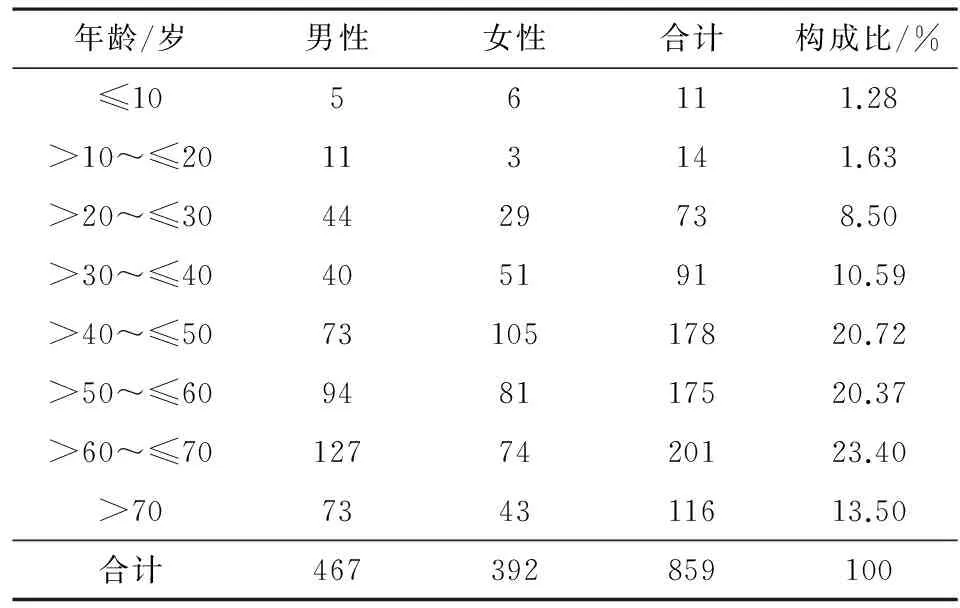
表1 ADR患者的性别、年龄分布及其构成比/例
2.3引发ADR的给药途径分布情况859例ADR报告中,引发ADR较多的前3种给药途径分别是:静脉滴注625例(72.76%),口服给药189例(22.00%),静脉注射21例(2.44%),具体情况见表2。

表2 引发ADR的给药途径分布及其构成比
2.4引发ADR的药品分类情况859例ADR报告涉及的药品共有16类,肿瘤用药居首位337例(39.23%),其次为感染疾病用药201例(23.40%)。以肿瘤用药引起的ADR为例,又以细胞毒类药物的ADR发生率最高,为142例(42.14%)。引发ADR的药品种类、引起ADR的肿瘤药物分类其构成比见表3,4。

表3 引发ADR的药品分类及其构成比

表4 引发ADR的肿瘤用药分类及其构成比
2.5ADR涉及的器官或系统及临床表现根据累及系统或器官对ADR统计时,涉及两个或者两个以上累及系统或器官进行累加统计,859例ADR中共统计累及系统或器官914例次。ADR报告中以消化系统损害最常见,有306例(33.48%),临床表现主要有恶心、呕吐、便秘、腹泻、腹痛等;其次为皮肤及其附件,有155例(16.96%),临床表现为皮肤皮疹、瘙痒、斑丘疹、红斑疹、荨麻疹等,结果见表5。
3讨论
3.1ADR报告类型及来源我院859例ADR中,临床医生和护士上报的ADR比例分别是73.11%和15.25%,由药师报告的100例ADR中临床药师报告的比例为88%,加上临床医生、护士上报说明直接面对患者的医务工作人员更容易发现和报告ADR。
从859例ADR报告统计数据上看,新的和严重的ADR数量较少(5.70%),一般的ADR数量较多(94.30%)。因新的和严重的ADR给药物临床应用的安全性评价意义相对较大,临床应注意加强监测和及时给予处理措施。
3.2患者的性别与年龄分布从859例ADR中可发现,ADR发生于各个年龄段的人群,男性略高于女性。60岁及以上患者发生率较高,这与老年的生理、病理状态有关。由于老年患者身体机能衰退,人体抵抗力下降,易发多种疾病,并用多种药物的可能性较大,且对药物的代谢和排泄机能降低,发生严重ADR的风险也因此加大[6]。另外,儿童处于生长发育期,身体各组织、器官还未完全成熟,对药物的吸收、分布、代谢、排泄等与成人有较大差别,更易受到药物不良反应的损害,安全用药方面存在较大的难度和隐患。因此,医生应根据老年人及儿童的生理、病理特点谨慎用药,应严格掌握药物的适应症、用法用量、不良反应、相互作用、禁忌症等,必要时可选择检测体内药物浓度并调整药物剂量,做好用药监护,避免和减少ADR的发生。
3.3ADR与给药途径的关系从给药途径来看,静脉给药(75.20%,包括静脉滴注和静脉注射)引起的 ADR 比例较高,明显高于口服给药(21.20%)及其他给药方式,与文献报道相近[7-8],这与住院患者临床给药选择大多是静脉给药方式有关。同时,静脉给药因药物直接进入血液循环,无肝脏首过效应,同时注射液的pH值、渗透压、微粒及内毒素等均为ADR的诱因。建议临床医生转变观念,尽量遵循WHO提倡的“能口服就不注射,能肌肉注射的就不静脉注射”的用药原则,这对减少ADR发生、保障临床用药安全有很大作用。如果因病情必须选择静脉给药时,应调整药物的滴速、减少联合用药,并做好用药过程中的监护。
3.4ADR与药物的种类关系从引发ADR的药物种类来看,肿瘤用药物引发的ADR(39.23%)占据首位,其中以细胞毒性药物比例最大,达42.14%。李德爱等[9]对肿瘤患者使用化疗药物发生骨髓抑制与药物之间的相关性进行了研究,发现细胞毒性药物发生骨髓抑制等ADR的概率大于其他类肿瘤药物,与我院ADR回顾性分析结果相近。此外,也与抗肿瘤药物的作用机制有关,细胞毒性药物在杀伤肿瘤细胞的同时也容易对正常组织、器官产生了损害或毒性作用。因此,在使用抗肿瘤药物时,应根据肿瘤类型、分期等首选毒副作用相对较低的药物或者剂型,并严格掌握药物的剂量、给药顺序,做好患者化疗时的防护及用药监护,尽可能减少ADR的发生。
抗感染疾病用药及中成药引起ADR数量也相对较多,与目前临床存在滥用和扩大适应证使用抗生素和中药注射剂有关。建议临床使用抗生素及中药注射剂应严格掌握适应证,切勿盲目使用,以免给患者增加身体损害和经济负担。
3.5ADR所致器官或系统的损害的特点与部分文献报道结果相近[10-11],我院859例ADR累及的器官系统中位居前列的是胃肠系统损害和皮肤及其附件损害,其中胃肠系统损害占33.48%,主要表现为恶心、呕吐、便秘、腹泻、腹痛、食欲下降等;皮肤及其附件损害占 16.96%,临床表现为皮肤皮疹、瘙痒、斑丘疹、红斑疹、多汗、荨麻疹等。可能原因为胃肠系统损害和皮肤及其附件损害相对容易判断,利于患者及医务人员及时发现并报告。
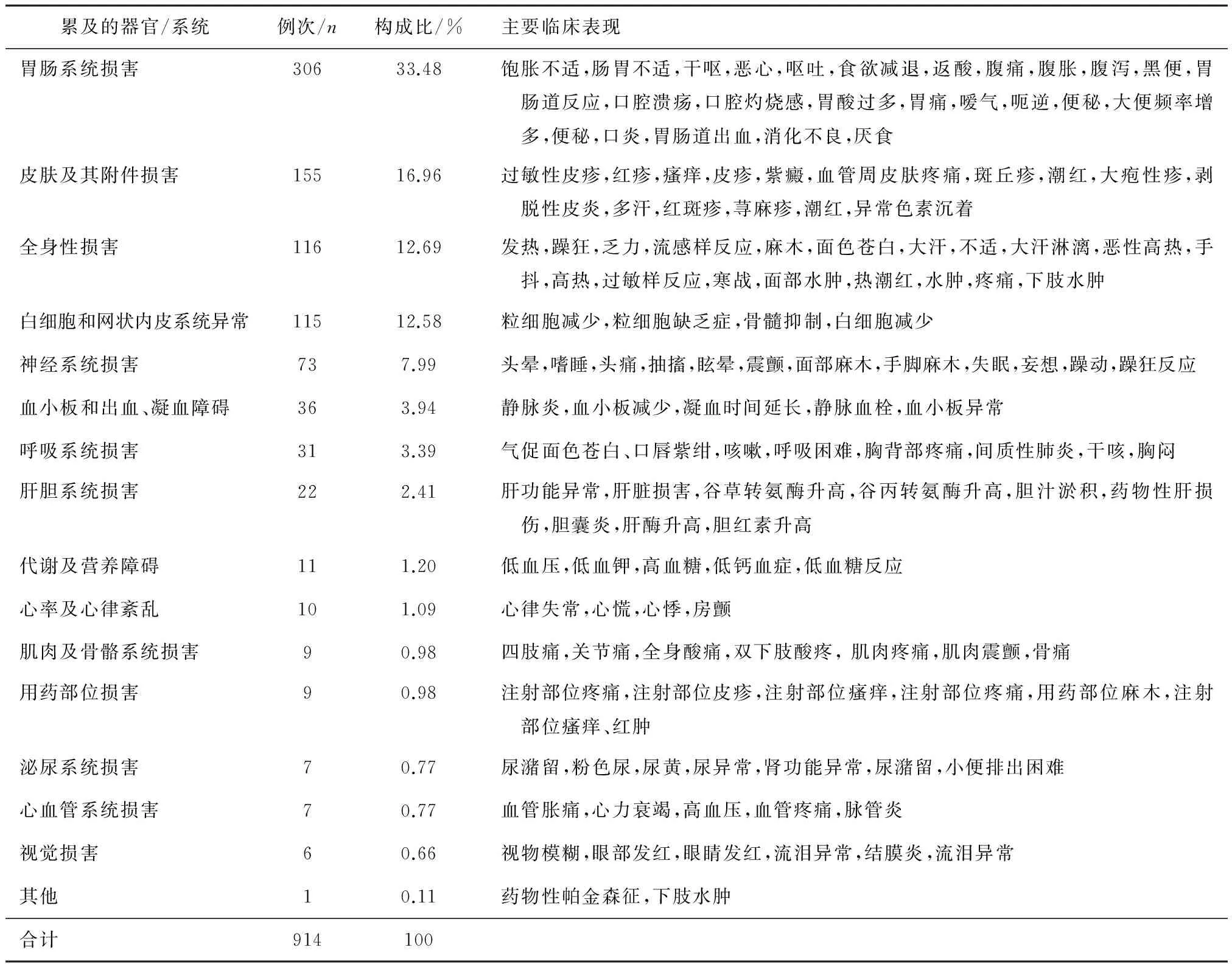
表5 ADR累及的器官/系统及临床表现
从我院的859例ADR报告可以看出,医疗机构应针对ADR报告的意义做好宣传工作,提高直接面对患者的医务人员报告ADR的积极性。临床中针对儿童和老年患者应做到慎重选药,做好用药监护。针对药物可能发生的ADR,向患者做好交待工作,帮助患者正确认识ADR,并做好积极应对措施,既保障患者用药安全,又提高患者就医满意度。
参考文献
[1]国家食品药品监督管理总局.药品不良反应报告和监测管理办法[J].中国药事,2004,18(4):203-206.
[2]颜敏.新的 《药品不良反应报告和监测管理办法》 的特点[J].中国药师,2004,8(7):592-593.
[3]国家食品药品监督管理总局.国家药品不良反应监测年度报告(2014年)[EB/OL].http://www.sda.gov.cn/WS01/CL0078/124407.html,2015-07-17.
[4]中国国家处方集编委会.中国国家处方集(化学药品与生物制品卷)[M].北京:人民军医出版社,2010.
[5]国家药品不良反应监测中心,国家食品药品监督管理局药品评价中心 编译.WHO药品不良反应术语集[M].北京:中国医药科技出版社,2003.
[6]葛文超,汪峰,黄萍.安徽省严重药品不良反应/事件报告回顾性分析[J].安徽医药,2015,19(7):1419-1422.
[7]李凌霞,王路,王淑梅.2012年我院346例药品不良反应报告分析[J].中国药业,2014,23(12):86-88.
[8]孙家跃.我院769例药品不良反应报告分析[J].中国药房,2012,23(18):1702-1704.
[9]李德爱,王大志.抗肿瘤药物与化疗患者发生骨髓抑制情况的药物流行病学研究[J].中国药学杂志,2010,45(24):1968-1970.
[10] 秦明明,陈奕,杨玲,等.某部队医院157例不良反应报告分析[J].西北药学杂志,2012,27(6):595-597.
[11] 郑艺.2013年我院药品不良反应报告分析[J].海峡药学,2015,27(1):235-236.
基金项目:国家科技支撑计划子课题(2013BAI06B04Y06130)
通信作者:吴新安,男,副主任药师,研究方向:医院药学,E-mail:xinanw@21cn.com
doi:10.3969/j.issn.1009-6469.2016.06.062
(收稿日期:2016-03-07,修回日期:2016-04-20)
