不同氧化铝对铜基甲醇水蒸气重整制氢催化剂活性的影响
2016-07-11严会成李华波李文静许云波
严会成 李华波 李文静 许云波 刘 阳
(四川蜀泰化工科技有限公司,四川大英,629300)
不同氧化铝对铜基甲醇水蒸气重整制氢催化剂活性的影响
严会成李华波李文静许云波刘阳
(四川蜀泰化工科技有限公司,四川大英,629300)
摘要
关键词:氧化铝CuO-ZnO/Al2O3催化剂甲醇水蒸气重整制氢催化活性
甲醇具有价廉易得、能量密度高,碳含量低,以及运输和贮存方便等优势,被誉为是最有希望的高携能燃料;其转化制氢方式主要包括直接裂解、水蒸气重整和部分氧化重整三种,其中甲醇水蒸气重整制氢是这三种制氢方式中氢含量最高的反应。该技术具有原料易得、工艺流程短、设备简单、投资少、能耗低,制氢成本低等优点,上个世纪90年代以来,该技术在国内开始受到重视,并且得到深入研究、开发[1-5]。特别是近几年来,小型制氢装置需求加大,加之甲醇市场价格持续低迷,甲醇水蒸气重整制氢的技术得到快速推广。
目前,国内市场所使用的甲醇水蒸气重整制氢催化剂主要以铜基催化剂为主,其主要成分是CuO、ZnO和Al2O3,其中铜是催化剂的活性组分,ZnO是催化剂的主要助剂,两者之间的关系研究较多,而对于Al2O3的选择研究鲜有报道[5-7]。但就工业使用反馈结果来看,催化剂的活性发挥好坏及使用寿命长短等关键性能跟Al2O3的选择息息相关。源于此,本文选用不同方式得到含有不同形式Al2O3的铜基甲醇水蒸气重整制氢催化剂,通过模拟工业上列管反应器对甲醇水蒸气重整制氢性能进行评价,考察不同类型的Al2O3对催化活性的影响。
1实验部分
1.1实验原料及仪器
1.1.1实验原料
硝酸铜、硝酸锌,自制;氢氧化铝(拜耳法生产),市售;九水硝酸铝,市售;氢氧化铝(碳酸氢铵法生产),市售;氢氧化铝(拜耳烧结联合法生产),市售。
1.1.2主要仪器
1000 mL分液漏斗,天津玻璃仪器厂;10 L中和桶,自制;5 L布氏漏斗,天津玻璃仪器厂;101型电热鼓风干燥箱,北京中兴伟业仪器有限公司;箱式电阻炉,沈阳市节能电炉厂;ZP25-4压片机,宁波北仑药化机械厂;SC-200型气相色谱仪,重庆川仪分析仪器公司。
1.2催化剂制备
所有催化剂均采用共沉淀法制备。
1.2.1以氢氧化铝作为氧化铝原料催化剂的制备
将金属离子总浓度为2 mol/L的Cu(NO3)2、Zn(NO3)2混合溶液置于一个分液漏斗中,将0.5 mol/L的Na2CO3溶液置于另一个分液漏斗中,在不断搅拌下将两者并流滴加到中和桶中,控制中和过程的pH值为7~7.5,中和温度为70±2℃,沉淀结束后搅拌老化1 h;然后加入一定比例的氢氧化铝,继续搅拌老化30min,而后过滤,滤饼经多次洗涤、过滤,直至Na+含量低于0.01%。将洗涤合格的滤饼于120~150 ℃干燥4~8 h,干燥后的物料加适量水混合后碾料、造粒,最后将具有一定粒度的物料在400℃下焙烧3~5 h后,加适量石墨用压片机压制得到Cu-Zn-A1催化剂(催化剂尺寸为Φ5mm×5 mm的圆柱体)。通过改变加入不同生产方式的氢氧化铝,得到含有不同种类Al2O3的Cu-Zn-A1催化剂。
1.2.2加硝酸铝作为氧化铝来源催化剂的制备
将金属离子总浓度为2.5mol/L的Cu(NO3)2、Zn(NO3)2、Al(NO3)3.9H2O混合溶液置于一个分液漏斗中,将0.5 mol/L的Na2CO3溶液置于另一个分液漏斗中,在不断搅拌下将两者并流滴加到中和桶中,控制中和过程的pH值为7~7.5,中和温度为70±2 ℃,沉淀结束后搅拌老化1.5 h;而后过滤,滤饼经多次洗涤、过滤,直至Na+含量低于0.01%。将洗涤合格的滤饼于120~150℃干燥4~8 h,干燥后的物料加适量水混合后碾料、造粒,最后将具有一定粒度的物料在400℃下焙烧3~5 h后,加适量石墨用压片机压制得到Cu-Zn-A1催化剂(催化剂尺寸为Φ5mm×5 mm的圆柱体)。
为了方便记忆,我们将以拜耳法生产的氢氧化铝为原料制备的催化剂记为催化剂A;以拜耳烧结联合法生产的氢氧化铝为原料制备的催化剂记为催化剂B;以碳酸氢铵法生产的氢氧化铝为原料制备的催化剂记为催化剂C;以市售九水硝酸铝为原料制备的催化剂记为催化剂D。
1.3催化剂活性评价方法
甲醇水蒸气重整制氢催化剂活性评价在固定床连续流动反应装置中进行,反应器采用模拟工业列管的304不锈钢反应管(尺寸为Φ25 mm×3 mm×750 mm)。催化剂活性评价时,首先将紧密堆积的30 mL原粒度(Φ5mm×5mm)催化剂样品装入反应管的等温层,然后用N2吹扫反应管,紧接着改通入H2-N2混合气进行升温还原,还原完成后缓慢降低还原气流量,同时用计量泵将甲醇水混合溶液输入反应系统,等还原气完全关闭、反应稳定1 h后,在30min内逐渐将系统压力提升至反应要求压力。在此条件下稳定反应2 h后,经六通阀取样进气相色谱仪对干基气体进行在线分析。
甲醇转化率:
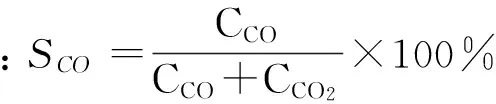
其中,FR为重整尾气流量(L/min),F为液体进料量(mL/min),ρmix为混合液密度(g/mL),α为混合液中甲醇质量含量,CCO、CCO2为尾气中CO、CO2含量,T1、P1为实际反应评价时的温度(K)和压力(kPa),T2、P2为标准状况下的温度(273.15K)和压力(101.325kPa)。
3结果与讨论
3.1不同种类氧化铝催化剂活性比较
设定反应温度为230 ℃,反应压力为1.20 MPa,原料液(甲醇与水的质量比为1∶1)的进料速率为30 mL/h;选用不同工艺生产的氢氧化铝及硝酸铝制得的含不同类型氧化铝的铜基甲醇制氢催化剂对甲醇水蒸气反应制备氢气的催化活性如表1所示。
(注:反应温度为230 ℃,反应压力为1.20 MPa,原料液(甲醇与水的质量比为1∶1)的进料速率为30 mL/h。)
在铜基催化剂存在条件下,甲醇与水蒸气重整制氢的主要反应方程式如下:
主反应:CH3OH=CO+2H2
CO+H2O=CO2+H2
总反应:CH3OH+H2O=CO2+3H2
由表1可以发现,4种不同类型的氧化铝对铜基甲醇制氢催化剂的甲醇转化率及出口转化气中CO选择性表现各异。总体来看,催化剂C、D的催化活性较好,这可能是由于在制备过程中,氧化铝的分散效果较好。具体来说,催化剂C所选用的原料氢氧化铝比重轻,在分散过程中分散好,使Cu晶粒分布均匀,不易聚集, 能充分发挥其催化活性,而催化剂A、B所使用的氢氧化铝比重较重,分散效果较差,易团聚,从而使还原后的Cu晶粒易团聚长大,催化中心减少,催化效果变差;对于催化剂D而言,虽然中和过程中看似较催化剂A、B、C的加料方式分散得更加均一,但是其比重仍然高,可能分散度仍不及催化剂C中分布均一,因而其催化效果仍不及催化剂C的效果理想。
3.2高温耐热后催化剂活性
耐热试验:反应压力控制为常压,原料混合液(甲醇与水的质量比为1∶1)的流速控制为30 mL/h,1 h内将反应温度从230 ℃升至400 ℃,并在400℃恒温4 h,紧接着在1.5 h内将反应温度从400 ℃降至230℃,然后升压至1.20 MPa,稳压2 h后,测定催化剂的催化活性,如表2所示。
(注: 400 ℃耐热4 h后,控制反应温度为230 ℃,反应压力为1.20 MPa,原料液(甲醇与水的质量比为1∶1)的进料速率为30 mL/h。)
表2中的测试结果表明,4种催化剂在400 ℃条件下耐热4 h后,催化剂的活性均有所变差,但是催化剂C的催化活性明显高于其它3种催化剂。另外,从表2中我们还可以发现,耐热后催化剂的活性出现衰减,对CO的选择性也同样减弱,这可能与甲醇水蒸气采用分步反应的原理有关,虽然催化剂的甲醇裂解效率变低,但是CO转化为CO2的选择性未受到影响,变换效率仍然较好。
3.3不同催化剂活性稳定性比较
反应压力控制为1.20 MPa,反应温度控制为230 ℃,原料混合液(甲醇与水的质量比为1∶1)的进料速率设定为30 mL/h,甲醇转化率随反应时间的变化如图2所示。
图2中曲线的变化趋势表明,催化剂C、D的活性稳定性较催化剂A、B好,但催化剂D相比催化剂C而言,活性稳定性又要略差。综合来看,催化剂C的活性稳定性是4种催化剂中稳定性最好的,完全能满足工业化使用需要。
3.4反应温度反复升降对催化活性影响
反应压力控制为1.20 MPa,原料混合液(甲醇与水的质量比为1∶1)的进料速度控制为30 mL/h,调整反温度从230 ℃升至280 ℃,升温速率控制为20 ℃/h,280℃稳定3 h,然后以20 ℃/h降温至230 ℃,230℃恒温3 h,如此反复5次,每次均在230 ℃条件下测定甲醇转化率,测试结果如图3所示。
根据图3曲线的走势,我们可以观察得到,催化剂C对温度的敏感程度较另外3种催化剂要低得多,这说明催化剂C使用温区更宽,能更好地应对生产装置中温度升降的突发情况。
4结论
(1)不同类型Al2O3所制备的CuO-ZnO/ Al2O3催化剂的催化活性、耐热后催化活性、活性稳定性表现不一。
(2)综合来看,选用碳酸氢铵法所制备的Al(OH)3作为制备CuO-ZnO/ Al2O3催化剂的原料,所制备CuO-ZnO/ Al2O3催化剂的催化性能最优,较适合于工业装置的稳定运行。
参考文献
[1]李永红, 任杰, 孙予罕. 低温高活性甲醇水蒸气重整制氢催化剂的研究[J]. 化工催化剂及甲醇技术, 2000, 5: 1-2.
[2] 秦建中, 张元东. 甲醇裂解制氢工艺与优势分析[J]. 玻璃, 2004, 176(5):28-32.
[3] 王锡波, 韩晓玲, 赵欣, 等. 甲醇裂解制氢技术应用[J]. 山东化工, 2013, 42(3):43-45.
[4] 严会成, 许云波, 李华波, 等. 铜基甲醇水蒸气重整制氢催化剂活性研究[J]. 山东化工, 2015, 44(15): 23-24.
[5] 张文斌, 梅华, 陈晓蓉,等. CuZnAl催化剂甲醇水蒸气重整制氢催化性能研究[J]. 石油炼制与化工,2013, 44(10): 22-26.
[6] 蔡迎春, 刘淑文, 徐贤伦, 等. La助剂对甲醇水蒸气转化制氢CuO-ZnO/Al2O3催化剂性能的影响[J]. 石油化工, 2001, 30 (6): 429-432.
[7] 张文斌, 梅华, 陈晓蓉, 等. CuZnAl催化剂甲醇水蒸气重整制氢催化性能研究[J]. 石油炼制与化工, 2013, 44(10): 22-26.
Effect of Different Alumina on Catalytic Activity of Methanol Steam Reforming Cu-based Catalysts
YanHuicheng,LiHuabo,LiWenjing,XuYunbo,LiuYang
(SichuanShutaiChemicalTechnologyCo.,Ltd.Daying629300,Sichuan,China)
Key words:alumina; CuO-ZnO/Al2O3catalysts; hydrogen production from methanol steam reforming; catalytic activity
Abstract:Simulating industrial tubular reactor, the effects of different types of Al2O3on the catalytic activity of CuO-ZnO/Al2O3catalysts were investigated. Experiment results indicated that catalytic activity, heat-resistant catalytic activity and catalytic activity stability of CuO-ZnO/Al2O3catalysts are better, that the raw material Al(OH)3was prepared by ammonium bicarbonate method. This kind of CuO-ZnO/Al2O3catalysts is more suitable for the stable operation of industrial device.
通过模拟工业列管反应装置,研究了不同类型Al2O3对CuO-ZnO/Al2O3催化剂活性的影响。对比试验结果表明:选用碳酸氢铵法生产的Al(OH)3所制备的CuO-ZnO/Al2O3催化剂,其催化活性、耐热后催化活性及活性稳定性均表现良好,较适合工业装置稳定运行。
