AC/X-G吸附剂的制备及CH4/N2吸附分离性能
2016-07-07张冬梅程文萍张明胜崔杏雨马静红李瑞丰太原理工大学化学化工学院山西太原03004太原理工大学精细化工研究所山西太原03004
张冬梅,程文萍,张明胜,崔杏雨,马静红,李瑞丰,(太原理工大学化学化工学院,山西 太原 03004;太原理工大学精细化工研究所,山西 太原 03004)
AC/X-G吸附剂的制备及CH4/N2吸附分离性能
张冬梅1,程文萍1,张明胜1,崔杏雨2,马静红2,李瑞丰1,2
(1太原理工大学化学化工学院,山西 太原 030024;2太原理工大学精细化工研究所,山西 太原 030024)
摘要:采用浓度为0.2 g·ml−1的葡萄糖溶液对13X沸石/活性炭复合材料(AC/X)进行碳沉积,研究沉积次数对复合吸附剂(AC/X-G)孔结构、表面性质和CH4/N2吸附分离性能的影响。通过X射线衍射,77 K下的N2吸附/脱附,扫描电镜,CO2-TPD以及红外光谱表征样品的晶型、孔结构和表面性质,在298 K、100 kPa下对其CH4和N2吸附等温线进行测定,并将吸附结果与文献中碳材料和13X沸石的吸附性能进行比较。结果表明:随着沉积次数的增加,AC/X-G吸附剂中X型沸石的相对含量降低,微孔比表面积和微孔体积减少。AC/X-G的表面被碳膜覆盖,碱量降低,但出现强碱位和含氧基团C—O键。AC/X-G的CH4和N2吸附量下降,但吸附分离系数提高,沉积3次的样品AC/X-G-3的CH4/N2吸附分离系数达到3.0,表面的含氧基团有利于提高复合材料的CH4/N2吸附分离性能。
关键词:吸附剂;葡萄糖;碳沉积;吸附;分离
2015-10-23收到初稿,2016-03-03收到修改稿。
联系人:程文萍。第一作者:张冬梅(1991—),女,硕士研究生。
Received date: 2015-10-03.
Foundation item: supported by the National Natural Science Foundation of China (51204120), the Natural Science Foundation of Shanxi Province (2014021014-1, 2012011005-6) and the Key Scientific and Technological Project of Coal Fund of Shanxi Province (FT201402-03).
引 言
甲烷作为洁净高效的能源和重要的化工原料,其分离提纯对于缓解能源危机和环境保护均具有积极意义。因CH4和N2的物理化学性质相近,使其分离提纯尤为困难[1]。目前用于CH4/N2分离提纯技术主要有膜分离法[2-4]、水合物法[5]、深冷法[6-7]、溶剂法[8]和变压吸附分离法[9],其中变压吸附分离法由于可操作性强而被广泛关注。变压吸附分离技术的核心是高性能吸附剂的制备,而影响吸附剂性能的关键是其孔结构[10]和表面性质[11-12]。
Baksh等[13]用Br2或ICl对活性炭表面进行单层沉积,沉积之后的复合吸附剂对CH4的吸附量不变而对N2的吸附量下降,CH4/N2平衡分离系数达到4。杨明莉[14]用十二烷基硫酸钠和正二十四烷为改性剂对活性炭进行了表面亲烃改性,提高了对CH4的吸附性能,在更大的压力范围内提高了活性炭对CH4/N2的分离效果,但是CH4和N2在活性炭上的吸附容量较低,影响了其吸附分离的效果。Ahmad 等[15]研究了苯沉积对棕榈壳碳分子筛吸附性能的影响,实验表明其对CO2/CH4和O2/N2的动力学选择性分别达到了16和7.06,提高了碳分子筛的吸附分离性能。另有研究者[16-17]用CH4作为沉积剂进行高温碳沉积制备出的碳分子筛可将混合气中N2的浓度提高至97.5%。李瑞丰等提出了13X沸石/活性炭复合材料的制备方法,该材料结合了13X沸石和活性炭两种材料的孔结构和表面性质[18],对CH4和N2的吸附容量较高,但是吸附平衡分离比较低,为2.0[19]。因此,本文将在13X沸石/活性炭复合材料的基础上,以葡萄糖作为沉积剂,对复合材料的孔结构和表面性质进行调节,以期获得适宜的孔结构和理想的表面性质,从而提高复合吸附剂对CH4/N2吸附分离性能。
1 实验部分
1.1样品制备
1.1.1复合材料的制备将煤矸石粉、沥青和白炭黑按一定比例混匀成型、烘干,在管式炉中氮气保护下,1123 K炭化2 h,再通入CO2,1123 K活化24 h。将活化后的样品置入一定浓度的NaOH溶液中,338 K凝胶12 h,室温老化12 h,363 K晶化24 h,洗涤、干燥制得沸石/活性炭复合材料[18],记为AC/X。
1.1.2沉积样品的制备取5 g AC/X加入0.2 g·ml−1葡萄糖溶液20 ml,室温搅拌2 h,洗涤过滤,然后在453 K下静置干燥固化2 h,再放入管式炉内,氮气保护下,823 K炭化2 h。依据沉积次数的不同,分别命名为AC/X-G-1、AC/X-G-2、AC/X-G-3 和AC/X-G-4。
1.2样品表征
采用日本岛津LabX XRD-6000型X射线衍射仪(XRD)对样品的晶型进行表征。CuKα为射线源(λ=0.15406 nm),石墨单色器,工作电压40 kV,管电流30 mA,扫描速率(2θ) 8(°)·min−1,扫描角度5°~35°,扫描步长0.01°。采用美国Quantachrome公司Quantachrome Quadrasorb SI型吸附仪测定样品的N2吸附-脱附等温线。经BET方程计算样品的比表面积(SBET),以p/p0=0.98时氮气的吸附量计算样品的总孔容,由t-plot方法计算样品的微孔比表面积(Smic)、外比表面积(Sext)和微孔体积(Vmic)。采用美国Quantachrome公司的NOVA1200e型吸附仪对样品在273 K时的CO2吸附等温线进行测定,由NLDFT模型获得样品的微孔孔分布以及<1 nm的微孔体积(V<1 nm)。采用日本岛津FT-IR型傅里叶变换红外分析仪分析样品的表面性质(样品与KBr的质量比为1:200)。采用日本S-4800型扫描电子显微镜对复合材料的形貌特征进行观测,并对碳沉积后材料进行表面成分分析。采用美国Micromeritics公司Chemsorb2720型全自动程序升温化学吸附仪,进行CO2-TPD测定。
1.3CH4和N2吸附量的测定
采用美国Quantachrome公司的NOVA1200e型吸附仪测定样品在298 K、100 kPa时CH4和N2的吸附等温线。
2 结果与讨论
2.1X射线衍射分析
由图1不同沉积次数样品的XRD谱图可知,所有样品在2θ为6.10°、10.00°、15.40°、20.05°、23.30°、26.60°、30.90°均出现了13X沸石的特征峰。并且随着沉积次数的增加,特征峰强度逐渐减弱,这表明随着沉积次数的增加,AC/X-G样品中活性炭的相对含量增多,X沸石的相对含量降低。

图1 样品XRD谱图Fig.1 XRD patterns of samples
2.2扫描电镜(SEM)
图2(a)、(b)是样品AC/X和AC/X-G-3的电镜图。从图(a)可以看出,复合材料AC/X中部分八面体X型沸石裸露在碳材料的外面,图2(b)中AC/X-G-3的X型沸石则被沉积的碳包裹,并且经EDS对材料表面进行成分分析,沸石13X表面C、O含量分别为37.7%、35.3%,这说明用葡萄糖溶液进行浸渍、沉积之后,在复合材料的表面形成了碳膜,将其中X型沸石完全包裹,并且随着沉积次数的增加,碳膜的量增大,也因此改变了复合吸附剂AC/X-G-3的孔结构和表面性质。

图2 AC/X和 AC/X-G-3的SEM图及AC/X-G-3的EDS分析Fig 2 SEM images of AC/X and AC/X-G-3, and EDS analysis of AC/X-G-3
2.3液氮吸附-脱附表征
图3中样品在77 K下N2吸附/脱附等温线,具有Ⅰ型和Ⅳ型吸附等温线的特征,并且在p/p0>0.8时,出现了明显突跃,表明复合材料中不仅含有大量微孔,而且存在一定量的介孔和大孔。从表1中样品的孔结构参数可以看出,随着沉积次数的增加,样品的BET比表面积、微孔比表面积和微孔体积依次下降,而外比表面积增加,相对含量升高。由273 K下CO2吸附等温线得到,微孔分布主要在0.45~0.55、0.55~0.70和0.70~1.0 nm3个区间,随着浸渍次数的增加,各区间范围内的孔体积均呈下降趋势,表明碳沉积对复合材料微孔调节效果明显。这一结果与电镜的结果一致,由于复合材料表面被碳膜覆盖,所以微孔表面积和微孔体积下降,外比表面积的相对含量增加。
2.4红外光谱表征
AC/X-G吸附剂中活性炭的表面具有很多种官能团,表面含氧基团的种类也会极大影响复合材料的吸附分离性能。从样品的红外谱图(图4)中发现,与AC/X相比,AC/X-G在878、1046和2970 cm−1处出现了特征吸收峰。其中,878 cm−1处为C—H 3键弯曲振动峰,1046 cm−1处为C—O的伸缩振动峰,2970 cm−1处为C—H键的伸缩振动峰。由此可见,复合吸附剂AC/X-G的表面含有C—H键和含氧官能团C—O键,由于C—O键具有较强极化作用,使其对极化率较大的气体分子表现出较强的吸附能力[20]。

图3 样品在77 K下N2吸附等温线及由273 K CO2吸附等温线得到的ACX、ACX-G(1~4)样品V<1 nm微孔孔容Fig.3 N2adsorption isotherms at 77 K on samples and V<1 nmmicropore volume of ACX and ACX-G(1—4) samples obtained from CO2adsorption isotherms at 273 K

表1 样品的孔结构参数Table 1 Pore structure parameters of samples

图4 样品的红外谱图Fig.4 Infrared spectra of samples
2.5CO2-TPD表征
图5为AC/X和AC/X-G-3的CO2-TPD曲线图,AC/X在67℃附近的脱附位为弱碱脱附位,在209℃附近的脱附位为中强碱脱附位;AC/X-G-3在58℃附近的脱附位为弱碱脱附位,在190℃附近的脱附位为中强碱位,而其在410℃附近的脱附位为强碱位,表明AC/X-G-3在葡萄糖沉积后,虽然碱量降低,但具有明显的强碱脱附位,而强碱位的增加有利于提高CH4/N2的分离[21]。

图5 AC/X和AC/X-G-3的CO2-TPD曲线Fig.5 CO2-TPD profiles of AC/X and AC/X-G-3
2.6CH4和N2吸附性能表征
从表2中可见,一次沉积的吸附剂AC/X-G-1的CH4和N2吸附量大幅度降低,这一方面是由于AC/X-G-1的BET比表面积、微孔比表面积和微孔体积均下降所致,另一方面是因为沉积样品表面碱量的降低所引起的。而2~4次沉积后的吸附剂对CH4的吸附量未发生显著变化,这表明虽然随着微孔参数和表面碱量的降低会引起CH4吸附量的降低,但是强碱位的增加有利于非极性分子的吸附[21]。尽管CH4和N2均为非极性分子,但是CH4的极化率大于N2,与吸附剂表面的C—O键产生较强的吸附作用,因此,CH4的吸附量稳定在11.8 cm3·g−1,而N2的吸附量则依次降低。
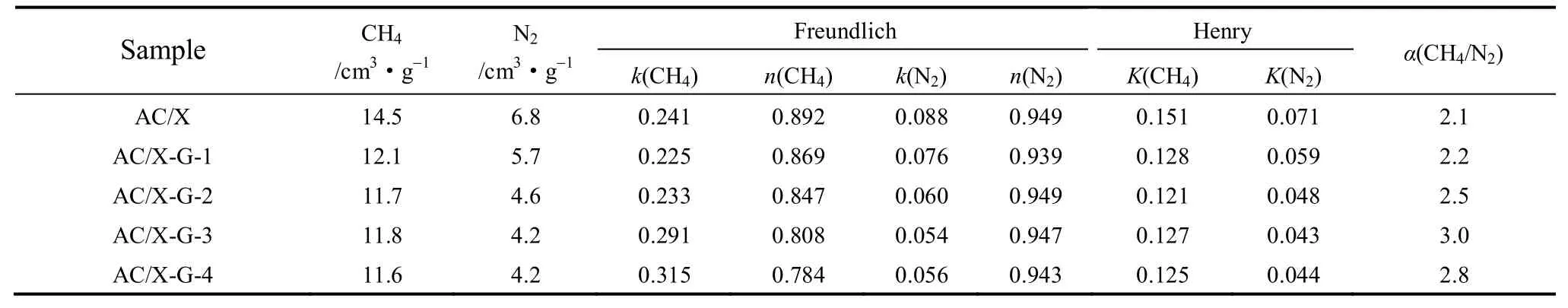
表2 N2和CH4在样品上的吸附参数Table 2 Adsorption parameters of N2and CH4on samples
由图6和表2可见,Freundlich吸附等温式(F式)比Henry(H式)更适于拟合298 K时CH4和N2在样品上的吸附等温线。在F式中,k值是与吸附剂的吸附能力相关的常数,n值在0~1之间,反映了吸附剂表面吸附位的多相性。由CH4的F式拟合结果可知,随着沉积次数的增加,k值增加,n值降低,这是因为AC/X-G吸附剂表面强碱位的增加使其CH4的吸附作用增强,同时导致吸附剂表面对于CH4吸附位的多相性增加。N2的n值很接近,k值降低,表明沉积之后复合材料表面对N2的吸附活性位均一性不变,但是吸附能力降低,这与AC/X-G微孔参数和表面碱量的降低有关。
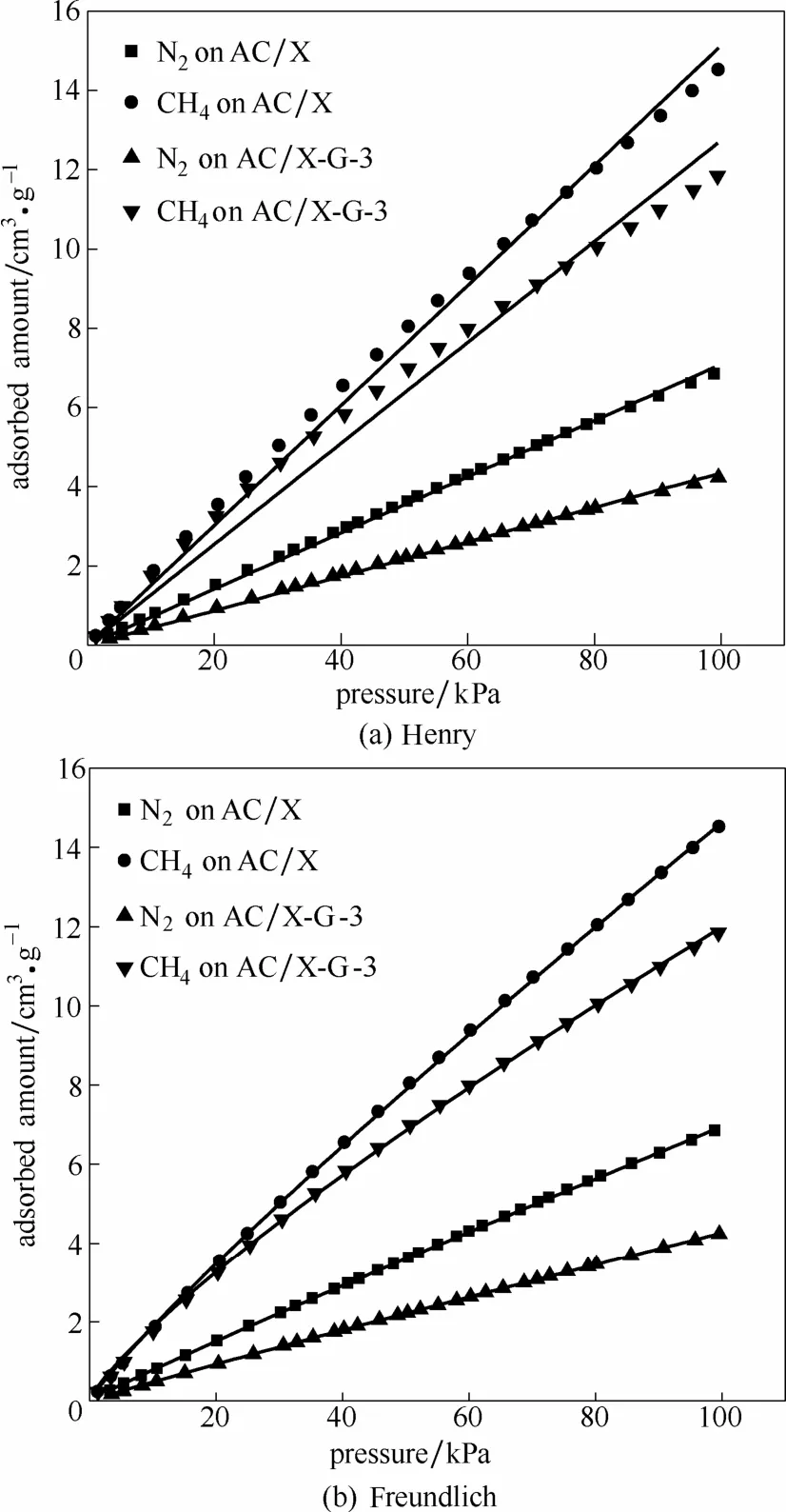
图6 298 K下AC/X和AC/X-G-3 CH4、N2吸附等温线的拟合Fig 6 Adsorption isotherms of N2and CH4on AC/X and AC/X-G-3 under 298 K
由亨利常数计算的CH4和N2平衡分离系数α(CH4/N2)(表2)可看出,AC/X-G-3的α (CH4/N2) 从AC/X的2.1增加到3.0,这也说明AC/X-G-3吸附剂对CH4和N2的吸附分离能力远高于AC-X,这是由于沉积样品表面的C—O键具有较强极化作用,对极化率较高的CH4吸附作用更强,有利于CH4和N2的吸附分离。
2.7吸附剂的性能比较
表3为文献报道的不同活性炭吸附剂、13X沸石和本文制备的AC/X-G-3吸附剂对于CH4和N2吸附性能的比较。由表可见,Anderson AX-21和Carbon(G2X7/12)两种活性炭吸附剂都表现出较高的CH4和N2平衡吸附量及分离比,与之相比,AC/X-G-3吸附剂具有较高的平衡分离比,而平衡吸附量偏低。但是AC/X-G-3与文献中的13X沸石、Carbon(PVDC)及Carbon(FFAD)吸附剂相比,CH4和N2平衡吸附量接近,而平衡分离比却有较大提高;与Carbon(CMS-2)和Vulcan carbon吸附剂相比,CH4和N2的平衡分离比接近,但是平衡吸附量大大提高。相比之下,AC/X-G-3不仅具有较高的平衡吸附量,而且平衡分离比达到3.0,能够满足变压吸附分离甲烷和氮气对于吸附剂的要求。
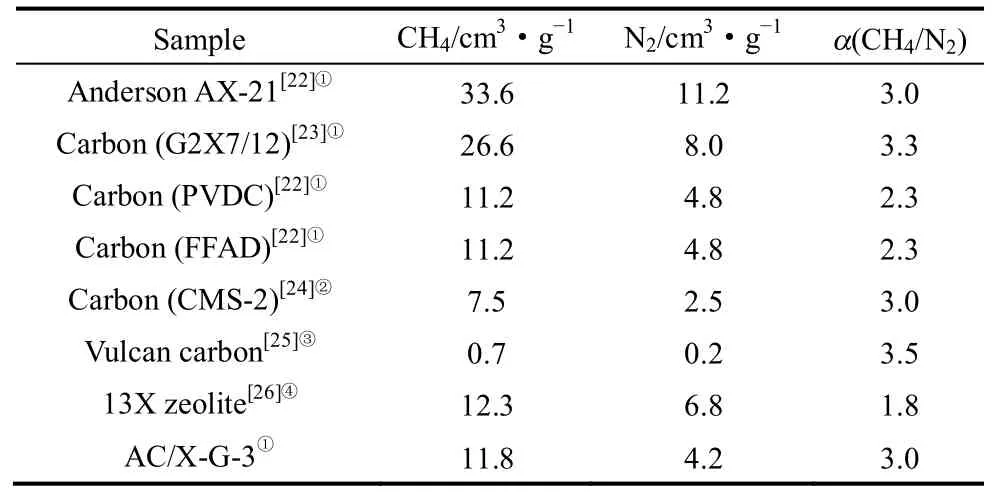
表3 各种吸附剂的CH4和N2的吸附性能Table 3 Adsorption abilities of various adsorbents for CH4and N2
3 结 论
随着沉积次数的增加,AC/X-G吸附剂中X型沸石表面沉积碳膜的量增大,导致BET比表面积、微孔比表面积和微孔体积减小,表面碱量降低,但是AC/X-G吸附剂表面出现强碱位,并且存在极化作用强的C—O键。AC/X-G吸附剂的孔结构和表面性质的变化,对CH4和N2的吸附量影响较大,由于吸附剂表面C—O键较强的极化作用,使AC/X-G-3对CH4和N2的平衡分离系数增加至3.0,有望应用于变压吸附装置,实现低浓度甲烷的分离提纯。
References
[1]YANG H W, YIN C B, JIANG B, et al. Optimization and analysis of a VPSA process for N2/CH4separation [J]. Separation and Purification Technology, 2014, 134: 232-240.
[2]LOKHANDWALA K A, PINNAU I, HE Z J, et al. Membrane separation of nitrogen from natural gas: a case study from membrane synthesis to commercial deployment [J]. Journal of Membrane Science, 2010, 346(2): 270-279.
[3]BUONOMENNA M G, GOLEMME G, TONE C M, et al. Nanostructured poly(styrene-b-butadiene-b-styrene) (SBS) membranes for the separation of nitrogen from natural gas [J]. Advanced Functional Materials, 2012, 22(8): 1759-1767.
[4]阮雪华, 贺高红, 肖武, 等. 生物甲烷膜分离提纯系统的设计与优化[J]. 化工学报, 2014, 65(5): 1688-1695. RUAN X H, HE G H, XIAO W, et al. Design and optimization of membrane-based system for bio-methane purification [J]. CIESC Journal, 2014, 65(5): 1688-1695.
[5]ZHONG D L, LU Y Y, SUN D J, et al. Performance evaluation of methane separation from coal mine gas by gas hydrate formation in a stirred reactor and in a fixed bed of silica sand [J]. Fuel, 2015, 143: 568-594.
[6]范庆虎, 李红艳, 尹全森, 等. 低浓度煤层气液化技术及其应用[J].天然气工业, 2008, 28(3): 117-120. FAN Q H, LI H Y, YIN Q S, et al. Liquefaction technology on low-concentration CBM and its application [J]. Natur. Gas Ind., 2008, 28(3): 117-120.
[7]BRIAN R S. Process for removing nitrogen from natural gas: US 4352685 [P]. 1982-10-05.
[8]FRIESEN D T, BABCOCK W C, EDLUND D J, et al. Liquid of absorbent solutions for separating nitrogen from natural gas: US 6136222 [P]. 2000-10-24.
[9]WARMUZIŃSKI K, SODZAWICZNY W. Effect of adsorption pressure on methane purity during PSA separations of CH4/N2mixtures [J]. Chemical Engineering and Processing, 1999, 38: 55-60.
[10]GU M, ZHANG B, QI Z D, et al. Effects of pore structure of granular activated carbons on CH4enrichment from CH4/N2by vacuum pressure swing adsorption [J]. Separation and Purification Technology, 2015, 146: 213-218.
[11]MAROTO-VALER M M, ZHANG Y Z, GRANITE E J, et al. Effect of porous structure and surface functionality on the mercury capacity of a fly ash carbon and its activated sample [J]. Fuel, 2005, 84(1): 105-108.
[12]刘立恒, 辜敏, 鲜学福. 孔结构和表面化学性质对活性炭吸附性能的影响[J]. 环境工程学报, 2012, 6(4): 1299-1304. LIU L H, GU M, XIAN X F. Effect of pore structure and surface chemical properties on adsorption properties of activated carbons [J]. Chinese Journal of Environmental Engineering, 2012, 6(4): 1299-1304.
[13]BAKSH M S A, YANG R T, CHUNG D D L. Composite sorbents by chemical vapor deposition on activated carbon [J]. Carbon, 1989, 27(6): 931-934.
[14]杨明莉. 煤层甲烷变压吸附浓缩的研究[D]. 重庆: 重庆大学, 2004. YANG M L. Study on concentration of methane in coal bed by pressure swing adsorption [D]. Chongqing: Chongqing University, 2004.
[15]WAN DAUDA W M A, AHMAD M A, AROUA M K. Carbon molecular sieves from palm shell: effect of the benzene deposition times on gas separation properties [J]. Separation and Purification Technology, 2007, 57: 289-293.
[16]张香兰, 周玮, 张英, 等. 甲烷沉积法对甲烷/氮气分离炭分子筛性能的研究[J]. 化学工业与工程, 2011, 28(5): 20-25. ZHANG X L, ZHOU W, ZHANG Y, et al. Effect of CH4sedimentary conditions on performance of carbon molecular sieve in methane/nitrogen separation process [J]. Chemical Industry and Engineering, 2011, 28(5): 20-25.
[17]VILLAR-RODIL S, NAVARRETE R, DENOYEL R, et al. Carbon molecular sieve cloths prepared by chemical vapour deposition of methane for separation of gas mixtures [J]. Microporous and Mesoporous Materials, 2005, 77(2): 109-118.
[18]LI Z L, CUI X Y, MA J H, et al. Preparation of granular X-type zeolite/activated carbon composite from elutrilithe by adding pitchand solid SiO2[J]. Materials Chemistry and Physics, 2014, 147(3): 1003-1008.
[19]薛彩龙, 程文萍, 崔杏雨, 等. X沸石/活性炭孔结构对CH4/N2分离的影响[J]. 煤炭转化, 2015, 38(3): 92-96. XUE C L, CHENG W P, CUI X Y, et al. Effect of pore structure of zeolite X/ activated carbon composite on CH4/N2separation [J]. Coal Conversion, 2015, 38(3): 92-96.
[20]张薄, 辜敏, 鲜学福. 碳分子筛的结构和表面性质对其吸附分离CH4/N2和CO2/N2的影响[J]. 功能材料, 2012, 43(20): 2858-2862. ZHANG B, GU M, XIAN X F. Effects of structure and surface property on adsorptive separation of carbon molecular sieve for CH4/N2and CO2/N2[J]. Functional Materials, 2012, 20(43): 2858-2862.
[21]刘立恒, 辜敏, 鲜学福, 等. 黏结剂对颗粒活性炭 PSA 分离CH4/N2性能的影响[J]. 材料研究学报, 2011, 25(3): 249-254. LIU L H, GU M, XIAN X F, et al. Effect of binders on CH4/N2performances of granular activated carbons by pressure swing adsorption [J]. Chinese Journal of Materials Research, 2011, 25(3): 249-254.
[22]QUINN D F. Supercritical adsorption of ‘permanent’ gases under corresponding states on various carbons [J]. Carbon, 2002, 40(15): 2767-2773.
[23]OLAJOSSY A, GAWDZIK A, BUDNER Z, et al. Methane separation from coal mine methane gas by vacuum pressure swing adsorption [J]. Chemical Engineering Research and Design, 2003, 81(4): 474-482.
[24]张进华, 车永芳, 李兰廷, 等. 煤基碳分子筛的制备及CH4/N2分离性能研究[J]. 洁净煤技术, 2011, 17(2): 64-67. ZHANG J H, CHE Y F, LI L T, et al. Preparation of coal-based carbon molecular sieve and its application effects in CH4/N2separation [J]. Clean Coal Technology, 2011, 17(2): 64-67.
[25]KLUSON P, SCAIFE S, QUIRKE N. The design of microporous graphitic adsorbents for selective separation of gases [J]. Separation and Purification Technology, 2000, 20(1): 15-24.
[26]MOFARAHI M, BAKHTYARI A. Experimental investigation and thermodynamic modeling of CH4/N2adsorption on zeolite 13X [J]. Journal of Chemical & Engineering Data, 2015, 60(3): 683-696.
Preparation of AC/X-G adsorbent and CH4/N2adsorption separation performance
ZHANG Dongmei1, CHENG Wenping1, ZHANG Mingsheng1, CUI Xingyu2, MA Jinghong2, LI Ruifeng1,2
(1College of Chemistry and Chemical Engineering, Taiyuan University of Technology, Taiyuan 030024, Shanxi, China;2Institute of Special Chemicals, Taiyuan University of Technology, Taiyuan 030024, Shanxi, China)
Abstract:The 13X/activated carbon composite was treated by 0.2 g·ml−1glucose solution for carbon deposition. The effect of deposition times on the pore structure, surface properties and separation performance of CH4/N2were studied. The crystalline, pore structure and surface properties of the samples were investigated by X-ray diffraction (XRD), N2adsorption-desorption isotherms at 77 K, scanning electron microscopy (SEM), CO2-TPD and Fourier transform infrared spectrum (FT-IR). The adsorption isotherms of CH4and N2were tested at 298 K and 100 kPa,and compared with the adsorption separation properties of carbon materials and 13X zeolite reported in the literatures. The experimental results showed that the relative content of X zeolite, the micropore surface area and the micropore volume of AC/X-G were gradually decreased with the increase of deposition times. The surface of samples was covered by carbon membrane, which led to decrease of the alkaline functional groups but increase of containing C—O groups. The adsorption capacities of CH4and N2decreased, while the adsorption separation coefficient was improved. After third deposition, the adsorption separation coefficient of CH4/N2reached 3.0. The oxygen-containing functional groups on the surface of AC/X-G were beneficial to improve the separationperformance of CH4/N2.
Key words:adsorbent; glucose; carbon deposition; adsorption; separation
中图分类号:TQ 424
文献标志码:A
文章编号:0438—1157(2016)06—2386—07
DOI:10.11949/j.issn.0438-1157.20151606
基金项目:国家自然科学基金项目(51204120);山西省青年科技研究基金项目(2014021014-1);山西省自然科学基金项目(2012011005-6);山西省煤基重点科技攻关项目(FT201402-03)。
Corresponding author:CHENG Wenping, chengwenping@tyut.edu.cn
