炭负载金催化剂在乙炔氢氯化反应中的研究进展
2016-06-29杨雪超蓝国钧浙江工业大学工业催化研究所浙江杭州310014
杨雪超,蓝国钧,李 健,王 言,李 瑛(浙江工业大学工业催化研究所,浙江杭州310014)
炭负载金催化剂在乙炔氢氯化反应中的研究进展
杨雪超,蓝国钧,李健,王言,李瑛
(浙江工业大学工业催化研究所,浙江杭州310014)
摘要:从载体修饰、助剂添加、制备方法和催化剂的失活与再生等方面对乙炔氢氯化炭负载金催化剂的研究现状进行了综述,分析了炭载金催化剂产业化存在的问题,展望了金催化剂在乙炔氢氯化反应中应用的前景,为新一代乙炔氢氯化反应无汞催化剂的开发提供参考。
关键词:乙炔氢氯化;金催化剂;炭载体;无汞催化剂
聚氯乙烯(PVC)是世界第二大通用性合成树脂,具有优异的物理、化学和机械性能,在工业、建筑、农业、包装、电力等行业中有着广泛的用途,是以塑代钢,以塑代木的重要有机材料。中国的PVC行业飞速发展,依照国内“富煤、贫油、少气”的能源特点,相比源于石油化工路线的乙烯法,煤化工路线的乙炔法制备氯乙烯的工艺有着一定的能源及成本优势[1]。工业上,乙炔法合成氯乙烯所用催化剂是活性炭负载氯化汞催化剂。随着国内外汞污染防控政策的步步紧逼和国内汞资源的日渐枯竭,电石法PVC行业面临着严峻考验。
1968年,Smith[2]等研究了金属氯化物负载在SiO2上用于乙炔氢氯化反应催化性能,提出催化剂的活性和金属阳离子的电子亲和能有关联。1975年,在相同的反应条件下,Shinoda[3]系统地考察了30多种单金属氯化物负载在活性炭上催化乙炔氢氯化反应活性,对不同催化体系中乙炔转化率的数据进行统计,提出乙炔转化率与金属阳离子的电子亲能有关。在此基础上Hutchings[4]进一步关联了单金属氯化物的标准电极电势与乙炔的转化率的关系,根据Hutchings的假设,标准电极电势比汞离子高的金属阳离子,其催化乙炔氢氯化反应活性较高。根据这个原则,Hutchings预测了金催化剂应该具有较好的乙炔氢氯化反应性能。1988年,Hutchings等通过实验证实了金催化剂的乙炔氢氯化反应活性[5]。同时,金催化剂在选择氧化、加氢及诸多其他反应中[6]的催化应用也获得了飞速的发展,现在已经成为了催化领域的一个研究热点。
国家工信部于2010年6月4日发布的《电石法聚氯乙烯行业汞污染综合防治方案》,要求全行业在2015年全面采用低汞催化剂,到2020年催化剂向无汞催化剂转化,因此无汞催化剂的研发迫在眉睫。炭负载金催化剂在所有无汞催化剂体系中活性最高,是最有可能率先实现产业化应用[7,8]。最近几年,国内外对乙炔氢氯化反应金催化剂的研究报道及专利申请数日趋增多,本文将从炭负载金催化剂的载体的修饰、助剂的添加、制备方法和催化剂的失活与再生等几个方面对乙炔氢氯化反应金催化剂进行综述。
1 负载金催化剂载体炭的研究
载体不仅对活性组分起到支撑和分散作用,而且往往会与活性组分发生相互作用。由于乙炔氢氯化反应体系中涉及到HCl原料,而且活性组分大多为金属氯化物,因此对载体具有一定的抗腐蚀性的要求。炭材料具有孔隙率高,抗腐蚀性和成本低廉等特点,是乙炔氢氯化反应催化剂优选的载体。目前选用的炭载体主要有活性炭、纳米炭管、高比表面石墨、C3N4等。可以通过对载体炭的改性,提高载体和金之间的相互作用,增加对反应物的吸附,来提高催化剂的性能。载体炭的改性方法主要有以下几种。
1.1氮改性炭载体
石河子大学的代斌[9]课题组用聚吡咯改性多壁碳纳米管负载的金催化剂,其表面氮物种的存在有助于提高催化剂的活性和稳定性。原因是氮物种与Au3+的相互作用有助于提高金颗粒的分散度以及活性相组分的稳定,并且氮物种与Au3+之间的电子传输作用提高了吸附氯化氢的能力。该课题组还研究了B和N改性的石墨烯[10]和氮改性的沥青基球形活性炭[11],通过DFT计算,改性过的催化剂都可以增强对HCl的吸附。该课题组又研究了氮改性的介孔炭[12]负载AuCl3催化剂催化乙炔氢氯化反应,与未经过氮改性的活性炭制备的Au/AC催化剂相比,乙炔氢氯化的初活性提高了53.7%。以氮改性的介孔炭作为载体的催化剂金的平均粒径只有4.9 nm,在载体表面单层分散,而Au/AC催化剂的金的粒径达到16.4 nm。马宁[13]等制备了一系列不同氮改性的介孔炭及Au/OMC催化剂,以三聚氰胺改性的Au/MOMC催化剂性能比未经改性的催化剂要好,Au/MOMC在反应24 h后,乙炔的转化率达到89%,比未改性的介孔炭负载的金催化剂转化率提高了30%。
浙江工业大学的赵佳[14]等研究了掺氮活性炭负载AuCl3催化剂,在乙炔空速为100 h-1,反应300 h以后,乙炔的转化率仍然可以达到99.9%。以尿素为氮源引入的氮原子更能有效的锚定活性组分Au3+并抑制Au3+还原为AuO,同时,Au-N之间的电子传输和相互作用还能提高催化剂吸附氯化氢的能力,使活性相更加稳定。
氮改性的介孔炭不仅可以加强和活性组分金的相互作用,而且本身也具有乙炔氢氯化反应活性。代斌[15]等报道了活性炭负载g-C3N4催化乙炔氢氯化反应。推测g-C3N4催化乙炔氢氯化反应的活性中心是吡啶氮位。包信和[16]等在SiC基底表面制备了一层掺氮无定型碳并将其作为直接催化乙炔氢氯化反应的催化剂,通过XPS表征得到不同氮物种的含量并与催化性能进行关联,他们推测活性中心是吡咯氮,并用密度泛函理论证明了这一点。
1.2磷改性活性炭
李伟[17]课题组以三苯基膦为磷源对活性炭进行磷修饰后制备了AuCl3催化剂,发现活性炭上的PO-3和PO3-4可以提高活性组分Au3+和Au+的分散以及抑制Au3+和Au+的还原,同时还可以抑制催化剂积炭。所制备催化剂在23 h内乙炔的转化率达到99.9%,氯乙烯的选择性为100%。
1.3氧化物修饰活性炭
石河子大学的代斌[18]课题组用TiO2修饰活性炭载体负载金催化剂应用于乙炔氢氯化反应的研究,TiO2的加入显著提高了催化剂的稳定性,由于TiO2和Au3+之间的相互作用,使得活性相Au3+周围的电子密度增加,加强了对反应物HCl的吸附,抑制了Au3+还原为AuO。张金利[19]等则研究了CeO2修饰的活性炭作为载体负载金催化剂,CeO2的加入使金高度分散,并且增强了催化剂对反应物的吸附能力,抑制了Au3+的还原和催化剂表面积炭。
浙江大学的田晓辉[20]用正硅酸乙酯为硅源在活性炭的表面覆盖了一层SiO2球状颗粒,然后采用浸渍法制备了AuCl3/SiO2-AC,发现SiO2提高了Au3+的分散度和热稳定性。
1.4炭载体的扩孔
韩伟杰[21]对市售的球形活性炭浸渍硝酸铁进行CO2二次活化进行扩孔,改性后的样品增加了对乙炔的吸附速率和吸附量,使得球形活性炭催化乙炔氢氯化反应比市售的活性炭转化率提高了1倍。
1.5其他炭材料
杨晓丹[22]等用活性炭预涂覆在SiC泡沫上为载体负载金催化剂应用于乙炔氢氯化反应,显现出较高的稳定性。他们认为该载体使金均匀分散,并且SiC泡沫具有较好的热传导性能,其孔状结构也降低了反应床层的压降,从而提高了催化剂的稳定性。
综上所述,炭载体改性后,从以下几个方面影响催化体系:(1)锚定活性组分,在成核过程中影响金属颗粒的沉积和成长,提高纳米颗粒的分散度;(2)载体本身作为活性位点,部分参与乙炔氢氯化反应;(3)修饰催化剂中纳米颗粒的电子结构,提高催化剂的性能;(4)提高金属-载体之间化学键的强度,增强催化剂的稳定性。
2 炭负载金催化剂的助剂
2.1双贵金属催化剂
Hutchings[23]等制备了活性炭负载的Au-M双金属催化剂(M=Pd、Ir、Pt、Rh、Ru),详细考察了其催化乙炔氢氯化反应的性能。Au-Pd催化剂中的Au和Pd能形成固溶体,微量Pd的加入能提高Au催化剂的初活性,但随着Pd含量的增加,活性会逐渐降低,Au-Pt的性质与Au-Pd的性质相似。而Au-Ir催化剂与Au-Rh催化剂在选择性基本不变的条件下有较高的初活性。Hutchings认为其他金属和AuCl3混合形成合金的标准电极电势都会随着其他金属的含量增加呈线性下降的趋势,从而导致催化剂的活性下降。
2.2碱金属及碱土金属助剂
王声洁[24]等研究发现以AuCl3为活性相,KCl为助剂制备Au-K/C催化剂分散度高,在乙炔空速为120 h-1,反应温度在170℃,原料配比n(C2H2)/ n(HCl)= 1∶1.1的评价条件下乙炔转化率大于96%,氯乙烯的选择性大于99.5%,并且在120 h的评价时间内催化剂没有明显的失活现象。
张金利[25,26]等先后研究了双金属Au-Ba、Au-Sr催化剂,Ba和Sr的加入均可以提高Au的分散度,抑制催化剂表面积炭,同时也增强了对反应物HCl、C2H2的吸附能力。Au-Sr催化剂比单金属Au/C的反应活性提高了24.3%。
浙江工业大学的赵佳[27-29]研究了助剂In和Cu 对Au-Cs催化剂的影响,In和Au之间的电子传输增加了Au3+周围的电子密度,强化了对HCl的吸附,而Cu的加入提高了Au的分散,稳定了活性相Au3+,并且使C2H2更容易脱附,因此提高了催化剂的稳定性。
2.3过渡金属助剂
张金利[30,31]等在总结了金催化剂催化乙炔氢氯化反应中表现出来的催化特征的基础上,提出根据助剂的电极电势优化AuCl3催化剂催化性能。经过比较发现电极电势有如下规律:Co3+>Au3+>Pd2+>Hg2+>Cu2+>Co2+>La3+,由于Co3+的标准电极电势高于Au3+以及Co3+比Au3+有更强的氯化氢吸附能力,因此加入助剂Co在制备催化剂过程中稳定活性物种Au3+,抑制积炭和催化剂烧结。在后续的研究中,又考察了添加Co(III)和Cu(II)双助剂,以球形活性炭为载体,制备了Au-Co(III)-Cu(II)三元催化剂。双助剂的加入,增强了对氯化氢的吸附能力,增加了活性组分Au3+和Au+的数目。催化剂在反应6 513 h后,乙炔的转化率还能达到99.7%,氯乙烯的选择性达到99.9%。他们还研究了助剂Ni[32]对乙炔氢氯化反应的影响。催化剂在乙炔空速为900 h-1,反应46 h后,转化率达到95.4%,Ni助剂的加入抑制了Au3+还原为AuO,并且在催化剂制备过程中,还能把AuO氧化为Au+,提高金的分散度,在乙炔氢氯化反应过程中有效抑制了催化剂表面的积炭,从而提高了催化剂的活性和稳定性。2015年又研究了Sn[33]助剂对金催化剂性能的影响,Sn的加入可以使Au均匀分散,提高对反应物的吸附和产物的脱附能力,降低催化剂表面积炭。
王声洁等[24]还报道了以CuCl2为助剂制备的AuCl3-CuCl2/C[34]催化剂,比负载AuCl3的催化剂的稳定性有显著的提高,CuCl2的加入可以稳定活性价态Au3+从而提高了催化剂的稳定性。
魏飞[35]等采用BiCl3作为金催化剂的助剂制备Au-Bi催化剂,加入Bi后Au主要以AuCl的形式存在,由于Au+的标准电极电势要高于Au3+,所以Au-Bi催化剂的活性提高。
2.4Au-稀土金属体系
代斌[36]等研究LaCl3助剂的影响,La助剂的加入在保持催化剂选择性不变的情况下提高AuCl3催化剂的反应活性和稳定性,催化剂稳定性的提高时因为助剂LaCl3的加入能显著的抑制催化剂表面积炭以及Au3+还原为AuO。
与Hutchings添加贵金属制备双金属催化剂调变金的标准电极电势的设计初衷不同,添加非贵金属催化剂主要是希望助剂的加入能提高金的分散度、稳定活性相的化学价态、增强活性中心的电子密度、抑制催化剂表面积炭和降低催化剂的成本等。
3 炭负载金催化剂的制备方法
炭负载的金属或者金属氯化物催化剂,浸渍法是一种最常用的方法,由于炭载体的比表面积高、吸附能力强,可以选择性的从水溶液中将活性组分吸附到表面,制备的催化剂具有分散度高、活性好等优点。
3.1浸渍法
石河子大学的王琴琴[37]采用等体积浸渍法,以盐酸为溶剂,制备出不同配比、不同价态的Au催化剂,在反应条件为C2H2空速360 h-1、温度130℃、n(C2H2)/n(HCl)=1.15∶1时,AuCl/AC活性较低,且失活较快。当加入第二组分AuCl3或AuO后,随着加入量的增加,催化活性和稳定性得到明显提高,并且当n(C2H2)/n(HCl)=2∶1时,催化剂的活性和稳定性最好。
Marco Conte[38]考察了不同溶剂(王水、盐酸、硝酸)对负载型AuCl3性能的影响,研究了硝酸和盐酸的体积比以及干燥过程中温度对催化剂性能的影响,使用王水作为溶剂可以提高活性相的含量和分散度,同时也会对活性炭表面的化学基团产生影响,进而影响催化剂的性能。
浙江大学的田晓辉[39]运用一种混合溶剂加真空干燥的方法制备AuO/C催化剂,用水和乙醇作为溶剂,活性炭为载体,在-95 kPa,60℃条件下浸渍6 h,然后在140℃条件下干燥12 h制备出AuO/C催化剂。和传统浸渍法制备的催化剂相比,所制备的AuO/C催化剂的活性是后者的2倍,提出AuO是初始反应的活性相,采用这种方法所制备的Au纳米粒子的粒径比浸渍法要小的多。
3.2络合物辅助浸渍法
朱明远等[40]研究了加入1,10-邻菲罗啉助剂对金催化剂性能的影响,所制备的催化剂[AuCl2(phen)]Cl具有较高的稳定性,反应40 h以后,乙炔的转化率还可以达到90%以上。通过比较HAuCl4和[AuCl2(phen)]Cl线性电位扫描伏安图,发现[AuCl2(phen)]Cl的还原峰有明显的正迁移,催化剂具有高的稳定性的原因是所加入的1,10-邻菲罗啉助剂与HAuCl4形成配合物,抑制Au3+在反应过程中的还原。
魏飞[41]等研究了添加KSCN助剂对金催化剂性能的影响。低含量的金催化剂(质量分数0.25%)与-SCN形成络合物,把Au3+的电极电势从0.926 V降到0.662 V,因此降低反应过程中活性组分Au3+被还原的可能性,反应3 000 h以后,乙炔的转化率仍大于95%,氯乙烯的选择性大于99%。
华东理工大学的王声洁[42]以乙二胺为配体先合成Au(en)2Cl3,后以KCl为助剂,将Au(en)2Cl3浸渍到活性炭上,载Au催化剂Au-K/ACS具有较高分散度,平均粒径为2.3nm,在温度180℃、空速240h-1、n(C2H2)/n(HCl)= 1.1∶1时,乙炔氢氯化反应的转化率可达98%以上,氯乙烯选择性不低于99.5%。
赵佳[43]等用[Prmim]Cl为离子液体制备[Prmim]AuCl4配合物,负载在活性炭上用于乙炔氢氯化反应,催化剂表现出较高的活性和稳定性。在反应温度为180℃,乙炔空速为30 h-1的条件下,反应300 h,乙炔的转化率只下降了3.7%。
3.3超声,微波辅助浸渍法
Wittanadecha等[44]利用浸渍法、超声波和微波辅助法制备金催化剂并研究其在乙炔氢氯化反应中性能。用浸渍法和超声波辅助法制备的催化剂比微波辅助法有较高的初活性,在乙炔空速GHSV=1 480 h-1,催化剂反应20 h后,超声波辅助法制备的催化剂依然有较高的活性和稳定性,乙炔转化率仍可达80%。这是因为超声波辅助的方法提高了活性组分Au3+的分散度并且增大了载体的孔容和孔径。
负载型金催化剂的制备方法有多种,催化剂的性能在很大程度上依赖于金颗粒的粒径大小及其分散度(粒径效应)和载体效应,当活性组分的几何结构和电子结构与反应物的几何结构和电子结构相适应时,催化剂才能呈现最大的活性。所以通过调控金属晶粒大小来改变反应物电子结构和金属的电子结构的适应性,可以提高金属催化剂的催化活性。
对金催化剂而言,其产业化存在的主要问题是高成本和催化剂的使用寿命。要实现工业化应用,主要有2个方面的问题需要解决:一方面,要降低金的负载量(降到0.25%以下才有竞争优势),这需要从催化剂的配方上进行优化;另一方面,要提高金催化剂的稳定性。金催化剂的稳定性较差是制约其工业化应用的主要瓶颈,所以研究负载型金催化剂的再生是很有必要的。应更加深入地探究金催化剂的失活机理,从微观结构的变化来解释它的失活过程,从本质上研究其再生方法,以使负载型金催化剂能够重复利用,降低其应用成本。下面对金催化剂的失活与再生进行综述。
4 金催化剂的失活与再生
4.1金催化剂的失活机理
1988年Hutchings[2]等对比研究了金催化剂和汞催化剂失活的不同,对使用后的催化剂原位用HCl处理6 h,HgCl2催化剂不能再生,通过分析反应后的催化剂的汞含量,有25%的汞流失。然而通过HCl处理的金催化剂的活性可以恢复到初始活性,分析反应后的金催化剂,其金含量并没有减少,见图1。
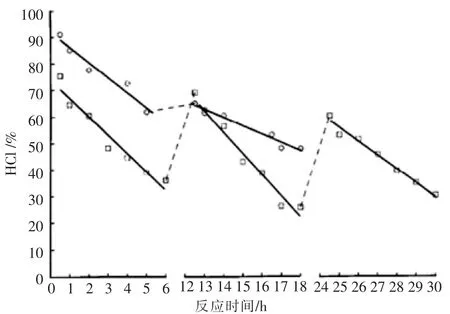
图1 HgCl2/C和HAuCl4/C催化剂在相同HCl条件处理后的活性对比
负载型AuCl3催化剂失活可归因于以下几个方面:AuCl3活性相的还原、聚集和催化剂表面积炭等原因,这几种失活过程可能同时发生。Nkosi[45]等在1991年研究了金催化剂在乙炔氢氯化反应中的失活机理,提出在高温区(120~180℃)进行反应时,活性组分被还原是主要的失活原因,而反应在低温区(60~100℃),催化剂表面积炭是主要的失活原因,见图2。
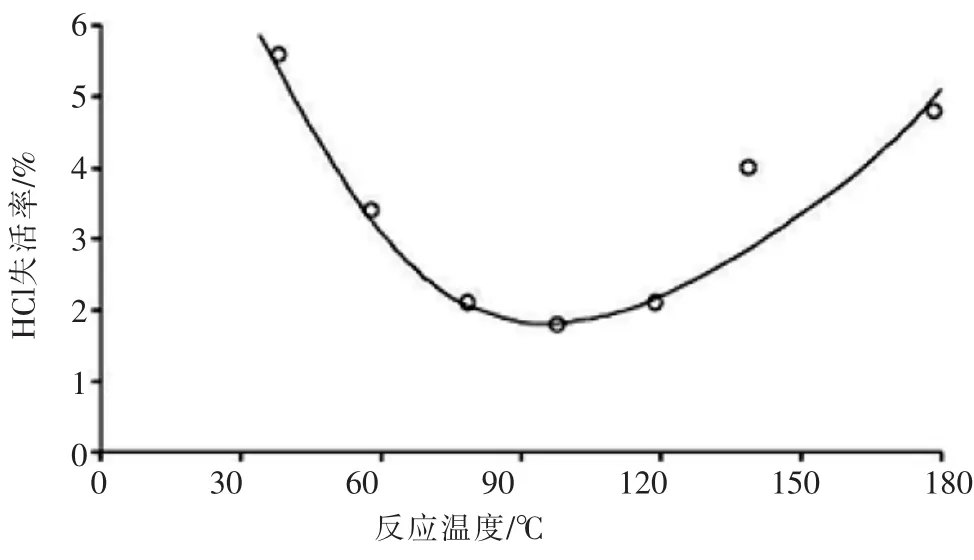
图2 金催化剂失活速率与反应温度的关系
华东理工大学的王雷[46]等对乙炔氢氯化反应的热力学进行了研究,热力学上的主、副反应均能自发进行,且为强放热反应,各反应的乙炔平衡转化率随温度的升高而降低,高温不利于主反应的进行。而在实际的反应过程中,主反应的产物氯乙烯很容易与过量的乙炔发生聚合,所以聚合副产物可能会沉积在催化剂表面引起积炭失活。
清华大学的魏飞[41]等负载低含量的AuCl3催化乙炔氢氯化反应,在200 h的长时间评价后对实际的积炭物种进行了分析,主要是芳烃以及芳烃的衍生物,且这些物种并不容易挥发,覆盖了催化剂的活性中心,造成了催化的失活。
而活性组分被还原导致金催化剂失活可以从金基催化剂的反应机理来阐述。Conte[47]等以负载型三价金离子化合物作为催化剂,通过量子化学密度泛函理论方法模拟计算后认为AuCl3均能吸附乙炔和氯化氢,但其对乙炔的吸附作用更强。而乙炔具有较强的还原性,这是导致催化剂失活的原因之一。
代斌[48]详细研究了金的价态和分散度在乙炔氢氯化反应中对催化剂失活的影响,随着反应的进行,Au3+被还原为AuO是催化剂失活的原因之一,而透射电镜分析金纳米粒子的团聚是催化剂失活的另一原因。
4.2再生方法
Hutchings等人采用还原过的Au/AC作为催化乙炔氢氯化反应的催化剂,发现该催化剂并不能催化该反应,采用王水氧化还原过的Au/AC催化剂的方法可以使得催化剂的活性恢复。
而Nkosi[49]等认为在乙炔氢氯化反应过程中加入N2、NO、N2O等气体对金催化剂的性能会有影响,在含有NO和N2O的条件下,催化剂的活性基本不变,这就说明加入氧化性气体使催化剂再生,而这些氧化性气体的加入并没有改变氯乙烯的选择性,这给金催化剂再生创造了条件。
刘楠[50]等在乙炔氢氯化反应中提到Cl2对氧化AuO是有效的,在100℃下,1 h就能恢复催化剂的活性。Nkosi也研究了用Cl2使负载金催化剂再生,在180℃,GHSV=1 140 h-1,n(C2H2)/n(HCl)的反应条件下,2%HAuCl4/C反应进行6 h后催化剂失活,失活的催化剂用Cl2在100℃下进行处理,可以使金催化剂再生。
2008年Conte等人在对乙炔氢氯化反应中金催化剂再生研究时用浸渍法制备金负载在活性炭的催化剂,反应失活后的金催化剂用煮沸的王水处理可以使其恢复催化活性,且达到了新鲜催化剂的初始活性;而华东理工大学的王声洁[51]等人在同样的反应中也证实了王水再生优于HCl再生。
5 金催化剂的产业化中试放大
基于对金催化剂的全面研究,其活性及稳定性都具有较好的产业化前景,最近国内对金催化剂的产业化也进行了一些研究,取得了较好的结果。
2014年,华东理工大学沈本贤课题组[52]对乙炔氢氯化无汞催化剂的中试进行了研究。以椰壳炭载体,将实验室方法放大125倍制得中试无汞催化剂。中试在天津大沽化工有限公司氯乙烯生产车间进行,对比考察无汞催化剂和工业HgCl2催化剂催化性能,在反应1 600 h后,无汞催化剂乙炔转化率从98%降至89%。而工业HgCl2催化剂在反应初期的前900 h活性很高,乙炔转化率>99%,随着反应继续进行,乙炔转化率急剧下降,当反应达到1 600 h以后,乙炔转化率仅为85%。同时,2种催化剂的氯乙烯的选择性均稳定大于99%。这表明所研发的无汞催化剂具有更好的稳定性。无汞催化剂的成本主要取决于黄金的价格,1 t无汞催化剂目前的成本为35万元/t,而目前工业氯化汞催化剂的成本为8.2万元/t。
陈万银[53]等介绍了新疆天业集团无汞催化剂的研发情况,提出了无汞催化剂的工业化应用面临的问题。他们对实验室研发的最优配方贵金属催化剂单管侧线工业条件下评价,催化剂的短期平均转化率在85%以上运行了近8 000 h,且副产物中只有极少量的1,1-二氯乙烷,选择性在99%以上。根据单管运行的情况来看,从技术角度该贵金属无汞催化剂具有一定的工业化前景。
自2007年起,Hutchings[6]和庄信万丰合作,对炭负载金催化剂的产业化也做了大量的研究,将不同金离子的配合物负载在活性炭上,最后选择Na3Au(S2O3)2负载在活性炭上,在长3 m、直径为50 mm的固定床反应器进行中试,乙炔和氯化氢的加料速度是0.6 kg/h,催化剂的平均转化率>85%,选择性>99%。
虽然无汞催化剂的成本高于汞催化剂,但无汞催化剂可以从多方面降低生产中的成本。首先,无汞催化剂消除了生产中汞污染的问题,节约了汞收集和汞处理的费用;其次,无汞催化剂使用后活性组分不流失,具有可再生的可能性,通过再生手段将失活的催化剂恢复活性,延长了催化剂的使用寿命,降低了催化剂的使用成本。
6 小结
在提倡“环境安全”、“人身安全”的现代社会和国际社会PVC生产“无汞”化的进程中,乙炔法合成氯乙烯用无汞触媒的研究重要性越来越受到人们的关注,而金催化剂具有较高的活性和选择性,是最具潜力替代汞触媒的催化剂。近年来,国内外科研工作者也对金催化剂做了大量的研究,取得了一定的进展。但是由于金催化剂稳定性较差、反应容易产生热点、价格昂贵等缺点,所以还需科研工作者的不断努力,使无汞催化剂不断成熟,并逐步走向工业化,促进氯碱行业更好、更快的发展。
参考文献:
[1]周莹,杨琴,罗芩,等.乙炔氢氯化低汞催化剂的研究进展.聚氯乙烯,2011,39(11):1-3.
[2]D. M. Smith,P. M. Walsh,T. L. Slager,et al. J. Catal.,1968,11:113-130.
[3]K. Shinoda. Chem. Lett. 1975:219 -220.
[4]G. J. Hutchings. Vapor phase hydrochlorination of acetylene:Correlation of catalytic activity of supported metal chloride catalysts . J. Catal.,1985,96(1):292-295.
[5]G. J. Hutchings. Vapor phase hydrochlorination of acetylene with group VII and IB metal chloride catalysts . Appl. Catal.,1988,43:33-39.
[6]A. Corma,A. Leyva -P erez,Maria J. Sabater,et al. Gold -Catalyzed Carbon Heteroatom Bond-Forming Reactions. Chem. Rev.,2011,111:1 657-1 712.
[7]M. Y. Zhu,Q. Q. Wang,K. Chen et al. Development of a Heterogeneous Non-Mercury Catalyst for Acetylene Hydrochlorination . ACS Catal.,2015,5:5 306-5 316.
[8]P. Johnston,N. Carthey,G. J. Hutchings,et al. Discovery,Development,and Commercialization of Gold Catalysts for Acetylene Hydrochlorination . J. Am. Chem. Soc.,2015,137:14 548 -14 557.
[9]X. Y. Li,M. Y. Zhu,B. Dai,et al. AuCl3 on polypyrrole -modified carbon nanotubes as acetylene hydrochlorination catalysts . Appl. Catal. B:Environ 2013,142-143:234-240.
[10]B. Dai,K. Chen. Boron and nitrogen doping in graphene for the catalysis of acetylene hydrochlorination. ACS Catal. 2015,5:2 541-2 547.
[11]X. G. Wang,B. Dai. Nitrogen -doped pitch -based spherical active carbon as a nonmetal catalyst for acetylene hydrochlorination . ChemCatChem,2014,6:2 339-2 344.
[12]B,Dai,X. Y. Li. Application of mesoporous carbon nitride as a support for an Au catalyst for acetylene hydrochlorination . Chem. Eng. Sci.,2015,135:472-478.
[13]马宁,朱明远,代斌,等.氮改性介孔碳的制备、表征及其对乙炔氢氯化反应的催化活性.石河子大学学报,2013,31(3):377-381.
[14]J.Zhao,J. T. Xu. Enhancement of Au/ACacetylene hydrochlorination catalyst activity and stability via nitrogen-modified activated carbon support . Chem. Eng. J.,2015,262:1 152-1 160.
[15]X. Y. Li,Y. Wang,et al. A novel,non -metallic graphitic carbon nitride catalyst for acetylene hydrochlorination . J. Catal.,2014,311:288-294.
[16]X. Y. Li,X. L. Pan,et al. Silicon carbide -derived carbon nanocomposite as a substitute for mercury inthecatalytic hydrochlorination of acetylene . Nat. Commun,2014,5:1-7.
[17]B. G. Wang,L. Yu,W. Li,et al. Phosphorus -doped carbon supports enhance gold-based catalysts for acetylene hydrochlorination . RSC Adv.,2014,4:15877-15885.
[18]C. F. Huang,M. Y. Zhu,L. H. Kang,et al. Active carbon supported TiO2-AuCl3/AC catalyst with excellent stability for acetylene hydrochlorination reaction . Chem. Eng. J.,2014,242:69-75.
[19]G. B. Li,W. Li,J. L. Zhang,et al. Non -mercury catalytic acetylene hydrochlorination over activated carbon supported Au catalysts promoted by CeO2. Catal. Sci. Technol.,2015,10.
[20]X. H. Tian,G. T. Hong. Catalytic performance of AuIII supported on SiO2 modified activated carbon . RSC Adv.,2014,4:36 316-36 324.
[21]韩伟杰,代斌.球形活性炭的孔道结构改性及其对乙炔氢氯化反应的影响.功能材料,2013,44:201-204.
[22]X. D. Yang,C. H. Jiang,J. S. Zhang,et al. Hydrochlorination of Acetylene Using SiC Foam Supported Structured C/Au Catalysts . J. Mater. Sci. Technol.,2014,30(5):434-440.
[23]M. Conte,A. F. Carley,G. Attard,et al. Hydrochlorination of acetylene using supported bimetallic Au-based catalysts . J. Catal.,2008,257:190-198.
[24]王声洁,沈本贤.Au-K/C催化剂用于乙炔氢氯化反应制氯乙烯的催化性能.华东理工大学学报,2010,36:20-24.
[25]G.B.Li,W.Li,J.L.Zhang,etal.Strontiumpromotedactivatedcarbonsupported gold catalysts for non -mercury catalytic acetylene hydrochlorination.Catal.Sci.Technol.,2015.
[26]H. Y. Zhang,W. Li. Non -mercury catalytic acetylene hydrochlorination over bimetallic Au- Ba(II)/AC catalysts,Catal. Sci. Technol.,2015,5:1 870-1 877.
[27]J. Zhao,T. T. Zhang. Nitrogen -modifi ed activated carbon supported bimetallic gold -cesium(I)as highly active and stable catalyst for the hydrochlorination of acetylene,RSC Adv.,2015,5:6925-6931.
[28]J. Zhao,T. T. Zhang. Activated carbon supported ternary goldcesium(I)-indium(III)catalyst for the hydrochlorination of acetylene,Catal. Sci. Technol.,2015,5:4 973-4 984.
[29]J. Zhao,S. C. Gu. Promotional effect of copper(II)on an activated carbon supported low content bimetallic gold -cesium(I)catalyst in acetylene hydrochlorination,RSC Adv.,2015,5:101427-101436.
[30]H. Y. Zhang,B. Dai. Non -mercury catalytic acetylene hydrochlorination over bimetallic Au-Co(III)/SAC catalysts for vinyl chloride monomer production. Green Chem.,2013,15:829-836.
[31]H. Y. Zhang,B. Dai,W. Li,et al. Non -mercury catalytic acetylene hydrochlorination over spherical activated-carbon-supported Au-Co(III)-Cu(II)catalysts. J. Catal.,2014,316:141-148.
[32]Y. F. Pu,J. L. Zhang,X. Wang,et al. Bimetallic Au-Ni/CSs catalysts for acetylene hydrochlorination . Catal. Sci. Technol.,2014,4 (12):4 426-4 432.
[33]Y. Z. Dong,H. Y. Zhang. Bimetallic Au -Sn/AC catalysts for acetylene hydrochlorination,J. Ind. Eng. Chem.,2015.
[34]S. J. Wang,B. X. Shen,Q. L. Song,et al. Kinetics of acetylene hydrochlorination over bimetallic Au -Cu/C catalyst . Catal. Lett.,2009,134:102-109.
[35]K. Zhou,W. Wang. Synergistic Gold -Bismuth Catalysis for Non -Mercury Hydrochlorination of Acetylene to Vinyl Chloride Monomer . ACS Catal.,2014,4:3 112-3 116.
[36]H. Y. Zhang,B. Dai. Hydrochlorination of acetylene to vinyl chloride monomer over bimetallic Au-La/SAC catalysts . J. Ind. Eng. Chem.,2012,18:49-54.
[37]王琴琴,朱明远,代斌,等.Au-基催化剂的制备及其在乙炔氢氯化反应中的催化活性.石河子大学学报院自然科学版,2015,33(1):1-6.
[38]M. Conte,C. J. Davies,D. J. Morgan,et al. Aqua regia activated Au/C catalysts for the hydrochlorination of acetylene . J. Catal.,2013,297:128-136.
[39]X. H. Tian,G. T. Hong,B. B. Jiang et al. Efficient Au0/C catalyst synthesized by a new method for acetylene hydrochlorination . RSC Adv.,2015,5:46 366-46 371.
[40]C. F. Huang,M. Y. Zhu. A novel high-stability Au(III)/Schiffbasedcatalyst for acetylene hydrochlorinationreaction. Catal. Commun.,2014,54:61-65.
[41]K. Zhou,J. C. Jia. Low content Au -based catalyst for hydrochlorination of C2H2and its industial scale -up for future PVC process . Green Chem.,2015,17(1):356-364.
[42]王声洁,沈本贤.乙炔氢氯化反应高分散载金催化剂的制备及催化性能.石油学报,2010,26(2):201-207.
[43]J. Zhao,S. C. Gu. Supported ionic-liquid-phase-stabilized Au(III)catalyst for acetylene hydrochlorination,Catal. Sci. Technol.,2015.
[44]W. Wittanadecha,N. Laosiripojana,A. Ketcong,et al. Preparation of Au/C catalysts using microwave-assisted and ultrasonicassisted methods for acetylene hydrochlorination. Appl. Catal. A:Gen. 2014,475:292-296.
[45]N. Bongani,J. C. Neil,G. J. Hutchings etal. Hydrochlorination of acetylene using gold catalysts:A study of catalyst deactivation. J. Catal.,1991,128:366-377.
[46]王雷,沈本贤.乙炔氢氯化反应体系热力学分析,化工进展. 2014,33:573-576.
[47]M. Conte,A. F. Carley,C. Heirene et al. Hydrochlorination of Acetylene Using a Supported Gold Catalyst:A Study of the Reaction Mechanism . J. Catal.,2007,250(2):231-239.
[48]B. Dai,Q. Q. Wang. Effect of Au nano-particle aggregation on thedeactivationoftheAuCl3/ACcatalystforacetylene hydrochlorination,Sci. Rep.,2015,DOI:10.1038/srep10553.
[49]G. J. Hutchings. Hydrochlorination of acetylene using carbonsupported gold catalyst:A study of catalyst reactivation . J. Catal.,1991,128:378-386
[50]J. L. Zhang,N. Liu,W. Li et al. Progress on cleaner production of vinyl chloride monomers over non-mercury catalysts . Front. Chem. Sci.Eng.,2011,5(4):514-520.
[51]王声洁,沈本贤.乙炔氢氯化非汞催化反应制取氯乙烯单体研究.上海:华东理工大学,2010.
[52]任若凡.乙炔氢氯化UDH无汞催化剂中试研究.上海:华东理工大学,2014.
[53]陈万银.乙炔氢氯化无汞催化剂研发进展及前景分析,中国氯碱,2015,8:20-24.
Progress on carbon supported gold catalysts for acetylene hydrochlorination
YANG Xue-chao,LAN Guo-jun,LI Jian,WANG Yan,LI Ying
(Institute of Industrial Catalysis,Zhejiang University of Technology,Hangzhou 310014,China)
Abstract:Recent progress on the modification of the support,the addition of other metal,preparation of gold catalysts and the deactivation and reactivation of gold catalysts for hydrochlorination of acetylene are reviewed in this paper. The development and trends of carbon supported gold catalysts for acetylene hydrochlorination were prospected. This paper can provide informations for the exploration of a new generation non-mercury catalysts of acetylene hydrochlorination.
Key words:hydrochlorination of acetylene;gold catalysts;carbon support;non-mercury catalyst
中图分类号:TQ314.24+2
文献标识码:B
文章编号:1009-1785(2016)04-0014-07
收稿日期:2016-01-18
