多糖类手性固定相超临界流体色谱法分离手性化合物
2016-06-22李冬艳郝芳丽陈小明
李冬艳, 吴 锡, 郝芳丽, 杨 洋, 陈小明
(大赛璐药物手性技术(上海)有限公司, 上海 200131)
多糖类手性固定相超临界流体色谱法分离手性化合物
李冬艳,吴锡,郝芳丽,杨洋,陈小明*
(大赛璐药物手性技术(上海)有限公司, 上海 200131)
摘要:采用超临界流体色谱法(SFC),在多糖固定相Chiralpak IA、IB、IC、ID、IE和IF上成功拆分了11种手性化合物。分离结果表明,这6支手性色谱柱对这些手性化合物具有良好的手性识别互补性,均可以在10 min之内得到良好的分离结果,具有较好的实用性。改性剂甲醇、乙醇和异丙醇对手性化合物的保留时间以及手性选择性均具有良好的调节作用,需要根据不同手性物质在手性柱上的分离情况加以区别,选择使用,并调节改性剂至合适的比例。针对键合型固定相溶剂通用性的特征,特殊改性剂的应用也有助于优化手性分离。
关键词:超临界流体色谱法;手性分离;手性固定相;多糖衍生物
近十多年来,超临界流体色谱(SFC)发展迅速,成为继GC与HPLC之后发展起来的又一项重要的色谱分离技术。尤其是在手性分离与分析领域,因其分析速度快、分离效率高、溶剂消耗少等优点,已经成为手性色谱法中不可或缺的重要分离技术之一[1,2],与HPLC、GC相互补充,特别适用于手性分离制备[3]。另一方面,可以用在SFC上配套使用的手性柱或手性填料也多种多样,使得手性分离的成功率极高,极大地推动了手性SFC的发展。目前,多糖类衍生物手性固定相,因其广泛的手性识别能力、良好的稳定性、耐用性、高负荷等优点,无论是用于手性分析,还是手性色谱制备,都是HPLC中使用最为广泛的手性固定相[4-6],由于该类固定相主要用于在正相流动相条件下实现手性分离,因此也非常适合于手性SFC分离[7]。国内也有一些SFC用于手性药物分离的文献综述[8,9];金薇等[10]报道采用SFC分离了左乙拉西坦及其右旋异构体。
本文以键合型多糖系列柱i-chiral 6: Chiralpak IA、IB、IC、ID、IE、IF为试验对象,尝试在SFC模式下对11种手性化合物进行手性分离,同时探讨了改性剂种类、浓度、碱性添加剂以及特殊改性剂对SFC手性分离的影响。
1实验部分
1.1仪器、试药与材料
超临界流体色谱仪(日本Jasco公司); 11个手性化合物样品均由本公司自主开发,其分子结构式如图1所示;i-chiral 6系列手性柱(日本Daicel公司): Chiralpak IA、IB、IC、ID、IE与IF(150 mm×4.6 mm, 5 μm),分别在硅胶载体上化学键合了系列多糖衍生物而得,各手性固定相的名称与结构式如图2所示。
CO2为上海空气化工公司提供,化学纯度99.99%,其他溶剂均为色谱纯。
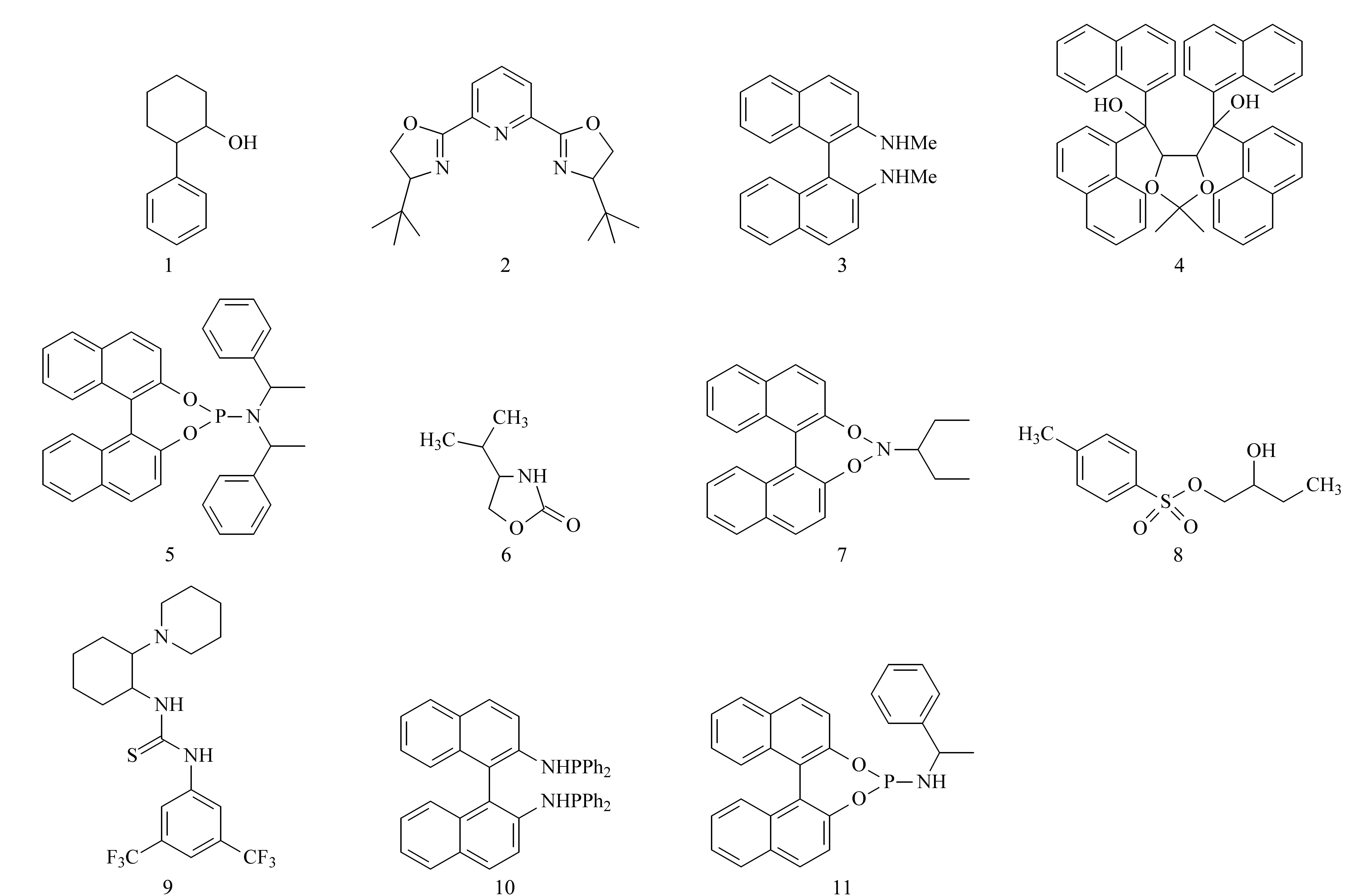
图1 11个手性化合物的分子结构式Fig. 1 Molecular structures of the 11 chiral compounds
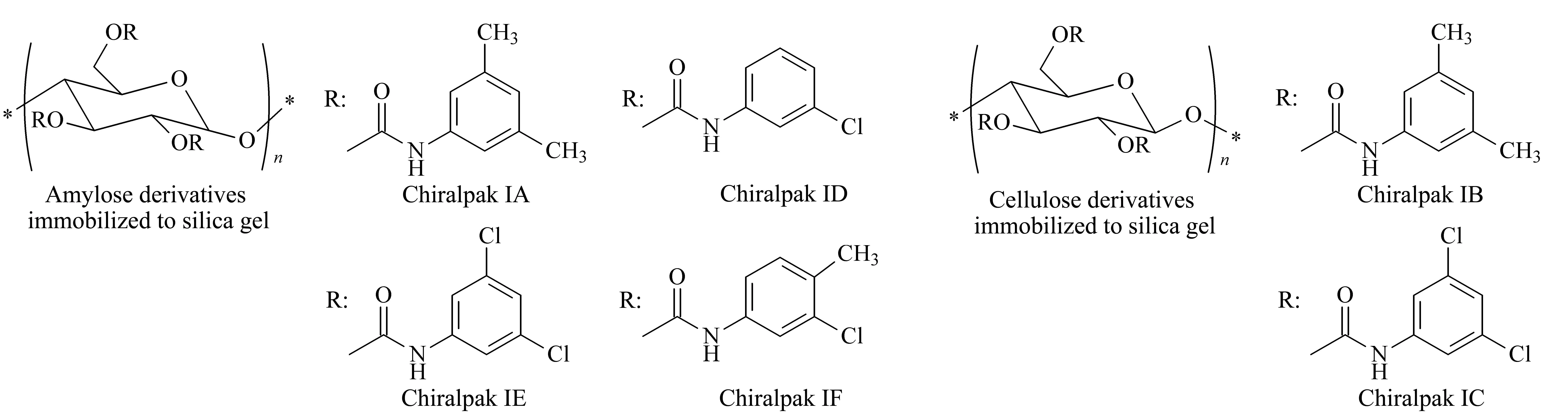
图2 i-chiral 6系列手性固定相的分子结构式Fig. 2 Molecular structures of the chiral stationary phases on i-chiral 6 IA: amylose tris(3,5-dimethylphenylcarbamate); IB: cellulose tris(3,5-dimethylphenylcarbamate); IC: cellulose tris(3,5-dichlorophenylcarbamate); ID: amylose tris(3-chlorophenylcarbamate); IE: amylose tris(3,5-dichlorophenylcarbamate); IF: amylose tris(3-chloro-4-methylphenylcarbamate).
1.2超临界色谱条件
除非特别说明,色谱条件均为:流速2 mL/min;背压10 MPa;检测波长220 nm(化合物6为203 nm)。
色谱柱死时间由1,3,5-三叔丁基苯在相同的色谱条件下分别进样测定。
1.3手性样品溶液的配制
11种手性化合物均由两种构型的对映体混合而得,溶解在甲醇溶液中,质量浓度约为1~3 g/L。
2结果与讨论
2.1i-chiral 6系列手性柱手性识别能力的互补性
i-chiral 6系列手性柱是在硅胶载体上键合了一系列结构非常相似的多糖衍生物[11]。其中,IA、ID、IE、IF属于直链淀粉衍生物,IB、IC属于纤维素衍生物。因而这6种手性柱既相似又有区别。表1中列出了11种手性化合物在6支不同的手性柱上的手性识别结果。可以看出,这6支手性柱对11种化合物的识别能力如下:IA可以识别其中的10个,IB识别5个,IC识别7个,ID识别9个,IE识别8个,IF识别8个。需要说明的是,表中所统计的结果仅仅是根据化合物在柱子上有无选择性来判断,并不能显示其手性识别的强弱与分离的程度;并且流动相也不一样,包含了甲醇、乙醇、异丙醇从10%~30%(v/v)多种色谱条件下的分离结果。从化合物方面看,化合物2、4、5、7在6支柱子上均能被识别。本实验中,虽然样本数偏少,并不非常具有代表性,但也基本上可以说明这6支手性柱在SFC模式下的共性与个性,对大部分手性化合物往往具有较好的手性识别互补性。

表 1 11个手性化合物在i-chiral 6系列柱上的手性识别结果
√: with chiral recognition;×: without chiral recognition. Modifiers: 10%, 20% or 30% (v/v) alcohol (methanol, ethanol or 2-propanol).
2.2不同改性剂对手性分离的影响
由于CO2的洗脱能力较弱,要成功实现手性SFC分离,往往需要在CO2中添加一定量的极性改性剂,如在HPLC上常用的一些溶剂醇、乙腈等。加入改性剂的主要目的有:增加洗脱强度;调节样品与手性固定相之间的选择性与分离度;改善样品在CO2中的溶解度等。本文考察了甲醇、乙醇、异丙醇等3种常用在SFC上的改性剂对手性分离的影响,分离结果见表2。
表2中列出了化合物1~5在IA、IC、ID、IE和IF柱上的分离结果。化合物1、2、5随着改性剂由甲醇变为异丙醇,选择因子α与分离度Rs都减小,而化合物3、4则相反。另外,对于保留因子k的影响,只有化合物3在ID柱上是随着由甲醇变为异丙醇的过程增大,其他的化合物都表现为相反的规律。可见,在SFC模式下,各种醇类改性剂对手性分离的影响并没有非常明显的规律,结果与待分离的样品紧密相关。要开始新的SFC筛选,一般可以从甲醇开始尝试,然后依次尝试乙醇、异丙醇。
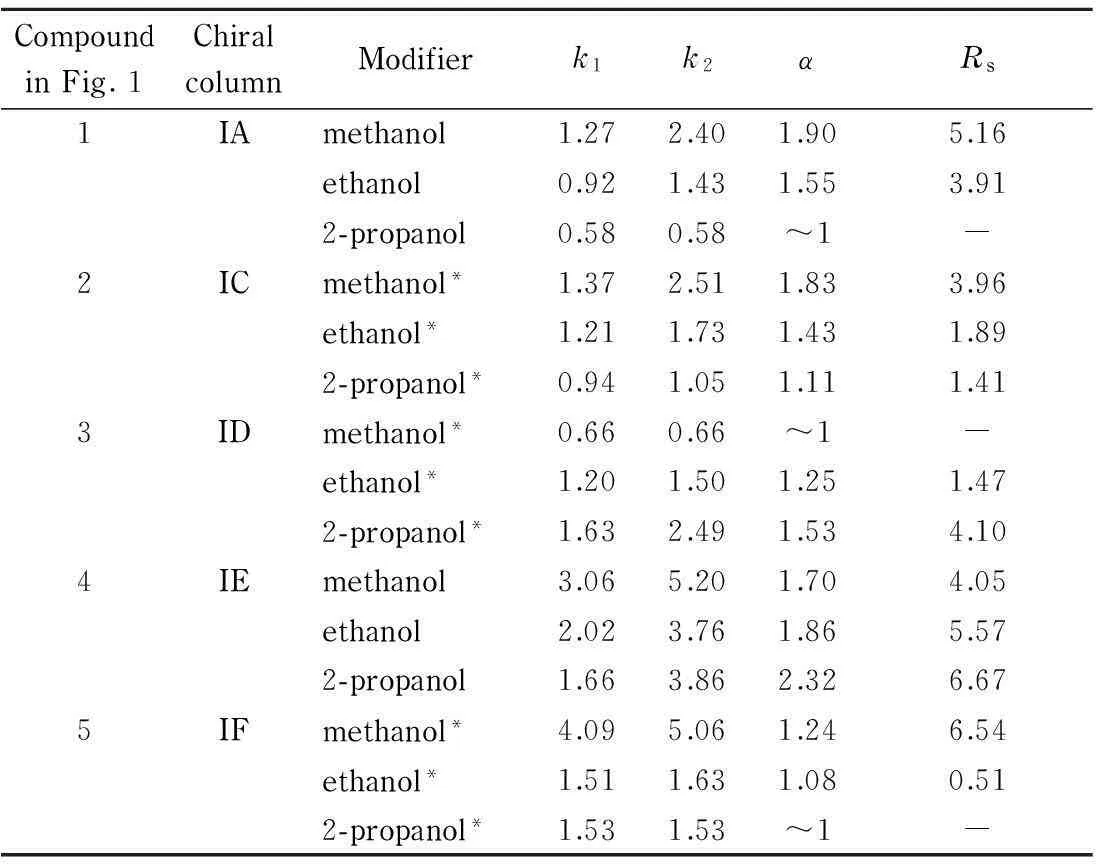
表 2 不同改性剂条件下的手性分离结果
* With 0.1% (v/v) diethylamine (DEA).
2.3改性剂的浓度对手性分离的影响
本研究中,我们分别用含10%、20%、30%(v/v)甲醇的改性剂考察化合物6~9在IA、IC、ID和IE柱上的分离,结果如表3所示。从表3中可以看出,随着甲醇改性剂含量的增大,保留因子k1、k2,以及Rs均变小。这主要是因为改性剂含量增大以后,洗脱能力显著增强,因而在色谱柱上出峰时间变快,保留变小,这与正相手性HPLC保留行为基本相符。对于选择因子,我们发现化合物6、7、8随着甲醇比例的增大变化不太,但化合物9则比较明显,当甲醇体积分数增加到30%时,基本上不能被识别。
2.4特殊改性剂对手性分离的影响
多糖类手性固定相根据生产工艺主要可以分为两大类:涂布型与键合型。涂布型固定相是通过物理吸附的方法将多糖高分子涂覆在多孔硅胶表面,因而不能使用那些能将多糖衍生物溶解或溶胀的溶剂作流动相组分,如二氯甲烷(DCM)、乙酸乙酯、四氢呋喃等,这里称这些溶剂为特殊改性剂。新一代键合型i-chiral 6手性柱则可以很好地解决这一问题:HPLC的常用溶剂,只要在流动相中是互溶的,都可用作流动相的成分之一,这样就大大方便了手性分离方法的建立,尤其是以制备分离为目的的方法开发时,更能体现其调节样品溶解度与分离度的优势[8]。在SFC模式下,同样也可以根据实验的需要使用这些特殊改性剂来优化手性分离,得到满意的分离结果。

表 3 添加甲醇条件下的手性分离结果
* With 0.1% (v/v) DEA.
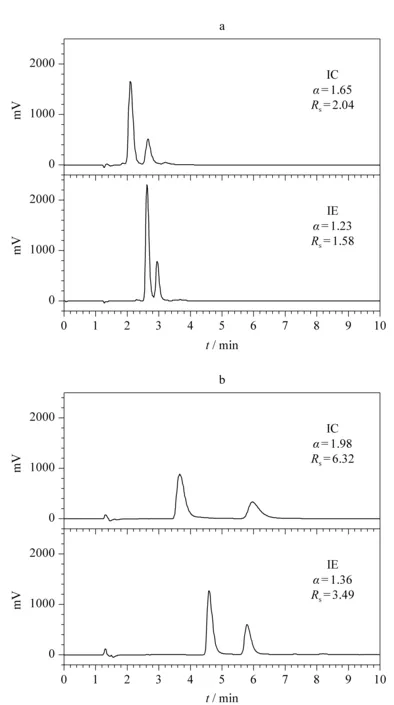
图3 化合物11在IC与IE手性柱上的分离谱图Fig. 3 Chromatograms of compound 11 on chiral columns IC and IE Modifiers: (a) 30% (v/v) 2-propanol+0.1% (v/v) DEA; (b) 30% (v/v) Co-solvent with 0.1% (v/v) DEA. Co-solvent: the mixture of 2-propanol and dichloromethane (1∶1, v/v).
如图3所示,我们比较了IC、IE两支手性柱分离化合物11的结果,分别用异丙醇或异丙醇与二氯甲烷混合物作为改性剂。可以看出,当添加二氯甲烷为改性剂时,不仅改善了选择因子,同时也提高了分离度,达到了优化分离的目的。
另外,在SFC模式中,有一点不太确定的就是样品在CO2中的溶解度。目前为止还没有很好的方法可以测定待分离样品在CO2中的溶解度。这也是SFC和HPLC的一个显著的区别。一般来说,样品溶于改性剂之后与CO2混合,然后进入色谱柱。如果样品在改性剂中的溶解度比较好,也许不会遇到任何问题。但如果样品在改性剂中的溶解度比较小,甚至微溶,那么就要特别注意了。因为CO2可能是助溶剂,也可能相反。前者对分离有利,后者则可能会出现样品在CO2中析出,导致手性柱柱压升高,出峰怪异,甚至样品结晶吸附在手性固定相上不被洗脱等现象。尤其是当SFC用于手性制备分离时,溶解度的因素尤其要引起重视。而加入特殊改性剂,往往可以改善样品的溶解度。
2.5碱性添加剂对手性分离的影响
在正相手性HPLC分离模式中,对于酸性、碱性手性样品一般都需要在流动相中添加微量的有机酸或碱,才能确保酸、碱化合物的有效分离。SFC条件下一般也需要遵循这个规则。只不过由于CO2本身具有一定的酸性,因而对于部分酸性不是很强的化合物,不必添加酸性添加剂也能实现良好的分离。本研究中,由于样品的限制,只针对碱性化合物9进行了对比试验。如图4所示,在Chiralpak IE柱上,以中性的10%(v/v)甲醇作为改性剂时,色谱峰拖尾,分离度很小,几乎不能被有效分离;但添加了0.1%(v/v)的DEA时,色谱分离效果得到了明显改善。由此可见,碱性添加剂对碱性化合物的分离至关重要。
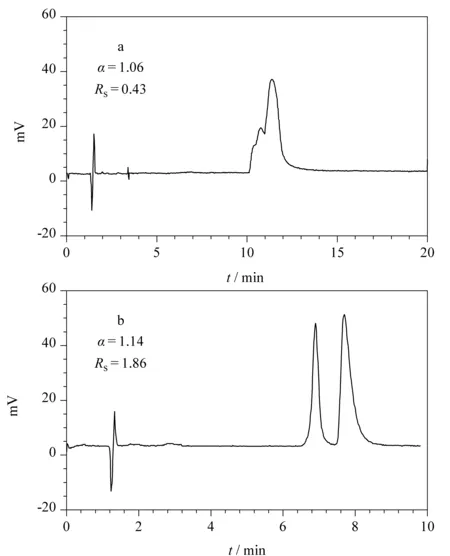
图4 化合物9在Chiralpak IE手性柱上的色谱图Fig. 4 Chromatograms of compound 9 on chiral column Chiralpak IE Modifiers: (a) 10% (v/v) methanol; (b) 10% (v/v) methanol+0.1% (v/v) DEA.
3结论
11个手性化合物通过手性SFC取得了良好的分离,均可以在10 min之内完成快速分析。11个手性化合物在i-chiral 6上的拆分结果也表明了i-chiral 6系列手性柱手性识别能力的互补性,为实现成功的手性SFC分离提供了重要的基础。手性SFC中,改性剂的种类与浓度对手性SFC分离都有非常大的影响。实际分离过程中,可以根据实验需要分别考虑采用甲醇、乙醇或异丙醇为改性剂,并且调整到合适的比例来优化手性分离结果。另外,如二氯甲烷等特殊改性剂的使用,对于某些手性化合物可以达到在i-chiral 6上分离的目的。对于碱性化合物,在改性剂中添加微量的碱性添加剂对于实现良好的手性分离至关重要。
参考文献:
[1]Terfloth G. J Chromatogr A, 2001, 906: 301
[2]Ward T J, Ward K D. Anal Chem, 2012, 84: 626
[3]Miller L. J Chromatogr A, 2012, 1250: 250
[4]Okamoto Y, Yashima E. Angew Chem Int Ed, 1998, 37: 1020
[5]Yashima E. J Chromatogr A, 2001, 906: 105
[6]Francotte E. J Chromatogr A, 2001, 906: 379
[7]Lee J, Lee J T, Watts W L, et al. J Chromatogr A, 2014, 1374: 238
[8]Ren Q L, Su B G, Huang M, et al. Chinese Journal of Analytical Chemistry, 2000, 28(6): 772
任其龙, 苏宝根, 黄梅, 等. 分析化学, 2000, 28(6): 772
[9]Wu J, Feng F. Progress in Pharmaceutical Sciences, 2004, 28(7): 300
武洁, 冯芳. 药学进展, 2004, 28(7): 300
[10]Jin W, Yang X L, Lu D, et al. Chinese Journal of Pharmaceutical Analysis, 2013, 33(5): 822
金薇, 杨新磊, 陆丹, 等. 药物分析杂志, 2013, 33(5): 822
[11]Zhang T, Franco P, Nguyen D, et al. J Chromatogr A, 2012, 1269: 178
Separation of enantiomers by supercritical fluid chromatography on polysaccharide derivative-based chiral stationary phases
LI Dongyan, WU Xi, HAO Fangli, YANG Yang, CHEN Xiaoming*
(Daicel Chiral Technologies (China) Co. Ltd., Shanghai 200131, China)
Abstract:Eleven kinds of chiral compounds have been well separated within 10 min on polysaccharide derivative-based chiral stationary phases named Chiralpak IA, IB, IC, ID, IE and IF by supercritical fluid chromatography (SFC). The chiral recognition of these chiral compounds has demonstrated good complementary enantioselectivities of the six chiral columns, which were proved to be useful for chiral SFC. Both the elution time and enantioselectivies could be significantly affected by the modifier types and their concentrations, such as methanol, ethanol and isopropanol, which should be optimized during the experiments. In addition, the solvent versatility of the immobilized chiral stationary phase on the optimization of the chiral separation was helpful.
Key words:supercritical fluid chromatography (SFC); chiral separation; chiral stationary phase; polysaccharide derivatives
DOI:10.3724/SP.J.1123.2015.10039
*收稿日期:2015-10-26
中图分类号:O658
文献标识码:A
文章编号:1000-8713(2016)01-0080-05
色谱手性分离专刊·研究论文
*通讯联系人.E-mail:chen_xiaoming@dctc.daicel.com.
