基于美国FDA MAUDE数据库的医学影像存储传输系统可疑不良事件分析
2016-06-05单晓晖王姝迟戈赵鑫宋飞
单晓晖王姝迟戈赵鑫宋飞
1 辽宁省药械审评与监测中心 (沈阳 110003)
2 辽宁省食品药品监督管理局行政服务中心 (沈阳 110003)
3 沈阳药科大学 (沈阳 110016)
基于美国FDA MAUDE数据库的医学影像存储传输系统可疑不良事件分析
单晓晖1王姝2迟戈1赵鑫1宋飞3
1 辽宁省药械审评与监测中心 (沈阳 110003)
2 辽宁省食品药品监督管理局行政服务中心 (沈阳 110003)
3 沈阳药科大学 (沈阳 110016)
通过对美国FDA MAUDE数据库2014年1月1日至2014年12月31日收集到的医学影像存储传输系统不良事件报告进行统计分析,分析其不良事件特点,初步探讨其安全性影响因素,为进一步开展监测工作提供参考。
医学影像存储传输系统 不良事件 分析
医学图像存储与传输系统(Picture Archiving and Communication System,PACS),是利用现代放射技术、数字成像技术、计算机及通信技术,准确高效地采集、存储、归档、传送、显示和管理医学影像信息与病人入口信息的数字化影像系统[1]。按规模及覆盖范围,PACS分为单一影像模式PACS、科室级PACS、全院级PACS及区域级PACS[2~3]。近年来,临床上常将PACS与放射科信息系统RIS、医院信息系统HIS、检验科信息系统LIS等整合,通过网络将医院的CT、CR、DSA、MRI、数字胃肠、彩色超声、黑白超声、喉镜、内窥镜等影像检查设备连接起来,实现数字化图像信息无胶片化快速存储、传输。同时,借助计算机技术对医学影像进行分析、计算、处理,得出初步的诊断数据[4~5]。为进一步探讨医学影像存储传输系统的安全性,降低风险,减少不良事件重复发生率,指导临床合理、安全用械,通过检索FDA MAUDE数据库,对2014年 1月1日至2014年12月31日收集到的1348例医学影像存储传输系统不良事件报告进行统计分析,提出对该类产品的评价意见。
1.资料与方法
检索FDA MAUDE 数据库,2014年1月1日至2014年12月31日共检索到医学影像存储传输软件不良事件报告1348例,除去9份与PACS不相关的报告,共有1339份有效报告。对这1339例不良事件报告应用Microsoft Excel进行统计学分析。
2.结果
2.1 不良事件情况统计
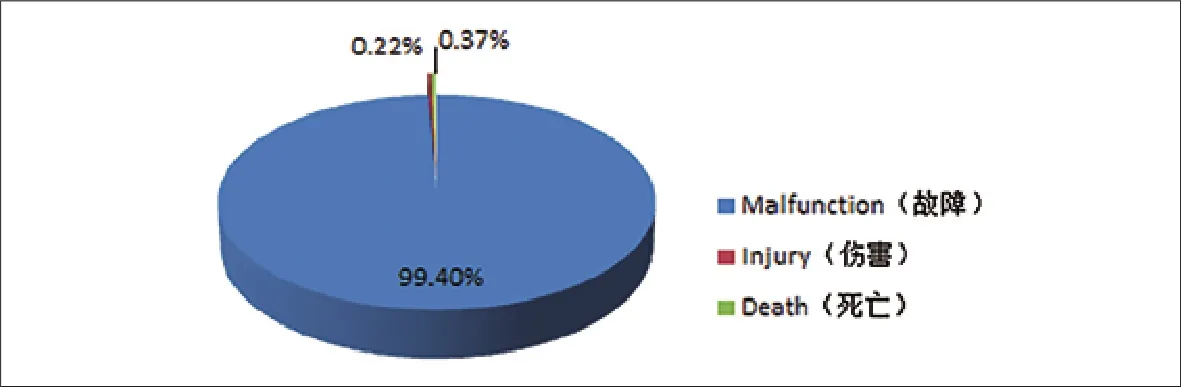
图1. 不良事件类型统计
对1339例医学影像存储传输系统不良事件报告中的不良事件表现进行统计分析,除去10例描述不清和不能明确原因的报告,共有1329例有效报告。1329例有效报告中,“系统诊断术语不准确”出现最多,为1150例,占86.53%;其次为“系统的预设清除缓存功能(MPD)故障”,出现61例,占4.59%;“PACS系统无法校准”、“PACS系统登录异常系统异常关闭”、“PACS系统双显示器显示结果不一致”等情况较为少见,详见表1。
2.2 不良事件类型
根据MAUDE数据库相关填写规范以及不良事件对患者造成的伤害程度,统计1339例医学影像存储传输系统不良事件报告类型情况如下:出现设备故障的1331例,占99.40%;造成伤害的3例,占0.22%;导致死亡的5例,占0.37%,详见图1。
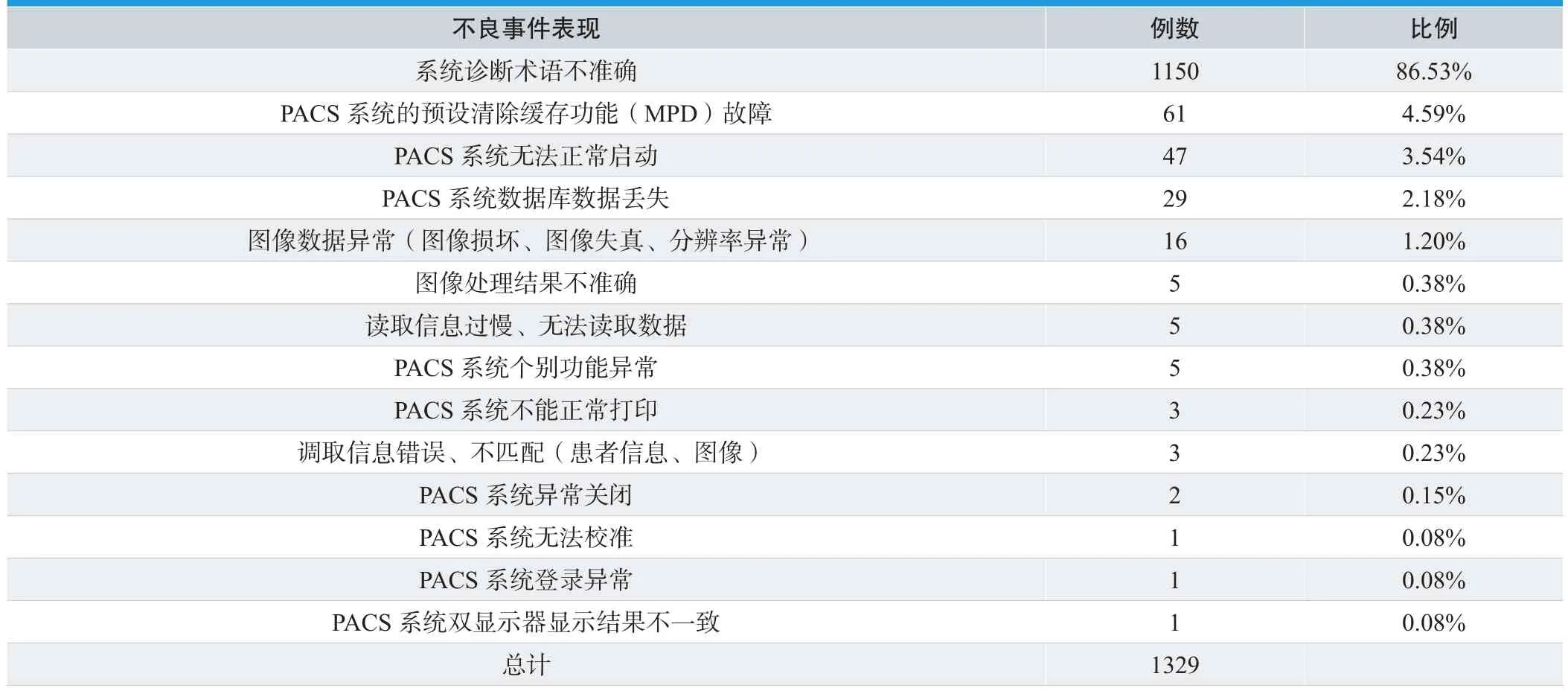
表1. 不良事件情况
2.3 死亡报告分析
对检索到的5例死亡报告进行分析讨论,1例与使用医学影像存储传输系统无关,另外4例均与使用医学影像存储传输系统有关。其中,1例是重症病人,在使用PACS进行医学影像传输时,耽误治疗死亡;1例是医生无法访问患者早前报告,患者在此期间死亡;另外2例是未按操作说明使用造成的,1例是行羊膜穿刺术造成胎儿自发流产,患者此前经医学影像存储传输系统计算存在三染色体风险,经调查,医学影像存储传输系统进行风险计算时未遵循操作手册程序要求;另1例是重症患者影像数据报告无法查到,患者在此期间死亡,经调查,是人为操作错误。
3.讨论
3.1 不良事件临床表现
报告中不良事件主要表现为:系统诊断术语不准确;系统清楚缓存功能故障;无法正常启动;数据丢失、图像异常;处理结果不准确以及附加功能异常、启动登录异常等。其中,诊断术语不准确情况最多,占86.53%。
3.2 不良事件原因分析
3.2.1 诊断不准确可能原因分析
近年来,临床使用的PACS软件,多与具有影像诊断功能的软件整合使用,通过对医学影像进行分析、计算、处理,得出初步诊断结果的功能。在此处理过程中,由于影像存储传输不准确、影像数据处理不当或诊断依据不充分,可能出现诊断不准确等异常情况。从本次研究结果来看,“系统诊断术语不准确”出现的情况较多,其原因可能为两方面:一是系统预设的诊断术语库不完备,部分诊断术语未纳入系统术语库,在影像数据处理后,因缺少对应的诊断术语,而造成诊断术语选择错误;二是软件界面不科学,诊断术语选择界面中,不同术语间排布过于紧密,字号过小,操作中极易将临近术语误选为诊断结果。
3.2.2 系统预设功能故障可能原因分析
本次研究中,“PACS系统的预设清除缓存功能(MPD)故障”多次出现,预设清除功能主要用于清除因长期归档和数据海量存储残留的缓存图像数据,此功能故障,造成系统中缓存数据无法清除。根据不良事件报告内容分析,该预设功能故障的原因可能是软件出厂设置错误,软件出厂时,未对此项功能进行设置,因而在使用中软件不具备此项功能;也可能是由于使用者误操作取消了此项功能,造成系统缓存数据无法清除。
3.2.3 系统启动异常可能原因分析
PACS系统启动异常主要表现为:电脑主机无法启动、显示器黑屏、电脑反复重启、软件系统无法打开等。其中,电脑主机无法启动和显示器黑屏属于硬件故障。发生原因可能是由于电脑具有开机自动检测功能,在开机时检测到CPU、电源风扇等配件电压、温度不正常,或电脑参数设置不正常,因而自动采取保护措施,造成主机无法启动[6]。电脑反复重启、软件系统无法打开属于软件故障,发生的原因可能是电脑操作系统出现问题造成的电脑系统故障,也可能是PACS软件部分程序误删除或PACS软件存储路径改变,导致的PACS软件无法打开。
3.2.4 系统数据异常可能原因分析
PACS系统数据异常主要表现为:数据库数据丢失、图像数据异常、调取信息错误等。其原因可能是由于软件设计缺陷或软件退化造成的。由于软件产品没有物理实体,在开发和使用过程中存在人为因素影响,存在软件设计缺陷;同时,随着软件使用和更新,存在软件退化问题;而软件测试受时间和成本的限制,不能穷尽所有情况,因而软件产品缺陷无法避免[7]。系统数据异常的原因,也可能是由于原数据中患者基本信息录入错误或缺失,查阅图像等数据时,输入的调取条件与原数据不匹配,无法正确调取图像等信息。此外,数据库数据丢失也可能是由于数据存储设 备损坏造成的。
4.风险控制建议
随着计算机科学技术的迅猛发展,PACS在临床领域的使用范围也逐步扩大,从单一影像科室诊断到区域PACS,未来依托于远程医疗技术,PACS也将实现远程访问。在PACS为影像诊断提供有力技术支持的同时,应对其在临床使用中出现的不良事件提高重视,从研发、生产、使用、监管等环节出发,确保该产品安全性、有效性。
4.1 研发生产的建议
生产企业作为医疗器械安全有效责任人,应承担起减少PACS可疑不良事件的主要责任。加强PACS产品的研发工作,注重软件设计的科学性、完备性,及时更新改进软件设计,使人机界面更易于操作,降低软件固有风险;通过软件出厂测试,正确配置软件预设置功能,提升产品质量,避免不合格品出厂;在PACS说明书、操作手册中明确软件安装使用环境、操作程序、使用注意事项、警示信息等,加强对临床医务人员的培训,降低误操作风险,规范PACS软件的安装、使用、维护,减少不良事件的发生;并建立健全医疗器械不良事件报告制度,及时上报可疑不良事件。
4.2 临床使用的建议
本次研究结果表明,PACS软件操作使用不规范可能导致不良事件的发生。在临床使用中,应合理配置电源、主机、存储设备等硬件设施,维持适宜的软件运行环境;定期进行日常维护,对PACS软件进行测试、检测清除病毒,及时备份数据信息;制定PACS软件相关使用制度,合理设置各级操作用户权限,定期更换用户口令;加强医务人员PACS系统操作基础培训,严格按照说明书及要求操作,注意警示信息等内容,以减少因使用问题导致的可疑不良事件。针对具有诊断功能的PACS,应严格按照诊疗规范进行操作,仔细核对患者信息,不单纯依赖系统给出的诊断,综合判断,确认诊断结论是否准确,防止出现因诊断信息错误而造成的医疗器械不良事件。出现不良事件后要针对不同的情况采取有效的治疗措施,并及时上报可疑医疗器械不良事件报告。
4.3 监管监测的建议
通过对国外监测数据分析,个别PACS产品存在质量问题,可能造成使用故障,建议加强对此类软件产品的监督抽验,以减少质量问题引发的产品风险。此外,针对软件类产品存在的设计缺陷、软件退化等固有风险,建议加强日常对此类产品的不良事件监测,发挥监测工作在产品上市后风险管理的地位和作用,及时发现产品风险,发布预警信号,减少不良事件发生,保障公众用械安全。
[1] 凌寿佳.医学影像存储与传输系统技术的发展趋势[J].微创医学,2009,4(3):259-262.
[2] 王文生,王鹏程,谢晋东,等.PACS在我国的应用与进展[J].中国医学装备,2008,5(3):59-61.
[3] 黄祥国,李燕,等.医学影像设备学[M].3版.北京:人民卫生出版社,2014:323-324.
[4] 李桂祥,王放,任莉,等.全院PACS/HIS中影像科室工作流程的优化[J].医疗设备信息,2003,18(7):33-35.
[5] 狄幸波,濮俊辉.PACS系统的可靠性分析[J].中国医疗器械信息,2005,11(3):21-23.
[6] 于良宁,赵振平,陈湘云.PACS系统在骨伤科医院的临床应用及维护[J].中国医疗设备,2010,25(9):136-137.
[7] 国家食品药品监督管理总局. 医疗器械软件注册技术审查指导原则 [EB/OL].(2011-08-05)[2015-12-25]. http://www. sda.gov.cn/WS01/CL1421/126244.html.
Analysis of Adverse Event Report of PACS in MAUDE Database
SHAN Xiao-hui1WANG Shu2CHI Ge1ZHAO Xin1SONG Fei3
1 Liaoning Centre for Drug and Medical Device Evaluation and Monitoring (Shenyang 110003)
2 Administrative Service Center, Liaoning Food and Drug Administrative (Shenyang 110003)
3 Shenyang Pharmaceutical University (Shenyang 110016)
The article analyzed the adverse events of PACS which collected from FDA MAUDE database on January 1, 2014 to December 31, 2014 and the characteristics of the adverse events. The safety factors of PACS were discussed, in order to provide effective information for further adverse event monitoring.
picture archiving and communication system, adverse event, analysis
1006-6586(2016)03-0035-04
R197.324
A
2015-11-24
单晓晖,硕士研究生,工程师