原发性肾病综合征相关的可逆性后部脑白质综合征
2016-06-01黄力周岩张志强周玉超孙涛夏正坤程震
黄力 周岩 张志强 周玉超 孙涛 夏正坤 程震
原发性肾病综合征相关的可逆性后部脑白质综合征
黄力1周岩1张志强2周玉超1孙涛3夏正坤3程震1
目的:分析原发性肾病综合征(NS)合并可逆性后部脑白质综合征(PRLS)的特点,探讨NS合并PRLS可能的发病机制和危险因素。方法:回顾性分析7例儿童NS合并PRLS患者的临床、实验室检查及影像学资料。结果:7例患者中,男性4例,女性3例,年龄6~17岁,平均(12.7±3.53)岁,3例未行肾活检,2例行肾活检诊断肾小球足细胞病,2例膜性肾病。尿蛋白定量(4.1±5.4)g/24h,血清白蛋白(21.8±2.7)g/L。发生PRLS前3例(43%)血压正常,4例(57%)发病前有轻度高血压。发生PRLS时,6例临床癫痫大发作,1例为复杂部分性癫痫发作。5例患者行头部CT检查,4例见双侧斑片状低密度灶,1例头部CT正常。7例患者MRI平扫均出现双侧对称的额、顶及枕叶大脑皮层浅部异常信号,在T1WI上呈低信号、T2WI高信号略模糊影,DWI上病变呈低信号。4例(66%)合并急性肾损伤,电解质紊乱者4例(66%),合并感染者4例(66%)。结论:本组发生7例PRLS的患者均为原发性肾病综合征,儿童、轻度高血压、合并电解质紊乱、血清肌酐升高及感染。
肾病综合征可逆性后部脑白质综合征影像学
可逆性后部脑白质综合征(PRLS)是一种临床与影像学综合征,患者常急性起病,以头痛、癫痫发作、视觉异常、精神改变为主要临床表现,影像学常见大脑后部(以顶、枕叶为主)白质血管源性脑水肿,多数病情可逆,预后较好。既往认为其主要诱发因素为严重的高血压导致脑血管病变,其他常见的诱因包括感染、休克、系统性红斑狼疮或有免疫抑制剂如环孢素等应用史。近年临床工作中连续发现多例原发性肾病综合征(NS)患者突发意识丧失、抽搐等表现,影像学检查符合PRLS的特点。现对原发性NS合并PRLS的7例患者进行回顾性分析,探讨此类患者可能的发病机制和危险因素。
对象和方法
研究对象选取2010年~2014年间南京军区南京总医院肾脏科住院的患者,符合以下标准:(1)临床表现NS,排除继发性肾脏疾病,排除既往癫痫病史、肾移植术后、应用环孢素及恶性高血压患者; (2)出现头痛、癫痫发作等神经系统表现,影像学表现局灶性血管源性脑水肿。筛选出符合上述条件的患者7例。根据《中国高血压防治指南》2010年修订版,轻度(Ⅰ级)定义高血压为收缩压140~159 mmHg和(或)90~99 mmHg;中度(Ⅱ级)定义高血压为收缩压160~179 mmHg和(或)100~109 mmHg。儿童高血压诊断参照2010年米杰等[1]制定的中国儿童青少年血压参照标准。
临床观察指标回顾性分析患者的病史,记录临床表现、性别、年龄、血清肌酐、尿素氮、电解质、尿蛋白、血清白蛋白、D-二聚体、血压、病理诊断、治疗、有无感染、发病后头部CT、MRI情况。
影像学方法6例采用GE signa 1.5 T磁共振扫描仪、1例采用Siemens Trio 3T磁共振扫描仪进行影像学检查,检查序列包括轴位T1加权成像(T1WI)和T2加权成像(T2WI)、冠状位T2液体衰减反转恢复(图T2-FLAIR)序列,轴位弥散加权成像(DWI)。5例于15~30d后进行MRI复查。影像学图片均由同一放射科医师通过盲法判读,评价病变位置、分布、异常信号的严重程度等。
统计学方法采用SPSS 13.0软件进行统计分析,计量资料采用均数±标准差表示。
结果
一般资料与用药情况7例患者中,男性4例,女性3例,年龄6~17岁,平均(12.7±3.53)岁。3例发病前血压正常,4例有轻/中度高血压。7例患者均接受免疫抑制剂治疗,其中5例单用泼尼松,1例联合他克莫司3 mg/d(发病前1个月血药谷浓度5.12 ng/ml),1例联合吗替麦考酚酯。发病时4例患者合并感染,2例皮肤感染患者均使用哌拉西林他唑巴坦抗感染,2例肺部感染,其中1例院外使用抗生素不详,1例院外癫痫发作前未使用抗生素(表1)。

表17 例患者的一般临床资料与用药情况
肾脏损害及实验室检查7例患者均为NS,各有2例肾活检诊断为足细胞病和膜性肾病,3例未行肾活检。发生PRLS时,4例合并急性肾损伤,另3例肾功能正常。尿蛋白定量(4.1±5.4)g/24h,血清白蛋白(21.8±2.7)g/L。电解质紊乱4例,低钾、低钠3例,高钾、高钠1例(表2)。
临床表现及影像学检查6例表现癫痫大发作,1例为复杂部分性发作,3例伴头痛,1例伴呕吐,1例发作前有视物模糊。5例患者行头部CT检查,其中4例表现为双侧斑片状低密度灶,1例头部CT正常。7例患者MRI平扫均表现为双侧对称的额、顶及枕叶大脑皮层浅部异常信号,在T1WI上呈低信号、T2WI高信号略模糊影,T2FLAIR像病变边界较明显(图1、2);2例患者病变呈一定占位效应;DWI上病变呈低信号,4例表现为表观弥散系数(ADC)的升高,3例表现为ADC高信号边缘可见低信号。治疗后复查,2例MRI信号的完全恢复正常,3例残留少许T1WI低信号及T2WI高信号影(表3)。
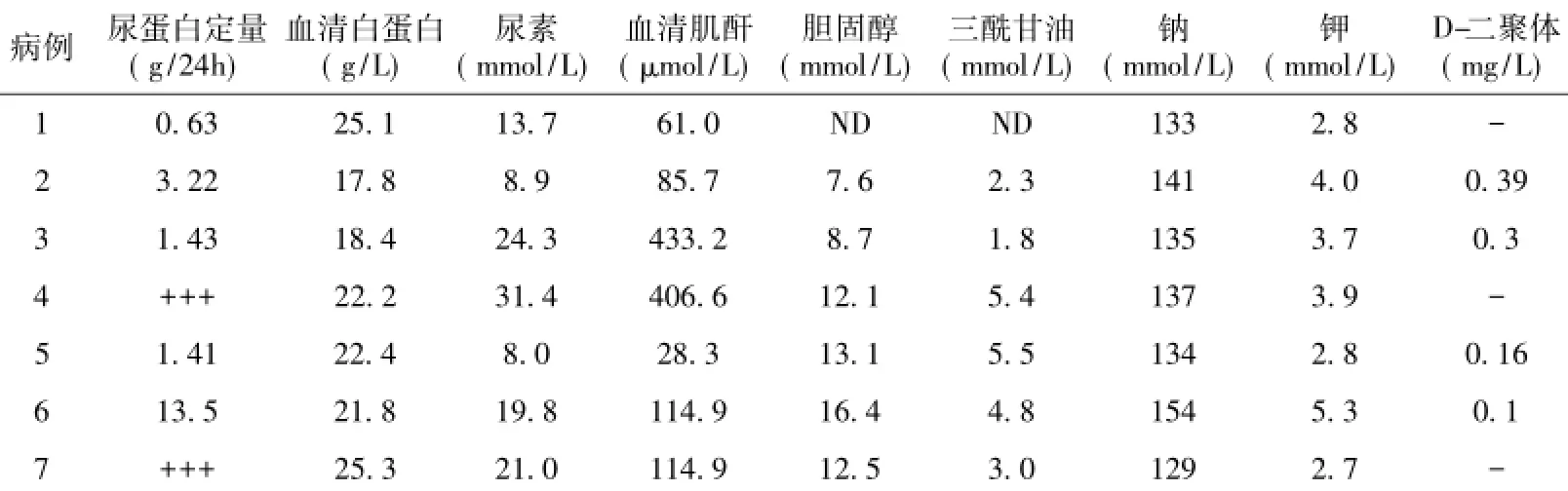
表27 例患者实验室检查

表37 例患者临床表现与影像学检查的对照
治疗及预后急性发作时给予脱水、降压、抗癫痫等对症支持治疗,意识恢复后给予口服丙戊酸钠/卡马西平,直至复查影像学病灶基本消失后停药,神经系统症状均能得到控制,无反复发作。2例患者合并急性左心心力衰竭,1例接受连续性肾脏替代治疗(CRRT)后心力衰竭纠正,后加用激素肾脏疾病获得缓解,另一例患者家属因经费问题放弃治疗,出院后失随访。余5例患者门诊随访NS均获完全缓解,未再发神经系统症状,无后遗症。
讨论
1996年,Hinchey等[2]首先提出PRLS起初发现继发于肾功能不全、免疫抑制剂治疗或高血压患者,原发病包括高血压脑病、子痫、血栓性微血管病、肾移植术后等[3-10],病例报道增多逐渐拓展了对这一概念的认识。由于病变的部位并不局限于后部脑及脑白质,有文献提出了后部可逆性脑病综合征(PRES)、高灌注脑白质病、可逆性后部脑水肿综合征等名称描述此类临床综合征。
PRLS逐渐受到关注归功于目前的影像学发展,PRLS患者的头部CT无特异性,部分患者CT检查可完全正常。MRI DWI序列结合ADC有助于PRLS的诊断和鉴别诊断及判断预后[11-12]。MRI表现为T1WI低信号及T2WI高信号;特异的DWI等或低信号、ADC升高提示血管源性水肿[12],随着PRLS病情发展而无有效治疗,呈现DWI高信号,疾病由可逆的血管源性水肿发展为不可逆的细胞毒性水肿,提示预后不良[13]。
血管源性水肿的发病机制尚不明确,目前有“高灌注”学说和“内皮损伤”学说。当全身血压在一定范围内波动时,脑部血管可进行自身调节以维持恒定的脑部供血,当血压升高超过脑血流自动调节的阈值(中心动脉压>140 mmHg)时,自身调节将被破坏,引起脑血管的高灌注。免疫抑制剂(如环孢素、他克莫司)直接损伤内皮、促进内皮细胞产生内皮素、前列环素、血栓烷A等缩血管物质[14-19],血栓性微血管病的患者血管内微血栓形成致使脑动脉闭塞、缺血、缺氧引起内皮细胞损伤,被认为是此类患者发生PRLS的主要机制。
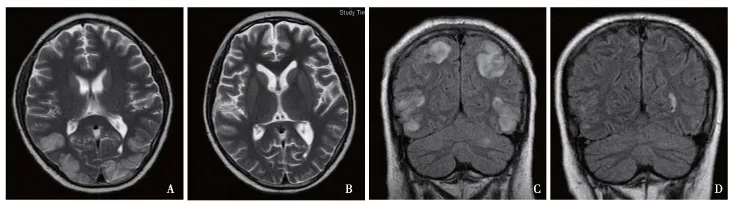
图1 例3患者治疗前后头部MRI(T2WI)
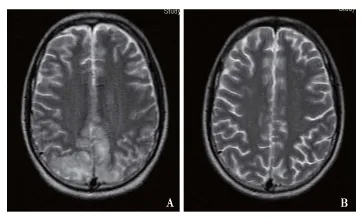
图2 例2患者治疗前后头部MRI(T2WI)
本研究是目前为止最大样本的原发性NS导致的PRLS病例总结。与既往报道不同的是,高血压与免疫抑制剂似乎不是本组患者PRLS的最主要原因。7例患者中,3例发病前血压正常,血压偏高的4例患者也远远达不到高血压脑病的诊断标准;7例患者均未使用环孢素A,虽有文献报道他克莫司可诱发本病,但本文的1例患者发病时血药浓度不高,病情好转后再次服用未再发生神经系统病变。目前暂无口服糖皮质激素与PRLS相关性的报道,在NS合并PRLS的患者中,均同时合并激素治疗,本文观察的7例患者中,除1例放弃治疗后失随访外,另6例患者发生PRLS后未停用激素,积极治疗后症状也可缓解。因此高血压和药物不是引起本研究中患者发生PRLS的主要原因,国内外文献也有类似报道[20-23]。
NS患者血浆胶体渗透压降低、血管通透性增加[24],易引起组织水肿,引起脑部血管源性水肿;体内存在的免疫炎症状态、氧化应激等均可造成血管内皮细胞损伤[25-26],为发生PRLS的高危因素。本研究中有3例患者完善了内皮相关指标的检查,其VCAM均高于正常值,我们推测NS状态下脑组织的水肿和内皮损伤可能在PRLS的发生发展中起到重要作用。在此基础上,轻度的血压升高即可成为诱发脑病的危险因素。本组7例患者中,4例合并急性肾损伤、4例合并感染、4例合并电解质紊乱,这些因素可能参与了血管源性脑水肿的发生,本研究的7例患者均是未成年人,提示可能儿童NS患者更容易发生此类疾病。内皮细胞是构成血脑屏障的主要结构,儿童NS患者PRLS发病率高是否与儿童的血脑屏障的通透性比成年人高有关,仍有待进一步研究。
该报道的7例患者中,有3例完善了MRV检查排除了静脉窦血栓形成,另4例患者D-二聚体正常未行相关检查。因NS的患者体内高凝状态,合并神经系统症状时,建议行D-二聚体检查,在完善头部核磁的同时行头部MRV排除静脉窦血栓形成。
PRLS并非完全可逆,本病早期为可逆性的血管源性脑水肿病理过程,但延误治疗有可能造成神经细胞进一步损害至不可逆变性死亡。有文献报道1例PRLS患者早期抽搐反复发作处理不及时[27],最后遗留皮质盲,另外1例开始发作时神经系统损害症状可恢复,后期由于原发病不能控制,发作逐渐频繁,神经系统损害进行性加重,最后昏迷死亡。本组7例患者由于及时处理,未出现抽搐反复发作,但2例出现急性左心心力衰竭,1例同时合并血清肌酐升高,提示我们再这类患者的治疗中,更应积极处理原发病,密切监测容量状态,警惕伴发心力衰竭、急性肾损伤等并发症。
本文总结7例原发NS合并PRLS的患儿,发病时合并血压轻度升高、电解质紊乱、血清肌酐升高、感染等因素,可能与诱发可逆性后部脑白质病有关。NS患者突发头痛、抽搐等神经系统的症状,应想到PRLS的可能,早期识别、及时处理多数患者预后较好。
1米杰,王天有,孟玲慧,等.中国儿童青少年血压参照标准的研究制定.中国循证儿科杂志,2010,5(1):4-14.
2Hinchey J,Chaves C,Appignani B,et al.A reversible posterior leukoencephalopathy syndrome.N Engl J Med,1996,334(8): 494-500.
3Hauser RA,Lacey DM,Knight MR.Hypertensive encephalopathy: magnetic resonance imaging demonstration of reversible cortical and white matter lesions.Arch Neuro,1988,45(10):1078-1083.
4Duncan R,Hadley D,Bone I,et al.Blindness in eclampsia:CT and MR imaging.J J Neurol Neurosurg Psychiatry,1989,52(7):899-902.5Raroque HG Jr,Orrison WW,Rosenberg GA.Neurologic involvement in toxemia of pregnancy:reversible MRI lesions.Neurology,1990,40 (1):167-169.
6Hughes RL.Cyclosporine-related central nervous system toxicity in cardiac transplantation.N Engl J Med,1990,323(6):420-421.
7Freise CE,Rowley H,Lake J,et al.Similar clinical presentation of neurotoxicity following FK 506 and cyclosporine in a liver transplant recipient.Transplant Proc,1991,23(6):3173-3174.
8EidelmanBH,Abu-ElmagdK,WilsonJ,etal.Neurologic complications of FK 506.Transplant Proc,1991,23(6):3175-3178.
9Merimsky O,Chaitchik S.Neurotoxicity of interferon-alpha.Anticancer Drugs,1992,3(6):567-570.
10 Cohen RB,Abdallah JM,Gray JR,et al.Reversible neurologic toxicity in patients treated with standard-dose fludarabine phosphate for mycosis fungoides and chronic lymphocytic leukemia.Ann Intern Med,1993,118(2):114-116.
11 Bartynski WS.Posterior Reversible Encephalopathy Syndrome,part 2: controversies surrounding pathophysiology of vasogenie edema.AJNR Am J Neuroradiol,2008,29(6):1043-1049.
12 Horbinski C,Bartynski WS,Carson-Walter E,et al.Reversible Encephalopathy after Cardiac Transplantation:histologic evidence of endothelialactivation,t-cellspecifictrafficking,andvascular endothelial growth factor expression.AJNR Am J Neuroradiol,2009,30 (3):588-590.
13 StottVL,HurrellMA,AndersonTJ.Reversibleposterior leukoencephalopathy syndrome:a misnomer reviewed.Intern Med J,2005,35(2):83-90.
14 Benigni A,Morigi M,Perico N,et al.The acute effect of FK506 and cyclosporine on endothelial cell function and renal vascular resistance.Transplantation,1992,54(5):775-780.
15 Fogo A,Hakim RC,Sugiura M,et al.Severe endothelial injury in a renal transplant patient receiving cyclosporine.Transplantation,1990,49(6):1190-1192.
16 Zoja C,Furci L,Ghilardi F,et al.Cyclosporininduced endothelial cell injury.Lab Invest,1986,55(4):455-462.
17 Bunchman TE,Brookshire CA.Cyclosporine-induced synthesis of endothelin by cultured human endothelial cells.J Clin Invest,1991,88 (1):310-314.
18 Shutter LA,Green JP,Newman NJ,et al.Cortical blindness and white matter lesions in a patient receiving FK506 after liver transplantation.Neurology,1993,43(11):2417-2418.
19 Mueller AR,Platz KP,Bechstein WO,et al.Neurotoxicity after orthotopic liver transplantation:a comparison between cyclosporine and FK506.Transplantation,1994,58(2):155-170.
20 Aksoy DY,Arici M,Kiykim AA,et al.Posterior leukoencephalopathy syndrome and nephrotic syndrome:just a coincidence?Am J Med Sci,2004,327(3):156-159.
21 Yu EC,Wong SN,Yeung CY.Encephalopathy associated with steroid treated nephrotic syndrome.Int J Pediatr Nephrol,1987,8(3): 135-146.
22 Li Looi J,Christiansen JP.Reversible posterior leukoencephalopathyassociated with minimal change nephrotic syndrome.NZMJ,2006,119 (1243):U2257.
23都娟,赵晓燕,刘伟力,等.儿童肾病综合征并发可复性后部脑病综合征2例.解放军医学杂志,2001,36(12):1379.
24 Rostoker G,Behar A,Lagrue G.Vascular hyperpermeability in nephrotic edema.Nephron,2000,85(3):194-200.
25 Joles JA,Stroes ES,Rabelink TJ.Endothelial function in proteinuric renal disease.Kidney Int Suppl,1999,71:S57-61.
26 Dogra GK,HerrmannS,IrishAB,etal.Insulinresistance,dyslipidaemia,inflammation and endothelial function in nephritic syndrome.Nephrol Dial Transplant,2002,17(12):2220-2225.
27郝红琳,刘秀琴,黄颜,等.可逆性后部脑病综合征的病因、临床及影像学特点.中国医学杂志,2009,89(17):1171-1174.
Primary nephritic syndrome complicated posterior leukoencephalopathy syndrome
HUANG Li1,ZHOU Yan1,ZHANG Zhiqiang2,ZHOU Yuchao1,SUN Tao3,XIA Zhengkun3,CHENG Zhen11National Clinical Research Center of Kidney Diseases,Jinling Hospital,Nanjing University School of Medicine,Nanjing 210016,China
2Department of medical Imaging,Jinling Hospital,Nanjing University School of Medicine,Nanjing 210016,China3Department of Pediatric,Jinling Hospital,Nanjing University School of Medicine,Nanjing 210016,China
CHENG Zhen(E-mail:chengzhen33@189.cn)
Objective:To investigated the clinical and neuroimaging features of patients with primary nephritic syndrome who developed reversible posterior leukoencephalophathy syndrome(PRLS),and to characterize the risk factors of PRLS in these patients.Methodology:The clinical and neuroimaging features of seven patients with PRLS were analyzed retrospectively.Results:They were 4 males and 3 females with an average age of(12.7±3.53)years old.The mean urine protein was(4.1±5.4)g/24h,and serum albumin was(21.8±2.7)g/L.Among them,4 cases accompanied with acute kidney injury,4 cases had electrolyte disorders,and 4 cases complicated with infection.4 cases received renal biopsy,and the histological diagnosis was minimal change disease in 2 cases,and membranous nephropathy in other 2 cases.3 patients had normal blood pressure,and the other 4 cases have mild hypertension.6 cases manifested as tonicclonic seizures,and one case showed as complex partial seizure.5 patients underwent CT examination,4 cases showed bilateral patchy low density foci,and one showed no abnormity.For the first MRI scan,all the 7 cases showed bilateral symmetry abnormal signal on the cerebral cortex of frontal lobe,parietal lobe and occipital lobe,with low signal on T1WI,high signal on T2WI.Conclusion:Our data suggested that the idiopathic nephritic syndrome patients with younger or children,with high pressure,with electrolyte disturbance,with elevated serum creatinine,and with infection are more susceptible to PRLS.
nephritic syndromereversible posterior leukoencephalophathy syndromeneuroimaging
2015-05-25
(本文编辑律舟凡心)
10.3969/cndt.j.issn.1006-298X.2016.01.002
国家科技支撑计划课题(2013BAI09B04,2015BAI12B05),江苏省临床医学科技专项(BL2012007)
1南京军区南京总医院国家肾脏疾病临床医学研究中心全军肾脏病研究所(南京210016),2影像科,3儿科
程震(E-mail:chengzhen33@189.cn)
2016年版权归《肾脏病与透析肾移植杂志》编辑部所有
