不同厂家及批次麻黄配方颗粒质量差异的研究
2016-05-18汪贤梅张志强
汪贤梅,张志强,唐 方
(1.天津医科大学总医院中医科,天津300052;2.天津红日药业股份有限公司,天津301700)
论著
不同厂家及批次麻黄配方颗粒质量差异的研究
汪贤梅1,张志强2,唐 方1
(1.天津医科大学总医院中医科,天津300052;2.天津红日药业股份有限公司,天津301700)
目的:考察不同厂家及不同批次麻黄配方颗粒剂质量差异。方法:采用红外光谱(FTIR)法明确麻黄颗粒剂与麻黄对照药材成分的相似度;高效液相色谱法(HPLC)对其主要生物碱成分麻黄碱和伪麻黄碱进行含量测定,分析柱:WondaSil C18(250 mm×4.6 mm,5 μm),流动相:乙腈-0.3%磷酸溶液(含0.05%三乙胺)(4∶96,v:v),流速:1.0 mL·min-1,柱温:30℃,检测波长:210 nm。结果:不同厂家各批次麻黄配方颗粒与麻黄对照药材红外特征图谱的相似度≥92%;不同品牌麻黄颗粒剂中,麻黄碱和伪麻黄碱含量存在显著性差异(P<0.01);同厂家不同批次麻黄颗粒剂中麻黄碱和伪麻黄碱含量间存在差异,有统计学意义(P<0.05,P<0.01)。结论:不同厂家、同厂家不同批次麻黄配方颗粒剂中麻黄碱和伪麻黄碱含量存在显著差异。
麻黄配方颗粒剂;红外光谱;高效液相色谱法;麻黄碱;伪麻黄碱
中药配方颗粒是一种有别于传统中药饮片的新型制剂,通过现代制药技术制成的单味中药制剂[1]。目前我国批复试点生产中药配方颗粒的企业共6家,均已具备独立的质量标准和工艺规范。该产品与传统饮片水煎剂相比,其便于携带、储存、调配等优势,正逐渐受到医疗市场的认可、推广与使用。但由于配方颗粒剂生产企业缺乏统一、规范化生产工艺及统一的质量标准,导致同品种存在规格不一、等效剂量不一等问题。目前有5家企业生产的麻黄配方颗粒剂在医疗市场流通,但尚未有对不同厂家及同厂家不同批次间样品比较的报道。本试验选取其中3个企业共6批次的麻黄配方颗粒剂,通过红外光谱技术对其进行定性鉴别,并采用高效液相色谱法(HPLC)测定其主要有效成分麻黄碱和伪麻黄碱的含量,以比较其存在的差异,为产品质量控制提供依据,也为不同品牌配方颗粒剂在临床中交互应用提供便利。
1 材料与方法
1.1 材料
1.1.1 仪器 Spectrum Two IR(PerkinElmer公司);FW-5压片机(天津博天胜达科技发展有限公司);岛津LC-2010AHT高效液相色谱仪【四元泵、SPD-10AVP紫外检测器、COT-10AVP柱温箱、WondaSil C18(250 mm×4.6 mm,5 μm)(岛津企业管理(中国)有限公司)】。
1.1.2 试药及试剂 盐酸麻黄碱对照品(批号:171241-201007)、盐酸伪麻黄碱对照品(批号: 171237-201208)由中国食品药品检定研究院提供;草麻黄对照药材(批号:121051-201005)由中国食品药品检定研究院提供。甲醇、乙腈均为色谱纯(赛默飞世尔科技(中国)有限公司),屈臣氏蒸馏水(广州屈臣氏食品饮料有限公司),其它试剂均为市售分析纯。麻黄配方颗粒剂分别购自天津红日康仁堂(KRT)药业销售有限公司,批号:14006411(KRT1)、14017809(KRT2);四川新绿色(LS)药业科技发展股份有限公司,批号:13070157(LS1)、14030117(LS2);江阴天江(TJ)药业有限公司,批号:1309118(TJ1)、1403125(TJ2)。样品基源均标注为草麻黄。
1.2 方法
1.2.1 FTIR (1)仪器参数:光谱范围4000~400cm-1,分辨率4cm-1,信号扫描累加次数4次,自动增益,自动大气背景扣除。(2)测定方法:取样品粉末(过9号筛)约1.5 mg加溴化钾200 mg,压片,待测。每个样品取样4次测定,求取其平均光谱进行数据分析。
1.2.2 HPLC
1.2.2.1 色谱条件及系统适用性[2-6]:色谱柱:WondaSil C18(250mm×4.6mm,5μm),流动相:乙腈-0.3%磷酸溶液(含0.05%三乙胺)(4∶96,v:v),流速:1.0 mL·min-1,柱温:30℃,检测波长:210 nm。
1.2.2.2 对照品溶液制备:取盐酸麻黄碱对照品和盐酸伪麻黄碱对照品,精密称定,加甲醇制成1 mL约含盐酸麻黄碱和盐酸伪麻黄碱各40 μg的混合对照品溶液,备用。
1.2.2.3 供试品溶液制备:取麻黄配方颗粒剂粉末0.25 g,精密称定,置具塞锥形瓶中,精密加入1.44%磷酸溶液50 mL,称定质量,超声处理(功率600 W,频率50 kHz)20 min,冷却,再称定质量,用1.44%磷酸溶液补足减失的质量,摇匀,滤过,取续滤液,即得。
1.2.2.4 专属性试验:分别取对照品溶液10 μL和供试品溶液5 μL,按照“1.2.2.1”项下色谱条件进样测定。
1.2.2.5 线性范围考察:精密吸取对照品贮备液分别以 1、2、4、6、8、10、12、14、16 μL进样,按照“1.2.2.1”项下色谱条件进样测定。
1.2.2.6 精密度试验:取盐酸麻黄碱和盐酸伪麻黄碱混合对照品溶液,按照“1.2.2.1”项下色谱条件进样测定,连续进样6次,进样量10 μL,记录峰面积和保留时间。
1.2.2.7 重复性试验:取厂家KRT1麻黄配方颗粒剂粉末6份,按“1.2.2.3”项下方法制备供试品溶液,按照“1.2.2.1”项下色谱条件进样10 μL测定,记录峰面积并计算含量。
1.2.2.8 稳定性试验:取厂家TJ1麻黄颗粒剂供试品溶液,按照“1.2.2.1”项下色谱条件,分别于0、2、4、6、8、12、24 h进样10 μL测定,记录峰面积和保留时间。
1.2.2.9 加样回收率试验:取已测知含量的厂家KRT1麻黄颗粒剂粉末6份,精密称定,分别精密加入一定量的盐酸麻黄碱和盐酸伪麻黄碱对照品溶液,按“1.2.2.3”项方法制备供试品溶液,按照“1.2.2.1”项下色谱条件,进样10 μL测定,记录峰面积并计算回收率。
1.2.2.10 样品含量测定:6批次麻黄配方颗粒剂,按“1.2.2.3”项方法制备供试品溶液,按照“1.2.2.1”项下色谱条件,各进样5 μL进行测定,记录峰面积并计算含量。
1.3 统计学方法 采用SPSS 18.0统计软件分析,计量资料以s表示,组内比较采用t检验,组间比较用单因素方差分析,P<0.05具有统计学意义。
2 结果
2.1 FTIR结果 不同厂家、不同批次麻黄配方颗粒与草麻黄对照药材(r=1)红外特征图谱相比较,相似度均不低于92%,即3个厂家麻黄配方颗粒剂在大生产过程中,其有效药用成分保留相对完整(图1)。
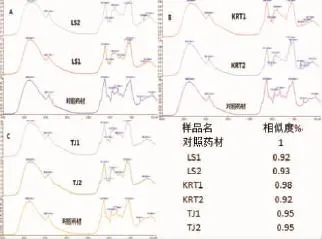
图1 配方颗粒剂与对照药材红外图谱比较Fig 1 Comparison of IR fingerprint about formula particles and contrast medicinal material
2.2 HPLC
2.2.1 专属性试验结果 按照HPLC测定方法及相应浓度,绘制色谱图,见图2。由图可知,该色谱条件下,盐酸麻黄碱保留时间为19.726 min,盐酸伪麻黄碱保留时间为21.649 min,峰形良好,且与其他峰分离较好。
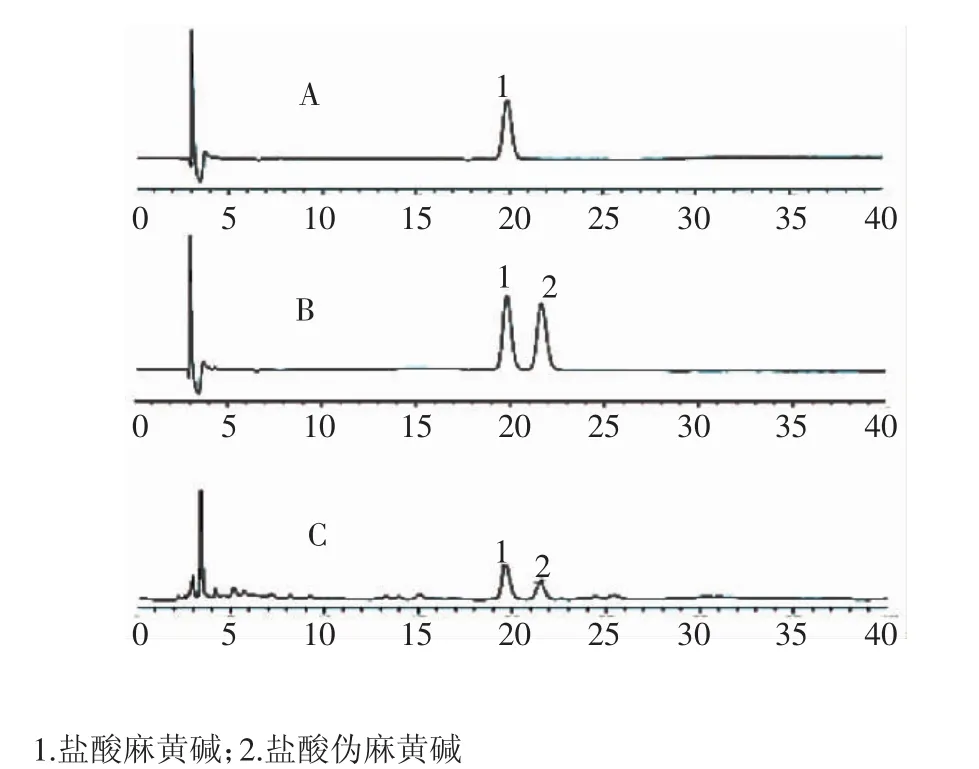
图2 盐酸麻黄碱对照品(A)、混合对照品(B)及其样品(C)HPLC图Fig 2 HPLC chromatograms of reference substance(A),mixed reference substances(B)and sample(C)
2.2.2 线性范围考察结果 以进样量(X)为横坐标、峰面积(Y)为纵坐标,绘制标准曲线,得到盐酸麻黄碱和盐酸伪麻黄碱的回归方程分别是:Y= 108 242X+2 046.2(r=0.999 7,n=7);Y=104 371X+ 14 018(r=0.999 9,n=7)。表明盐酸麻黄碱和盐酸伪麻黄碱分别在0.05~0.74 μg、0.04~0.71 μg成良好的线性关系。
2.2.3 精密度试验结果 盐酸麻黄碱和盐酸伪麻黄碱的保留时间的RSD分别是0.76%和0.83%,峰面积的RSD分别是1.22%和0.91%,均小于2%,说明仪器的精密度良好。
2.2.4 重复性试验结果 盐酸麻黄碱和盐酸伪麻黄碱含量的RSD(n=6)分别是1.01%和0.65%,表明本方法重复性良好。
2.2.5 稳定性试验结果 盐酸麻黄碱和盐酸伪麻黄碱的保留时间的RSD分别是0.66%和0.71%,峰面积的RSD分别为0.22%和0.52%(n=7),表明供试品溶液在24 h内稳定。
2.2.6 加样回收率试验结果 盐酸麻黄碱和盐酸伪麻黄碱平均回收率分别为96.27%、103.37%,RSD分别为0.40%和1.00%(n=6)。
2.2.7 样品含量结果 如表1所示,不同品牌麻黄颗粒剂中,麻黄碱和伪麻黄碱含量存在显著性差异(P<0.01);同厂家不同批次麻黄颗粒剂中麻黄碱和伪麻黄碱含量间存在差异,有统计学意义(P<0.05,P<0.01)。

表1 不同厂家及批次麻黄配方颗粒剂中麻黄碱和伪麻黄碱含量(mg·g-1)(n=4)Tab 1 The content of ephedrine and d-pseudephedrine in mahuang formula granules from different factories and batches(mg·g-1)(n=4)
3 讨论
本研究首先采用FTIR测定麻黄颗粒剂与对照药材成分的相似度,结果显示,3个厂家6个批次麻黄配方颗粒与麻黄对照药材的红外特征图谱相似度≥92%,提示各厂家在药用有效成分保留上相对完整,且同一厂家不同批次麻黄颗粒剂红外特征图谱相似度比较相似度差异<10%,提示各厂家质量控制相对稳定。虽然麻黄配方颗粒保留了麻黄饮片的水煎液的物质基础,但仅以大生产过程中成分保留相对完整作为评价麻黄配方颗粒达到“全成分转移”的质控标准并不十分完善。
为此,在药用有效成分对比分析基础上,利用HPLC技术对不同厂家及批次麻黄配方颗粒样品进行了主成分含量比较。结果显示,不同厂家间及部分厂家不同批次间麻黄碱和伪麻黄碱含量均存在差异,这与文献报道[7-8]由于工艺不同导致配方颗粒剂主成分含量存在显著性差异相吻合。另外,各厂家颗粒剂在外观性状上也存在差异。以上结果证实工艺间缺乏统一性、规范化标准是影响各厂家相同产品主成分含量不一,不同厂家同产品间难以交互通用的主要因素。提示以中药红外指纹图谱对配方颗粒成分结构给予的定性鉴别,与高效液相色谱法对配方颗粒主成分含量的定量分析相结合是完善质控标准,保证产品质量的必要措施。
2010版《中国药典》收载的麻黄为草麻黄Ephedra sinica Stapf、中麻黄 Ephedra intermedia Schrenk et C.A.Mey.或木贼麻黄Ephedra equisetina Bge.的干燥草质茎[9],目前市售麻黄药材多把3种麻黄混同使用,以草麻黄为主。大量文献报道[10-12],中药材的产地、种属等都会影响药物主成分含量。本课题前期研究结果证实:麻黄种属与主成分麻黄碱、伪麻黄碱含量的变化呈显著正相关,且种属间存在极显著差异(P<0.01)。由此提示,制定配方颗粒剂相关企业统一的质控标准和工艺规范,是提高配方颗粒剂质量的重要措施。而科学规范地确认、选择药材资源亦是确保麻黄配方颗粒剂主成分含量相对稳定的又一重要措施。
[1]马露,邵利洁,唐方.厚朴配方颗粒药效学评价方法初探[J].中国中药杂志,2014,39(8):1490
[2]冯欣,周刚,王茜,等.HPLC法测定藏药五味甘露药浴颗粒中槲皮素、山柰素和盐酸麻黄碱[J].中成药,2015,37(1):120
[3]刘睿,王宁,刘志辉.RP-HPLC同时测定宣肺止咳口服液中盐酸麻黄碱、盐酸伪麻黄碱及苦杏仁苷含量[J].中国实验方剂学杂志,2011,17(16):91
[4]太成梅,那微,赵晓霞,等.HPLC法测定小儿肺热咳喘口服液中盐酸麻黄碱及盐酸伪麻黄碱的含量[J].中国药品标准,2010,11(5):380
[5]宋玉国,张新茹,李秀芬,等.HPLC测定清咳平喘颗粒中盐酸麻黄碱和盐酸伪麻黄碱的含量[J].中国现代中药,2014,16(4):319
[6]曾永长,张莉,曾晓燕,等.HPLC法测定馥感啉口服液中盐酸麻黄碱和盐酸伪麻黄碱的含量[J].中药新药与临床药理,2015,26(2):252
[7] 蔡乐,刘萍,郭桂明,等.不同厂家茜草配方颗粒中大叶茜草素含量的比较[J].北京中医药,2011,30(11):856
[8]陈晓鹏,鄂秀辉,夏忠庭,等.HPLC法同时定量测定养血清脑颗粒中7个主要成分[J].中成药,2013,35(9):1921
[9]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010:300-301
[10]游元元,万德光,杨文宇,等.HPLC法比较不同产地桑叶药材品质差异[J].中国药房,2010,12(35):3314
[11]盛萍,张立福,时晓娟,等.麻黄药材中麻黄碱含量与产地生态环境关系的初步研究[J].中医药信息,2014,2(2):1
[12]姜秋,李慧芬,梁晓,等.HPLC同时测定不同产地远志饮片中6种寡糖酯类成分[J].中成药,2015,37(2):360
(2015-09-20收稿)
Research on the quality differences of mahuang formula grarules between different manufacturers and batches
WANG Xian-mei1,ZHANG Zhi-qiang2,TANG Fang1
(1.Department of Traditional Chinese Medicine,General Hospital,Tianjin Medical University,Tianjin 300052,China;2.Tianjin Chase Sun Pharmaceutical.,TLD,Tianjin 301700,China)
Objective:To compare qualities of mahuang formula particles from different manufacturers and batches.Methods:First of all,the similarity of contrast medicinal material and mahuang formula granules of different manufacturers was defined by using the FTIR fingerprint.Then content of ephedrine and d-pseudephedrine in mahuang formula granules was determined with HPLC,chromatographic column was WondaSil C18(250 mm×4.6 mm,5 μm),the mobile phase was V(methylcyanide):V(0.3%ammonium dihydrogen phosphate solution including 0.05%triethylamine)=4∶96,flow rates was 1.0 mL·min-1,the temperature was 30℃,and length of detection wave was 210 nm.Results:FTIR showed the similarity of all components between each sample and contrast medicinal material were higher than 92%.Comparison between different manufacturers,there were significant differences between ephedrine and d-pseudephedrine (P<0.01);comparison of different batches of the same manufacturer,there were differences of pehedrine and d-pseudephedrine,with statistical significance(P<0.01,P<0.05).Conclusion:The contents of ephedrine and d-pseudephedrine of all samples from different manufacturers and different batches are significantly different.
mahuang formula granules;FTIR;HPLC;ephedrine;d-pseudephedrine
R92
A
1006-8147(2016)02-0168-03
汪贤梅(1989-),女,硕士在读,研究方向:中药有效成分含量分析;通信作者:唐方,E-mail:zhongyi3599@sina.com。
