艾纳香油质量标准初步研究
2016-05-14胡璇陈振夏王凯黄梅吴丽芬庞玉新
胡璇 陈振夏 王凯黄梅 吴丽芬 庞玉新

摘 要 以不同批次的艾纳香油为对象,通过观察其外观性状,测定其溶解性、比旋度以及相对密度等物理特性,并采用薄层层析法(TCL)和气相(GC)指纹图谱对收集的艾纳香油成分进行定性分析,对艾纳香油的质量标准进行初步研究。结果表明:艾纳香油为澄清、棕红色的液体,有特异的芳香气,易溶于乙醇、氯仿、乙醚,几乎不溶于水,比旋度宜为-26°~-30°,相对密度宜为0.94~0.98,β-石竹烯和l-龙脑TCL斑点清晰,分离良好,GC指纹图谱得到17个共有峰,均含有有效成分β-蒎烯、芳樟醇、樟脑、l-龙脑、β-石竹烯,相似度均在0.90以上。分析检测方法简便、可靠,可为艾纳香油的质量控制提供参考依据。
关键词 艾纳香油 ;物理性状 ;薄层色谱 ;GC指纹图谱 ;质量控制
中图分类号 O656.6 文献标识码 A Doi:10.12008/j.issn.1009-2196.2016.09.018
Abstract Different batches of Blumea Balsamifera Oil were sampled to observe their appearant traits and determine their physical traits such as solubility, specific rotation, relative density ratio, etc. Qualitative analysis was made of the samples by using thin layer chromatography (TLC) and gas chromatography (GC) finger-print. The results showed that B. balsamifera oil was pellucid and red-brown with specific aroma. It was easily dissolved in ethanol, trichloromethane, diethyl ether, almost insoluble in water. Its specific rotation was between -26°~30°, and the density ratio between 0.94~0.98. TLC spots of β-caryophyllene and l-borneol were clear and separated well. Seventeen common peaks were collected and all contained the effective constituents of β-pinene, linalool, camphor, l-borneol and β-caryophyllene, with their similarities being higher than 0.90. These two methods were simple and reliable and can be used for providing reference and basis for the quality control of B. balsamifera Oil.
Keywords Blumea Balsamifera oil ; physical properties ; TLC ; GC finger-print ; quality control
艾纳香为菊科植物艾纳香Blumea Balsamifera (L.) DC.的新鲜或干燥地上部分,俗称“娜龙” (黎药名)、“大风艾”,具有祛风除湿、温中止泻、活血解毒等功效,广泛分布于海南、贵州、广西、广东等省区[1-2]。艾纳香主要作为提取艾粉、艾片和艾纳香油的原料,具有悠久的使用历史,其新鲜茎叶经提取加工制成的结晶为艾片(左旋龙脑)[3],在精制艾片的过程中,粗提物经压榨分离而得到的油即为艾纳香油,艾纳香油中主要含有l-龙脑、β-石竹烯、樟脑、α-蒎烯、β-蒎烯、柠檬醇、芳樟醇等活性成分,分别具有发汗、镇惊、平喘、强心、镇咳、驱虫、祛痰、抗病毒、抗菌等作用[4]。
艾纳香油被广泛应用于药品和化妆品行业,以艾纳香油为主要成分的产品大量涌现,例如艾纳香咽立爽滴丸、银丹脑心通软胶囊、心胃止痛胶囊、金喉喷健雾剂、银冰消痤酊、复方一支黄花喷雾剂等[5],它的独特功效已得到广大消费者的认可。目前,艾纳香油的研究主要集中在单一化学成分以及毒理药理研究方面[6-7],缺少关于艾纳香质量控制的相关研究报道。本文以收集不同批次的艾纳香油为对象,对其相关物理性状进行观察和测定,并对其有效成分进行定性分析,为艾纳香油在生产应用中的质量控制提供参考依据。
1 材料和方法
1.1 材料
1.1.1 样品
艾纳香油样品分别来源于贵州省艾源生态药业开发有限公司(S1-S6、S12、S13),贵州省江口县苗药生物科技有限公司(S7-S8),贵州利生香中药科技有限公司(S9-S10),湖北丹圣医药科技有限公司(S11),经中国热带农业科学院庞玉新副研究员鉴定为菊科植物艾纳香Blumea Balsamifera (L.) DC.的提取物艾纳香油。
1.1.2 仪器与试剂
Agilent 7890A气相色谱仪(配有氢火焰离子化检测器FID)(载气高纯氮气,助燃气为空气,燃气为氢气),HP-5毛细管柱(30 m×0.32 mm,0.25 μm),OpenLAB CDS 工作站,G4513A自动进样器;电子天平(Sartorius公司); WZZ-2S自动数显旋光仪(上海精密仪器仪表有限公司)。
对照品β-蒎烯(纯度≥98%,批号:P-011-131204,购自成都瑞芬思生物科技有限公司);芳樟醇(纯度≥98.74%,批号:2N1117BC13,购自上海源叶生物科技有限公司);樟脑(纯度≥98%,批号:21506,购自Aladdin公司);l-龙脑(纯度≥98%,批号:10147015,购自Alfa Aesar公司);β-石竹烯(纯度≥98.8%,批号:201001,购自中国食品药品检定研究院);乙酸乙酯为色谱纯(Fisher Scientific公司),其它试剂均为分析纯。
1.2 方法
1.2.1 理化性质
1.2.1.1 溶解性
按《中国药典》[3]2015版一部凡例中“性状”项下对溶解度的测定法:取各批次艾纳香油1 mL,置试管中,分别加入不同体积蒸馏水、乙醇、氯仿、乙醚,每隔5 min强力振摇30 s,观察30 min内的溶解情况。
1.2.1.2 比旋度
按《中国药典》[3]2015版一部附录Ⅶ E旋光度测定法:在20℃的条件下,取艾纳香油1 g,精密称定,置50 mL容量瓶中,加入乙醇至刻度定容,摇匀,备用。每次测定前以乙醇作空白校正,测定后,再校正1次,以确定在测定时零点有无变动;如第2次校正时发现零点有变动,则应重新测定旋光度。将测定管用艾纳香油供试液冲洗数次,缓缓注入艾纳香油供试液适量(勿使发生气泡),置于旋光计内检测读数,即得供试液的旋光度。用同法对每份样品测定旋光度3次,取3次的平均数,即得供试品的比旋度。
1.2.1.3 相对密度
参照《中国药典》[3]2015版一部附录Ⅶ A相对密度测定第二法:取20℃时相对密度等于1的韦氏比重秤,将新沸过的冷水倒入所附玻璃圆筒至八分满,不断搅动玻璃圆筒内的水(置于20℃的水浴中),使之温度调至20℃,将悬于秤端的玻璃锤慢慢浸入圆筒内的水中,游码悬挂于秤臂右端1.000 0处,调节秤臂左端的螺旋使平衡,倾去玻璃圆筒内的水,拭干,加入艾纳香油至相同的高度,并用同样的方法调节温度,将玻璃锤拭干后浸入艾纳香油中,通过调节游码在秤臂上的数量与位置使之平衡,数值读取,即得艾纳香油的相对密度。
1.2.2 TCL鉴别
1.2.2.1 对照品溶液的制备
取l-龙脑对照品、β-石竹烯对照品适量,分别加乙醇制成每1 mL含3、2、1 mg的溶液,作为对照品溶液。
1.2.2.2 供试品溶液的制备
称取25.0 mg艾纳香油样品,加乙醇4 mL使其溶解,作为供试品溶液。
1.2.2.3 不同溶剂展开
参照2015版药典薄层色谱鉴定方法[3],用定量毛细管分别吸取供试品及对照品溶液各2~5 μL,分别点于同一硅胶G薄层板上,分别以不同展开剂系统进行展开,取出,晾干,喷以0.5%香草醛硫酸乙醇(10%)溶液,在105℃加热至斑点显色清晰。
1.2.3 指纹图谱建立
1.2.3.1 供试品溶液的制备
取艾纳香油样品0.1 g,精密称定,置25 mL容量瓶中,加乙酸乙酯至刻度,摇匀,然后再精密量取1 mL置10 mL容量瓶中,加乙酸乙酯稀释至刻度,摇匀,0.45 μm微孔滤膜滤过,即得。
1.2.3.2 参照物溶液的制备
分别精密称取β-蒎烯、芳樟醇、樟脑、l-龙脑、β-石竹烯对照品适量,加乙酸乙酯溶解并定容,制成质量浓度分别为1.578、0.784、3.545、8.243、4.472 mg/mL的混合液,作为混合对照品储备液。
1.2.3.3 色谱条件
色谱柱:HP-5毛细管柱(30 m×0.32 mm,0.25 μm),程序升温(40℃保持3 min,以2℃/min升温至100℃,保持5 min,以5℃/min快速升温至200℃,保持10 min),载气为高纯氮气,流量6.5 mL/min;进样量0.6 μL,不分流,FID检测器温度240℃,进样口温度220℃。按l-龙脑计算理论塔板数及分离度。结果理论塔板数不低于50 000,分离度大于4,符合指纹图谱的相关要求。该色谱条件作为GC条件。
2 结果与分析
2.1 理化性质
2.1.1 性状
各批次艾纳香油为澄清、棕红色的液体,有特异的芳香气。
2.1.2 溶解性
结果表明艾纳香油易溶于乙醇、氯仿、乙醚,几乎不溶于水,见表1。
2.1.3 比旋度
不同批次艾纳香油比旋度见图1。由图1可知,13批样品比旋度变化较小,说明艾纳香油的比旋度较稳定,为此艾纳香油在质量控制的过程中比旋度宜为-26°~-30°。
2.1.4 相对密度
不同批次艾纳香油相对密度见图2。由图2可知,13批样品相对密度变化较小,说明艾纳香油的相对密度较稳定,为此艾纳香油在质量控制的过程中相对密度宜为0.94~0.98。
2.2 TCL鉴别
不同溶剂展开系统试验结果见表2。试验结果表明,选择石油醚-乙酸乙酯(9∶1)作为展开体统较为适宜。供试品色谱中,在与对照品色谱相应的位置上,l-龙脑、β-石竹烯分别显相同颜色的斑点,斑点可见。
2.3 指纹图谱研究结果
2.3.1 检测方法的检验
2.3.1.1 精密度试验
取同一供试品续滤液,按“1.2.3.3”色谱条件连续进样6次,以l-龙脑为参照峰,计算各共有峰的相对保留时间RSD<0.1%,相对峰面积RSD<2%,结果表明仪器精密度良好(图3)。
2.3.1.2 重复性实验
取同一批样品6份,按照供试品溶液制备方法制备,续滤液进样,按“1.2.3.3”色谱条件色谱条件分别进样,以l-龙脑为参照峰,计算各共有峰的相对保留时间RSD<0.05%,相对峰面积RSD<2%。结果表明,该方法重复性良好。
2.3.1.3 稳定性实验
取同一供试品续滤液,按“1.2.3.3”色谱条件,分别在0、2、4、8、12、24 h进样,以l-龙脑为参照峰,计算各共有峰的相对保留时间RSD<0.05%,相对峰面积RSD<2%。结果表明,供试品溶液在24 h内稳定。
2.3.2 指纹图谱及技术参数
2.3.2.1 指纹图谱采集及共有峰的标定[8]
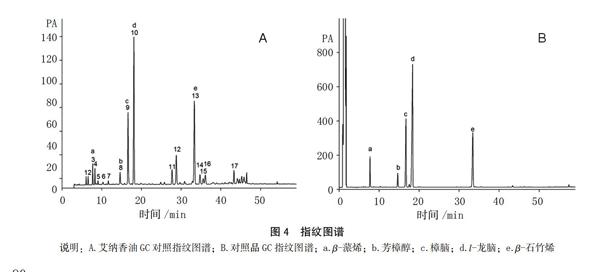
将13批艾纳香油药材按“1.2.3.1”供试品溶液制备方法得到进样样品,依法测定记录色谱图得到13批药材GC指纹图谱,将其全部导入《中药指纹图谱相似度评价系统2004 A版》,生成对照指纹图谱,见图4-A,共选择反映艾纳香油内在质量的17个共有色谱峰。通过对照品保留时间的定性作用可以鉴定部分色谱峰,可知3号峰为β-蒎烯(7.73 min)、8号峰为芳樟醇(14.65 min)、9号峰为樟脑(16.71 min)、10号峰为l-龙脑(18.39 min)、13号峰为β-石竹烯(33.41 min),见图4-B中a、b、c、d、e。结合不同批次艾纳香油GC色谱峰状况,发现10号峰l-龙脑保留时间稳定,峰型对称,响应值高并且为艾纳香油中主要药效指标成分,故选择其为内标参照峰,计算其余各峰的相对保留时间和相对峰面积。
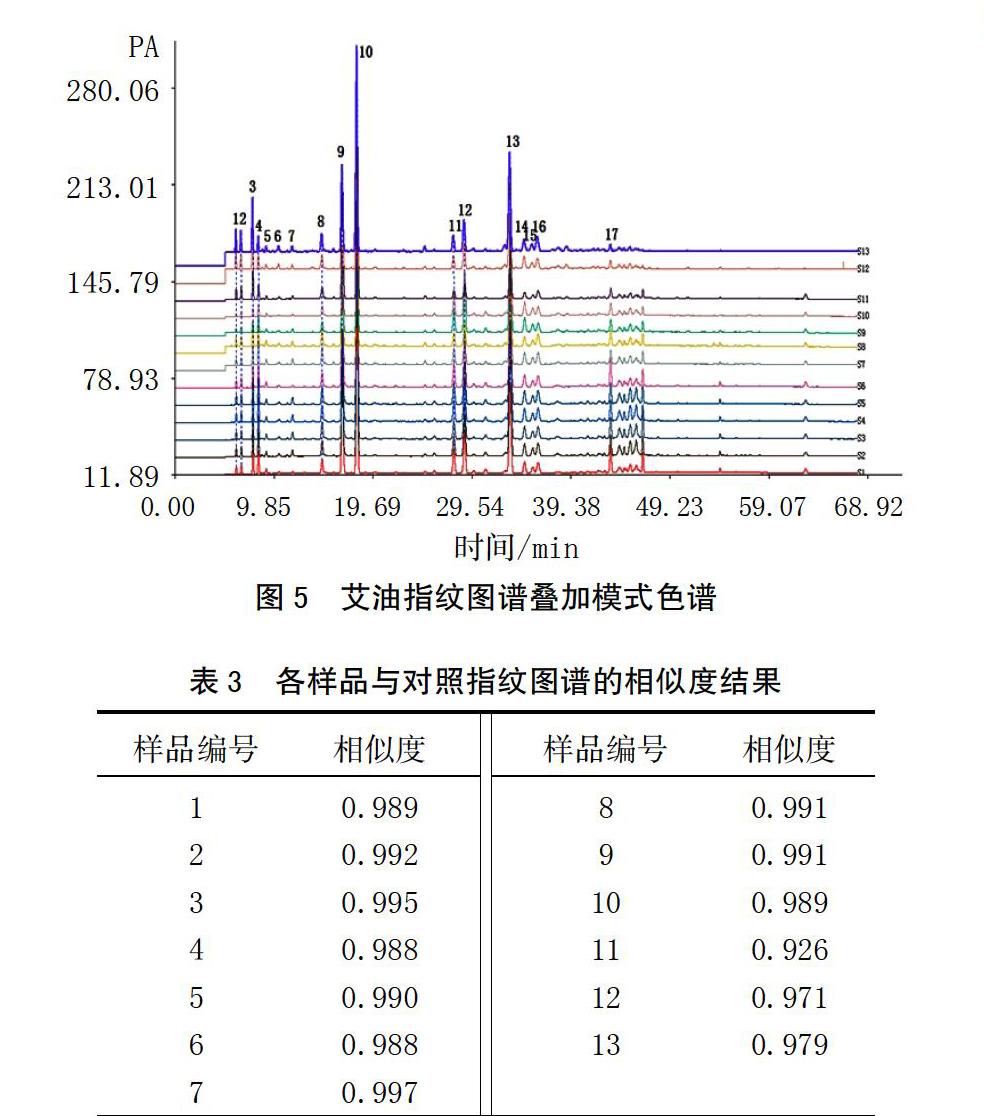
2.3.2.2 特征指纹图谱的建立及相似度评价
特征指纹图谱见图5。根据所建立的GC指纹图谱方法,连续得到13批艾纳香油的指纹图谱,建立了艾纳香油指纹图谱叠加模式色谱图,将各色谱图与特征指纹图谱相比较,采用相似系数进行了相似度判别,相似度均大于0.90。结果见表3。
3 讨论与结论
本文通过对艾纳香油物理性状的观察和测定对其质量进行初步评价。TCL鉴别中采用4种不同展开溶剂分别针对艾纳香油中β-石竹烯和l-龙脑进行薄层鉴别,采用石油醚-乙酸乙酯(9∶1)能使两个极性不同的化合物得到分离,虽然显色不够清晰,各斑点分开较好,Rf值较适宜。因此,以此展开条件为展开系统。
在指纹图谱建立的过程中,对柱温进行了考察,比较不同程序升温方法,采用不同升温方法进样分析,发现快速升温至200℃,保持10 min,共能检测出46个峰,样品在60 min内出峰完全,且色谱基线平稳,各色谱峰分离达到最佳效果,故确定该方法为最佳程序升温法。
目前,相关报道均是对不同产地艾纳香药材进行指纹图谱研究[9],艾纳香油作为其主要提取物,药材本身的质量、提取工艺以及储藏都会对其质量产生影响。本实验首次对不同批次生产的艾纳香油指纹图谱进行研究,共制定17个共有峰,以l-龙脑作为参照峰,分别计算共有峰的相对峰面积和相对保留时间RSD,结果所建立的方法精密度、重复性、稳定性良好。利用《中药色谱指纹图谱相似度评价系统》(2004A版)对艾纳香油指纹图谱的相似性进行研究,其相似度均在0.90以上,艾纳香油化学成分相对稳定。实验结果表明,该方法能够较好地反映艾纳香油的指纹性,可结合薄层鉴别条件以及相关物理性状对艾纳香油的质量进行初步研究,为艾纳香油在生产过程中的质量控制提供参考依据。
参考文献
[1] 袁 媛,庞玉新,王文全,等. 中国艾纳香属植物资源与民族药学研究 [J]. 热带农业科学,2011,31(4):22.
[2] 江苏新医学院. 中药大辞典:上册[M]. 上海:上海科学技术出版社,1985:562-563.
[3] 国家药典委员会. 中华人民共和国药典(一部)[M] . 北京:化学工业出版社,2015:88-89.
[4] 庞玉新. 艾纳香提取物及其制备方法和在口腔清洁护理产品中的应用[P].中国,ZL 201110444901.6 2013-06-05.
[5] 师琴丽,覃军章,王用平,等. 贵州优势苗族药物艾纳香及其产品[J]. 中药材,2003,26(z1):87-88.
[6] 王 丹,付万进,庞玉新,等. 艾纳香油过敏性和急性毒性实验研究[J]. 热带作物学报,2013(12):2 499-2 502.
[7] 孙明玉. 艾纳香油含量测定的方法学验证[J]. 贵州医药,2011(8):757-759.
[8] 罗国安,梁琼鳞,王义明,等. 中药指纹图谱-质量评价、质量控制与新药研发[M]. 北京:化学工业出版社,2009.
[9] 夏稷子,赵 智,安 军,等. 不同产地艾纳香药材的GC指纹图谱研究[J]. 中国药事,2011,25(12):1 191-1 194.
