原位法合成颗粒增强Al-Cu基复合材料的热力学机理研究
2016-05-11格日乐
格日乐,宋 辉
(呼伦贝尔学院矿业学院,内蒙古呼伦贝尔 021008)
原位法合成颗粒增强Al-Cu基复合材料的热力学机理研究
格日乐,宋 辉
(呼伦贝尔学院矿业学院,内蒙古呼伦贝尔 021008)
通过对原位法合成颗粒增强Al-Cu基复合材料的热力学机理进行分析,从热力学角度确定反应进行的可能性,并确定热力学相关工艺参数。结果表明,原位法合成颗粒增强Al-Cu基复合材料在热力学理论上为强放热反应,反应的吉布斯自由能为-1 108 kJ/mol,绝热温度为5 100 K,反应可自发进行且进行彻底。
复合材料;原位反应;热力学机理
本文主要研究原位合成法的热力学机理及进行原位反应的相关热力学条件,从热力学角度确定反应进行的可能性,并制定出制备原位合成颗粒增强Al-Cu基复合材料的热力学工艺参数。
1 选择原位反应体系的热力学基础
由氧化位理论[2]可知,自由能图中位置愈低的金属愈容易氧化,所得氧化物愈稳定;位置低的金属常能从位置较高的金属氧化物中夺取氧,而生成低位置金属的氧化物和高位置的金属元素。因此,从自由能图可知,铝的氧化物(A12O3)位置较低,铝可以用来还原位置较高的金属氧化物,生成A12O3和较高位置的金属。本文所选的A1+CuO反应体系,Cu的氧化物(CuO和Cu2O)均在A12O3的上方,很容易被A1还原,而且Cu的氧化物的位置远高于A1的氧化物的位置,因此本原位反应是高放热反应,反应可自发进行,同时所生成金属元素Cu,作为合金元素与Al组成二元化合物的形式,增强铝基复合材料的基体[3]。
2 Gibbs自由能的计算
根据吉布斯函数的定义[4],吉布斯函数

式中,G、H、S分别为温度为TK时的吉布斯自由能、焓、熵。
热力学机理中,在恒温恒压且非体积功为零的条件下,系统的吉布斯函数减少则反应过程能够自动进行,吉布斯函数不变时反应处于平衡状态,不会发生吉布斯函数增大的过程。因此本文计算Gibbs自由能,作为反应过程自发进行的判据。
吉布斯函数判据:
dGT,P≤0(自发进行)(恒温,恒压,非体积功为零) (2)
本文中的铝热反应可在瞬间完成,因此可视为怛温怛压,且非体积功为零,所以根据热力学基本方程,对于任一反应,反应能否进行的条件为:
It is assumed that the shape of the contact region, the relative motion and the interaction force between the stator and rotor of the ultrasonic motor do not vary with time. If t=0, the equation of the contact surface of the stator and rotor is in the following
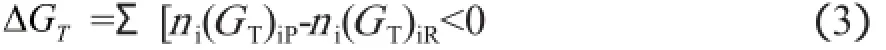
式中,ni(GT)iP为所有生成物的吉布斯自由能值;ni(GT)iR为所有反应物的吉布斯自由能值。
而式(4)中的HT和ST又分别为:


将式(5)、(6)代入式(4)可得
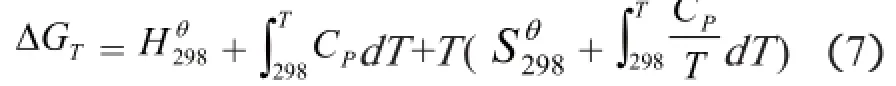
本文的原位反应采用了CuO与Al的放热反应,反应方程式如下:
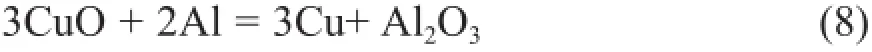
查阅参考文献[5],将Al、Al2O3、Cu、CuO的相关的热力学数据代入方程(7),反应温度为850 ℃时CuO+Al反应体系的△GT的值为△GT= -1 107.95 kJ/mol。
根据吉布斯函数判据,可知反应可以自发进行。从数值大小可以看出,制备Al2O3P/Al-Cu基复合材料时的反应进行得较为彻底。
3 绝热温度Tad
绝热温度Tad是发生原位反应时的放热,使反应体系能达到的最高温度,是描述原位反应特征的最重要的热力学参数。它不仅可以作为判断体系能否发生反应、反应的趋势、反应后能否自我维持以及反应放热能否使产物熔化或汽化等,而且还可以对反应的状态进行预测,并可为反应体系的成分设计提供理论依据。
反应发生时间非常短暂,因此本研究假定:反应体系绝热、产物与反应物的比热不随温度变化、而且反应物按化学方程式100%发生反应,且不可逆。反应产物在升温过程中经历了相变、熔化、汽化等过程,则生成物的相对摩尔焓可以表示为[6]:
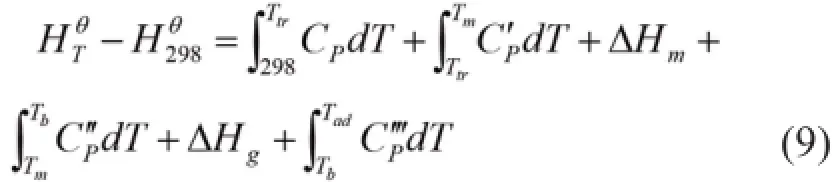
查阅参考文献[5],将热力学关数据代入式(9),计算原位反应的绝热温度的计算公式简化为
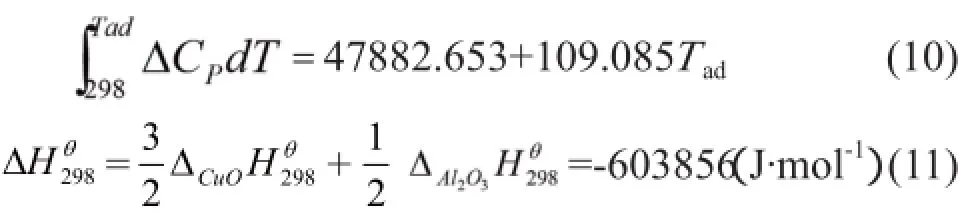
由式(10)和(11)可解得出反应(8)的绝热温度:Tad=5 100 K。
根据热力学原理,任何一个反应只要自由能变化为负即能发生反应,但是SHS自蔓延反应的理论认为,要使反应能自行维持进行,必须Tad>1 800 K。
4 结论
通过对原位法合成颗粒增强Al-Cu基复合材料的热力学机理进行分析,选取绝热温度很高的(Al+CuO)作为原位反应体系,因为它基本满足上文所要求的热力学条件:①CuO和Al的铝热还原反应的自由能变化小于零,而且绝对值较大,在自由能图上CuO和Cu2O都处在Al2O3的上方,所以CuO可以被Al完全还原;②Al+CuO的反应体系的绝热温度很高,远大于1 800 K,一旦启动反应,其自动蔓延的速度快,且反应产物Cu是铝合金中的常用合金元素,适当控制其含量,可以在生成原位增强颗粒的同时实现原位合金化。
[1] 严学华,蒋宗宇,孙少纯.原位反应Al-Cu复合材料的反应机理分析[J].江苏大学学报,2002,23(2):70-73.
[2] 陈新民.物理化学[M].北京:冶金工业出版社.1997:136-152.
[3] 格日乐,田芳.原位反应Al2O3p/Al-Cu基复合材料的强化机理研究[J].热加工工艺,2015,44(14):172-174.
[4] 王正烈,周正平.物理化学[M].天津:高等教育出版社,2003:1-155.
[5] 梁英教,车荫昌.无机物热力学手册[M].沈阳:东北大学出版社,1993:49-381.
[6] 殷声.燃烧合成[M].北京:冶金工业出版社,1999:1-321.
Thermodynamics theory research of the particles reinforced Al-Cu matrix composites by the method of in situ reaction preparation
Gerile, SONG Hui
(Hulunbuir college institute of mining technology,Hulunbeier 021008, Inner Mongolia, China)
This paper analyzes thermodynamics mechanism of particles reinforced Al - Cu matrix composites by the method of in situ reaction preparation; confirms the possibility of the reaction from the viewpoint of thermodynamics and thermodynamics related process parameters. The results show that the particles reinforced Al-Cu matrix composites by the method of in situ reaction preparation is a strongly exothermic reaction in thermodynamics theory, the gibbs free energy is -1108 kJ/mol, the adiabatic temperature is 5 100 K, the reaction can be carried out spontaneously and completely.
composites;in situ reaction;thermodynamics theory
TG115.21+3;
A;
1006-9658(2016)05-0021-02
10.3969/j.issn.1006-9658.2016.05.005
2016-03-27
稿件编号:1603-1307
格日乐(1976—),女,硕士研究生,讲师,主要研究方向为材料的组织与力学性能.
