西格列汀治疗二甲双胍不耐受的新诊断2型糖尿病临床观察
2016-05-10李秀梅杨秀红董陆玲
李秀梅 杨秀红 董陆玲
·论著·
西格列汀治疗二甲双胍不耐受的新诊断2型糖尿病临床观察
李秀梅 杨秀红 董陆玲
目的 观察磷酸西格列汀治疗新诊断2型糖尿病(T2DM)的有效性及安全性。方法 对30例初诊T2DM患者因胃肠道反应不耐受二甲双胍,给予磷酸西格列汀治疗12周,比较应用磷酸西格列汀治疗前后体重指数(BMI)、血糖(PG)、血压、三酰甘油(TG)、总胆固醇(TC)、胰岛素(FINs)水平、糖化血红蛋白(HbA1c)、尿微量白蛋白排泄率(UAER)、高敏C反应蛋白(hs-CRP)、胰岛素抵抗指数(HOMA-IR)及胰岛β细胞功能指数(HOMA-β)。结果 治疗后患者PG、HbA1c、TC、TG、UAER、hs-CRP、HOMA-IR降低,FINs及HOMA-β增加,差异有统计学意义(P<0.05),BMI及血压无明显变化,差异无统计学意义(P>0.05)。结论 磷酸西格列汀治疗初诊T2DM能显著降糖、调脂、减轻炎性反应、减少尿微量白蛋白,改善胰岛素抵抗及胰岛β细胞功能。
磷酸西格列汀;初诊;2型糖尿病;二甲双胍
中国成年人2型糖尿病(T2DM)发病率11.6%,该病是由环境、遗传等多种因素相互作用引起的代谢性疾病。胰岛β细胞功能衰退是T2DM的重要病理基础,多数患者初诊为T2DM时已有大于50%的β细胞功能缺失,并且随着病程的延长,胰岛β细胞数目进行性减少及功能逐渐衰竭;而胰岛β细胞分泌胰岛素缺陷和 α细胞分泌胰高血糖素过高是胰岛细胞功能进行性衰退的另一个进展的重要原因,两者共同作用导致T2DM病情依然会进展。指南推荐新诊断T2DM患者首选二甲双胍,但在临床有部分患者不能耐受或不愿接受二甲双胍治疗。胰高血糖素样肽(GLP-1)可通过促进胰岛素分泌、抑制胰高糖素分泌同时延缓胃排空来发挥降糖作用,生理状态下GLP-1在体内的半衰期非常短,可被二肽基肽酶-4(DPP-4)快速分解而失活,DPP-4是一种跨膜丝氨酸蛋白酶,DPP-4抑制剂通过与DPP-4结合形成复合物来抑制DPP-4的活性,增加活性GLP-1和GIP的水平,以葡萄糖依赖的方式促进胰岛细胞分泌胰岛素,在高血糖的情况下调节α细胞降低胰升血糖素水平,对血糖进行双向调节作用;同时可抑制肝糖的产生,增加组织对葡萄糖的摄取。DPP-4抑制剂是一种高选择性可逆的底物样DPP-4抑制剂,不仅降糖,同时不增加体重、修复胰岛细胞、抗炎和保护心血管等作用,作为二肽基肽酶-4抑制剂磷酸西格列汀,通过口服可增加活性肠促胰素水平降低血糖并改善胰岛功能。本文观察磷酸西格列汀治疗不耐受二甲双胍的新诊断2型糖尿病患者30例,总结如下。
1 资料与方法
1.1 一般资料 2014年1月至2015年6月在张家口市第一医院内分泌科门诊收治的初诊T2DM患者30例,男18例,女12例;年龄38.2~68.4岁,平均年龄(45±8)岁;糖化血红蛋白(HbA1c)7.5%~10.1%。纳入标准:初次就诊;糖尿病诊断标准符合1999年WHO标准;患者服用二甲双胍因胃肠道反应不能耐受或患者因各种原因不愿接受该药物治疗;无磷酸西格列汀用药禁忌证。排除标准:无糖尿病急性并发症如糖尿病酮症酸中毒、高血糖高渗综合征、乳酸酸中毒等急性并发症,无感染及手术等必须应用胰岛素治疗的应激情况;谷氨酸脱羧酶抗体和胰岛细胞自身抗体均阴性;1型糖尿病或其他特殊类型的糖尿病患者;无内分泌腺体如垂体、甲状腺、肾上腺、胰腺等影响糖代谢的疾病;无明显的肝(丙氨酸氨基转移酶或天冬氨酸氨基转移酶高于正常上限的3倍,或总胆红素高于正常上限的1.5倍)、肾(血肌酐>115 mmol/L)疾病者;严重心脏疾病、恶性肿瘤等重要脏器功能障碍;妊娠或哺乳期女性;无糖皮质激素等影响血糖的药物服用史。
1.2 方法 所有患者要求其进行血糖自我监测同时接受糖尿病健康教育(饮食、运动、自我血糖监测),每周复查时均要接受10 min的健康教育,包括饮食管理、运动控制,糖尿病日记,糖尿病可能出现的并发症及如何早期发现,血糖、血脂及血压等的个体化的控制目标。药物选择默克公司生产的口服制剂:磷酸西格列汀(规格:100 mg/片), 用法:100 mg口服,1次/d,疗程12周。低血糖以血糖≤3.9 mmol/L为标准。观察病情变化,记录血糖、低血糖事件发生及药物不良反应(皮疹、胃肠道反应如恶心及呕吐等、关节疼痛等)。
1.3 观察指标 治疗前后测定身高、体重、血压、空腹血糖(FPG)、餐后2 h血糖(2 h PG)、空腹胰岛素(FINs)、HbA1c、空腹血清hs-CRP、三酰甘油(TG)、总胆固醇(TC)及8 h尿白蛋白排泌率(UAER)。
1.4 检测方法 计算体重指数(BMI)=体重/身高2;使用袖带式血压计测量坐位血压;采用葡萄糖氧化酶法测定FPG及2 h PG;采用化学发光法测定FINs;采用离子交换层析高压液相分析法测定HbA1c;采用速率散射比浊法测定空腹血清hs-CRP;使用生化分析仪测定TG、TC及UAER。
1.5 胰岛细胞功能及抵抗指数 稳态模型胰岛β细胞功能指数(HOMA-β)=20×空腹胰岛素(U/L)/[空腹血糖(mmol/L)-3.5];稳态模型评估法胰岛素抵抗指数(HOMA-IR)=空腹血糖(mmol/L)×空腹胰岛素(U/L)/22.5。
1.6 不良反应及事件 包括药物过敏反应出现皮疹;低血糖反应及表现;头晕及头痛;胃肠道表现:恶心、呕吐、腹痛及腹泻;关节疼痛等。

2 结果
2.1 治疗前后血压、BMI比较 治疗后,收缩压(SBP)及舒张压(DBP)较治疗前降低,但差异无统计学意义(P>0.05);BMI无显著变化,差异无统计学意义(P>0.05)。见表1。
表1 治疗前后BMI、血压比较
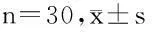

时间BMI(kg/m2)SBP(mmHg)DBP(mmHg)治疗前26.8±2.4124±1485±2.8治疗后26.4±2.5120±1283±3.1
2.2 治疗前后FPG、2 hPG、HbA1c比较 治疗后,FPG、2 hPG、HbA1c较治疗前明显降低[下降值分别为(1.89±0.59) mmol/L,(2.91±0.49)mmol/L,(1.15±0.33)%],差异有统计学意义(P<0.05)。见表2。
2.3 治疗前后血脂比较 治疗后,患者总胆固醇(TC)、三酰甘油(TG)较治疗前均有明显降低[下降值分别为 (1.52±0.24) mmol/L,(1.01±0.37)mmol/L],差异有统计学意义(P<0.05)。见表3。
表2 治疗前后FPG、2 hPG、HbA1c比较
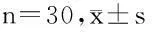

时间FPG(mmol/L)2hPG(mmol/L)HbA1c(%)治疗前8.03±1.0112.6±1.97.6±0.8治疗后6.82±0.29*8.4±1.6*6.7±0.6*
注:与治疗前比较,*P<0.05
表3 治疗前后血脂比较


时间TCTG治疗前5.8±1.92.6±0.9治疗后4.3±1.1*1.8±0.2*
注:与治疗前比较,*P<0.05
2.4 治疗前后胰岛细胞功能、胰岛素水平及胰岛素抵抗指数比较 治疗后,HOMA-β及FINs水平升高[升高值分别为(10.8±5.5),(3.1±0.9)μU/ml],差异有统计学意义(P<0.05);HOMA-IR水平下降[下降值(1.01±0.06)],差异有统计学意义(P<0.05)。见表4。
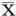
表4 治疗前后胰岛细胞功能、胰岛素水平及胰岛素抵抗指数比较 ±s
注:与治疗前比较,*P<0.05
2.5 治疗前后8 h UAER比较 治疗前UAER(41±12)μg/min,治疗后UAER(20±10)μg/min,治疗后,UREA水平下降[下降值(12±5)μg/min],差异有统计学意义(P<0.05)。
2.6 治疗前后空腹血清hs-CRP比较 治疗前空腹hs-CRP(12.4±2.13)mg/L,治疗后hs-CRP(7.76±1.62)mg/L,hs-CRP水平下降[下降值(3.54±1.02)mg/L],差异有统计学意义(P<0.05)。
2.7 不良反应 在治疗过程中初期有发生恶心或轻度腹泻5例,病情程度轻,随着用药时间延长症状逐渐减轻,均未中断治疗;未见明显低血糖及关节疼痛等其他不良反应的发生。
3 讨论
T2DM是全球范围内发病率持续增高的慢性病之一,胰岛素抵抗和胰岛β细胞功能障碍是T2DM发生发展的主要病理生理机制,β细胞胰岛素分泌缺陷和α细胞胰升糖素不适当的分泌增加造成的胰岛素与胰升糖素比例失调也参与其中。 GLP-1和糖依赖性胰岛素释放肽(GIP)是肠道分泌两种肠促胰岛激素, GLP-1是多种肠促胰岛激素中发挥胰岛素促泌作用的主要物质,促进胰岛细胞分泌胰岛素,正常人在空腹状态下血浆中GLP-1和GIP 激素水平低下,进餐后其血浆水平会迅速升高,GLP-1增加胰岛素分泌占餐后胰岛素分泌的50%以上,降低餐后血糖,从而将血糖控制在稳定水平,这种以葡萄糖浓度依赖方式增加胰岛素分泌,不引起低血糖。正常情况下这些肠促胰岛激素在2~3 min即会被DPP-4降解,DPP-4使循环中的GLP-1很快降解,无法起到有效降糖的作用。DDP-4 是T细胞活化抗原CD26,也是一种腺苷脱氨酶结合蛋白,参与GLP-1和GIP的降解,在维持血糖稳定方面发挥重要的作用;其生理作用还有与炎症、免疫、血管功能、细胞凋亡等有关。DPP-4抑制剂通过抑制 DPP-4的灭活,增加活性的GLP-1和GIP的血浆浓度水平; DPP-4抑制剂不仅可通过抑制DPP-4酶作用而增加GLP-1,延长GLP-1的生理活性持续时间;其还可能直接增加细胞c-AMP水平激活ERK-1信号而刺激GIP-1分泌[1],GLP-1抑制胰岛β细胞凋亡、促进β细胞增殖、改善β细胞功能[2],促使 β细胞合成及分泌胰岛素,抑制胰岛α细胞分泌胰高糖素,使胰岛素/胰高血糖素比值恢复正常,减少肝糖输出及糖异生,具有延缓胃排空[3]的作用,改善餐后β细胞对葡萄糖的反应[4]及β细胞体积减少。2型糖尿病患者不仅β细胞功能丧失,同时GLP-1分泌水平也下降,而且肠促胰素效应也显著降低,餐后胰岛素释放延迟和减少,同时不能抑制胰高血糖素的释放而使血糖升高[5]。磷酸西格列汀是高选择性DPP-4抑制剂,是有效的新型口服降糖药,具有促进胰岛素同时抑制胰高血糖素的分泌、降低肝糖输出、延缓胃排空、抑制食欲及不增加体重等多种有益于降糖的作用[6,7]。本研究亦提示经过西格列汀12周治疗后血糖水平下降,而体重无明显变化。
T2DM也被认为是一种慢性低度炎症性疾病,在T2DM的发生发展过程中多种脂肪细胞因子及炎性因子参与其中,超敏C-反应蛋白(high sensitivity C-reactive protein,hs-CRP)是一种重要的炎性反应标志物,近年研究发现DPP-4抑制剂具有一定的抗炎作用。Makdissi等[8]研究发现发现应用DPP- 4抑制剂后,不仅血糖改善,同时C-反应蛋白水平下降,改善患者血管内皮细胞功能及炎性反应状态,通过抑制DPP-4/CD26活性影响T细胞功能,减少促炎因子的释放;同时降低氧化应激及抑制TNF-α的表达来降低炎症[9]。本研究结果经过西格列汀12周治疗hs-CRP水平下降与此研究类似。
DPP-4抑制剂通过抑制肾小管细胞凋亡,抗氧化保护肾脏。Azuma等[10]研究表明西格列汀在降糖同时能够显著降低受试者尿白蛋白排泄率而不降低受试者的估计肾小球滤过率,并可避免尚未出现白蛋白尿的T2DM患者尿中出现白蛋白,与其降糖、降压以及缓解炎性反应的作用有关。Liu等[11]认为DPP-4 抑制剂有减少蛋白尿,改善肌酐清除率,延缓肾小球硬化等作用。本研究经过西格列汀12周治疗后尿微量白蛋白排泌率水平下降。
DPP-4抑制剂可减少空腹状态下脂肪的脂解作用、减少进餐后脂肪动员;增加脂肪在骨骼肌中消耗来调节脂代谢[12]。Tremblay 等[13]研究发现2 型糖尿病患者给予西格列汀100 mg,1次/d,服药6周后与安慰组相比脂蛋白水平著降低,三酰甘油及低密度脂蛋白也有不同程度的下降,表明西格列汀能够改善糖尿病患者的血脂水平。本研究亦提示经过西格列汀12周治疗后血脂水平下降。
西格列汀是通过抑制DPP-4的活性,减少GLP-1降解,增强胰岛β细胞分泌胰岛素活性,以葡萄糖依赖的方式降低血糖,同时能保护β细胞功能。Mohan等[14]研究发现在有中国人参加的临床饮食及运动干预后血糖无法得到有效控制的T2DM患者经西格列汀治疗18周后降糖效果显著,反映β细胞功能的胰岛素原和胰岛素比值及β细胞功能指数均得到显著改善,患者耐受性良好。本研究结果与上述文献报道一致:HOMA-β升高,HOMA-IR下降。
总之,本研究中对于初诊T2DM患者应用西格列汀单药治疗12周后观察BMI、FPG、HbA1c、血压、血脂、UREA及hs-CRP,结果显示FPG、2 hPG、HbA1c、UREA、TC、TG及hs-CRP均较治疗前显著降低,HOMA-β升高,HOMA-IR下降,血压与体重变化不明显,与上述文献报道一致。
西格列汀治疗前后BMI无显著变化,提示西格列汀不增加体重,整个治疗过程中患者不良反应轻,耐受性良好,无低血糖发生。在研究中西格列汀治疗过程中有6例出现恶心、轻度呕吐或腹泻,未出现低血糖等其他不良反应,并且恶心、呕吐等不良反应程度随用药时间延长症状逐渐完全缓解。提示西格列汀的胃肠道反应较轻,且可随服药时间的延长不良反应逐渐耐受,每天服药1次,与进餐时间无严格要求,依从性较好,用药方便。
综上所述,西格列汀通过延长内源性肠促胰素GLP-1的活性;增加胰岛β细胞胰岛素的分泌,降低α细胞胰高血糖素的分泌,调正胰岛素与胰升糖素比例失调,起到双激素调控作用;同时修复胰岛β细胞的功能缺陷,维持血糖相对平稳;降低空腹状态下脂肪分解来调控血脂,减少脂毒性;具有一定的抗炎作用;减少尿蛋白预防糖尿病肾病的发生。不良反应轻,避免其它降糖药物治疗过程中较易发生低血糖的风险,治疗过程中无体重增加。DPP-4抑制剂可以单独用药,或与二甲双胍、磺脲类、噻唑烷二酮类及胰岛素药物联合用药增强降糖疗效[15]。本研究显示西格列汀降糖效果与二甲双胍相当,但胃肠道不良反应发生风险低于二甲双胍,且程度较轻,对体重无影响,不增加低血糖风险,不良反应少,依从性高,除对于胰岛β细胞具有保护作用还具有降糖外的多器官保护功能,对于初发新诊断的T2DM中等程度高血糖的患者有良好的降糖效果,疗效良好,值得临床推广。
1 Chung HS,Lee MK.Efficacy of sitagliptin when added to on going therapy in korean subjects with type 2 diabetes mellitus.J Diabets Metab,2011,35:411-417.
2 宁光.肠促胰素在血糖稳态调节和2型糖尿病治疗中的作用.中华内分泌代谢杂志,2010,26:1-4.
3 王颖峥,路敏,周颖,等.沙格列汀联合二甲双胍治疗 2 型糖尿病有效性和安全性的meta分析.药物不良反应杂志,2012,14:277-281.
4 Aroda VR,Henry RR, Han J,et al.Efficacy of GLP-1 receptor agonists and DPP-4 inhibitors: meta-analysis and systematic review.J Clin Ther,2012,34:1247-1258.
5 唐甜甜,郭立新.肠促胰素类药物的不良反应.药品评价,2013,10:24-27.
6 廖二元.DDP-4抑制剂—糖尿病治疗新里程碑.药品评价,2011,8:6-7.
7 邹大进.二肽基肽酶IV抑制剂类降糖药的临床认识.中国实用内科杂志,2014,10:952-958.
8 Makdissi Y,Ghanim H,Vora K,et al.Sitagliptin axerts an antinflammatory action.J Clin Endocrinol Metab,2012,97:3333- 3341.
9 Asahara N,Sasaki Y, Wada H, et al.A dipeptidyl peptidase- 4 inhibitor,sitagliptin,exerts anti- inflammatory effects in type 2 diabetes patients.J Metabolism,2013,62:347-351.
10 Azuma K,Radikova Z,Maneino J,et al.Measurements of islet function and glucose metabolism with the dipeptidy peptidase 4 inhibitor vildagliptin in patients with type 2 diabetes.J Chin Endocrinol Metab,2008,93:459-464.
11 Liu WJ,Xie SH,Liu YN,et al.Dipeptidyl peptidase Ⅳ inhibitor attenuates kidney injury in streptozotocin-induced diabetic rats.Pharmacol Exp Ther,2012,340: 248-255.
12 Bosehmann M,Engeli S,Dobberstein K,et al.Dipeptidyl-peptidase-IV inhibition augments postprandial lipid mobilization and oxidation in type 2 diabetic patients.J Clin Endocrinol Metab,2009,94:846-852.
13 Tremblay AJ,Iamarche B,Deacon CF,et al.Effect of sitagliptin therapy on postprandial lipoprotein levels in patients with type 2 diabetes.Diabetes Obes Metab,2011,13: 366-373.
14 Mohan V,Yang WY,Son HY,et al.Efficacy and safety of sitafliptin in the treatment of patients with 2 diabetes in Chain,India,and Korea.Diabetes Res Clin Pract,2009,83:106-116.
15 徐焱成,杨文英. 可平衡α和β细胞功能的二肽基肽酶-4抑制剂:维格列汀.中华糖尿病杂志,2011,3:436-437.
10.3969/j.issn.1002-7386.2016.08.022
076350 河北省崇礼县人民医院(李秀梅);河北省张家口市第一医院(杨秀红、董陆玲)
R 587.1
A
1002-7386(2016)08-1189-04
2015-11-20)
