水溶性荧光探针的制备、固载及对水中汞离子的识别
2016-05-04郑舒丹
焦 扬, 郑舒丹, 周 硼*
(1. 大连理工大学 化学学院, 辽宁 大连 116024; 2. 大连理工大学 精细化工重点实验室, 辽宁 大连 116024 )
水溶性荧光探针的制备、固载及对水中汞离子的识别
焦 扬1, 郑舒丹2, 周 硼1*
(1. 大连理工大学 化学学院, 辽宁 大连 116024; 2. 大连理工大学 精细化工重点实验室, 辽宁 大连 116024 )
通过将5-氨基间苯二甲酸乙酯与葡萄糖相连,设计合成了一种具有良好水溶性的荧光探针PN,该探针能够高选择性地识别水中的汞离子,与汞离子作用后会引起荧光猝灭和紫外吸收减弱。将探针PN固载于介孔硅材料SBA-15,得到材料化的荧光探针SBA-PN,SBA-PN可在pH值4~10范围内使用,对水中的汞离子具有更好的选择性和识别能力。固载之后的探针在实际应用中更加方便,适用于水体系中汞离子的识别。
荧光探针; 固载; 识别; 汞离子
1 引 言
汞是一类能够在生物体内富集的重金属污染物,可以通过饮用水或食用被污染水域中的海产品等方式进入到人体内并且不断累积。汞及其化合物对于生物体系最大的危害来自于其对蛋白质和酶中硫醇基团的高度亲和力,导致细胞功能紊乱,最终对中枢神经、内分泌系统以及肾脏等器官造成严重损伤[1]。因此,环境中少量的汞离子也会对人体健康造成严重危害,需要建立一种简便快速地检测汞离子的方法用于生物和环境中的汞离子的实时监测。在多种检测汞离子的方法中,荧光光谱法因其检测限低、操作简便及成本较低等优点,成为最便捷的检测方法之一[2-4]。
在过去的几十年里,荧光传感方法广泛用于环境和生命体系中金属离子的检测。Yoon等[5]合成了两种分别连接硫醇和羧酸基团的罗丹明衍生物作为汞离子检测的荧光传感器,两个荧光传感器与汞离子在水溶液中作用后都会在罗丹明部分开环,引起大幅度的荧光增强和颜色变化。Lin等[6]报道了一系列包含硫醇和炔烃基团的汞离子荧光探针,可以高选择性地识别汞离子,过程伴随较大的荧光增强,具有较低的检测线,并可以应用于活体细胞。Carlar等[7]报道了三种基于香豆素的荧光化学传感器,这些传感器以硫/氮杂环为接收基团与汞离子作用,对汞离子展现出由OFF到ON的荧光响应,同时探针也能对非洲绿猴肾细胞里的汞离子做出响应。Rao等[8]报道了一种汞离子荧光探针,该探针将葡萄糖跟蒽的衍生物相连,具有较好的生物相容性,可以很好地识别血清或牛奶中的汞离子。
水溶性较好的分子荧光探针在环境检测方面具有潜在的应用价值,但小分子荧光探针溶解在待测体系后不易分离,近年来荧光探针领域出现了许多利用固载材料来优化荧光探针性能的报道。杂化探针的最主要优势在于其可以在水中很好地识别金属离子,同时还可以较方便地从水体系中分离出来,为水中金属离子的检测和去除提供了很大的便利[9-10]。
Jung[9]将荧光分子卟啉功能化在Au@SiO2芯/壳纳米粒子,具有高表面积、低生物毒性等优点。功能化的探针有较强的荧光呈红色,加入汞离子后,10 s之内溶液颜色变为绿色,在其他金属离子的存在下仍然能够高选择性地检测汞离子。识别过程可以通过加入EDTA恢复,探针具有良好的可逆性。Kim等[11]将偶氮苯与接收基团耦合后固载于二氧化钛纳米粒子(AR-TiO2),随着悬浮液中汞离子的加入,AR-TiO2的颜色由黄色变为深红色。Ros-Lis等[12]设计合成了一种用于检测汞离子的荧光传感材料,以共价连接的方式固载于硅胶树脂。汞离子与其作用后会向溶液中释放方酸染料,此时溶液会变为深蓝色,荧光显著增强。孟庆涛等[13]将1,8-萘二甲酰亚胺衍生物P1固载于介孔硅材料,制备了杂化探针SBA-P1。该探针对汞离子具有较高的选择性,还可以用于检测天然水中的汞离子。由于介孔材料具有有序的孔道、孔径尺寸可调,还有良好的热稳定性、耐酸耐碱性、高比表面积和高孔隙率以及易于修饰等一系列优点,是广泛应用于荧光分子探针的固载材料。
为获得水溶性良好的探针,本文将5-氨基间苯二甲酸乙酯通过希夫碱缩合反应与葡萄糖相连,设计合成了一种分子荧光探针PN,研究其对于汞离子的识别性能。并将其固载于介孔硅材料SBA-15,得到材料化荧光探针SBA-PN,研究其对汞离子的识别,观察体系pH值等对于检测结果的影响。
2 实 验
2.1 仪器与试剂
实验仪器:核磁测试采用美国Varian公司Varian INOVA 400核磁共振谱仪,1H NMR的频率为400 MHz,谱宽为10 000 Hz,脉冲重复时间为10 s,脉冲角为30°,温度为25 ℃(TMS内标)。荧光测试采用Edinburgh instruments FS920型稳态荧光仪,激发和发射狭缝均为2 nm。紫外测试采用北京普析通用仪器有限责任公司的TU-1900型双光束紫外-可见分光光度计。固体紫外采用Shimadzu 的UV-240PC型紫外-可见漫反射光谱仪。
化学试剂:分析纯葡萄糖购于天津市博迪化工股份有限公司;分析纯的高氯酸铜、高氯酸银、高氯酸亚铁、高氯酸镁、高氯酸锌、高氯酸锰、高氯酸镍、高氯酸钙、高氯酸镉、高氯酸钴、高氯酸汞、高氯酸铅、高氯酸钾、高氯酸钠购于Alfa Aesar;分析纯5-氨基间苯二甲酸购于Admas;分子筛SBA-15购于长春吉大高科技股份有限公司。
2.2 探针PN的合成
探针PN的合成路线如图1所示。

图1 PN的合成路线
2.2.1 化合物5-氨基间苯二甲酸乙酯的合成
参照文献[14]的方法,将5-氨基间苯二甲酸(5.00 g,0.028 0 mol)溶于约150 mL的乙醇中,滴加5滴浓硫酸作为催化剂,120 ℃下回流12 h。反应结束后,将反应液冷却至室温,用碳酸钠饱和溶液调节反应液的pH值至9,加压蒸馏除去乙醇。粗产物用水和乙酸乙酯萃取(3×150 mL),收集有机相,用无水硫酸钠干燥,减压蒸馏除去溶剂,得到干燥的白色固体6.20 g,产率约为93.3%。
1H-NMR(400 MHz,d6-DMSO)δ:7.63(s, 1H), 7.40 (s, 2H) , 5.72 (s, 2H), 4.29 (m, 4H), 1.29 (m, 6H)。
2.2.2 PN的合成
参照文献[15]方法,将5-氨基间苯二甲酸乙酯(1.00 g,4.29 mmol)和葡萄糖(0.690 g,3.84 mmol)溶于100 mL乙醇中,回流24 h。反应结束后,反应液冷却至室温,减压蒸馏除去乙醇,硅胶柱层析法(二氯甲烷∶甲醇体积比8∶1)纯化产物,得到纯净白色固体1.02 g。产率为60.1%。
1H-NMR(400 MHz,d6-DMSO)δ: 7.76(s, 1H), 7.52 (s, 2H), 7.00 (d, 1H), 5.04 (d, 1H), 4.93 (d, 2H) , 4.47(t, 1H), 4.38 (t, 1H), 4.29 (m, 4H), 3.62 (m, 1H) , 3.46 (m, 1H), 3.27 (m, 2H) , 3.15 (m, 2H), 1.31 (m, 6H)。元素分析C18H25NO9理论值:C:54.13%,H:6.31%,N:3.51%;实际值:C:54.11%,H:6.36%,N:3.49%。

图2 PN的核磁氢谱
2.2.3 SPA-PN的合成
将1.00 g 的SBA-15与0.20 g 的PN溶于50 mL干燥甲苯中,氮气保护下回流24 h。反应结束后,冷却至室温,过滤,并用干燥甲苯洗涤后得到产物SBA-PN。

图3 探针SBA-PN结构示意图
3 结果与讨论
3.1 探针PN的质谱分析
将探针PN溶于甲醇中,选用电喷雾质谱(ESI-MS)对探针PN进行分析,结果表明探针PN具有较强的稳定性,在质荷比为400.16处有明显的质谱分子离子峰,可以归属为C18H25NO9∶400.16(PN+H)。

图4 探针PN的质谱
3.2 探针PN对汞离子的光谱响应
PN对汞离子的荧光和紫外光谱响应见图5。荧光滴定表明,向含有1.0×10-4mol/L探针PN的水溶液中逐渐滴加汞离子,探针PN在340 nm处激发,420 nm处的荧光发射峰逐渐猝灭(图5(a))。当汞离子的加入量达到PN的20倍时,PN与汞离子1∶2作用,荧光的猝灭程度趋于平衡,为探针未加入汞离子时荧光强度的2/5,猝灭常数为1.48×107mol-2·L2。探针PN对水中汞离子的紫外-可见吸收光谱见图5(b),从图中可以看出探针PN在334 nm处有明显的紫外吸收峰,当向该溶液中加入汞离子后,334 nm处的吸收峰猝灭。当加入汞离子的量达到探针PN的20倍时,334 nm处的吸收峰减弱趋于平衡,此时的吸收强度相当于未加入汞离子时的1/3,PN与汞离子1∶2作用,猝灭常数为1.51×107mol-2·L2,与荧光滴定的结果一致。

图5 探针PN对Hg2+的滴定光谱图。 (a)荧光光谱; (b)紫外-可见吸收光谱。
Fig.5 (a) Fluorescence spectra of PN in H2O upon the addition of Hg2+. (b) UV-Vis spectra of PN in H2O upon the addition of Hg2+.
3.3 pH值对PN荧光光谱的影响
在水中测试探针PN以及识别汞离子过程中荧光强度随pH的变化,结果见图6。从图中可以看出,pH值在4~10范围内时,探针PN以及与汞离子结合后的荧光发射强度(420 nm)变化不大,说明探针PN在pH=4~10范围内稳定存在,且与汞作用过程中受pH值影响不大,可以用于检测pH值在4~10范围水中的汞离子。

图6 PN及PN-Hg的pH稳定性
Fig.6 Variations of fluorescence intensity of PN and PN upon the excess Hg2+
3.4 PN 对阳离子的选择性
研究探针PN对Hg2+、Ag+、Ca2+、Cd2+、Co2+、Cu2+、Fe2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Zn2+的选择性。由图7可知,当向含有1.0×10-4mol/L探针PN的水溶液中加入20倍量的各种金属离子时,只有汞离子的荧光信号发生了较为明显的猝灭,加入其他金属离子时溶液荧光信号变化较小,相对于加入汞离子后荧光信号的变化可以忽略不计,探针PN对汞离子有很好的选择性。同时,研究探针PN与不同金属离子的竞争性,当向含有20倍量的各种金属离子的探针PN水溶液中加入20倍量汞离子时,溶液的荧光强度有明显的猝灭,其他金属离子的存在基本不会干扰探针PN对汞离子的识别。该探针PN对汞离子的专一性比较好,可以选择性地识别汞离子,且不受其他金属离子的影响。

图7 PN对金属离子的选择竞争
Fig.7 Fluorescence respective responses of PN in the presence of different ions (light bars) and in each group upon subsequent addition of Hg2+to the above solution (black bars)
3.5 杂化探针的表征
将PN修饰到介孔硅材料SBA-15制备得到杂化探针SBA-PN, 并对其进行表征。
红外光谱(图8)表明, SBA-15的吸收峰主要集中在467,804,1 090,1 632,3 433 cm-15个位置。其中,1 090 cm-1处出现的很强吸收峰归属于Si—O—Si键反对称伸缩振动峰;804 cm-1处吸收峰归属于Si—O—Si键对称伸缩振动峰;467 cm-1出现的吸收峰是Si—O键的弯曲振动所致;1 632 cm-1处为吸附水的羟基变形振动的吸收峰;3 433 cm-1处为端基Si—OH反对称伸缩振动和水分子引起的宽峰。而修饰过探针PN后,SBA-PN在1 381,1 705,2 928,2 986 cm-1四处出现新的吸收峰。其中,1 381 cm-1处的吸收峰是由烷烃的对称变形振动所致,1 705 cm-1处的吸收峰是酯官能团的特征峰,2 986 cm-1和2 928 cm-1处的吸收峰是甲基和亚甲基的伸缩振动峰。这些特征峰的出现表明探针PN已经成功修饰到介孔硅材料SBA-15。

图8 SBA-15和SBA-PN的红外光谱图
由TEM(图9)可以看出探针PN固载在分子筛SBA-15之后的功能化材料SBA-PN与介孔材料SBA-15的结构类似,仍然保持着良好的孔道结构,探针PN只是固载在SBA-15的骨架结构上并未破坏其孔道结构。
进一步研究了固载后的荧光探针SBA-PN的紫外-可见漫反射光谱的变化。从图10可以看出,SBA-15在290 nm处有很弱的紫外吸收峰,PN在380 nm处有很强的紫外吸收峰。将PN固载于SBA-15之后, 在380 nm有明显紫外吸收峰,说明PN已经成功修饰到SBA-15表面。从图10还可以看出探针PN与汞离子作用后,在380 nm处的吸收消失,说明汞离子的加入使得SBA-PN紫外吸收减弱。

图9 SBA-15(a)和SBA-PN(b)的透射电镜图

图10 SBA-15、PN、SBA-PN、SBA-PN-Hg的紫外-可见固体漫反射光谱。
Fig.10 UV-Vis diffuse reflectance spectra of SBA-15, PN, SBA-PN, SBA-PN-Hg, respectively.
3.6 杂化探针对汞离子的识别
固载后的杂化探针SBA-PN在450 nm处出现了较强的荧光发射峰(图11),与PN相比发生了30 nm的红移。当向2×10-5的SBA-PN水溶液中滴加汞离子时, 450 nm处的荧光峰逐渐减弱,当汞离子的加入量为杂化探针的20倍时,荧光的猝灭程度趋于平衡,为杂化探针荧光强度的1/5。SBA-PN与汞离子1∶2作用,猝灭常数为2.45×107mol-2·L2,说明固载后的杂化材料SBA-PN对汞离子的识别比有机小分子探针PN效果略好。
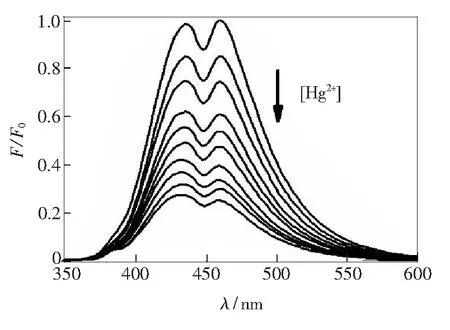
图11 探针SBA-PN在水中对Hg2+的荧光滴定光谱图
Fig.11 Fluorescence spectra of SBA-PN in H2O upon the addition of Hg2+
杂化探针SBA-PN保持了对汞离子的良好选择性。从图12可知,当向含有2×10-5探针SBA-PN的水溶液中加入4×10-4的金属离子Ag+、Ca2+、Cd2+、Co2+、Cu2+、Fe2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Zn2+时,450 nm处的荧光峰没有明显变化;只有当加入汞离子时,荧光信号发生了较为明显的猝灭,说明SBA-PN对汞离子有很好的选择性。当向上述含有4×10-4的各种金属离子的探针SBA-PN水溶液中加入4×10-4的汞离子时,溶液的荧光强度发生明显的猝灭,其他金属离子的存在基本不会干扰SBA-PN对汞离子的识别。
进一步考察pH值对杂化探针SBA-PN识别过程的影响。如图13所示,pH值在4~10范围内,杂化探针SBA-PN的荧光强度没有明显变化;而与汞离子作用后,位于450 nm的荧光峰也保持了很好的稳定性。由此得知,杂化探针SBA-PN可在pH=4~10范围内对水中的汞离子进行识别。

图12 SBA-PN对金属离子的选择竞争
Fig.12 Fluorescence respective responses of SBA-PN in the presence of different ions (light bars) and in each group upon subsequent addition of Hg2+to the above solution (black bars)

图13 SBA-PN及SBA-PN-Hg的pH稳定性
Fig.13 Variations of fluorescence intensity of SBA-PN and SBA-PN upon the excess Hg2+
考察探针对实际水样中汞离子的检测和识别能力,选取饮用自来水(DW)、水库水(RW)与实验室纯净水(LW)进行比较。用上述三种水样分别配制成含有2×10-5探针SBA-PN的悬浊液,测试时分别取2 mL的悬浊液,加入20倍量的汞离子,结果如图14所示。从图中可以看出,荧光强度猝灭的比例没有明显的变化,说明探针SBA-PN对水中汞离子检测和识别的灵敏度受水质影响不大。
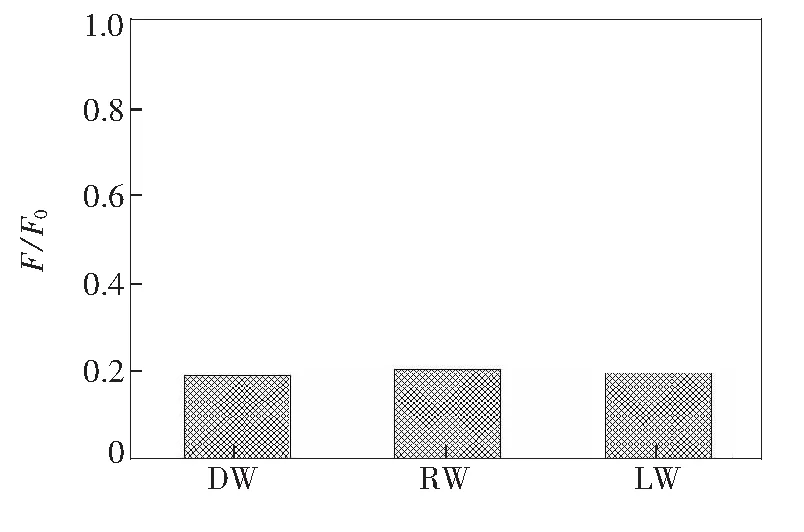
图14 水质对SBA-PN灵敏度的影响:自来水(DW)、西山水库水(RW)和实验室纯净水(LW)。
Fig.14 Influences of water source to the sensitivity of SBA-PN to Hg2+: Drinking water(DW), Reservoir Water(RW), and Laboratory pure water(LW).
4 结 论
本文设计合成了一种具有较好水溶性的汞离子荧光探针PN,并将其固载于介孔硅材料SBA-15,实现了荧光探针的材料化。PN中的葡萄糖基团增加了有机探针的水溶性,使得探针PN可以用于水中汞离子的检测。杂化探针SBA-PN保持了PN对汞离子的高选择性和抗其他金属离子干扰的能力,对汞离子的猝灭常数为2.45×107mol-2·L2,识别效果更好,且便于从水体中分离。SBA-PN可在pH值4~10范围内对水中的汞离子进行识别检测,是一种具有较好汞离子检测能力的荧光探针材料。
[1] MCRAE R, BAGCHI P, SUMALEKSHMY S,etal..Insituimaging of metals in cells and tissues [J].Chem.Rev., 2009, 109(10):4780-4827.
[2] MU Q, LI Y, XU H,etal.. Quantum dots-based ratiometric fluorescence probe for mercuric ions in biological fluids [J].Talanta, 2014, 119:564-571
[3] 赵清,常青,杨金龙,等. 碳点嫁接海藻酸钙复合结构的制备及其对Cu2+的检测 [J]. 发光学报, 2014, 35(3):387-392. ZHAO Q, CHANG Q, YANG J L,etal.. Preparation of complex carbon-dot-grafted calcium alginate and its application as fluorescent sensor for Cu2+[J].Chin.J.Lumin., 2014, 35(3):387-392. (in Chinese)
[4] AHAMED B N, ARUNACHALAM M, GHOSH P. Thiomethoxychalcone-functionalized ferrocene ligands as selective chemodosimeters for mercury (Ⅱ): single-crystal X-ray structural signature of the[Hg8(μ8-S)(SCH3)12]2+cluster [J].Inorg.Chem., 2010, 49(10):4447-4457.
[5] KIM H N, NAM S W, SWAMY K M K,etal.. Rhodamine hydrazone derivatives as Hg2+selective fluorescent and colorimetric chemosensors and their applications to bioimaging and microfluidic system [J].Analyst, 2011, 136(7):1339-1343.
[6] LIN W Y, CAO X W, DING Y D,etal.. A highly selective and sensitive fluorescent probe for Hg2+imaging in live cells based on a rhodamine-thioamide-alkyne scaffold [J].Chem.Commun., 2010, 46(20):3529-3531.
[7] BAZZICALUPI C, CALTAGIRONE C, CAO Z F,etal.. Multimodal use of new coumarin-based fluorescent chemosensors: Towards highly selective optical sensors for Hg2+probing [J].Chemistry, 2013, 19(43):14639-14653.
[8] MITRA A, MITTAL A K, RAO C P. Carbohydrate assisted fluorescence turn-on gluco-imino-anthracenyl conjugate as a Hg (Ⅱ) sensor in milk and blood serum milieu [J].Chem.Commun., 2011, 47(9):2565-2567.
[9] CHO Y, LEE S S, JUNG J H. Recyclable fluorimetric and colorimetric mercury-specific sensor using porphyrin-functionalized Au@SiO2core/shell nanoparticles [J].Analyst, 2010, 135(7):1551-1555.
[10] LENG B, ZOU L, JIANG J B,etal.. Colorimetric detection of mercuric ion (Hg2+) in aqueous media using chemodosimeter-functionalized gold nanoparticles [J].Sens.ActuatorsB, 2009, 140(1):162-169.
[11] KIM E, SEO S, SEO M L,etal.. Functionalized monolayers on mesoporous silica and on titania nanoparticles for mercuric sensing [J].Analyst, 2010, 135(1):149-156.
[13] MENG Q T, ZHANG X L, HE C,etal.. A hybrid mesoporous material functionalized by 1, 8-naphthalimide-base receptor and the application as chemosensor and absorbent for Hg2+in water [J].Talanta, 2011, 84(1):53-59.
[14] KAMAL A, SHAIK A B, REDDY G N,etal.. Synthesis, biological evaluation, and molecular modeling of (E)-2-aryl-5-styryl-1, 3, 4-oxadiazole derivatives as acetylcholine esterase inhibitors [J].Med.Chem.Res., 2014, 23(4):2080-2092.
[15] NIAZI S, JAVALI C, PARAMESH M,etal.. Study of influence of linkers and substitutions on antimicrobial activity of some Schiff bases [J].Int.J.Pharm.Pharm.Sci., 2010, 2(3):108-112.
Synthesis and Immobilization of Water-solubility Fluorescent Probe and Recognition of Mercury(Ⅱ) Ions in Water
JIAO Yang1, ZHENG Shu-dan2, ZHOU Peng1*
(1.ChemistryCollege,DalianUniversityofTechnology,Dalian116024,China, 2.StateKeyLaboratoryofFineChemicals,DalianUniversityofTechnology,Dalian116024,China)
*CorrespondingAuthor,E-mail:zhoupeng@dlut.edu.cn
Fluorescent molecular probes with high sensitivity, high selectivity, fast and convenient real-time in-field testing, are widely used to detect heavy metal ions. In this paper, we designed and synthesize a water-soluble fluorescent probe PN. PN could selectively detect mercury(Ⅱ) ions in aqueous solution. The small molecule probe PN afforded fluorescent intensity quench and decrease absorption of UV/Via spectrum in the presence of mercury(Ⅱ) ions. In order to achieve practical applications, PN is immobilized on the surface of SBA-15. The immobilization of fluorescent probe (SBA-PN) could selectively and sensitively detect mercury(Ⅱ) ions in a relatively wide pH range(4-10). Comparing with PN, the composite probe is more suitable for the recognition of mercury(Ⅱ) ions in water.
fluorescent probe; immobilization; recognition; mercury(Ⅱ) ions

焦扬(1984-),女,辽宁大连人,博士,讲师,2013年于大连理工大学获得博士学位,主要从事分子识别与传感方面的研究。
E-mail: jiaoyang@dlut.edu.cn

周硼(1965-)女,辽宁兴城人,博士,副教授,2003年于大连理工大学获得博士学位,主要从事荧光探针识别方面的研究。
E-mail: zhoupeng@dlut.edu.cn
1000-7032(2016)03-0379-07
2015-09-23;
2015-12-16
中央高校基本科研业务费专项资金(DUT14RC(3)048); 科技部重大仪器专项(2012YQ0901970403)资助项目
0482.31
A
10.3788/fgxb20163703.0379
